Fluorescens Time-lapse Imaging af Complete<em> S. venezuelae</em> Life Cycle Brug af en mikrofluidapparat
Summary
Streptomyces are characterized by a complex life cycle that has been experimentally challenging to study by cell biological means. Here we present a protocol to perform fluorescence time-lapse microscopy of the complete life cycle by growing Streptomyces venezuelae in a microfluidic device.
Abstract
Live-cell imaging of biological processes at the single cell level has been instrumental to our current understanding of the subcellular organization of bacterial cells. However, the application of time-lapse microscopy to study the cell biological processes underpinning development in the sporulating filamentous bacteria Streptomyces has been hampered by technical difficulties.
Here we present a protocol to overcome these limitations by growing the new model species, Streptomyces venezuelae, in a commercially available microfluidic device which is connected to an inverted fluorescence widefield microscope. Unlike the classical model species, Streptomyces coelicolor, S. venezuelae sporulates in liquid, allowing the application of microfluidic growth chambers to cultivate and microscopically monitor the cellular development and differentiation of S. venezuelae over long time periods. In addition to monitoring morphological changes, the spatio-temporal distribution of fluorescently labeled target proteins can also be visualized by time-lapse microscopy. Moreover, the microfluidic platform offers the experimental flexibility to exchange the culture medium, which is used in the detailed protocol to stimulate sporulation of S. venezuelae in the microfluidic chamber. Images of the entire S. venezuelae life cycle are acquired at specific intervals and processed in the open-source software Fiji to produce movies of the recorded time-series.
Introduction
Streptomycetes er jordboende bakterier, der er kendetegnet ved en kompleks udviklingsmæssig cyklus involverer morfologisk differentiering fra en flercellede, næringsstof-latrintømning mycelium til hvilende, unigenomic sporer 1-3.
Under gunstige vækstbetingelser, en typisk Streptomyces Spore begynder at spire ved ekstrudering én eller to mikroberør (figur 1). Disse rør langstrakt med tip udvidelse og vokse ind i en forgrenet hyfe netværk kendt som den vegetative mycelium. Polar vækst og hyfeforgrening er instrueret af den væsentlige protein DivIVA. Denne coiled-coil-protein er en del af en stor cytoplasmatisk kompleks kaldet polarisome, hvilket er afgørende for indsættelse af nye celle kuvert materiale ved strækker spidsen 4-7. Under vegetativ vækst, de svampetrådenes filamenterne bliver ruminddelt af sjældne dannelse af såkaldte cross-vægge 8. Dannelsen af disse tværgående vægge re quires FtsZ, tubulin-lignende cytoskeletale protein der er essentielt for celledeling i de fleste bakterier 9. I Streptomyces, men disse vegetative cross-vægge ikke fører til indsnævring og celle-celle-adskillelse og derfor myceliemassen forbliver som et netværk af indbyrdes forbundne syncytial rum. Som reaktion på næringssaltbegrænsning og andre signaler, der ikke er godt forstået, specialiserede lufthyfer bryde væk fra den vegetative mycelium og vokse i luften 3. Opførelsen af disse strukturer initierer reproduktive udviklingsfase, hvor den lange multi-genomisk lufthyfer blive opdelt i snesevis af lige store unigenomic prespore rum. Denne massive celledeling begivenhed er drevet af den synkrone konstriktion af flere FtsZ ringe inden enkelt sporogenic hyfer 2,10. Morfologisk differentiering er afsluttet ved frigivelse af hvilende, tykvæggede, pigmenterede sporer.
t "fo: holde-together.within-side =" 1 ">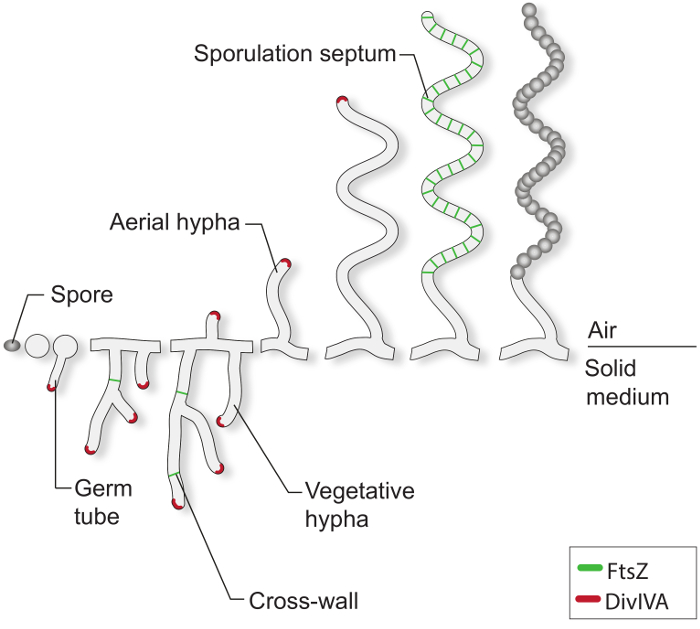
Figur 1:. Den Streptomyces livscyklus på faste medier Dette er en model af livscyklus baseret på klassiske studier af S. coelicolor vokser på agarplader. Den cellulære udvikling af en sporesuspension begynder med dannelsen af en eller to mikroberør, som vokser ved spids forlængelse for at danne et netværk af forgrenende hyfer. Polar vækst og forgrening af den vegetative hyfer er instrueret af DivIVA (rød). Dannelsen af vegetative cross-vægge kræver FtsZ (grøn). Som svar på begrænsninger næringsstoffer og andre signaler, der lufthyfer rejst. Anholdelse af antenne vækst er tæt koordineret med samling af en stige af FtsZ-ringe, som giver anledning til den sporuleringen septa, der inddeler den sporogenic hyfer i box-lignende prespore rum. Disse rum samle en tyk spore- væg og er til sidst Released som modne pigmenterede sporer.
De vigtigste udviklingsmæssige begivenheder i Streptomyces livscyklus er godt karakteriseret 1,3. Men hvad er stadig sparsomme er celle biologiske undersøgelser, der beskæftiger fluorescens time-lapse mikroskopi til at give indsigt i de subcellulære processer understøtter differentiering, såsom protein lokalisering dynamik, kromosom bevægelse og udviklingsmæssigt kontrolleret celledeling. Lev-cell imaging af Streptomyces udvikling har været en udfordring på grund af kompleksiteten af livscyklus og de fysiologiske egenskaber af organismen. Tidligere undersøgelser på den vegetative vækst og de indledende stadier af sporedannelse septumdannelse har ansat oxygenpermeable billeddannende kamre, eller agarose-understøttede vækst af Streptomyces coelicolor på et mikroskop stadium 11-15. Disse metoder er imidlertid begrænset af en række faktorer. Nogle systemer tillader kun kortvarig billeddannelse af cellevækst end fluorescerende proteiner før celler lider under utilstrækkelig ilttilførsel eller vokse ud af fokusplanet på grund af den tredimensionale mønster af hyfe udvikling. I tilfælde, hvor langsigtet billeddannelse er mulig, dyrke celler på agarose puder grænser eksperimentel fleksibilitet, fordi cellerne ikke kan udsættes for alternative vækst- eller stresstilstande, og baggrunden fluorescens fra mediet i agarose puder alvorligt begrænser muligheden for at overvåge svagere fluorescerende signaler.
Her beskriver vi en protokol for live-cell imaging af komplette Streptomyces livscyklus med fremragende præcision og følsomhed. Ved at dyrke Streptomyces i et mikrofluidapparat tilsluttet en fluorescens vidvinklede mikroskop (Figur 2), er vi nu i stand til at overvåge spiring, vegetativ vækst og sporedannelse septumdannelse over en tidsperiode på op til 30 timer. Dette er i høj grad lettes ved anvendelse af de nye model organisme Streptomyces </em> venezuelae fordi det sporulates til nær færdiggørelse i nedsænket kultur og derved overvinder begrænsningen af den klassiske model arter S. coelicolor, som kun sporulates på faste medier 16-20. At hjælpe med at visualisere vegetativ vækst og sporedannelse, vi coudtrykke fluorescens mærkede versioner af cellepolaritet markør DivIVA og nøglen celledeling protein FtsZ.
Vi bruger en kommercielt tilgængelig mikrofluidanordning, der er blevet anvendt med held til mycobakterier, Escherichia coli, Corynebacterium glutamicum, Bacillus subtilis og gær 21-25. Systemet fælder celler i et enkelt fokalplan og tillader kontrol med kontinuerlig perfusion af dyrkningsmedium fra forskellige reservoirer. I detaljeret protokol tager vi fordel af denne funktion til at udsætte S. venezuelae vegetativ mycelium til en ernæringsmæssig nedgearing til fremme sporedannelse.
Protokollen deScribed er for live-cell imaging af hele Streptomyces livscyklus, men alternative medier betingelser eller mikroskop indstillinger kan vælges, hvis specifikke udviklingstrin er af særlig interesse.
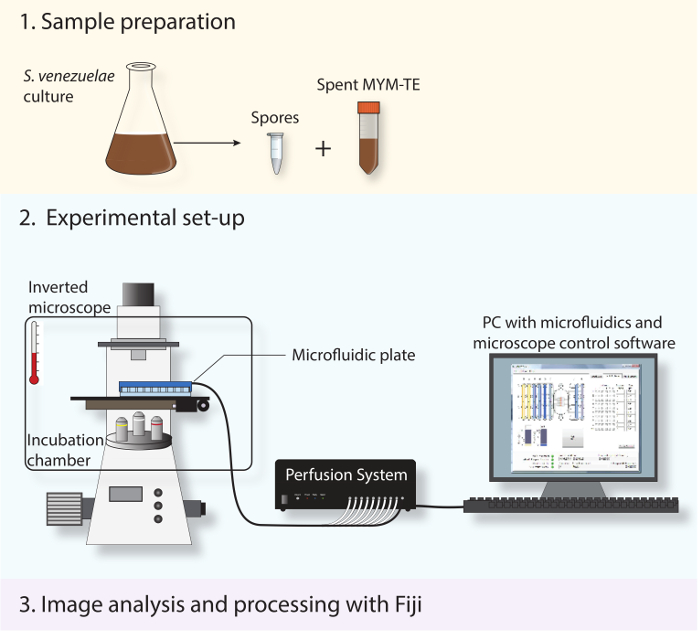
Figur 2: Skematisk afbilder eksperimentelle arbejde-flow. De tre vigtigste trin, der er beskrevet i protokollen, er vist. Først sporer og brugte medium fremstilles ud fra en stationær fase kultur. For det andet er de friske sporer fyldt i en mikrofluidsystem og S. venezuelae afbildes hele dets udviklingsmæssige livscyklus hjælp af et fuldt automatiseret inverteret mikroskop med en inkubation kammer til at opretholde en optimal væksttemperatur. For det tredje er det time-lapse-serien opnåede analyseres og behandles med open source-software Fiji.
Protocol
Representative Results
Discussion
Time-lapse mikroskopi af Streptomyces livscyklus har været teknisk udfordrende i fortiden. Her præsenterer vi en robust protokol til at udføre live-cell imaging af det komplette livscyklus anvendelse af fluorescerende protein fusioner til cellepolaritet markør DivIVA og celledeling protein FtsZ at hjælpe med at visualisere og spore progression gennem udviklingsmæssige program (figur 2).
Centralt for denne fremgangsmåde er dyrkning af S. venezuelae i en mikrofluid enhed, som giver konstant medium perfusion og udveksling af normal vækstmedium (MYM-TE) med brugt medium (brugt MYM-TE). Ændringen af kultur tilstand er vigtig for den beskrevne protokol, fordi den ernæringsmæssige downshift som brønde som nogen endnu uidentificerede ekstracellulære signaler (f.eks quorum sensing signaler) i det brugte dyrkningsmedium, fremme sporulering, mens en konstant forsyning af næringsrige medium stimulerer vegetativ growth med næppe sporedannelse (data ikke vist). Således dyrkning af celler i dette mikrofluidsystem er overlegen i forhold til dyrkning af celler på agarose, fordi det giver mere eksperimenterende fleksibilitet og muliggør langsigtet overvågning af ændringer i bakterievækst som reaktion på skiftende dyrkningsbetingelser. Selvom mikrofluide plader er designet til engangsbrug, strømningskanaler, der ikke er podet med celler kan anvendes i efterfølgende eksperimenter. Vi anbefaler at bruge alle kanaler i en mikrofluid plade inden for en uge, som vi har oplevet problemer forsegling manifolden til plader der er blevet åbnet i længere tid.
Ved opsætning af et eksperiment, fandt vi, at frisk tilberedt sporer spiret inden for to timer for at blive læsset ind i strømmen kammeret, mens sporer afledt af en frossen glycerol lager kræves mindst 6 timer før kimtråde opstået (data ikke vist). Denne forsinkelse i spiring udvider længden af eksperimentet og kan forstyrreudstyr tilgængelighed og eksperimentelle betingelser. Det er også vigtigt at starte eksperimentet med perfusion af MYM-TE i mindst 3 timer for at give tilstrækkelige næringsstoffer til udvikling og udvækst af kim rør. Perfusion med MYM-TE kan udvides ud over den indledende 3 timer, hvis eksperimentet er designet til at studere vegetativ vækst. Mens sporer giver det foretrukne valg af udgangsmateriale, kan korte hyfefragmenter også lægges i mikrofluid plade. Men lastning effektivitet ved brug af klippet mycelium er væsentligt lavere og ofte kræver flere lastning kørsler, som kan udgøre en begrænsning ved undersøgelsen ikke-sporulerende mutanter. Uanset typen af inokulum anvendes, er det vigtigt ikke at overbelaste kultur kammer med sporer eller hyfefragmenter da dette vil føre til hurtig overbelægning, der kan forstyrre medier diffusion og komplicere billedanalysen.
Det er vigtigt at planlægge opførelsen af reporter-proteiner carefully til brug i fluorescens time-lapse billeddannelse i Streptomyces. Linker længde mellem målproteinet og det fluorescerende reporter og valget af N- eller C-terminale fusioner kan være kritisk. Desuden optimale forsøgsbetingelser, herunder billeddannelse frekvens og eksponeringstid, skal fastlægges på forhånd for hver fluorescens-mærkede protein. S. venezuelae hyfer udviser auto-fluorescens i grøn / gul kanal, der kan blive problematisk, når afbildning af et fluorescensmærket protein, der udtrykkes i lave niveauer. Desuden bør det bemærkes, at, under spiring og den indledende vegetative vækstfase, S. venezuelae er særligt følsomme over for korte bølgelængde (fx ved anvendelse af proteinfusioner til FFP).
På trods af de løbende fremskridt i billeddiagnostiske teknikker og fluorescerende reporter systemer til live-cell imaging af bakterier, de fleste af de software-pakker (f.eks MicrobeTracker, Schnitzelcalen, CellProfiler) til efterfølgende automatisk behandling af disse former for datasæt understøtter ikke analysen af billeder, der er afledt af trådformede bakterier med en flercellet livsstil 27-29. Således er der et behov for at udvikle en passende algoritme til kvantitativ high-throughput analyse af billeddata fra Streptomyces og andre trådformede bakterier.
Sammenfattende den her beskrevne arbejde viser det enorme potentiale for S. venezuelae som ny model udviklingsmæssig system til slægten, på grund af dens evne til at danne sporer i væske. Den mikrofluid dyrkning enhed er enkel at bruge, selv for uerfarne brugere. Det giver en fremragende platform til at studere celle biologiske processer er centrale for Streptomyces livscyklus, herunder dynamisk protein lokalisering, polariseret vækst, og den morfologiske differentiering af en flercellet mycelium i kæder af unigenomic sporer. Desuden indstille denne eksperimentelle up tilvejebringer også en fristende udgangspunkt at undersøge begivenheder i den udvikling, der kræver skiftevis dyrkningsbetingelser, eller anvendelse af fluorescerende farvestoffer, såsom fluorescerende D-aminosyrer til overvågning peptidglykansyntese eller propidiumiodid og 4 ', 6-diamidino-2-phenylindol (DAPI) at visualisere kromosom organisation 30,31.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors thank Grant Calder for technical assistance with the microscope, Matt Bush for comments on the protocol, and the John Innes Centre for purchase of the Zeiss widefield microscope. This work was funded by BBSRC grant BB/I002197/1 (to M.J.B), by BBSRC Institute Strategic Programme Grant BB/J004561/1 to the John Innes Centre, by Swedish Research Council grant 621-2010-4463 (to K.F.), and by a Leopoldina Postdoctoral Fellowship (to S.S.).
Materials
| B04A CellAsic ONIX plate for bacteria cells | Merck-Millipore | B04A-03-5PK | Microfluidic culture plates |
| CellAsic ONIX Microfluidic Perfusion System and ONIX FG (version 5.0.2) | Merck-Millipore | EV-262 | The latest ONIX vesion (July 2015) and instructions on how to use the programme can be found here: http://www.merckmillipore.com |
| Axio Observer.Z1 Microscope | Zeiss | 431007-9902-000 | Fully automated and motorized inverted widefield microscope |
| Incubator XL multi S1 with Temperature Module S1 and Heating unit XL S2 | Zeiss | 411857-9061-000 | Environmental chamber surrounding the microscope |
| Plan-Apochromat 100x/1.46 Oil DIC objective | Zeiss | 420792-9800-000 | |
| Ocra FLASH 4 V2 | Hamamatsu Photonics K.K. | C11440-22CU | |
| Illuminator HXP 120V | Zeiss | 423013-9010-000 | |
| FL Filter Set 46 HE YFP shift free | Zeiss | 489046-9901-000 | Fluorescent filter set, excitation 500/25 nm, emission 535/30 nm |
| FL Filter Set 63 HE RFP shift free | Zeiss | 489063-0000-000 | Fluorescent filter set, excitation 572/25 nm, emission 629/30 nm |
| Mounting frame K-M for multiwell plates | Zeiss | 000000-1272-644 | Stage holder for microfluidic plate |
| ZEN pro 2012 | Zeiss | 410135-1002-120 | Microscope control software |
| ZEN Module Time Lapse | Zeiss | 410136-1031-110 | Software module to set up time-lapse microscopy experiments |
| ZEN Module Tiles/Positions | Zeiss | 410136-1025-110 | Software module to save specific stage positions (xzy) |
| Fiji | open-source software package | http://fiji.sc/Fiji | Generation of time-lapse movies |
| Maltose-Yeast Exctract-Malt Extract (MYM) 4 g Maltose 4 g Yeast extract 10 g Malt extract add 1 L H2O using 50 % tap water and 50 % reverse osmosis water and supplement with 200 ml of R2 trace element solution per 100 ml after autoclaving |
Sporulation medium used to culture S. venezuelae SV60 | ||
| R2 Trace element solution (TE) 8 mg ZnCl2 40 mg FeCl3-6H2O 2 mg CuCl2-2H2O 2 mg MnCl2-4H2O 2 mg Na2B4O7-10H2O 2 mg (NH4)6Mo7O24-4H2O add 200 ml H2O Autoclave and store at 4 oC |
Add 0.002 volumes to MYM | ||
| PBS (phosphate buffered saline) | Sigma | P4417-100TAB | Used to refill inlet wells of unused lanes in B04A plates in order to prepare plate for short-term storage. |
| 0.22 µm syringe filters | Satorius stedim | 16532-K | Preparation of spent MYM-TE |
| SV60 | John Innes Centre strain collection | S. venezuelae strain expressing divIVA-mcherry and ftsZ-ypet |
References
- Bush, M. J., Tschowri, N., Schlimpert, S., Flärdh, K., Buttner, M. J. c-di-GMP signalling and the regulation of developmental transitions in streptomycetes. Nat. Rev. Microbiol. 13, 749-760 (2015).
- Jakimowicz, D., van Wezel, G. P. Cell division and DNA segregation in Streptomyces.: how to build a septum in the middle of nowhere?. Mol. Microbiol. 85, 393-404 (2012).
- McCormick, J. R., Flärdh, K. Signals and regulators that govern Streptomyces development. FEMS Microbiol. Rev. 36, 206-231 (2012).
- Flärdh, K., Richards, D. M., Hempel, A. M., Howard, M., Buttner, M. J. Regulation of apical growth and hyphal branching in Streptomyces. Curr. Opin. Microbiol. 15, 737-743 (2012).
- Hempel, A. M., et al. The Ser/Thr protein kinase AfsK regulates polar growth and hyphal branching in the filamentous bacteria Streptomyces. Proc. Natl. Acad. Sci. U S A. 109, E2371-E2379 (2012).
- Fuchino, K., et al. Dynamic gradients of an intermediate filament-like cytoskeleton are recruited by a polarity landmark during apical growth. Proc. Natl. Acad. Sci. U S A. 110, E1889-E1897 (2013).
- Holmes, N. A., et al. Coiled-coil protein Scy is a key component of a multiprotein assembly controlling polarized growth in Streptomyces. Proc. Natl. Acad. Sci. U S A. 110, E397-E406 (2013).
- McCormick, J. R., Su, E. P., Driks, A., Losick, R. Growth and viability of Streptomyces coelicolor. mutant for the cell division gene ftsZ. Mol. Microbiol. 14, 243-254 (1994).
- Margolin, W. FtsZ and the division of prokaryotic cells and organelles. Nat. Rev. Mol. Cell Biol. 6, 862-871 (2005).
- Grantcharova, N., Lustig, U., Flärdh, K. Dynamics of FtsZ assembly during sporulation in Streptomyces coelicolor A3(2). J. Bacteriol. 187, 3227-3237 (2005).
- Richards, D. M., Hempel, A. M., Flärdh, K., Buttner, M. J., Howard, M. Mechanistic basis of branch-site selection in filamentous bacteria. PLoS Comput. Biol. 8, e1002423 (2012).
- Hempel, A. M., Wang, S. B., Letek, M., Gil, J. A., Flärdh, K. Assemblies of DivIVA mark sites for hyphal branching and can establish new zones of cell wall growth in Streptomyces coelicolor. J. Bacteriol. 190, 7579-7583 (2008).
- Wolanski, M., et al. Replisome trafficking in growing vegetative hyphae of Streptomyces coelicolor A3(2). J. Bacteriol. 193, 1273-1275 (2011).
- Jyothikumar, V., Tilley, E. J., Wali, R., Herron, P. R. Time-lapse microscopy of Streptomyces coelicolor.growth and sporulation. Appl. Environ. Microbiol. 74, 6774-6781 (2008).
- Willemse, J., Borst, J. W., de Waal, E., Bisseling, T., van Wezel, G. P. Positive control of cell division: FtsZ is recruited by SsgB during sporulation of Streptomyces. Genes. Dev. 25, 89-99 (2011).
- Glazebrook, M. A., Doull, J. L., Stuttard, C., Vining, L. C. Sporulation of Streptomyces venezuelae. in submerged cultures. J. Gen. Microbiol. 136, 581-588 (1990).
- Bibb, M. J., Domonkos, A., Chandra, G., Buttner, M. J. Expression of the chaplin and rodlin hydrophobic sheath proteins in Streptomyces venezuelae.is controlled by sigma(BldN) and a cognate anti-sigma factor, RsbN. Mol. Microbiol. 84, 1033-1049 (2012).
- Al-Bassam, M. M., Bibb, M. J., Bush, M. J., Chandra, G., Buttner, M. J. Response regulator heterodimer formation controls a key stage in Streptomyces development. PLoS Genet. 10, e1004554 (2014).
- Bush, M. J., Bibb, M. J., Chandra, G., Findlay, K. C., Buttner, M. J. Genes required for aerial growth, cell division, and chromosome segregation are targets of WhiA before sporulation in Streptomyces venezuelae. MBio. 4, e00684-e00613 (2013).
- Tschowri, N., et al. Tetrameric c-di-GMP mediates effective transcription factor dimerization to control Streptomyces development. Cell. 158, 1136-1147 (2014).
- Mirouze, N., Ferret, C., Yao, Z., Chastanet, A., Carballido-Lòpez, R. MreB-Dependent Inhibition of Cell Elongation during the Escape from Competence in Bacillus subtilis. PLoS Genet. 11, e1005299 (2015).
- Zopf, C. J., Maheshri, N. Acquiring fluorescence time-lapse movies of budding yeast and analyzing single-cell dynamics using GRAFTS. J. Vis. Exp. (e50456), (2013).
- Meniche, X., et al. Subpolar addition of new cell wall is directed by DivIVA in mycobacteria. Proc. Natl. Acad. Sci. U S A. 111, E3243-E3251 (2014).
- Donovan, C., Schauss, A., Kramer, R., Bramkamp, M. Chromosome segregation impacts on cell growth and division site selection in Corynebacterium glutamicum. PLoS One. 8, e55078 (2013).
- Rojas, E., Theriot, J. A., Huang, K. C. Response of Escherichia coli. growth rate to osmotic shock. Proc. Natl. Acad. Sci. U S A. 111, 7807-7812 (2014).
- Flärdh, K. Essential role of DivIVA in polar growth and morphogenesis in Streptomyces coelicolor A3(2). Mol. Microbiol. 49, 1523-1536 (2003).
- Sliusarenko, O., Heinritz, J., Emonet, T., Jacobs-Wagner, C. High-throughput subpixel precision analysis of bacterial morphogenesis and intracellular spatio-temporal dynamics. Mol. Microbiol. 80, 612-627 (2011).
- Young, J. W., et al. Measuring single-cell gene expression dynamics in bacteria using fluorescence time-lapse microscopy. Nat. Protoc. 7, 80-88 (2012).
- Carpenter, A. E., et al. CellProfiler: image analysis software for identifying and quantifying cell phenotypes. Genome Biol. 7, R100 (2006).
- Kuru, E., Tekkam, S., Hall, E., Brun, Y. V., Van Nieuwenhze, M. S. Synthesis of fluorescent D-amino acids and their use for probing peptidoglycan synthesis and bacterial growth in situ. Nat. Protoc. 10, 33-52 (2015).
- Szafran, M., et al. Topoisomerase I (TopA) is recruited to ParB complexes and is required for proper chromosome organization during Streptomyces coelicolor. sporulation. J. Bacteriol. 195, 4445-4455 (2013).

