Syntesen av RGD-funksjon Hydrogeler som et verktøy for Therapeutic Applications
Summary
We present a protocol for the synthesis of RGD-functionalized hydrogels as devices for cell and drug delivery. The procedure involves copper catalyzed alkyne-azide cycloaddition (CuAAC) between alkyne-modified polyacrylic acid (PAA) and a RGD-azide derivative. The hydrogels are formed using microwave-assisted polycondensation and their physicochemical properties are investigated.
Abstract
The use of polymers as biomaterials has provided significant advantages in therapeutic applications. In particular, the possibility to modify and functionalize polymer chains with compounds that are able to improve biocompatibility, mechanical properties, or cell viability allows the design of novel materials to meet new challenges in the biomedical field. With the polymer functionalization strategies, click chemistry is a powerful tool to improve cell-compatibility and drug delivery properties of polymeric devices. Similarly, the fundamental need of biomedicine to use sterile tools to avoid potential adverse-side effects, such as toxicity or contamination of the biological environment, gives rise to increasing interest in the microwave-assisted strategy.
The combination of click chemistry and the microwave-assisted method is suitable to produce biocompatible hydrogels with desired functionalities and improved performances in biomedical applications. This work aims to synthesize RGD-functionalized hydrogels. RGD (arginylglycylaspartic acid) is a tripeptide that can mimic cell adhesion proteins and bind to cell-surface receptors, creating a hospitable microenvironment for cells within the 3D polymeric network of the hydrogels. RGD functionalization occurs through Huisgen 1,3-dipolar cycloaddition. Some PAA carboxyl groups are modified with an alkyne moiety, whereas RGD is functionalized with azido acid as the terminal residue of the peptide sequence. Finally, both products are used in a copper catalyzed click reaction to permanently link the peptide to PAA. This modified polymer is used with carbomer, agarose and polyethylene glycol (PEG) to synthesize a hydrogel matrix. The 3D structure is formed due to an esterification reaction involving carboxyl groups from PAA and carbomer and hydroxyl groups from agarose and PEG through microwave-assisted polycondensation. The efficiency of the gelation mechanism ensures a high degree of RGD functionalization. In addition, the procedure to load therapeutic compounds or biological tools within this functionalized network is very simple and reproducible.
Introduction
Hydrogelene er tre-dimensjonale nettverk dannet av hydrofile tverrbundne polymerer, som er naturlig eller syntetisk, og kjennetegnet ved en karakteristisk tredimensjonal struktur. Disse enhetene blir stadig mer attraktive i de biomedisinske innen levering av legemidler, tissue engineering, som bærer genet og smarte sensorer 1,2. Faktisk, deres høyt vanninnhold, samt deres reologiske og mekaniske egenskaper gjør dem egnede kandidater til å etterligne bløtvev microenvironments og gjøre dem effektive verktøy for vannløselig cytokin eller vekstfaktor levering. En av de mest lovende anvendelse er som et injiserbart biomateriale som bærer celler og bioaktive forbindelser. Hydrogeler kan forbedre celleoverlevelse og kontroll stamcelle skjebne ved å holde og nøyaktig levering av stamcelle-regulerende signaler i et fysiologisk relevant måte, som observert i in vitro og i in vivo-forsøk 3,4. Den ledende Fordelen med dette er mulighetenfor å opprettholde injiserte celler innenfor sonen for inokulering (in situ), noe som reduserer mengden av celler som forlater området og ekstravaserer i sirkulasjons-cast, migrerer over hele kroppen og mister målet mål 5. Stabiliteten til tredimensjonale hydrogel nettverk er på grunn av sin tverrbindende områder, dannet av kovalente bindinger eller sammenhengende krefter blant polymerkjedene 6.
I denne rammen, ortogonale selektiv kjemi anvendt på polymerkjedene er et allsidig verktøy i stand til å forbedre hydrogel forestillinger 7. Faktisk kan modifiseringen av polymerer med egnede kjemiske grupper bidra til å gi passende kjemiske, fysiske og mekaniske egenskaper for å forbedre cellenes levedyktighet og deres anvendelse i vev formasjon. På samme måte, blant teknikker for å laste celler eller vekstfaktorer innenfor den gel-matrise, bruk av RGD-peptidet tillater forbedringer i celleadhesjon og overlevelse. RGD er en tripeptide komponertav arginin, glysin og asparaginsyre, som er den desidert mest effektive og ofte ansatt tripeptid på grunn av sin evne til å ta mer enn én celle adhesjon reseptor og dens biologiske virkning på celle forankring, atferd og overlevelse 8,9. I dette arbeidet, er syntesen av RGD-funksjonalisert hydrogeler studert med det mål å utforme nettverk kjennetegnet ved tilstrekkelige biokjemiske egenskaper for et gjest celle mikromiljøet.
Bruken av mikrobølgestråling i hydrogelen syntese gir en enkel prosedyre for å minimalisere sidereaksjoner og oppnå høyere reaksjonshastigheter og utbytter i et kortere tidsrom sammenlignet med de konvensjonelle termiske prosesser 10. Denne metoden krever ikke at rensetrinn og utbytter sterile hydrogeler på grunn av interaksjoner av polymerene og fravær av organisk oppløsningsmiddel i reaksjonssystemet 11. Derfor sikrer den høye prosenter av RGD knyttet til polymernettverk fordi ingen modifications er nødvendig for å polymer kjemiske grupper som er involvert i geldannelse. Karboksylgrupper, fra PAA og karbomer, og hydroksylgrupper, fra PEG og agarose, gi opphav til den hydrogel tredimensjonale struktur gjennom en polykondensasjonsreaksjon. De nevnte polymerer som anvendes for syntesen av hydrogeler i ryggmargsskade reparasjons behandlinger 12. Disse anordninger, som rapportert i tidligere arbeider 13,14, viser høy biokompatibilitet, så vel som mekaniske og fysikalsk-kjemiske egenskaper som ligner de av mange levende vev og i tiksotropisk natur. Videre må de forbli lokalisert in situ, ved sonen av injeksjon.
I dette arbeidet, er PAA carboxylgrupper modifisert med et alkyn-del (figur 1), og en RGD-azid Forbindelsen blir syntetisert utnytte reaktiviteten av tripeptidet terminal gruppe -NH 2 med en forberedt kjemisk forbindelse med struktur (CH2) n – N 3 (<strong> Figur 2). Deretter reagerer det modifiserte PAA med den RGD-azidderivat gjennom CuAAC klikk reaksjon 15-17 (figur 3). Bruken av et kobber (I) katalysator fører til store forbedringer i både reaksjonshastigheten og regioselektivitet. Den CuAAC Reaksjonen blir mye brukt i organisk syntese, og i polymervitenskap. Den kombinerer høy effektivitet og høy toleranse overfor de funksjonelle grupper, og det er upåvirket ved bruk av organiske oppløsningsmidler. En høy selektivitet, en hurtig reaksjonstid og en enkel rensemetode tillate oppnåelse av stjerne-polymerer, blokk-kopolymerer eller kjettinger innpoding ønskede andeler 18. Dette klikket strategien gjør det mulig å modifisere polymerer som etter polymerisering for å tilpasse de fysiske og kjemiske egenskaper i henhold til den endelige biokjemiske søknad. De CuAAC forsøksbetingelser er lett reproduserbare (reaksjonen er ufølsom for vann, mens kobber oksydasjon kan forekomme minimal), og arten avdannet triazol sikrer stabiliteten av produktet. Bruken av kobbermetall kan betraktes som en kritisk punkt, på grunn av sin potensielt toksisk virkning mot celler og i den biologiske mikromiljøet, men dialyse anvendes som en rensemetode for å tillate fullstendig fjerning av katalytiske rester. Til slutt, PAA modifisert RGD anvendes i hydrogel-syntese (Figur 4), og de fysikalsk-kjemiske egenskapene til de resulterende nettverk er undersøkt, for å kontrollere potensialet funksjonaliteten av disse systemene som celler eller medikamenter bærere.
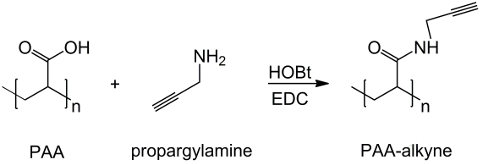
Figur 1: PAA endret alkyn syntese En ordning med PAA funksjon med alkyn gruppe;. "n" indikerer monomerer med karboksylgruppen reagerer med propargylamin. Klikk her for å seen større versjon av dette tallet.
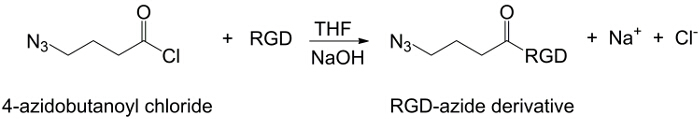
Figur 2:.. RGD-azid syntese Syntesen av RGD-azidderivat Klikk her for å se en større versjon av dette tallet.
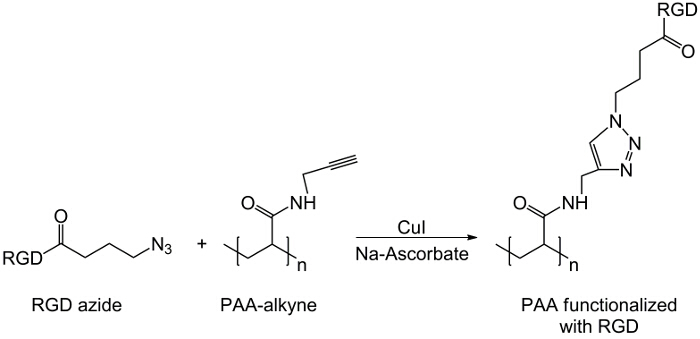
Figur 3: Klikk reaksjon Scheme av klikk reaksjon mellom RGD-azidderivat og alkyn-PAA.. Klikk her for å se en større versjon av dette tallet.
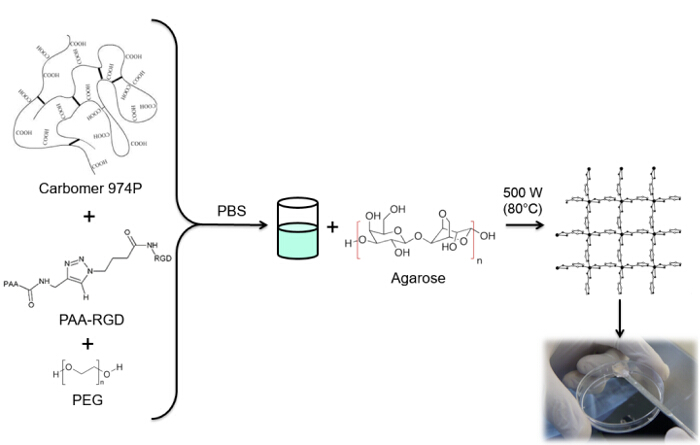
Figur 4: Hydrogel synthesis. RGD funksjon hydrogel syntese prosedyre. Klikk her for å se en større versjon av dette tallet.
Protocol
Representative Results
Discussion
The PAA post-polymerization modification with alkyne moieties and the RGD functionalization with the azide group guarantee the formation of a stable bond between the polymer and the peptide. Indeed, triazole serves as a rigid linking unit among the carbon atoms, attached to the 1,4 positions of the 1,2,3-triazole ring and it cannot be cleaved hydrolytically or otherwise. In addition, triazole is extremely difficult to oxidize and reduce, unlike other cyclic structures such as benzenoids and related aromatic heterocycles<…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne ønsker å takke Prof. Maurizio Masi for fruktbar diskusjon og Miss Chiara Allegretti for språk redigering. Forfatter forskning er støttet av Bando Giovani Ricercatori 2010 (Minis della Salute GR-2010- 2312573).
Materials
| Poly(acrylic acid) solution average Mw ~ 100,000, 35 wt % in H2O | Sigma Aldrich | 523925 | CAS 9003-01-4 |
| Poly(ethylene glycol) 2,000 | Sigma Aldrich | 84797 | CAS 25322-68-3 |
| Carbomeer 974P | Fagron | 1387083 | |
| Agarose | Invitrogen Corp. | 16500-500 | UltraPure Agarose |
| RGD peptide | abcam | ab142698 | |
| 4-azidobutanoic acid | Aurum Pharmatech | Z-2421 | CAS 54447-68-6 |
| Oxalyl chloride | Sigma Aldrich | O8801 | CAS 79-37-8 |
| Propargylamine hydrochloride 95% | Sigma Aldrich | P50919 | CAS 15430-52-1 |
| Copper(I) iodide | Sigma Aldrich | 3140 | CAS 7681-65-4 |
| Sodium ascorbate | Sigma Aldrich | Y0000039 | CAS 134-03-2 |
| Phosphate buffered saline | Sigma Aldrich | P4417 | |
| Dialysis Membrane | Spectrum Laboratories, Inc. | 132725 | Spectra/Por 3 Dialysis Membrane Standard RC Tubing MWCO: 3,5 kD |
References
- Slaughter, B. V., Khurshid, S. S., Fisher, O. Z., Khademhosseini, A., Peppas, N. A. Hydrogels in Regenerative Medicine. Adv. Mater. 21 (32-33), 3307-3329 (2009).
- Rossi, F., Perale, G., Papa, S., Forloni, G., Veglianese, P. Current options for drug delivery to the spinal cord. Expert Opin. Drug Deliv. 10 (3), 385-396 (2013).
- Huebsch, N., et al. Harnessing traction-mediated manipulation of the cell/matrix interface to control stem-cell fate. Nat. Mater. 9 (6), 518-526 (2010).
- Mothe, A. J., Tam, R. Y., Zahir, T., Tator, C. H., Shoichet, M. S. Repair of the injured spinal cord by transplantation of neural stem cells in a hyaluronan-based hydrogel. Biomaterials. 34 (15), 3775-3783 (2013).
- Khetan, S., et al. Degradation-mediated cellular traction directs stem cell fate in covalently crosslinked three-dimensional hydrogels. Nat. Mater. 12 (5), 458-465 (2013).
- Ashley, G. W., Henise, J., Reid, R., Santi, D. V. Hydrogel drug delivery system with predictable and tunable drug release and degradation rates. Proc. Natl. Acad. Sci. U S A. 110 (6), 2318-2323 (2013).
- Rossi, F., van Griensven, M. Polymer Functionalization as a Powerful Tool to Improve Scaffold Performances. Tissue Eng. Part A. 20 (15-16), 2043-2051 (2014).
- Gould, S. T., Darling, N. J., Anseth, K. S. Small peptide functionalized thiol-ene hydrogels as culture substrates for understanding valvular interstitial cell activation and de novo tissue deposition. Acta Biomater. 8 (9), 3201-3209 (2012).
- Azagarsamy, M. A., Anseth, K. S. Wavelength-Controlled Photocleavage for the Orthogonal and Sequential Release of Multiple Proteins. Angew. Chem. Int. Edit. 52 (51), 13803-13807 (2013).
- Larrañeta, E., et al. Microwave-Assisted Preparation of Hydrogel-Forming Microneedle Arrays for Transdermal Drug Delivery Applications. Macromol. Mater. Eng. 300 (6), 586-595 (2015).
- Cook, J. P., Goodall, G. W., Khutoryanskaya, O. V., Khutoryanskiy, V. V. Microwave-Assisted Hydrogel Synthesis: A New Method for Crosslinking Polymers in Aqueous Solutions. Macromol. Rapid Comm. 33 (4), 332-336 (2012).
- Perale, G., et al. Multiple drug delivery hydrogel system for spinal cord injury repair strategies. J. Control. Release. 159 (2), 271-280 (2012).
- Rossi, F., Perale, G., Storti, G., Masi, M. A Library of Tunable Agarose Carbomer-Based Hydrogels for Tissue Engineering Applications: The Role of Cross-Linkers. J. Appl. Polym. Sci. 123 (4), 2211-2221 (2012).
- Frith, J. E., et al. An injectable hydrogel incorporating mesenchymal precursor cells and pentosan polysulphate for intervertebral disc regeneration. Biomaterials. 34 (37), 9430-9440 (2013).
- Kolb, H. C., Finn, M. G., Sharpless, K. B. Click chemistry: Diverse chemical function from a few good reactions. Angew. Chem. Int. Edit. 40 (11), (2001).
- Sacchetti, A., Mauri, E., Sani, M., Masi, M., Rossi, F. Microwave-assisted synthesis and click chemistry as simple and efficient strategy for RGD functionalized hydrogels. Tetrahedron Lett. 55 (50), 6817-6820 (2014).
- Ossipov, D. A., Hilborn, J. Poly(vinyl alcohol)-based hydrogels formed by "click chemistry". Macromolecules. 39 (5), 1709-1718 (2006).
- Truong, V., Blakey, I., Whittaker, A. K. Hydrophilic and Amphiphilic Polyethylene Glycol-Based Hydrogels with Tunable Degradability Prepared by "Click" Chemistry. Biomacromolecules. 13 (12), 4012-4021 (2012).
- Hou, R. Z., et al. New synthetic route for RGD tripeptide. Prep. Biochem. Biotechnol. 36 (3), 243-252 (2006).
- Rossi, F., Chatzistavrou, X., Perale, G., Boccaccini, A. R. Synthesis and Degradation of Agar-Carbomer Based Hydrogels for Tissue Engineering Applications. J. Appl. Polym. Sci. 123 (1), 398-408 (2012).
- Mauri, E., Rossi, F., Sacchetti, A. Tunable drug delivery using chemoselective functionalization of hydrogels. Mater. Sci. Eng. C. 61, 851-857 (2016).
- Joaquin, A., Peppas, N. A., Zoldan, J. Hydrogel Polymer Library for Developing Induced Pluripotent Stem Cell Derived Cardiac Patches. Tissue Eng. Part A. 20, S55-S55 (2014).
- Rossi, F., et al. Tunable hydrogel-Nanoparticles release system for sustained combination therapies in the spinal cord. Colloids Surf. B Biointerfaces. 108, 169-177 (2013).
- Kolb, H. C., Sharpless, K. B. The growing impact of click chemistry on drug discovery. Drug Discov. Today. 8 (24), 1128-1137 (2003).
- Ossipov, D. A., Yang, X., Varghese, O., Kootala, S., Hilborn, J. Modular approach to functional hyaluronic acid hydrogels using orthogonal chemical reactions. Chem. Commun. 46 (44), 8368-8370 (2010).
- Anderson, S. B., Lin, C. C., Kuntzler, D. V., Anseth, K. S. The performance of human mesenchymal stem cells encapsulated in cell-degradable polymer-peptide hydrogels. Biomaterials. 32 (14), 3564-3574 (2011).
- Caron, I., et al. A new three dimensional biomimetic hydrogel to deliver factors secreted by human mesenchymal stem cells in spinal cord injury. Biomaterials. 75, 135-147 (2016).
- Lee, J. W., Kim, H., Lee, K. Y. Effect of spacer arm length between adhesion ligand and alginate hydrogel on stem cell differentiation. Carbohyd. Polym. 139, 82-89 (2016).
- Liu, Y., Fan, Z., Wang, Y., Yu, L. Controlled Release of Low Molecular Protein Insulin-like Growth Factor-1 through Self-Assembling Peptide Hydrogel with Biotin Sandwich Approach. J.Biomed. Eng. 32 (2), 387-392 (2015).

