Strukturell information från enda molekyl FRET Experiment Använda Fast Nano-positioneringssystem
Summary
We present the setup and experimental procedure to obtain smFRET data from large donor-acceptor networks with a TIRF microscope. The step-by-step analysis of these measurements with the Bayesian inference software Fast-NPS yields high-resolved structural information via the application of adapted dye models.
Abstract
Single-molecule Förster Resonance Energy Transfer (smFRET) can be used to obtain structural information on biomolecular complexes in real-time. Thereby, multiple smFRET measurements are used to localize an unknown dye position inside a protein complex by means of trilateration. In order to obtain quantitative information, the Nano-Positioning System (NPS) uses probabilistic data analysis to combine structural information from X-ray crystallography with single-molecule fluorescence data to calculate not only the most probable position but the complete three-dimensional probability distribution, termed posterior, which indicates the experimental uncertainty. The concept was generalized for the analysis of smFRET networks containing numerous dye molecules. The latest version of NPS, Fast-NPS, features a new algorithm using Bayesian parameter estimation based on Markov Chain Monte Carlo sampling and parallel tempering that allows for the analysis of large smFRET networks in a comparably short time. Moreover, Fast-NPS allows the calculation of the posterior by choosing one of five different models for each dye, that account for the different spatial and orientational behavior exhibited by the dye molecules due to their local environment.
Here we present a detailed protocol for obtaining smFRET data and applying the Fast-NPS. We provide detailed instructions for the acquisition of the three input parameters of Fast-NPS: the smFRET values, as well as the quantum yield and anisotropy of the dye molecules. Recently, the NPS has been used to elucidate the architecture of an archaeal open promotor complex. This data is used to demonstrate the influence of the five different dye models on the posterior distribution.
Introduction
Bestämma strukturen för en biomolekyl är en viktig förutsättning för att förstå dess funktion. Två väletablerade metoder för strukturbestämning är Cryo-elektronmikroskopi och röntgenkristallografi 1, 2. Idag, båda metoderna ger hög upplösning strukturinformation med en upplösning ner till Ångström nivå. Dessa två metoder har använts i stor utsträckning för att klarlägga strukturen av stora biomolekyler, såsom proteinkomplex. Även de befintliga metoderna har ständigt förbättrats under de senaste decennierna, utgör komplexiteten i biologiska strukturer fortfarande en stor utmaning för strukturbiologi, i synnerhet när stora, dynamiska och transienta komplex undersöks tre.
För att studera dynamiken i makromolekylära komplex och struktur-funktionsförhållandet i synnerhet enda molekyl metodologier har provIDed användbar information 4. Flera nya strategier utvecklades ger en ortogonal strategi för att förvärva strukturell och dynamisk information. Exempel är höghastighets AFM 5, mekanisk manipulering 6, fluorescenslokalisering mikroskopi 7, såväl som enda molekyl Förster Resonance Energy Transfer (smFRET) 8, 9. Sedan ganska tidigt FRET har benämnts en molekylär linjal, på grund av avståndet beroende av längdskalan av biomakromolekyler 10.
En särskilt intressant tillämpning av smFRET är att använda avståndsinformationen som erhålls från smFRET mätningar för att härleda strukturell information 11, 12, 13, 14, 15 </sup>, 16, 17, 18, 19, 20, 21, 22, 23. Grund av den höga tidsupplösningen smFRET kan läget av mobila delar av en proteinstruktur vara lokaliserad. Men för att utvinna kvantitativ information från smFRET uppgifter viktiga korrigeringsparametrar om färgmolekyler måste bestämmas under mätningen 24. Med dessa korrigeringsfaktorer, kan FRET effektiviteten E FRET beräknas med hjälp av formeln
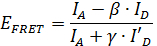 ,
,
där jag A och jag D </sub> är fluorescensintensiteter av givaren och acceptormolekylen, respektive (se figur 2). Den β-faktorn står för överhörning, läckage av emissions donator in i acceptom kanalen och beräknas genom att
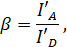
där jag A och jag skulle är fluorescensintensiteter av givaren och acceptormolekylen efter fotoblekning av acceptormolekylen.
Den γ-faktorn korrigerar skillnaden i de relativa effektivitet upptäckt i de två kanalerna samt skillnader i fluorescenskvantutbytet för givaren och acceptor-färgämne. Den beräknas från varje individ tidskurva efter
<p class="jove_content" fo:keep-together.within-page="1" fo:text-align="center" sTyle = "text-align: center;">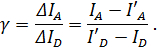
Notera, att denna beskrivning försummar direkt excitation av acceptormolekylen, som ibland blir viktigt och skulle behöva korrigeras för också. För att bestämma dessa korrektionsfaktorer är det lämpligt att excitera både givaren och acceptorn i en omväxlande ordning 25 för att skilja mellan foto fysiska förändringar och strukturdynamik.
För att inte bara få kvantitativa smFRET effektivitet men även kvantitativ strukturell information, var Nano-Positioning System (NPS) infördes 2008 26. Namnet valdes på grundval av sina likheter med det satellitbaserade Global Positioning System (GPS). NPS är en hybrid teknik som kombinerar smFRET och röntgenkristallografi data för lokalisering av okända färgämnes positioner i biomacromolecular komplex. crystal struktur tjänar som referensramen och de smFRET resultaten används för att erhålla avståndsinformation mellan en okänd fluorofor position (antenn) och ett läge känt från kristallstrukturen (satellit). I rad experiment avstånden mellan antennen och flera satelliter mäts och positionen för antennen bestäms med hjälp av en statistiskt noggrann analys system baserat på Bayesian parameteruppskattning. Som ett resultat, är inte bara den mest sann positionen av antennen beräknas, men dess fullständiga 3D osäkerhet fördelning, den så kallade bakre, visualiserades genom trovärdiga volymer. Dessutom var NPS utvidgas för att möjliggöra analys av kompletta smFRET nätverk 27.
NPS har använts för att lösa ett antal viktiga frågor i eukaryot transkription, nämligen loppet av den uppströms belägna DNA: t, den icke-mall-DNA och den begynnande mRNA inom töjning co RNA-polymeras IImplex 12, 28, även visar effekten av transkriptionsinitiering faktorer 26 och den dynamiska arkitektur av en öppen-promotor komplex 29. Dessutom var NPS används för att belysa strukturen hos archaeal RNA-polymeras öppen komplex 30 och i synnerhet läget för transkriptionsinitiering faktor TFE, som konkurrenskraftigt binder till samma plats som transkriptionsförlängningsfaktor Spt4 / 5 31.
Sedan dess har ett antal smFRET baserade strukturella metoder publicerats 15, 18, 21, 23. När man jämför olika smFRET baserade strukturella metoder, blir det tydligt att den uppenbara precisionen av metoden är mycket beroende av det särskilda valet av färgämnesmodeller. Man bör notera attfärgmolekyler kan uppvisa olika rumsliga och orienterings beteende beroende på deras närmiljö.
För detta ändamål var snabb-NPS infördes 32. Snabb NPS använder en avancerad provtagning algoritm minska beräkningstider drastiskt. Dessutom tillåter snabb-NPS en att utföra en strukturell analys och för varje färgämne molekyl kan användaren välja från en uppsättning av fem olika färgmodeller som kommer att beskrivas härnäst. Den mest konservativa modellen kallas klassisk, förutsätter att färgämnet endast upptar en, men okänd, läge. Vid denna position, kan fluoroforen rotera fritt inom en kon, vars storlek bestäms från dess respektive (tidsberoende) fluorescensanisotropi. Orienteringen av könen är inte känt, vilket leder till stora osäkerheter vid konvertering uppmätta smFRET effektivitet i avstånd. I detta avseende är konservativa modellen, eftersom det kommer att leda till den minsta precision jämfört med den andra färgämneslägels. Endast för mycket korta sträckor bör de antaganden som gjorts av den klassiska modellen leder till en märkbart felaktig positionsbestämningen. För typiska smFRET värden, är den korrekta positionen alltid inneslutna i den jämförelsevis stora trovärdig volym.
Eftersom en högre precision är önskvärd, är det viktigt att utveckla och testa alternativa färgmodeller, vilket kan bidra till att förbättra precisionen. Om färgämnet roterar mycket snabbare än dess inneboende fluorescenslivstid, kan den så kallade ISO-modellen tillämpas. Här, orienteringsfaktorn K 2 (som behövs för att beräkna den karakteristiska isotropiska Förster radie 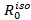 ) Är inställd på 2/3. Som ett resultat, de beräknade trovärdiga volymerna är nästan två storleksordningar mindre jämfört med dem i den klassiska modellen 32. I det fall att fluoroforen förekommer i en miljö som gör det möjligt inte bara snabbt reorisentation, men dessutom fast motion hela dess tillgängliga volym bör meanpos-iso modell användas. I denna modell, färgämnet effektivt upptar bara en genomsnittlig läge, där den spatiala medelvärdes utgörs av ett polynom avstånd omvandling 15. Denna modell gäller om till exempel den (allmänt hydrofoba) färgämne är fäst vid ett hydrofilt område, t.ex., DNA: t. Tillämpning av meanpos-ISO-modellen leder till en ytterligare reduktion av storleken av de trovärdiga volymerna med en faktor av cirka två. Däremot kan ett färgämne kopplad till ett protein binder reversibelt till flera hydrofoba fläckar i dess steriskt tillgängliga volymen (AV). En fluorofor som omedelbart växlar mellan dessa områden, men inom en region genomgår fri rotation och snabb lokal rörelse beskrivs bäst av VAR-meanpos-ISO-modellen. För en liknande situation i vilken färgämnet är inte fri att rotera VAR-meanpos modell tillämpas. mer d etails om dessa modeller kan hittas i vår senaste publikation 32.
) Är inställd på 2/3. Som ett resultat, de beräknade trovärdiga volymerna är nästan två storleksordningar mindre jämfört med dem i den klassiska modellen 32. I det fall att fluoroforen förekommer i en miljö som gör det möjligt inte bara snabbt reorisentation, men dessutom fast motion hela dess tillgängliga volym bör meanpos-iso modell användas. I denna modell, färgämnet effektivt upptar bara en genomsnittlig läge, där den spatiala medelvärdes utgörs av ett polynom avstånd omvandling 15. Denna modell gäller om till exempel den (allmänt hydrofoba) färgämne är fäst vid ett hydrofilt område, t.ex., DNA: t. Tillämpning av meanpos-ISO-modellen leder till en ytterligare reduktion av storleken av de trovärdiga volymerna med en faktor av cirka två. Däremot kan ett färgämne kopplad till ett protein binder reversibelt till flera hydrofoba fläckar i dess steriskt tillgängliga volymen (AV). En fluorofor som omedelbart växlar mellan dessa områden, men inom en region genomgår fri rotation och snabb lokal rörelse beskrivs bäst av VAR-meanpos-ISO-modellen. För en liknande situation i vilken färgämnet är inte fri att rotera VAR-meanpos modell tillämpas. mer d etails om dessa modeller kan hittas i vår senaste publikation 32.
Dessa modeller ger en omfattande repertoar att specifikt redogöra för de olika miljöerna ett färgämne som kan uppstå och tillämpa dem på ett klokt sätt optimerar dess lokalisering precision. I Snabb-NPS varje färgämnesmolekyl fäst till en specifik position kan tilldelas en enskild modell, så att FRET-partner får ha olika modeller. Detta möjliggör obegränsad och nära till naturen modellering. Det är dock viktigt att man utför rigorösa statistiska tester för att säkerställa att det uppnådda resultatet av den slutliga modellen kombinationen är fortfarande i överensstämmelse med de experimentella data. Dessa tester ingår i Fast-NPS programvara.
För att tillämpa Snabb NPS till experimentella data krävs mätning av (endast) tre inparametrar. För det första färg par specifika isotropisk Förster radier (/54782/54782eq5.jpg "/>) Har inte fastställts. Därför kvantumutbytet (QY) för donator-färgämnet, donatorfluorescensemissionsspektra och acceptorn absorptionsspektra behöver mätas. Kan Dessa mätningar utföras i bulk, med användning av en standard-spektrometer och en standardfluorescensspektrometer. för varje par, är R 0 sedan beräknas med hjälp av freeware PhotochemCAD och kan användas i NPS-analys. Dessutom är de (tidsupplöst) fluorescens anisotropier av färgämnesmolekylerna behöver erhållas med hjälp av en polarisering (och tid) känslig fluorescensspektrometer. Men de viktigaste ingångsparametrar för snabb-NPS är smFRET effektivitet mäts på en enda molekyl fluorescensmikroskopi installation, såsom en total inre reflektion fluorescensmikroskop (TIRFM) .
Här presenterar vi en steg-för-steg-protokoll för att erhålla smFRET uppgifter och tillämpa Snabb NPS (Figur 1).
Protocol
Representative Results
Discussion
Vi presenterar installationen och experimentell procedur för att exakt bestämma FRET effektivitet mellan färgämnen fästa via flexibla linkers till biomakromolekyler, det vill säga, nukleinsyror och / eller proteiner.
För att säkerställa exakta smFRET mätningar (avsnitt 3), är det viktigt att utesluta luft från flödet kammaren när som helst under mätningen. Dessutom, se till att inte överbelasta flödet kammaren med fluoroforer. Fluoroforema måste vara klart åtskilda för att säkerställa korrekt analys. Som smFRET par, som inte uppvisar blekning av givaren måste uteslutas från analysen, se till att> 80% av molekylerna i synfältet bleks i slutet av filmen. Att ta hänsyn till inhomogeniteter i provet den β-faktorn och γ-faktorn, korrigera de överhörn och relativa detektions effektiviteter av givaren och acceptorn kanal, respektive, beräknas för varje FRET para ihop individuellt.
<p class= "Jove_content"> De kamerainställningar (integration tid, elektron multiplikator vinst, förstärkningsförförstärkare och avläsning ränta som beskrivs i avsnitt 3.9) bör ställas in på värden som ger den bästa kompromissen mellan signal-brusförhållande, dynamiskt omfång och tidsupplösning. De måste återjusteras för olika experiment eller om olika hårdvara används. Antalet ramar måste vara tillräckligt hög för att säkerställa att det mesta av donatormolekyler blekmedel inom observationstiden.För mätningarna på fluorescensspektrometer (§§ 7 till 9) en bra kompromiss mellan signalstyrkan och den spektrala upplösning av de registrerade uppgifterna måste hittas. För detta ändamål de slitsar i excitations- och emissionsvägen för den fluorescensspektrometer måste anpassas beroende av det instrument som används och provkoncentrationen.
Dessutom presenterar vi Fast-NPS analysmetod för att erhålla strukturell information övergående eller dynamisk MACROMolecular komplex. NPS har tillämpats för att avslöja banan för den icke-templat-DNA-strängen och positionen för transkriptions initieringsfaktorer i archaeal RNA-polymeras öppen komplex. Använda nätverk av mer än 60 olika avståndsmätningar, visade vi att Snabb NPS, utrustad med en nyligen genomfört provtagning motor (Eilert, T., Beckers, M., Drechsler, F., & Michaelis, J. under utarbetande), minskar den tid som behövs för analys av denna komplexa smFRET nätverk genom ≈2 tiopotenser, jämfört med den ursprungliga globala NPS metod 27. Algoritmen robusthet har sina rötter i en sampler Metropolis-i-Gibbs kombination med en parallell anlöp system. Snabb NPS visar exakt reproducerbarhet av nätverksresultat och är i linje med resultat publicerade tidigare 30.
Flera olika metoder har publicerats i syfte att härleda strukturell information från smFRET mätningar 11 </supp>, 12, 13, 14, 15, 16, 17, 18. Alla dessa metoder ger endast en viss färg modell. Således, färgämnen, som inte uppfyller de antaganden som gjorts av respektive modell kan inte användas eller leda till felaktiga strukturell information. Snabb NPS, tvärtom, gör det möjligt att välja för varje färgämne molekyl en annan modell. Detta bidrar till att redogöra för olika konformationsbeteende av båda, färgämnesmolekylen i sig, liksom den linker som används vid fastsättningen. De lokala molekylära omgivningarna färgämnesmolekylen, liksom dess fysikaliska egenskaper kommer att avgöra vilken modell som är mest lämpligt.
För det analyserade smFRET nätverk av archaeal inledande komplexa, en isotrop antagande för alla färgmolekyler leder till en drastisk minskning in storleken på de trovärdiga volymer jämfört med den klassiska modellen. I kombination med en dynamisk ställning i genomsnitt för alla färgmolekyler medianen av alla trovärdiga volymstorlekar (95%) minskar till mindre än 0,5 nm 3. Emellertid dessa färgämnesmolekyl posteriors inte längre överensstämmer med deras smFRET mätningar, vilket indikerar att de antaganden görs leda till falska strukturell information. I motsats därtill posteriors bestämda i den klassiska modellen är i överensstämmelse med de bestämda smFRET effektiviteter.
Eftersom antagandet av isotropiska och / eller dynamisk ställning i genomsnitt för alla färgämnen leda till inkonsekvenser, Snabb NPS kan färgämnesmolekylen priors där varje färgämne kan tilldelas en av de fem modeller. Varje modell använder samma tillgängliga volymen. Algoritmen för beräkning av de färgämnes AVs görs flera antaganden. Först är fluoroforen rumsliga form approximeras med en sfär. Således, en diameter med hänsyn tagen till fluoroforen s width, höjd och tjocklek ska användas (12 §). Vidare är linkern s formen approximeras med en böjlig stav. De värden som presenteras i avsnitt 12 beräknades för färgämnet Alexa 647 fäst via en 12-C-länk. Hittills är det inte möjligt att noggrant bestämma a priori vilken modell som är mest lämpad, med tanke på en experimentell geometri, och därmed alla modeller bör testas. I allmänhet kommer man välja den modell som ger minsta möjliga bakre storlek, medan det fortfarande är i överensstämmelse med data. För att testa om ett urval av modeller är förenlig med smFRET uppgifter beräknar vi både den bakre och sannolikheten. Konsekvens innebär att mer än 90% av de prover som tagits från den bakre ligger inom 95% konfidensintervall av sannolikhet.
Även om det är sant att ju lägre anisotropi, desto mindre avstånd osäkerheten i en smFRET nätverk geometriska arrangemang av färgmolekyler måste också beaktas. Således, medan representing färgmolekyler med låg fluorescens anisotropi med en ISO-modellen är en typisk första val, ger konsekvens testet en mer direkt sätt för att välja rätt färgmodellen. Det optimala valet av färgämnes modeller kan leda till en drastisk ökning av lokaliserings precision och samtidigt behålla nätverkets samstämmighet med FRET data.
Sammanfattningsvis möjliggör snabb-NPS att få strukturell och dynamisk information av stora makromolekylära komplex. I motsats till gemensamma strukturella metoder såsom röntgenkristallografi eller cryo elektronmikroskopi detta medger övervakning mycket flexibla eller transienta komplex, vilket avsevärt bredda vår mekanistisk förståelse av komplexa biologiska processer.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors thank B. Gruchmann for the mechanical drawings of the flow chamber. Further, we want to express our gratitude to Max Beckers and Florian Drechsler for insightful comments and discussions regarding NPS and the underlying sampling engine.
Materials
| Flowchamber preparation | |||
| Customized metall sample holder | self-built | n/a | |
| quartz-glass slides, 76 x 26 mm | Technical Glass Products | 26007 | |
| coverslips, 60 x 24 mm | Marienfeld | 101242 | |
| detergent, Hellmanex II | Hellma | 320.001 | |
| ultra-pure water from Synergy UV | Millipore | 2512600 | |
| Zepto plasma cleaner | Diener | n/a | |
| (3-aminopropyl)-triethoxysilane, p.a. | Sigma-Aldrich | A3648 | |
| methoxy PEG-succinimidyl valerate, 5 kDa | Laysan Bio Inc. | MPEG-SVA-5000-1g | |
| biotinylated PEG-succinimidyl valerate, 5 kDa | Laysan Bio Inc. | BIOTIN-PEG-SVA-5000 | |
| Sodium biocarbonate | Sigma-Aldrich | S5761 Sigma | |
| Sodium carbonate | Sigma-Aldrich | S2127 Sigma-Aldrich | |
| sealing film (Nescofilm) | Fisher Scientific | 12981805 | |
| Tygon Flexible Silicone Tubing, 0.8 mm ID, 2.4 mm OD | Saint-Gobain Performance Plastics | 720958 | |
| Fine-Bore Polyethylene Tubing, 0.58 mm ID, 0.96 mm OD (Smiths Medical) | Fisher Scientific | 12665497 | |
| Neutravidin | Life Technologies | A2666 | |
| Name | Company | Catalog Number | Comments |
| Total internal reflection fluorescence microscope | |||
| Nd:YAG Laser, 532 nm | Newport Spectra-Physics | EXLSR-532-100-CDRH | |
| diode-pumped solid-state laser, 491 nm, Calypso | Cobolt | 904010050 | |
| diode laser 643 nm, iBeam smart | Toptica | iBEAM-SMART-640-S | |
| dichroic mirror, 532 RDC | Chroma | F33-540 | |
| dichroic mirror, 476 RDC | Chroma | F33-476z | |
| acousto-optic tunable filter | AA Opto-Electronic | AOTFnC-VIS | |
| plano-convex cylindrical lens, f = 75 mm | Thorlabs | LJ1703L1-A | |
| plano-concave cylindrical, f = -300 mm | Thorlabs | ||
| prism, PS 991 | Thorlabs | PS991 | |
| focussing lens, f = 75 mm | Thorlabs | LA1608-B | |
| syringe pump, PHD 2000 | Harvard Apparatus | 70-2002 | |
| 2 stepper motors, Z812B | Thorlabs | Z812B | |
| piezoelectric actuator, PE4 | Thorlabs | PE4 | |
| IR diode laser | Edmund Optics | CPS808 | part of the autofocus system |
| dichroic mirror, 775 DCXR | Chroma | 775 DCXR | |
| position-sensing detector (PSD), PDP90A | Thorlabs | PDP90A | part of the autofocus system |
| water-immersion objective, Plan Apo 60X WI, NA 1.2 | Nikon | MRD07601 | |
| dichroic mirror, 645 DCXR | Chroma | 645 DCXR | part of the emission pathway |
| emission filter, 3RD550-510 | Omega Optical | 3RD550-510 | green channel in the emission pathway |
| emission filter, 3RD660-760 | Omega Optical | 3RD660-760 | red channel in the emission pathway |
| EMCCD camera, iXon+ DU897EBV | Andor | AND-20-00032 | |
| EMCCD camera, iXon3 DU897D-BV | Andor | AND-20-000141 | |
| Name | Company | Catalog Number | Comments |
| Miscellaneous | |||
| Varian 50 | Cary | UV-VIS spectrometer | |
| Fluorolog2 | SPEX | fluorescence spectrometer | |
| Solis (V4.15) | Andor | control software for the EM-CCD camera | |
| Apt user utility (V1.022) | Thorlabs | control software for the piezo-motors | |
| Norland Optical Adhesive 68 | Thorlabs | adhesive | |
| PC-AFN-0.8 Nile red | Kisker Biotech | avidin-coated fluorescent multispec beads | |
| Matlab | Mathworks | technical computing language for custon written software | |
| Origin (V9.0) | Originlab | scientific graphing and data analysis software | |
| Hellma 105-202-15-40 | Hellma | 105-202-15-40 | absorption cuvette of 1 cm path length |
| Hellma 105-251-15-40 | Hellma | 105-251-15-40 | fluorescence cuvette with 3 mm path length |
References
- Cheng, Y. Single-Particle Cryo-EM at Crystallographic Resolution. Cell. 161, 450-457 (2015).
- Garman, E. F. Developments in X-ray Crystallographic Structure Determination of Biological Macromolecules. Science. 343 (6175), 1102-1108 (2014).
- Sali, A. Outcome of the First wwPDB Hybrid/Integrative Methods Task Force Workshop. Structure. 23, 1156-1167 (2015).
- Hopfner, K. P., Michaelis, J. Mechanisms of nucleic acid translocases: lessons from structural biology and single-molecule biophysics. Curr Opin Struct Biol. 17, 87-95 (2007).
- Ando, T., Uchihashi, T., Kodera, N. High-speed AFM and applications to biomolecular systems. Annu Rev Biophys. 42, 393-414 (2013).
- Neuman, K. K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nat Methods. 5, 491-505 (2008).
- Yildiz, A. Myosin V walks hand-over-hand: single fluorophore imaging with 1.5-nm localization. Science. 300 (5628), 2061-2065 (2003).
- Joo, C., Balci, H., Ishitsuka, Y., Buranachai, C., Ha, T. Advances in Single-Molecule Fluorescence Methods for Molecular Biology. Annu Rev Biochem. 77 (1), 51-76 (2008).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chem Soc Rev. 43 (4), 1156-1171 (2014).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proc Natl Acad Sci U S A. 58 (2), 719-726 (1967).
- Rasnik, I., Myong, S., Cheng, W., Lohman, T. M., Ha, T. DNA-binding Orientation and Domain Conformation of the E. coli Rep Helicase Monomer Bound to a Partial Duplex Junction: Single-molecule Studies of Fluorescently Labeled Enzymes. J Mol Biol. 336 (2), 395-408 (2004).
- Andrecka, J. Single-molecule tracking of mRNA exiting from RNA polymerase II. Proc Natl Acad Sci U S A. 105 (1), 135-140 (2008).
- Schröder, G. F., Grubmüller, H. FRETsg: Biomolecular structure model building from multiple FRET experiments. Comput Phys Commun. 158 (3), 150-157 (2004).
- Margittai, M. Single-molecule fluorescence resonance energy transfer reveals a dynamic equilibrium between closed and open conformations of syntaxin 1. Proc Natl Acad Sci U S A. 100 (26), 15516-15521 (2003).
- Kalinin, S. A toolkit and benchmark study for FRET-restrained high-precision structural modeling. Nat Methods. 9 (12), 1218-1227 (2012).
- Choi, J. N6-methyladenosine in mRNA disrupts tRNA selection and translation-elongation dynamics. Nat Struct Mol Biol. 23 (August 2015), 110-115 (2015).
- Svensson, B. FRET-based trilateration of probes bound within functional ryanodine receptors. Biophys J. 107 (9), 2037-2048 (2014).
- Stephenson, J. D., Kenyon, J. C., Symmons, M. F., Lever, A. M. L. Characterizing 3D RNA structure by single molecule FRET. Methods. (2016), 1-11 (2016).
- Lee, N. K. Accurate FRET measurements within single diffusing biomolecules using alternating-laser excitation. Biophys J. 88 (4), 2939-2953 (2005).
- McCann, J. J., Choi, U. B., Zheng, L., Weninger, K., Bowen, M. E. Optimizing methods to recover absolute FRET efficiency from immobilized single molecules. Biophys J. 99 (3), 961-970 (2010).
- Brunger, A. T., Strop, P., Vrljic, M., Chu, S., Weninger, K. R. Three-dimensional molecular modeling with single molecule FRET. J Struct Biol. 173, 497-505 (2011).
- Schuler, B. Single-molecule FRET of protein structure and dynamics – a primer. J nanoboitechnology. 11, 1-17 (2013).
- Choi, U. B. Single-molecule FRET-derived model of the synaptotagmin 1-SNARE fusion complex. Nat Struct Mol Biol. 17 (3), 318-324 (2010).
- Dale, R. E., Eisinger, J., Blumberg, W. E. The orientational freedom of molecular probes. The orientation factor in intramolecular energy transfer. Biophys J. 26 (2), 161-193 (1979).
- Kapanidis, A. N. Alternating-laser excitation of single molecules. Acc Chem Res. 38 (7), 523-533 (2005).
- Muschielok, A. A nano-positioning system for macromolecular structural analysis. Nat Methods. 5 (11), 965-971 (2008).
- Muschielok, A., Michaelis, J. Application of the nano-positioning system to the analysis of fluorescence resonance energy transfer networks. J Phys Chem B. 115 (41), 11927-11937 (2011).
- Andrecka, J. Nano positioning system reveals the course of upstream and nontemplate DNA within the RNA polymerase ii elongation complex. Nucleic Acids Res. 37 (17), 5803-5809 (2009).
- Treutlein, B. Dynamic Architecture of a Minimal RNA Polymerase II Open Promoter Complex. Mol Cell. 46 (2), 136-146 (2012).
- Nagy, J. Complete architecture of the archaeal RNA polymerase open complex from single-molecule. FRET and NPS. Nat Commun. 6, 6161 (2015).
- Grohmann, D., et al. The Initiation Factor TFE and the Elongation Factor Spt4/5 Compete for the RNAP Clamp during Transcription Initiation and Elongation. Mol Cell. 43 (2), 263-274 (2011).
- Beckers, M., Drechsler, F., Eilert, T., Nagy, J., Michaelis, J. Quantitative structural information from single-molecule FRET. Faraday Discuss. 184, 117-129 (2015).
- Bennink, M. L. Unfolding individual nucleosomes by stretching single chromatin fibers with optical tweezers. Nat Struct Biol. 8 (7), 606-610 (2001).
- Chandradoss, S. D. Surface passivation for single-molecule protein studies. J Vis Exp. (86), e50549 (2014).
- Würth, C., Grabolle, M., Pauli, J., Spieles, M., Resch-Genger, U. Relative and absolute determination of fluorescence quantum yields of transparent samples. Nat Protoc. 8 (8), 1535-1550 (2013).
- Lakowicz, J. R. . Principles of Fluorescence Spectroscopy. , (2006).
- Korkhin, Y. Evolution of complex RNA polymerases: The complete archaeal RNA polymerase structure. PLoS Biol. 7 (5), (2009).

