En generell metode for påvisning av Nitrosamide formasjon i In Vitro metabolismen av nitrosaminer av Cytochrome P450s
Summary
Α-hydroksylering av kreftfremkallende nitrosaminer ved cytochrome P450s er akseptert metabolske veien som produserer DNA-skade mellomprodukter, som føre til mutasjoner. Imidlertid viser nye data ytterligere oksidasjon til nitrosamides kan oppstå. Vi beskriver en generell metode for påvisning av nitrosamides produsert i vitro cytochrome P450-katalysert metabolismen av nitrosaminer.
Abstract
N-nitrosaminer er en veletablert gruppe av miljømessige kreftfremkallende, som krever cytochrome P450 oksidasjon viser aktivitet. Den aksepterte mekanismen av metabolske aktivering innebærer dannelsen av α-hydroxynitrosamines som spontant bryte ned til DNA alkylating agenter. Akkumulering av DNA skade og den resulterende mutasjoner kan til slutt føre til kreft. Nye bevis indikerer at α-hydroxynitrosamines kan videre oksideres å nitrosamides processively av cytochrome P450s. Fordi nitrosamides er vanligvis mer stabile enn α-hydroxynitrosamines og kan også alkylate DNA, kan nitrosamides spille en rolle i kreft. I denne rapporten beskriver vi en generell protokoll for å vurdere nitrosamide produksjon fra i vitro cytochrome P450-katalysert metabolisme av nitrosaminer. Denne protokollen bruker en generell tilnærming til syntesen av den relevante nitrosamides og i vitro cytochrome P450 metabolisme analysen ved hjelp av flytende kromatografi-nanospray ionization høy oppløsning tandem massespektrometri for gjenkjenning. Denne metoden oppdaget N′– nitrosonorcotinine som en mindre metabolitt av N′– nitrosonornicotine i eksempel studien. Metoden har høy følsomhet og selektivt grunn til nøyaktig masse gjenkjenning. Bruk av denne metoden på en rekke nitrosamine-cytochrome P450 systemer vil avgjøre omfanget til denne transformasjonen. Fordi cytochrome P450s polymorfe og varierer i aktivitet, kan bedre forståelse av nitrosamide formasjon hjelpe individuelle kreft risikovurdering.
Introduction
N-nitrosaminer er en stor klasse av kreftfremkallende faktorer i kosten, tobakksprodukter og generelle miljøet. de kan også dannes endogenously i menneskekroppen1. Mer enn 300 N –nitroso forbindelser har blitt testet og > 90% ble vurdert som kreftfremkallende i dyr modeller2,3. Å stille ut sine kreftfremkallende, må disse forbindelsene først aktiveres ved cytochrome P450s1,2,3. Forskning viser at cytochrome P450s lett oksidere nitrosaminer til α-hydroxynitrosamines (figur 1), som er svært reaktive stoffer med halv-liv ~ 5 før spontant separasjon til alkyldiazohydroxides. Sistnevnte kan alkylate DNA etter tapet av H2O og N2. Den resulterende DNA-addukter, hvis unrepaired, kan føre til mutasjoner som, hvis du er i kritisk onco- eller tumor suppressor gener, føre til kreft utvikling1. Av denne grunn store anstrengelser er brukt for å få en full forståelse av metabolske veier, DNA-addukter, og nedstrøms metabolitter av cytochrome P450 oksidasjon av kreftfremkallende nitrosaminer. Denne kunnskapen har potensiell program i individuelle kreft risiko vurdering4.
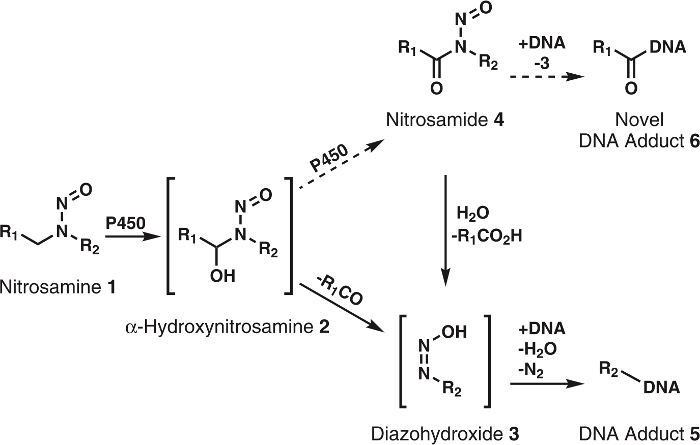
Figur 1: General og foreslåtte metabolismen av nitrosaminer.
Nitrosaminer (1) er oksidert av P450s til α-hydroxynitrosamines (2) som spontant bryte ned til alkyldiazohydroxides (3). Forbindelsene kan binde til DNA skjemaet DNA-addukter. Det er en teori om at 2 er ytterligere oksidert av P450s til nitrosamides 4. Dette kan direkte binde DNA til skjemaet romanen DNA-addukter eller være hydrolyzed 3 form kjent DNA-addukter. R1 og R2 representerer noen alkyl gruppe. Klikk her for å se en større versjon av dette tallet.
Selv om α-hydroxynitrosamine hypotesen er solid støttes av omfattende, er det noen inkonsekvenser; en stor en er den korte halveringstiden α-hydroxynitrosamines5,6. Det er kjent at disse forbindelsene er produsert på endoplasmatiske retikulum membranen og senere alkylate kjernefysiske DNA. Gitt livet av noen sekunder, er det rart hvordan disse mellomprodukter overleve ønsket reiser skjønt stoffer. En hypotese er at en del av α-hydroxynitrosamines er processively oksidert til nitrosamides7,8, som er ganske stabile i sammenligning9. Dette vil trolig skje via oppbevaring av α-hydroxynitrosamines i det cytochrome P450 aktive området. Presedens for denne typen oksidasjon har blitt sett med nikotin10, alkoholer11og enkel alkylnitrosamines12,13. Dessuten er nitrosamides direkte-fungerende kreftfremkallende2,3. Basert på deres reaktivitet9, antas disse forbindelsene å produsere DNA-addukter identisk med de som følge av α-hydroxynitrosamines sammen med nye, ukjente DNA-addukter (figur 1). Derfor denne hypotesen ikke bare forklarer transport gjennom stoffer, men også dannelsen av DNA skade produkter.
En generell protokoll for å vurdere i vitro cytochrome P450-mediert konvertering av nitrosaminer til nitrosamides er beskrevet i dette dokumentet. Tidligere rapportert konvertering av N′– nitrosonornicotine (NNN) til N′– nitrosonorcotinine (NNC) ved cytochrome P450 2A6 er vist som en eksempel14. Bruk av denne protokollen til en rekke substrat-enzym systemer vil avgjøre betydningen av nitrosamides i totale nitrosamine metabolisme.
Protocol
Representative Results
Discussion
Klargjørende metabolismen av nitrosaminer er en kritisk komponent å forstå deres kreftfremkallende. Siden den involvert cytochrome P450s og andre metabolsk enzymer polymorfe, kan ytterligere anvendelse av denne kunnskapen potensielt identifisere høy risiko individer1,4. Nye data indikerer at ytterligere oksidasjon av α-hydroxynitrosamines, de antatte store metabolitter av nitrosaminer involvert i DNA binding, nitrosamides er mulig; men er dette ikke robust t…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Denne studien ble støttet av grant ingen. CA-81301 fra National Cancer Institute. Vi takker Bob Carlson for redaksjonell bistand, Dr. Peter Villalta og Xun Ming massespektrometri hjelp i analytisk biokjemi delt ressurs av Masonic Cancer Center, og Dr. Adam T. Zarth og Dr. Anna K. Michel for deres verdifulle diskusjoner og innspill. Analytiske biokjemi delte ressursen er delvis støttet av National Cancer Institute Cancer Center støtte Grant CA-77598
Materials
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
References
- Rom, W. N., Markowitz, S. . Environmental and Occupational Medicine. , 1226-1239 (2007).
- Preussmann, R., Stewart, B. W., Searle, C. E. . Chemical Carcinogens, ACS Monograph 182. 2, 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R., Searle, C. E. . Chemical Carcinogens. ACS monograph 173. , 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. . ACS Symposium Series. 101, 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5′(1′)iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochemistry. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N’-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N’-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).

