Correlative lys elektronmikroskop (CLEM) for sporing og Imaging Viral Protein forbundet strukturer i Cryo-immobilisert celler
Summary
En correlative lys elektronmikroskop (CLEM) metode brukes bilde virus-indusert intracellulære strukturer via elektronmikroskop (EM) i cellene som er tidligere valgt av * lys (LM). LM og EM kombineres som en hybrid tenkelig tilnærming til å oppnå en integrert visning av virus-vert interaksjoner.
Abstract
På grunn av dens høy oppløsning er elektronmikroskop (EM) et uunnværlig verktøy for virologists. Men en av de største vanskelighetene når du analyserer virusinfiserte eller transfekterte celler via EM er lav effektiviteten av infeksjon eller hva, hindre undersøkelse av disse cellene. For å overkomme dette problemet, kan * lys (LM) utføres først for å tildele subpopulasjon av infisert eller transfekterte celler. Dermed dra nytte av fluorescerende proteiner (FPs) smeltet virale proteiner, LM brukes her til å registrere plasseringen av “positiv-transfekterte” cellene, uttrykke FP og vokser på en støtte med en alfanumerisk mønster. Deretter cellene behandles videre for EM høytrykk frysing (HPF), fryse substitusjon (AS) og harpiks innebygging. Det ultra rask frysing trinnet sikrer utmerket membran bevaring av de merkede cellene som kan deretter analyseres på ultrastructural nivå av overføring elektronmikroskop (TEM). Her, er en trinnvis correlative lys elektronmikroskop (CLEM) arbeidsflyt gitt, som beskriver eksempel forberedelse, bildebehandling og sammenheng i detalj. Eksperimentell design kan også brukes for å løse mange celle biologi spørsmål.
Introduction
Ideen om å kombinere to mikroskopi modaliteter å få et bedre bilde av en bestemt biologisk prosess er ganske gammel. Dermed ble den første studien om viruser benytter “correlative mikroskopi” utgitt i 1960 som to separate publikasjoner1,2. I denne studien analyserte forfatterne endringene i morfologi av kjernen indusert av adenoviruses ved hjelp av to mikroskopi teknikker. I den første utgivelsen var elektronmikroskop (EM) observasjoner som beskriver morfologiske detaljene knyttet adenovirus infeksjon rapportert1. I andre publikasjoner, var ulike strukturer observert av EM korrelert med * lys (LM) bilder av histochemical flekker mønstre, definere hva slags strukturer tidligere observert av EM2.
I disse tidlige studiene, men ble observasjonene utført med forskjellige infiserte celler forberedt som uavhengige eksperimenter. “Sammenheng” var faktisk ment som kombinasjonen av informasjon fra to tenkelig modaliteter å forstå en viss fenomen, sammenligne alle resultatene som er anskaffet med ulike analyser for å forstå en gitt biologisk prosessen.
I dag brukes begrepet correlative mikroskopi, også kjent som correlative lys og elektronmikroskop (CLEM), på et økende antall metoder (omtalt i referanser3,4,5), med felles at både Bildeteknikker (LM og EM) utføres på samme prøven. Kombinasjonen av begge metodene gir, dermed en multimodal, multi-skala og flerdimensjonal analyse av at eksempel3. Fordelene er at LM kan gi en bred oversikt over mange ulike celler, slik at identifikasjon av cellen subpopulasjoner uttrykke et protein eller proteiner av interesse i en heterogen celle befolkningen. EM overvinner oppløsning grensen på LM, gir et høyere oppløsning bilde av en bestemt intracellulær hendelse. Videre gjør EM visualisering av ikke-fluorescerende subcellular sammenheng, inkludert alle membran-bundet organeller, store macromolecular komplekser (f.eks ribosomer, centrioles, etc.) og cellen cytoskjelett elementer, og dermed gir ekstra romlig informasjon, den såkalte “referanse plass”6, og gi kontekst til lysrør stedet oppdages av LM.
De siste årene, CLEM har blitt et kraftig verktøy ikke bare for celle biologer5, men også for virologists (omtalt i referanse7) villig til å forstå komplekse virus-celle samhandlingene som fører til en vellykket virus overføring. Dermed er forstå hvordan virus endre celle membraner og organelles til sin egen fordel avgjørende å utvikle antivirale midler for å utrydde patogene virus.
Her beskrives en CLEM metode som tillater påvisning av LM celler uttrykke virale proteiner smeltet til et fluorescerende protein (FP). Disse cellene er senere cryo-immobilisert og mer forberedt for ultrastructural analyse via overføring elektronmikroskop (TEM) å få ny innsikt i hvordan uttrykket av disse proteinene omorganisere intracellulær membraner (figur 1). CLEM er utført med kjemisk fast celler i de fleste virologi studier publisert dato8,9,10,11,12,13,14 ,,15,,16,,17,,18,,19. Dette er hovedsakelig på grunn av behovet for å inaktivere smittsomme materiale for biosikkerhet grunner i grad-2 og -3 (BSL-2 og BSL-3) laboratorier, hvor cryo-immobilisering av cellene ikke er vanligvis mulig. For spørsmål som krever en optimal bevaring cellemembraner vitrifikasjon via høytrykk frysing (HPF), men anbefales20. I disse tilfellene kan CLEM protokollen beskrevet her brukes. Interessant, spesielt når du arbeider med smittefarlige prøver, kan HPF utføre på eksempler som har vært tidligere kjemisk deaktivert, for eksempel i BSL-2 og BSL-3 laboratorier. Kombinasjonen av kjemiske fiksering etterfulgt av HPF er en mulighet til å tjene minst delvis fordelene cryo-bevaring metoder21,22.
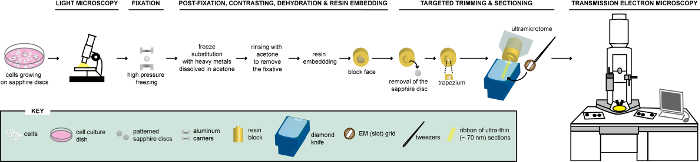
Figur 1 : Skjematisk fremstilling av arbeidsflyten for analyse av celler via CLEM. Cellene vokser på mønstret safir plater analyseres først av LM å lokalisere celler uttrykke FPs før behandlingen for EM. Når funnet, repareres umiddelbart celler av HPF og FS bygges deretter i harpiks. Ved polymerisering av harpiks, støtte der celler vokste (= safir plater) må fjernes fra harpiks blokken. Blokken som inneholder de innebygde cellene beskjæres til en liten trapes som de gjenværende cellene, uttrykke FPs, er delt med diamant kniv. Supertynn deler er samlet på sporet rutenett og videre undersøkt av TEM å få ultrastructural informasjon til disse cellene. Dette tallet er tilpasset og endret med tillatelse fra referanse29. Klikk her for å se en større versjon av dette tallet.
Protocol
Representative Results
Discussion
CLEM metodikken presentert her for å studere virkningen av en viral protein uttrykk i celle membraner har blitt brukt før for å belyse HCV replikering-assosiert strukturer, hovedsakelig dobbel membran blemmer (DMVs)21, samt bestemme kritisk byggesteinene kreves til disse HCV-indusert strukturer23. Merk at i vårt første arbeid bruk av CLEM HCV replikering21, en litt modifisert versjon av protokollen beskrevet her ble brukt. At studien, konvensjonelle 0.05 mm tykk safir plater, uten alfanumeriske mønster, ble brukt som en referanse mønster ble opprettet av karbon belegg dem med et finder rutenett på toppen (se Tabell for materiale). Denne versjonen av gjeldende protokollen kan til slutt brukes, med fordelen at “A” bærer for HPF kan brukes direkte, uten behov for å kutte det ned som i Figur 3A. Alternativt, som nevnt i protokollen, tykkere “A” bærer kan brukes (se Tabell for materiale) med mønstret safir plater, uten behovet av en “B” operatør.
Interessant, kan denne protokollen brukes ikke bare å studere BSL-1 eksempler, slik som celler transfekterte med virale proteiner som beskrevet her og andre steder19,23, men også å studere virus-infiserte celler. Selv om arbeide med mennesker er vanligvis begrenset til BSL-2 og BSL-3 laboratorier, i enkelte land er det fortsatt mulig å utføre cryo-immobilisering under disse biosikkerhet forhold. I disse BSL-2 og BSL-3 laboratorier der vitrifikasjon ikke er mulig på grunn av lokale bestemmelser eller fraværet av en HPF maskin, kan virus-infiserte celler fortsatt tilberedes bruke denne metoden hvis kjemiske fiksering med aldehyder er utført på forhånd, nemlig før avreise BSL-2 eller BSL-3 fasiliteter. Videre må aldehyder bli slukket umiddelbart etter fiksering holde fluorescens, mens resten av protokollen er identisk med den som er beskrevet her. Denne teknikken kan anses overflødig fordi cellene er fast to ganger, kjemisk og via vitrifikasjon. Men fører denne dobbel fiksering protokollen faktisk til en mye bedre bevaring av HCV-indusert DMVs i forhold til DMVs i cellene utsatt for kjemiske fiksering alene21.
For ytterligere endringer og feilsøking leseren kalles notatene hele delen protokollen i dette manuskriptet. Disse notatene beskriver fallgruvene å unngå, samt alternativer å overvinne mulige problemer som kan oppstå når du utfører denne metoden.
Det viktigste forutsetning for å bruke denne teknikken er en HPF maskin. Når cryo-immobilizing cellene via HPF er ikke gjennomførbart (på grunn av en HPF maskin) eller ikke nødvendig (når membranen bevaring ikke trenger å være optimalt), celler kan kjemisk fast og senere forberedt og analyseres av EM8, 9,10,11,12,13,14,15,16,17,18 ,19. Dette alternativet krever ikke bruk av safir plater, men celle kultur retter med gridded mønstre for flytting av celler eller cellen klynger. Hovedfordelen ved bruk av disse rettene er deres større diameter i forhold til safir plater, screening av større flater. Dermed har anvendelsen av denne CLEM protokollen vært anvendt studere effekten av en antiviral stoff mot HCV15 eller visualisere membran rearrangements indusert av nonstructural proteiner noroviruses19. En annen sak som kan begrense ytelsen til denne metoden er fraværet av en kommersiell FS-enhet. I dette tilfellet kan grunnleggende hjemmelaget FS systemer brukes i stedet. Selv om automatisk FS enheter kan redusere håndtering uhell, hjemmelagde enheter brukes med hell for eksempel på Kent McDonalds30 og Paul Walther labs.
Med hensyn til kjemiske fiksering sikrer protokollen beskrevet her en optimal bevaring av intracellulær strukturer20. Derfor, i tilfelle de nevnte HPF og FS enhetene er tilgjengelige, vitrifying cellene rundt vil bli foretrukket.
Fremtidige alternativer til denne CLEM tilnærmingen omfatter muligheten av benytter denne metoden ikke bare å kjøpe 2D informasjon på ultrastructural nivå, men også å få 3D-informasjon om arkitektur av membran og organelle endringer forårsaket av virus. 3D-EM metoder, inkludert elektron tomografi (ET) og fokusert ion bjelke-skanning elektronmikroskop (FIB-SEM) (grundig beskrevet i29), kan også brukes til celler som er utarbeidet etter denne gjeldende protokollen21, 31. I tillegg kan 3D-informasjon også hentes på LM nivå, når du bruker en AC confocal mikroskop, hvilke innrømmer oppkjøpet av z-stabler. Faktisk, anbefales dette valget når en presis sammenheng mellom LM og EM datasett er ønsket (se for eksempel17). Informasjonen som finnes i 3D z-stabler hjelpemidler for å forbedre sammenhengen med 2D TEM bilder. Dermed i et slikt scenario, kan best passer LM og EM bilder valgt og deretter utsatt for en av de korrelasjon programvare tilgjengelig, som EU-CLEM plugin ICY (http://icy.bioimageanalysis.org/)32 eller landemerke Correspondences plugg av Bildet J (http://imagej.net/Landmark_Correspondences), noe som resulterer i generasjon av overlappende LM-EM bilder.
Når timelige informasjon er nødvendig å forstå kinetics av en viss hendelse, kan tidsinnstilt bildebehandling brukes til å overvåke dynamikken i levende celler i kombinasjon med EM. Under arrangementet av interesse repareres celler umiddelbart generere en “frosset snapshot” som senere kan analyseres via EM, gir detaljert ultrastructural informasjon om det aktuelle øyeblikket ved immobilisering. For å få den “frosne snapshot”, etter observasjon i sanntid, kan cellene kjemisk fast33 eller cryo-immobilisert6. Siden mange mobilnettet prosesser skje raskere enn diffusjon prosessene av kjemiske fiksering, hvis mulig, skal ultra rask frysing utføres. Det er imidlertid viktig å ta hensyn til at HPF maskiner varierer i sine effektiv oppløsning34.
Videre, selv om denne protokollen utviklet for innebygging av celler i en epoxy harpiks, celler kan også bygges i lav viskositet harpikser, som Lowicryls, LR hvit eller LR gull. Bruk av disse innebygging media kan beholde antigenicity35,36, samt fluorescens37,38 , og derfor brukes hovedsakelig for post innebygging på delen immunolabeling39 , 40 og på-seksjonen CLEM41,42,43,44, der LM er gjort etter innebygging. Begge tilnærminger (immuno-EM og på-seksjonen CLEM) må være avgjørende for disse eksperimentene som ikke-karakteristisk strukturer lett kan finnes via TEM og/eller som en kontroll mot miscorrelation mellom LM og EM signaler. Likeledes, merking med antistoffer som kan visualiseres både tenkelig modaliteter (LM og EM) kan utføres45 for å, for eksempel identifisere transfekterte celler i LM (pre embedding scenen) og oppnå et mye mer nøyaktig lokalisering av den GFP signal via sine spesifikke merking av immuno-EM (etter innebygging scenen). Det må tas i betraktning, men at permeabilization utføres før LM tillater tilgang av antistoffer til intracellulær plass, noe som kan resultere i en sub-optimal bevaring av cellen arkitekturen på EM nivå. Denne protokollen er interessant også godt egnet for multi-farge eksperimenter som kan oppnås med bruk av andre fluorescerende koder, enn GFP (som vist her). I konklusjonen, finnes det mange mulige muligheter til å tilpasse denne protokollen, både på LM og/eller på EM sidene, avhengig av spørsmål som tas. En omfattende beskrivelse av protokoller alternativ kalles leseren5,46. Uansett hvordan mikroskopi modaliteter kombineres, er sammen resultatet en gevinst for, tillater oss å forstå hvordan virus og deres proteiner sammen med deres verter i det virkelige liv.
Det mest kritiske trinnet i denne metoden er samlingen av føljetong inndelinger fra cellene rundt. Som fremhevet i delen representant resultater krever dette ekspert ansatte, samt mye tålmodighet. Viktigere, er dette trinnet viktig å finne celler tilbake på EM nivå av to grunner. Først i denne slags CLEM protokollen bruker pre innebygging LM, vises koordinatene bare på LM nivå og på harpiks blokk ansiktet etter innebygging. Men vises de ikke på delene av TEM. Derfor må målrettet trimmer i blokk ansiktet ned til områder av interesse (ROIs) gjøres nøye med et barberblad slik at delene som hentes senere inneholder celler som uttrykker gitt FP. Andre er “skanning” flere deler nødvendig å finne beste overlappingen mellom LM og EM oppkjøp. I motsetning til metoder der LM er utført på post innebygging scenen, er i dette tilfellet LM-EM overlegg ikke så nøyaktig. Lav overlegg nøyaktigheten skyldes forskjeller i aksial oppløsning mellom LM og EM, krymping under eksempel behandling av EM og komprimering under snitting42. Likevel bidra effektiv oppfølgingsmetoder, som bruk av landemerker, til å finne celler tilbake. Dette inkluderer plasseringen av en celle til en annen, så vel som formen på cellene og deres kjernen. I denne forbindelse, som forklart i protokollen, gir DIC bilder “anatomiske” informasjon av cellene som er avgjørende for å forbedre sammenhengen. Alternativt kjerner eller andre godt-gjenkjennelig celle organeller (for eksempel mitokondrier eller lipid dråper) kan være farget før LM og brukt som landemerker.
Til slutt, det er bemerkelsesverdig å nevne at selv om dette manuskriptet fokuserer på bruk av denne teknikken for virologi studier, omfanget av denne eksperimentell design kan utvides for å håndtere mer generelle biologiske spørsmål.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi er veldig takknemlig for ansatte i den elektronmikroskop Core fasiliteter (EMCF) på EMBL (Heidelberg) og Universitetet i Heidelberg. Vi også gjerne takke Ulrike Herian, Stephanie Kallis og Andrea Hellwig (Universitetet i Heidelberg), samt Eberhardt Schmidt og Renate Kunz (University Ulm) for ekspert teknisk assistanse. Av R.B. og hans team (U.H. og I.R.-B.) ble støttet av Deutsche Forschungsgemeinschaft, SFB1129, TP11 og TRR83, TP13.
Materials
| UV Crosslinker | Stratagene | 400072 | Stratalinker 1800, 230Vac, equipped with 254-nm UV light bulbs, 8-watts/each. |
| Patterned sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 627 | They have a 0.3-mm diameter and are 0.16-mm thick, as well as an an etched alphanumeric pattern to allow for re-location of the cells. They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Slim and long tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | 72919-SS | "Style SS", for handling sapphire discs. |
| Cell culture medium | Thermo Fisher Scientific, Waltham, MA, USA | 41965-062 | Dulbecco's modified Eagle medium (DMEM) supplemented with 2 mM L-glutamine, nonessential amino acids, 100 units penicillin per ml, 100 µg streptomycin per ml and 10% fetal calf serum (DMEM complete, see below). Package containing 10 bottles, 500 ml/each. |
| L-glutamine | Thermo Fisher Scientific, Waltham, MA, USA | 25030-123 | Package containing 20 bottles of 100 ml/each. |
| Nonessential amino acids | Thermo Fisher Scientific, Waltham, MA, USA | 11140-068 | Package containing 20 bottles of 100 ml/each. |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Waltham, MA, USA | 15140-163 | Package containing 20 bottles of 100 ml/each. |
| Fetal calf serum | Sigma Aldrich, St. Louis, MI, USA | F7524 | Bottle of 50 ml. |
| Inverted microscope | Olympus Deutschland, Hamburg, Germany | CKX41 | It is an inverted microscope with trinocular head options and fluorescence upgrade capability. |
| Huh7-Lunet cells stably expressing the T7 RNA-polymerase | Avaliable at Prof. Dr. Ralf Bartenschlager laboratory | Not available | Contact Prof. Bartenschlager at: ralf.bartenschlager@med.uni-heidelberg.de. |
| Mirus TransIT-LT1 Transfection Reagent | Mirus Bio LLC, Madison, USA | MIR 2304 | Broad spectrum, low toxicity, DNA transfection reagent. Vial of 0.4 ml. |
| Inverted widefield fluorescence microscope | Carl Zeiss Microscopy GmbH, Germany | Zeiss Observer.Z1 | Inverted fluorescence microscope for experiments involving living cell cultures. |
| 1-hexadecene | Merck, Darmstadt, Germany | 8220640100 | Bottle of 100 ml. |
| "A" aluminium holders for high pressure frezing (HPF) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 241 | This is the holder that has been used for this protocol and has 2 different depths of 0.1 and 0.2-mm. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "B" aluminium holders for HPF | Engineering Office M. Wohlwend, Sennwald, Switzerland | 242 | This is the holder that has been used for this protocol.It is 0.3-mm thick.They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "A" aluminium holder for HPF (special for working with patterned sapphire discs) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 737 | This is the holder than can be used alone with the patterned sapphire disc (as an alternative to the current protocol), without the need of a "B" holder or the edition of the "A" holder. It is 0.84-mm thick. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 405 | These sapphires discs are the "conventional" one, with a 0.3-mm diameter and a thickness of 0.05 mm . They can be also used for CLEM as an alternative instead of patterned sapphire discs. |
| Finder grids | Electron Microscopy Sciences, Hatfield, Philadelphia, USA | LF135-Cu | These 135 mesh grids are used to create an alphanumeric pattern on "conventional" sapphire discs (described above) via carbon coating, so that they can be used for CLEM. 100 grids/vial. |
| HPF machine | ABRA Fluid AG, Widnau, Switzerland | HPM 01 | This HPF machine has been used for this protocol. |
| HPF machine | Leica Microsystems, Vienna, Austria | EMPACT 2 | "EMPACT 2", as an alternative to the use of the HPM machine that it has been used in this protocol (described above). |
| Cryo-tubes | Thermo Fisher Scientific, Waltham, MA, USA | Z763667-500EA | For long term-storage of cryo-immobilized samples in liquid nitrogen. Package containing 500 cryovials. |
| Liquid nitrogen dewar | Cole-Parmer GmbH, Wertheim, Germany | GZ-05094-60 | For long term-storage of cryo-immobilized samples in liquid nitrogen, equipped with cryo-racks with a capacity of 1600 cryo-tubes. |
| Automatic freeze substitution (AFS) machine | Leica Microsystems, Vienna, Austria | EM AFS2 | This machine performs freeze substitution and progressive lowering of temperature (PLT) techniques and allows low temperature embedding and polymerization of resins. |
| Osmium tetroxide (OsO4) | Electron Microscopy Sciences, Hatfield, PA, USA | 19150 | 4% aqueous solution, one box containing 10 x 2 ml ampules. |
| Uranyl-Acetate (UA) | Serva, Heidelberg, Germany | 77879.01 | Bottle containing 25 grs of (UA)-2 H2O. |
| Sonicator | Bandelin Electronic, Berlin, Germany | 329 | "Sonorex Super RK 31" is a high-power ultrasonic cleaning bath for aqueous cleaning solution that is used in this protocol to mix OsO4 and Ua when preparing the FS medium. |
| Glass-distilled acetone | Electron Microscopy Sciences, Hatfield, PA, USA | 10015 | Bottle of 100 ml. |
| Stereomicroscope | Leica Microsystems, Vienna, Austria | Leica M80 | Routine stereomicroscope for daily inspections, equipped with a camera for capturing images. |
| Epoxy resin | Electron Microscopy Sciences, Hatfield, PA, USA | 14120 | Embed 812 is a kit containing several components that must be mix together in the proportions given by the manufacturers. |
| Flow through rings | Leica Microsystems, Vienna, Austria | 16707157 | Package containing 100 pieces. |
| Reagent baths | Leica Microsystems, Vienna, Austria | 16707154 | Package containing 100 pieces. |
| Ultramicrotome | Leica Microsystems, Vienna, Austria | Leica EM UC7 | Ultramicrotome for preparation of semi- and ultrathin sections at room temperature. |
| Ultra 35° diamond knife | Diatome Ltd., Nidau Switzerland |
AGG339-735 | This knife have an edge length of 3 mm. |
| Ultra fine tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | E78318 | "Style 3X", for handling EM grids. |
| EM slot grids | Electron Microscopy Sciences, Hatfield, PA, USA | G2010-Cu | 100 grids/vial. |
| EM grid storage box | Electron Microscopy Sciences, Hatfield, PA, USA | 71155 | It has capacity for 100 grids. |
References
- Morgan, C., Godman, G. C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. I. Electron microscopy. Journal of Experimental Medicine. 112, 373-382 (1960).
- Godman, G. C., Morgan, C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. II. Light microscopy. Journal of Experimental Medicine. 112, 383-402 (1960).
- Caplan, J., Niethammer, M., Taylor, R. M., Czymmek, K. J. The power of correlative microscopy: multi-modal, multi-scale, multi-dimensional. Current Opinion in Structural Biology. 21, 686-693 (2011).
- de Boer, P., Hoogenboom, J. P., Giepmans, B. N. Correlated light and electron microscopy: ultrastructure lights up. Nature Methods. 12, 503-513 (2015).
- Müller-Reichert, T., Verkade, P. . Correlative light and electron microscopy III, First edition. , (2017).
- Brown, E., Mantell, J., Carter, D., Tilly, G., Verkade, P. Studying intracellular transport using high-pressure freezing and Correlative Light Electron Microscopy. Seminars in Cell and Developmental Biology. 20, 910-919 (2009).
- Bykov, Y. S., Cortese, M., Briggs, J. A., Bartenschlager, R. Correlative light and electron microscopy methods for the study of virus-cell interactions. FEBS Letters. , (2016).
- Spuul, P., et al. Assembly of alphavirus replication complexes from RNA and protein components in a novel trans-replication system in mammalian cells. Journal of Virology. 85, 4739-4751 (2011).
- Nagel, C. H., Dohner, K., Binz, A., Bauerfeind, R., Sodeik, B. Improper tagging of the non-essential small capsid protein VP26 impairs nuclear capsid egress of herpes simplex virus. PLoS One. 7, 44177 (2012).
- Sharma, M., Kamil, J. P., Coughlin, M., Reim, N. I., Coen, D. M. Human cytomegalovirus UL50 and UL53 recruit viral protein kinase UL97, not protein kinase C, for disruption of nuclear lamina and nuclear egress in infected cells. Journal of Virology. 88, 249-262 (2014).
- Kallio, K., et al. Template RNA length determines the size of replication complex spherules for Semliki Forest virus. Journal of Virology. 87, 9125-9134 (2013).
- Martinez, M. G., Snapp, E. L., Perumal, G. S., Macaluso, F. P., Kielian, M. Imaging the alphavirus exit pathway. Journal of Virology. 88, 6922-6933 (2014).
- Lebrun, M., et al. Varicella-zoster virus induces the formation of dynamic nuclear capsid aggregates. Virology. 454-455, 311-327 (2014).
- Madela, K., et al. A simple procedure to analyze positions of interest in infectious cell cultures by correlative light and electron microscopy. Methods in Cell Biology. 124, 93-110 (2014).
- Berger, C., et al. Daclatasvir-like inhibitors of NS5A block early biogenesis of hepatitis C virus-induced membranous replication factories, independent of RNA replication. Gastroenterology. 147, 1094-1105 (2014).
- van der Schaar, H. M., et al. Illuminating the Sites of Enterovirus Replication in Living Cells by Using a Split-GFP-Tagged Viral Protein. mSphere. 1, (2016).
- Vale-Costa, S., et al. Influenza A virus ribonucleoproteins modulate host recycling by competing with Rab11 effectors. Journal of Cell Science. 129, 1697-1710 (2016).
- Wang, L., et al. Visualization of HIV T Cell Virological Synapses and Virus-Containing Compartments by Three-Dimensional Correlative Light and Electron Microscopy. Journal of Virology. 91, (2017).
- Doerflinger, S. Y., et al. Membrane alterations induced by nonstructural proteins of human norovirus. PLOS Pathogens. 13, 1006705 (2017).
- Dahl, R., Staehelin, L. A. High-pressure freezing for the preservation of biological structure: theory and practice. Journal of Electron Microscopy Technique. 13, 165-174 (1989).
- Romero-Brey, I., et al. Three-dimensional architecture and biogenesis of membrane structures associated with hepatitis C virus replication. PLOS Pathogens. 8, 1003056 (2012).
- Sosinsky, G. E., et al. The combination of chemical fixation procedures with high pressure freezing and freeze substitution preserves highly labile tissue ultrastructure for electron tomography applications. Journal of Structural Biology. 161, 359-371 (2008).
- Romero-Brey, I., et al. NS5A Domain 1 and Polyprotein Cleavage Kinetics Are Critical for Induction of Double-Membrane Vesicles Associated with Hepatitis C Virus Replication. MBio. 6, 00759 (2015).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36, 280-290 (2003).
- Jou, M. J., Jou, S. B., Guo, M. J., Wu, H. Y., Peng, T. I. Mitochondrial reactive oxygen species generation and calcium increase induced by visible light in astrocytes. Annals of the New York Academy of Sciences. 1011, 45-56 (2004).
- McDonald, K. L., Morphew, M., Verkade, P., Muller-Reichert, T. Recent advances in high-pressure freezing: equipment- and specimen-loading methods. Methods in Molecular Biology. 369, 143-173 (2007).
- Walther, P., Ziegler, A. Freeze substitution of high-pressure frozen samples: the visibility of biological membranes is improved when the substitution medium contains water. Journal of Microscopy. 208, 3-10 (2002).
- White, J. G., Southgate, E., Thomson, J. N., Brenner, S. The structure of the nervous system of the nematode Caenorhabditis elegans. Philosophical Transactions of the Royal Society B: Biological Sciences. 314, 1-340 (1986).
- Romero-Brey, I., Bartenschlager, R. Viral Infection at High Magnification: 3D Electron Microscopy Methods to Analyze the Architecture of Infected Cells. Viruses. 7, 6316-6345 (2015).
- McDonald, K. L., Webb, R. I. Freeze substitution in 3 hours or less. Journal of Microscopy. 243, 227-233 (2011).
- Villinger, C., Neusser, G., Kranz, C., Walther, P., Mertens, T. 3D Analysis of HCMV Induced-Nuclear Membrane Structures by FIB/SEM Tomography: Insight into an Unprecedented Membrane Morphology. Viruses. 7, 5686-5704 (2015).
- Paul-Gilloteaux, P., et al. eC-CLEM: flexible multidimensional registration software for correlative microscopies. Nature Methods. 14, 102-103 (2017).
- Polishchuk, R. S., Mironov, A. A. Correlative video light/electron microscopy. Current Protocols in Cell Biology Supplement. , 8 (2001).
- McDonald, K. L. A review of high-pressure freezing preparation techniques for correlative light and electron microscopy of the same cells and tissues. Journal of Microscopy. 235, 273-281 (2009).
- Newman, G. R., Jasani, B., Williams, E. D. A simple post-embedding system for the rapid demonstration of tissue antigens under the electron microscope. The Histochemical Journal. 15, 543-555 (1983).
- Schwarz, H., Humbel, B. M. Influence of fixatives and embedding media on immunolabelling of freeze-substituted cells. Scanning Microscopy. 3, 57-63 (1989).
- Luby-Phelps, K., Ning, G., Fogerty, J., Besharse, J. C. Visualization of identified GFP-expressing cells by light and electron microscopy. Journal of Histochemistry and Cytochemistry. 51, 271-274 (2003).
- Nixon, S. J., et al. A single method for cryofixation and correlative light, electron microscopy and tomography of zebrafish embryos. Traffic. 10, 131-136 (2009).
- McDonald, K. L. Rapid embedding methods into epoxy and LR White resins for morphological and immunological analysis of cryofixed biological specimens. Microscopy and Microanalysis. 20, 152-163 (2014).
- Webster, P., Schwarz, H., Griffiths, G. Preparation of cells and tissues for immuno EM. Methods in Cell Biology. 88, 45-58 (2008).
- Kukulski, W., et al. Correlated fluorescence and 3D electron microscopy with high sensitivity and spatial precision. Journal of Cell Biology. 192, 111-119 (2011).
- Peddie, C. J., et al. Correlative and integrated light and electron microscopy of in-resin GFP fluorescence, used to localise diacylglycerol in mammalian cells. Ultramicroscopy. 143, 3-14 (2014).
- Hampoelz, B., et al. Pre-assembled Nuclear Pores Insert into the Nuclear Envelope during Early Development. Cell. 166, 664-678 (2016).
- Lemercier, N., et al. Microtome-integrated microscope system for high sensitivity tracking of in-resin fluorescence in blocks and ultrathin sections for correlative microscopy. Scientific Reports. 7, 13583 (2017).
- Takizawa, T., Powell, R. D., Hainfeld, J. F., Robinson, J. M. FluoroNanogold: an important probe for correlative microscopy. Journal of Biological Chemistry. 8, 129-142 (2015).
- Romero-Brey, I., Yamauchi, Y. 3D electron microscopy (EM) and correlative light electron microscopy (CLEM) methods to study virus-host interactions. Methods in Molecular Biology: Influenza Virus Methods & Protocols. , (2018).

