Användning av rekombinanta fusionsproteinerna i en fluorescerande proteas Assay plattform och deras i-gel utvinningsarbete
Summary
Här presenterar vi de detaljerade anvisningar av en nyligen utvecklad proteas assay plattform använder N-terminala hexahistidine/maltos-bindande protein och fluorescerande protein-smält rekombinant substrat kopplad till ytan av nickel-nitrilotriacetic sura magnetiska agaros pärlor. Efterföljande i-gel analys av assay proverna åtskilda av sodium dodecyl sulfate-polyakrylamid gelelektrofores presenteras också.
Abstract
Proteaser är intensivt studerade enzymer på grund av deras viktiga roller i flera biologiska spridningsvägar av levande organismer och i patogenesen; Därför är de viktiga målmolekyler. Vi har utvecklat en magnetisk-agaros-pärla-baserade test plattform för utredning av proteolytiska verksamhet, som bygger på användning av rekombinanta fusion protein substrat. För att demonstrera användningen av detta test system, presenteras ett protokoll på exemplet med humant immunbristvirus typ 1 (HIV-1) proteashämmare. Introducerade assay plattformen kan utnyttjas effektivt i biokemisk karakterisering av proteaser, inklusive enzym Aktivitetsmätningar i mutagenes, kinetic, hämning eller specificitet studier, och det kan vara lämplig för hög genomströmning substratet screening eller kan anpassas till andra proteolytiska enzymer.
I detta test system, de tillämpa substratesna innehåller N-terminala hexahistidine (hans6) och maltos-bindande protein (MBP) Taggar, klyvning platser för tobak etch virus (TEV) och HIV-1 proteaser och en C-terminala fluorescerande protein. Substratesna kan vara effektivt produceras i Escherichia coli -celler och renat enkelt med nickel (Ni) – kelat – belagda pärlor. Under analysen leder proteolytisk klyvning av pärla-knutna substrat till utsläpp av fluorescerande klyvning fragment, som kan mätas med fluorimetry. Klyvning reaktioner kan dessutom analyseras av sodium dodecyl sulfate-polyakrylamid gelelektrofores (SDS-PAGE). Ett protokoll för den i-gel utvinningsarbete assay komponenter beskrivs också, som delvis återställande av fluorescerande proteiner gör deras påvisande baserat på molekylvikt och fluorescens.
Introduction
Proteolytiska enzymer tillhör de mest intensivt undersökta enzym grupperna på grund av sin betydelse i metaboliska vägar och i industriella applikationer, liksom. Deras nyckelroll för virussjukdomar, reglering av blodets levringsförmåga, cancer och hjärt- och neurodegenerativa sjukdomar gör proteaser framträdande mål inom läkemedelsutveckling. Därför detaljerad karakterisering av substrat specificitet och hämmare profilering av proteashämmare (PR) av intresse är avgörande och utförs företrädesvis av snabba, kostnadseffektiva och robust biokemiska analyser1,2, 3.
Numera de allra flesta av in vitro-proteas analyser tillämpas inom läkemedelsutveckling för sammansatta profilering är homogen, fluorescerande peptid-baserad, och high-throughput screening (HTS)-kompatibla plattformar4. Dessutom märkt peptider är inte bara lämplig för bibliotek screening, men de erbjuder också bra verktyg för bestämning av enzymet kinetiska parametrar på de valda substratesna. I andra fall, om märkning av substratet inte är möjligt, kan separation-baserade analyser ge en möjlig lösning för att bedöma proteolytiska reaktioner3kinetiska egenskaper.
Allmänhet, in vitro-proteas analyser baseras på användningen av två typer av substrat: kort peptider eller hela proteiner. I de fall, där klyvning av kort peptid sekvenser återspeglar egenskaperna klyvning tillräckligt, de följande standardmetoder är tillämpliga: (i) att undersöka standard protein substrat såsom oxiderat insulin B-kedjan, (ii) testning kommersiellt tillgängligt substrat för andra proteaser, (iii) screening syntetiska och fluorescently märkt peptid-bibliotek som skapats av kombinatorisk kemi, eller (iv) med hjälp av genetiska metoder, exempelvis biologiska Visa teknik5, 6. Förutom konventionella klassificering, andra roman plattformar finns också för generering av substrat (t.ex. bildandet av proteom-derived peptid bibliotek7 eller särskilda subtyper av genetiska metoder, som den rekombinanta fusionen protein-baserade substrat8,9,10,11,12).
Alla ovannämnda substrat typer och analyser har sina egna fördelar och begränsningar, och utvecklingen av assay format att kombinera och/eller förbättra fördelarna med de kända plattformarna är fortfarande i efterfrågan. Här beskriver vi ett protokoll för en separation-baserade fluorescerande proteas analys, som använder rekombinant substrat. Dessa fusionsproteinerna består av hans6 och MBP Taggar smält till en kontroll klyvning platsen för TEV PR, som följs av substrat sekvens av intresse som är direkt ansluten till en C-terminala fluorescerande protein (FP) (figur 1A). Kloning av en DNA-sekvens som kodar för en klyvning platsen av intresse i ‘kloning kassetten’ kan utföras av en enda ligering reaktion till uttryck plasmiden, som har varit linearized tidigare av begränsning endonucleases.
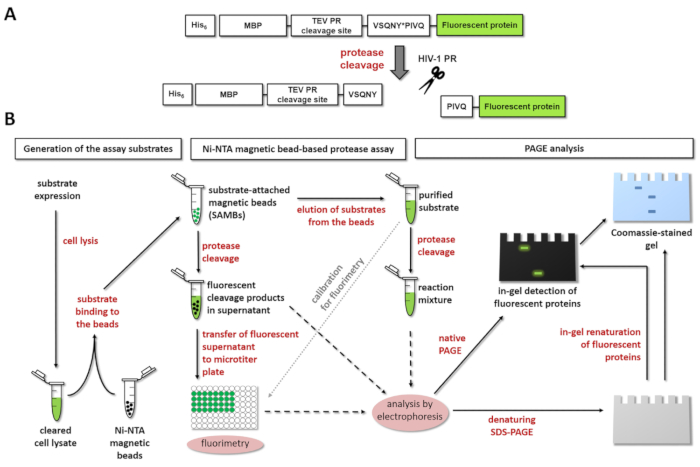
Figur 1: Princip fluorescerande proteas analysens. (A) schematisk representation av en fluorescerande substrat och dess klyvning av humant immunbristvirus typ 1 (HIV-1) proteas visas. Pilen visar klyvning position inom matrix/kapsid klyvning webbplats sekvensen i HIV-1 proteas (VSQNY * PIVQ). (B) fluorescerande substrat kan användas för att analysera enzymreaktioner av Ni-NTA magnetiska-pärla-baserade analysen och polyakrylamid gelelektrofores, samt, som visas i diagrammet arbetsflöde. Klicka här för att se en större version av denna siffra.
Även om proteolytiska analyser använder liknande rekombinant protein substrat som innehåller en affinitet-tagg, en proteolytisk klyvning webbplats och en fluorescerande protein-har redan beskrivits8,9,10, systemet presenteras här avser att integrera och förbättra fördelarna med dessa metoder. En viktig skillnad är att de fusion protein substratesna i denna analys plattform är utrustade med MBP att förbättra protein löslighet13 och innehåller en kontroll klyvning webbplats för TEV PRs. Dessutom innehåller substratesna ny generation fluorescerande proteiner, som är mycket stabil och har en monomer form att förhindra substrat aggregering. Förutom tidigare publicerade tillämpningen av mTurquoise2 – och mApple-smält former14visar här också vi resultaten ges genom användning av ett rekombinant substrat som innehåller en monomer enhanced gul fluorescerande protein (mEYFP) fluorescerande tagg. Härmed vi demonstrera systemet förenlighet med andra fluorescerande proteiner och representerar vissa allmänna typer av resultat som kan förvärvas av proteashämmare analysen.
Rekombinant fusionsproteinerna uttrycks i E. coli BL21(DE3) celler och används som underlag för analysen i ett nickel-nitrilotriacetic syra (Ni-NTA)-belagda magnetiska-agaros-pärla-anslutna form. C-terminal sönderdelningsprodukterna är befriade från pärla ytan i supernatanten vid klyvning av proteasen sevärdheter. Efter avskiljandet av supernatanten (som innehåller enzymet och sönderdelningsprodukterna) från de magnetiska pärlorna, kan fluorescensen mätas för att bestämma egenskaperna klyvning av enzymet. I motsats till de tidigare beskrivna metoderna, kvantifieras i systemet presenteras här, mängden substrat och C-terminal klyvningsprodukter unikt utifrån en detaljerad substrat kalibreringen. Assay systemet kan stödjas av en SDS-PAGE analys av assay proverna; en efterföljande fluorescerande i-gel visualisering kan tillämpas omedelbart efter elektrofores eller efter den i-gel utvinningsarbete nondenatured och denaturerat fluorescerande komponenter, respektive14.
Flexibiliteten och struktur av ‘kloning kassetten’ tillåta en tids – och kostnadseffektiva isättning av en mängd olika sekvenser i konstruktionen och främjar därmed, generering av substrat bibliotek. Eftersom alla analysstegen är automation – och HTS-kompatibla, kan systemet vara särskilt attraktiv för, till exempel proteas specificitet mätningar och mutagenes studier, eller det kan också utnyttjas effektivt för industriella proteas hämmare screening och/eller utveckling av antivirala läkemedel, liksom.
Enzymet kinetiska parametrar (kkatt, Km) kan bestämmas av den utvecklade Separationsbaserade analysen; Därför kan det vara lämpligt att utföra enskilda enzym kinetiska mätningar, såsom tid-kursen, substrat-beroende och hämning studierna. Detta bevisar att de rekombinanta fusion protein substratesna ger bra alternativ för de ofta utnyttjad syntetiska oligopeptide substratesna, och på grund av deras höga likhet de polyprotein substratesna, de representerar den naturligt förekommande enzym-substrat interaktioner mer exakt.
Protocol
Representative Results
Discussion
På grund av de intensiva industri- och akademiska utredningarna av proteolytiska enzymer och ständig efterfrågan på snabba och prisvärda HTS-kompatibel proteas assay plattformar med detta, har vi utvecklat ett magnetisk-pärla-baserade fluorescerande proteas assay. Analysen är baserad på användning av rekombinanta fusionsproteinerna som kan vara nya alternativ till de allmänt utnyttjad syntetisk peptid substratesna.
I formatet utvecklade analysen, är de fusion protein substratesna orörlig till ytbehandlar av Ni-kelat-coated magnetiska agaros pärlor. Substratet bilagan tillhandahålls av den N-terminalen hans6 affinitet tag av proteinet fusion, som smälts samman direkt på en MBP-tagg för att underlätta vikningen och förbättra vattenlösligheten av substrat13. MBP följs av klyvning platser av TEV PR och ett proteas sevärdheter. Den förstnämnda kan tjäna som en kontroll klyvning plats i analysen, medan den senare kan bearbetas av proteashämmaren för utredas. Webbplatsen för klyvning är utbytbara; en kort dsDNA sekvensen kodar för webbplatsen klyvning av intresse kan infogas i den flexibla ‘kloning kassetten’ av uttrycket plasmiden av ligering. Rekombinant fusionsproteinerna innehåller en mycket stabil, monomer fluorescerande protein tagg på C-terminalen, som möjliggör endpoint detektion av enzym-befriade, fluorescerande C-terminal sönderdelningsprodukterna släppt på proteolytisk klyvning ( Figur 1A). De renade fluorescerande intakt substrat löst i olika buffertar används också för kalibrering för att bedöma molara koncentrationerna av substrat och klyvningsprodukter. Dessutom, efter fluorimetry, kan assay komponenterna analyseras av SDS-PAGE, liksom. Både enhetliga (nondenatured) och denaturerat fluorescerande proteiner kan visualiseras i gel, omedelbart efter elektrofores eller efterföljande i-gel utvinningsarbete, respektive. Denna ytterligare förfarande-i kombination med en konventionell Coomassie Brilliant Blue färgning-kan användas effektivt för verifiering av assay resultaten (figur 1B).
Analysförfarandet består av enkla, lätt-att-utföra steg i en låg volym-format som kan vara fullt anpassade till en hög genomströmning automatisk miljö. Dock anses självständigt utföra analysen antingen manuellt eller med ett automationssystem, följande delar av analysen vara avgörande och behöver särskild uppmärksamhet medan du utför proceduren. (i) homogenitet av magnetiska pärla lösningen. En homogen magnetiska pärla lösning måste användas under hela analysen, både i rening och tvätt steg. Särskilt, beror tillförlitligheten av proteashämmare analyser starkt på korrekt alikvotering substrat-anslutna magnetiska pärla (SAMB) lager lösningarna. För att öka effektiviteten av indragning och spridning, är det rekommenderat att ställa pärla koncentrationen mellan 2% och 10% (v/v). Under provberedning, användning av buffertar kompletteras med Nonjonaktivt rengöringsmedel (t.ex. Triton x-100 eller Tween 20) upp till 2% kan också minska efterlevnaden av magnetiska pärlor plastytor. Efterlevnaden av pärlor till väggarna i ampuller prov kan undvikas om pärla upphängningarna tillämpas noggrant på bottnarna i injektionsflaskorna i stället för på väggarna i provrör. Homogenitet av magnetiska pärlor under den enzymatiska reaktionen är också kritiska och kan säkerställas genom kontinuerligt skakar proverna vid 600 rpm under inkubation. Pärlor är ordentligt dispergerade i rundade eller flatbottnade plast varor, medan användningen av V-botten injektionsflaskor inte rekommenderas. Ett suboptimala resultat som orsakats av felaktig pärla homogenisering är representerade i figur 4B. (II) upphörande av reaktion prover. En annan fördel med metoden är att den enzymatiska reaktionen kan sägas utan användning av denaturering värmebehandling eller någon potentiellt interfererande kemiska agenser15. Uppsägning kan utföras helt enkelt genom att separera de magnetiska pärlorna från reaktionsblandningen, använda en konventionell magnetiska partikel koncentrator. Medan den borttagna reaktion-bufferten innehåller aktiva enzymet och genererade C-terminala fluorescerande sönderdelningsprodukterna, kvar på uncleaved substrat till pärlorna. Tack vare förekomsten av aktiva enzymet i reaktion bufferten behöver avskiljandetillvägagångssättet utföras noggrant för tillförlitlig slutpunktsidentifiering. Innan placera provet injektionsflaskorna i anrikningsverket, rekommenderas det att tillämpa en kort spin centrifugering. Efter att placera rören i anrikningsverket, tillhandahålla minst 15 s för pärlorna ska samlas in. Liten rörelse av separatorn och tillbaka kan underlätta insamling av pärlorna. Överväg att uppsägning under en manuellt utförd separation, oftast tar längre tid än inledandet av reaktionerna. Därför rekommenderas en cirka 2 min registrerade fördröjning mellan initiationerna om samma inkubationstiden måste tillämpas på alla prover.
Principen beskrivs proteolytiska analysens är relativt enkel; men garanteras mångsidigheten hos systemet av flexibelt och stabilt substrat struktur. Enskilda optimering av analysen kan begränsas endast av affinitet pärlorna förenlighet med de tillämpade villkor, reagenser och tillsatser. I samförstånd med tillverkarens protokollet fann vi också att affinitet bindningen av substrat till Ni-NTA pärla ytbehandlar väsentligen försvagar vid pH ≤ 6,515. Därför rekommenderas att tillämpa substrat tom prover parallellt med reaktion proverna, och frekvensen av spontana substrat dissociation måste beaktas vid utvärderingen av resultaten.
I de fall, där magnetiska-pärla-baserade analyser inte kan utföras på grund av användning av pärla-inkompatibla komponenter eller lågt pH, kan i-lösning rötning av de renade rekombinant substratesna tillämpas också. I dessa fall reaktion blandningarna kan analyseras genom elektrofores, och proteinerna kan visualiseras i gel baserat på protokollet beskrivs. För att undersöka proteolytiska aktivitet, kanske också alternativa verktyg för fluorimetry i i-lösning matsmältningen och i-gel påvisande av proteiner. En nyhet i systemet utformat substrat är tillämpningen av en i-gel utvinningsarbete steg efter denaturering SDS-PAGE. Medan infödda (nondenatured) fluorescerande proteiner behåller sin fluorescens under elektrofores, avskaffas egenskapen fluorescerande vid denaturering (figur 7B). Dock kan fluorescensen av denaturerad proteiner återvinnas delvis genom avlägsnandet av SDS från gelen. Således gör en separation av reaktion komponenter med denatureringen villkor inte bara den fluorescens-baserade men molekylär-vikt-baserade identifiering möjligt. En annan fördel med fluorescerande i-gel upptäckt jämfört med analysen av en Coomassie-färgade gel är att de (native eller renatured) fluorescerande proteinerna lätt kan identifieras i gel baserat på deras fluorescens (se figur 7). Detta kan vara viktigt om klyvning reaktioner utförs på prover som innehåller nonfluorescent föroreningar eller proteiner som mycket liknar molekylvikt av varandra.
Proteas analyser använder Likaså utformade substrat har redan tidigare publicerade8,9,10, och även om webbplatsen klyvning av intresse i de fall var också ligger mellan en affinitet-tagg och en fluorescerande protein, assay systemet presenteras här upprepar inte endast de beskrivna idéerna men kombinerar olika fördelarna med tidigare plattformar och också kompletterar dem med ytterligare förbättringar: i) utnyttjandet av en MBP fusion partner, ii) de förekomsten av en TEV PR kontroll klyvning webbplats, iii) användningen av nyutvecklade monomer FPs, och iv) tillämpningen av en unik substrat kalibreringen. Analysen själv var särskilt utformad för att vara användbar för enzym specificitet och kinetiska studier i en säker, tids – och kostnadseffektiva sätt, utan behov av dyra instrumentering. Metoden syftar till att vara en lämplig och prisvärd verktyg för både industriell och akademisk forskning. På grund av flexibiliteten i ‘kloning kassett’ av uttrycket plasmiden, kan systemet vara lämpliga för snabb och billig generering av rekombinant substrat bibliotek. Häri beskrivna analysen är ett möjligt verktyg för genomförandet av substrat specificitet, enzym mutagenes, och hämning studier och även ge ett alternativt verktyg för att utföra enzymkinetik. Assay plattformen (från bakteriell cell störningar vid fastställandet av de kinetiska parametrarna) kan anpassas till en HTS – och automation-baserad miljö och, eventuellt, kan tillämpas i industriella proteas hämmare screening eller antivirala läkemedel utveckling. Anpassning av analysen för konkurrenskraftiga proteolys är dessutom även i framtiden omfattningen av vårt laboratorium. I en sådan konkurrenskraftiga analys, två olika substrat-varje innehållande en olika klyvning webbplats smält till en olika C-terminala fluorescerande tagg-är avsedda att användas samtidigt i samma klyvning reaktion för att undersöka preferensen av den studerade enzymet för givet mål sekvenser. Dessutom är användningen av en 96-well plate-anpassade assay form (figur 8) också att vara optimerad för mutation screening med hjälp av en rad substrat med modifierade klyvning webbplats sekvenser vid cysteinproteaser.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Detta arbete var stöds delvis av projektet ”PHARMPROT teaming” GINOP-2.3.2-15-2016-00044 och dessutom finansieras av högre utbildning institutionella Excellence programmet av ministeriet för mänskliga kapacitet i Ungern, inom ramen för den Bioteknik tematiska program av den Debrecens universitet. Författarna är tacksamma för medlemmarna i laboratorium av retrovirala biokemi för deras vetenskapliga hjälp under assay utvecklingen och även för deras tålamod under inspelningen analysen (särskilt till Norbert Kassay, Krisztina Joóné Matúz och Vanda Toldi, som dyker upp i bakgrunden i videon). Författarna vill även säga speciellt tack vare Gedeon Richter Plc., särskilt till Dr Zoltán Urbányi för att tillåta Beáta Bozókis arbete i Institutionen för biokemi och molekylärbiologi som gästforskare. Författarna vill också utöka sin tacksamhet till György Zsadányi, Balázs Tőgyi, Balázs Pöstényi och Zoltán Király från Multimedia och E-learning Technical Center av den Debrecens universitet för den professionella hjälpen som ljud och video produktion.
Materials
| 10K Amicon tubes | Merck-Millipore | UFC501096 | |
| 2-Mercaptoethanol (β-ME) | Sigma-Aldrich (St Louis, MO, USA) | M6250 | |
| 40% Acrylamide/Bis solution 37.5:1 | Bio-Rad | 1610148 | |
| Acetic acid | Merck | 100063 | |
| Agarose | SERVA | 11404.04 | |
| Alpha Imager HP gel documentation system | ProteinSimple | ||
| Ammonium persulfate (APS) | Sigma-Aldrich (St Louis, MO, USA) | A3678 | |
| Ampicillin sodium salt | Sigma-Aldrich (St Louis, MO, USA) | A9518 | |
| Beckman Coulter Allegra X-22 centrifuge | Beckman Coulter | 392185 | |
| Black half-area plates | Greiner bio-One | 675086 | |
| Bromophenol blue | Sigma-Aldrich (St Louis, MO, USA) | B0126 | |
| CutSmart buffer (10x) | New England Biolabs | B7204S | For plasmid linearization (step 1.1.1) |
| Dark Reader transilluminator | Clare Chemical Research | DR-45M | |
| DNase I | New England Biolabs | M0303L | |
| Dynamag-2 magnetic particle concentrator | Thermo Fischer Scientific | 12321D | |
| Escherichia coli BL21(DE3) competent cells | Thermo Fischer Scientific (Invitrogen) | C600003 | |
| Ethanol | Merc-Millipore | 100983 | |
| Ethylenediaminetetraacetic acid (EDTA) | Sigma-Aldrich (St Louis, MO, USA) | 798681 | |
| Gel Loading Dye, Purple (6X) | New England Biolabs | B7024S | |
| Glycerol | Merck | 356350 | |
| Glycine | Sigma-Aldrich (St Louis, MO, USA) | G7126 | |
| High-Speed Plasmid Mini Kit | GeneAid | PD300 | |
| Imidazole | Sigma-Aldrich (St Louis, MO, USA) | 56750 | |
| Isopropyl β-D-1-thiogalactopyranoside (IPTG) | Thermo Fischer Scientific (Invitrogen) | AM9464 | |
| Jouan CR 412 centrifuge | Jouan | CR412 | |
| Labinco LD-76 Rotator | Labinco | 7600 | |
| Luria-Bertani (LB) broth | Sigma-Aldrich (St Louis, MO, USA) | L3022 | |
| Lysozyme | Sigma-Aldrich (St Louis, MO, USA) | L6876 | |
| Magnesium chloride | Scharlau | MA0036 | |
| MERCK eurolab ultrasonic bath | MERCK | USR54H | |
| Millifuge Eppendorf spin centrifuge | Millipore | CT10 | |
| Mini-PROTEAN 3 Electrophoresis Cell | Bio-Rad | ||
| N,N,N′,N′-Tetramethylethylenediamine (TEMED) | Sigma-Aldrich (St Louis, MO, USA) | T9281 | |
| NanoDrop 2000 | Thermo Fischer Scientific | ||
| NheI-HF restriction endonuclease | New England Biolabs | R3131L | |
| Nickel(II) sulfate (NiSO4) | Sigma-Aldrich (St Louis, MO, USA) | 656895 | |
| Ni-NTA magnetic agarose beads | Qiagen | 36113 | |
| Orbital shaker | Biosan | OS-20 | |
| PacI restriction endonuclease | New England Biolabs | R0547L | |
| PageBlue Protein Staining Solution | Thermo Fischer Scientific | 24620 | |
| Phenylmethanesulfonyl-fluoride (PMSF) | Sigma-Aldrich (St Louis, MO, USA) | P7626 | |
| Protein Lobind Micro-centrifuge tubes | Eppendorf | 22431102 | |
| QIAquick Gel Extraction Kit | QIAGEN | 28704 | |
| Snijders Press-to-Mix shaker | Gemini | 34524 | |
| Sodium-acetate trihydrate | Sigma-Aldrich (St Louis, MO, USA) | S7670 | |
| Sodium-chloride | Sigma-Aldrich (St Louis, MO, USA) | S9888 | |
| Sodium-hydroxide | Sigma-Aldrich (St Louis, MO, USA) | S5881 | |
| SYBR Green I Nucleic Acid Gel Stain | Thermo Fischer Scientific | S7563 | |
| T4 DNA ligase | Promega | M180A | |
| Thermo shaker | Biosan | TS-100 | with SC-24 accessory block |
| Tris | Sigma-Aldrich (St Louis, MO, USA) | T1503 | |
| Tween 20 | Sigma-Aldrich (St Louis, MO, USA) | P2287 | |
| WALLAC VICTOR2 1420 multilabel counter | Wallac Oy, Turku, Finland |
References
- Meldal, M. Smart Combinatorial Assays for the Determination of Protease Activity and Inhibition. Molecular Informatics. 24 (10), 1141-1148 (2005).
- Rao, M. B., Tanksale, A. M., Ghatge, M. S., Deshpande, V. V. Molecular and biotechnological aspects of microbial proteases. Microbiology and Molecular Biology Reviews. 62 (3), 597-635 (1998).
- Zhang, G., Sittampalam, G. S., et al. Protease assays. The Assay Guidance Manual. , (2012).
- Woelcke, J., Hassiepen, U., Chen, T. Fluorescence-based biochemical assay formats. A Practical Guide to Assay Development and High-Throughput Screening in Drug Discovery. , (2010).
- Richardson, P. L. The determination and use of optimized protease substrates in drug discovery and development. Current Pharmaceutical Design. 8 (28), 2559-2581 (2002).
- Diamond, S. L. Methods for mapping protease specificity. Current Opinion in Chemical Biology. 11 (1), 46-51 (2007).
- Schilling, O., Overall, C. M. Proteome-derived, database-searchable peptide libraries for identifying protease cleavage sites. Nature Biotechnology. 26 (6), 685-694 (2008).
- Askin, S. P., Morin, I., Schaeffer, P. M. Development of a protease activity assay using heat-sensitive Tus-GFP fusion protein substrates. Analytical Biochemistry. 415 (2), 126-133 (2011).
- Chaparro-Riggers, J. F., Breves, R., Michels, A., Maurer, K. H., Bornscheuer, U. A GFP based assay for the determination of hydrolytic activity and substrate specificity of subtilisins under washing conditions. Journal of Molecular Catalysis B: Enzymatic. 35, 74-77 (2005).
- Patel, D., Frelinger, J., Goudsmit, J., Kim, B. In vitro assay for site-specific proteases using bead-attached GFP substrate. Biotechniques. 31 (5), 1194-1198 (2001).
- Branchini, B. R., et al. Sequential bioluminescence resonance energy transfer-fluorescence resonance energy transfer-based ratiometric protease assays with fusion proteins of firefly luciferase and red fluorescent protein. Analytical Biochemistry. 414 (2), 239-245 (2011).
- Zhou, C., Yan, Y., Fang, J., Cheng, B., Fan, J. A new fusion protein platform for quantitatively measuring activity of multiple proteases. Microbial Cell Factories. 13 (1), 44 (2014).
- Fox, J. D., Waugh, D. S. Maltose-binding protein as a solubility enhancer. Methods in Molecular Biology. 205, 99-117 (2003).
- Bozóki, B., et al. A recombinant fusion protein-based, fluorescent protease assay for high throughput-compatible substrate screening. Analytical Biochemistry. 540-541, 52-63 (2018).
- Mótyán, J. A., Miczi, M., Bozóki, B., Tözsér, J. Data supporting Ni-NTA magnetic bead-based fluorescent protease assay using recombinant fusion protein substrates. Data in Brief. 18, 203-208 (2018).
- Balleza, E., Kim, J. M., Cluzel, P. Systematic characterization of maturation time of fluorescent proteins in living cells. Nature Methods. 15, 47-51 (2018).
- Hebisch, E., Knebel, J., Landsberg, J., Frey, E., Leisner, M. High variation of fluorescence protein maturation times in closely related Escherichia coli strains. PLoS One. 8, e75991 (2013).
- Kapust, R. B., et al. Tobacco etch virus protease: mechanism of autolysis and rational design of stable mutants with wild-type catalytic proficiency. Protein Engineering, Design and Selection. 14, 993-1000 (2001).

