Laser induceret fluorescens emission (L.I.F.E.) som et nyt ikke-invasivt værktøj til in-situ-målinger af biomarkører i Kryosfæske habitater
Summary
Kulstof strømme i kryosfæren er næppe vurderet endnu, men er afgørende for klimaændringer. Her viser vi en roman prototype enhed, der fanger det foto trofiske potentiale i supraglacial miljøer baseret på Laser-induceret fluorescens emission (L.I.F.E.) teknologi tilbyder høj spektral og rumlig opløsning data under in situ betingelser.
Abstract
Den globale opvarmning påvirker mikrobielle samfund i en række økosystemer, især kryosfæske habitater. Men, lidt er kendt om mikrobielle-medierede Carbon flusmidler i ekstreme miljøer. Den metode til erhvervelse af prøver, der er beskrevet i de meget få tilgængelige undersøgelser, indebærer således to store problemer: A) data med høj opløsning kræver et stort antal prøver, hvilket er vanskeligt at opnå i fjerntliggende områder; B) uundgåelige prøve manipulation såsom skæring, savning og smeltning af iskerner, der fører til en misforståelse af in situ betingelser. I denne undersøgelse præsenteres en prototype anordning, der hverken kræver prøveforberedelse eller prøve destruktion. Anordningen kan anvendes til in situ-målinger med en høj spektral og rumlig opløsning i terrestriske og isøkosystemer og er baseret på den Laser-i-producerede Fluorescens E-mission (L.I.F.E.) teknik. Fotoautotrofisk supraglacial samfund kan identificeres ved påvisning af L.I.F.E. signaturer i photopigments. Den L.I.F.E. instrument kalibrering for porfyrin derivater klorofyla (CHLa) (405 nm laser excitation) og b-phycoerythrin (b-PE) (532 nm laser excitation) er påvist. Til validering af denne metode blev L.I.F.E. data ratificeret ved en konventionel metode til at kvantificereen kvantitativ bestemmelse, der involverede pigment ekstraktion og efterfølgende absorption spektroskopi. Prototypen anvendelighed i marken blev bevist i ekstreme Polar miljøer. Yderligere testning på terrestriske habitater fandt sted under Mars ‘ analoge simuleringer i den marokkanske dessert og på en østrigsk klippe gletscher. L.I.F.E. instrumentet muliggør scanninger i høj opløsning af store områder med acceptabel drifts logistik og bidrager til en bedre forståelse af det økologiske potentiale i supraglacial samfund i forbindelse med globale forandringer.
Introduction
Kryofæren huser havis, gletsjere, høje bjergsøer, sneområder, issø, Smelt vands vandløb og permafrost. Disse områder dækker ca. 11% af jordens landmasser1,2og er over hvælvede af atmosfæren som et anerkendt kryosfæisk miljø. Nylige undersøgelser viser, at massive områder af cryosfæren hurtigt trækker sig tilbage3,4. Den Antarktis5,6, Alperne7, Polar8, og andre regioner viser negative ismasse balancer. Tilbagetrækningen af iskapper og gletsjere fører til nedbrydningen af vores største ferskvandsreservoir på jorden. I nogle områder er Glacier Retreat ustoppelig5.
I lang tid blev isøkosystemer betragtet som sterile miljøer. Men på trods af barske forhold er tilstedeværelsen af aktivt liv i Jordens kryosfæren tydelig9,10,11,12,13,14,15 . På grund af tendensen til massive tab af is ved smeltning, er kryosfæren gennemgår et skift i biologisk aktivitet, der påvirker tilstødende habitater. For at forstå disse delvist uigenkaldelige ændringer kræver vi metoder til at undersøge biologisk aktivitet i is under in situ-forhold med høj rumlig og tidsmæssig opløsning.
I supraglacial miljøer, kan livet findes i cryoconite huller, snedække, smeltet vand, vandløb, og på bare is overflader. Men de mest indlysende supraglacial habitater er cryoconite huller. De optræder globalt i glacierede miljøer og blev først beskrevet af den svenske opdagelsesrejsende Adolf Erik Nordenskjold under en ekspedition til Grønland i 1870 ‘ erne16,17. Navnet stammer fra det græske ord “kryos” (kold) og “Konia” (støv). De Lipariske afledte mørke organiske og uorganiske rester fastgøres på isoverfladen og reducerer albedo lokalt. Solstråling fremmer smeltning af snavs i dybere islag, danner cylindriske bassiner med sediment (cryoconite) i bunden9. Cryoconite huller dækker 0,1-10% af glacial ablation zone11.
Cryoconite samfund består af vira, svampe, bakterier, cyanobakterier, mikroalger, og protozoer. Afhængigt af regionen kan der også findes metazoiske organismer som rotifers, nematoder, copepod’er, tardikvaliteter og insektlarver. Edwards og andre18 beskrive cryoconite huller som “iskold hotspots”. De har også sporet funktionelle gener i cryoconite huller, der er ansvarlige for N, fe, S og P cykling. Mini Lake økosystemer respire og fotosyntetisere ved satser fundet i meget varmere og mere næringsrige levesteder11. Disse fund understreger den vigtige rolle, som mikrobiel binding i supraglaciale miljøer spiller. Ved siden af levende samfund i kryoconite huller, er bare is overflader beboet af is alger. Deres fysiologi er godt undersøgt19 men deres rumlige fordeling er ikke blevet vurderet20. Deres tilstedeværelse i supraglaciale miljøer mindsker albedo og fremmer dermed smeltning, der fører til et næringsstof udad og næringsstoftilførsel til downstream-habitater9. Stigende temperaturer og dermed en højere tilgængelighed af flydende vand, påvirker netto økosystemets produktivitet i disse iskolde økosystemer.
I supraglaciale miljøer omdanner fotosyntetiske aktive organismer uorganisk kulstof og nitrogen til organiske, tilgængelige kilder til den mikrobielle fødevare web21,22. Indtil nu er der få undersøgelser, der estimerer supraglacial Carbon flusmidler11,20,23. Forskellen i foreslåede satser for kulstof flux skyldes en lav rumlig og tidsmæssig dataopløsning. Endvidere vurderes den rumlige fordeling af supraglaciale samfund uden for cryoconite-hullerne næppe. Cook og andre20 forudsagt i deres modeller, at supraglacial alge samfund Fix op til 11x mere kulstof end moderne cryoconite huller på grund af deres store overflade dækning. Påvisning af supraglaciale alge samfund, der sikrer prøvens integritet, hæmmes stadig på grund af manglende værktøjer til påvisning og kvantificering på stedet.
Som reaktion på vanskelighederne i logistikken undersøger isøkosystemerne mindre hyppigt end habitater i tempererede områder. Data opløsningen afhænger af antallet af vurderede prøver og afhænger af tilgængeligheden af forsøgs stederne. Standard prøvetagningsmetoder såsom savning, Coring og efterfølgende smeltning involverer manipulation af det mikrobielle samfund. For eksempel er klorofyla (CHLa) vurdering i faste isprøver umulig med standardmetoder uden væsentlig interferens. Derfor er smelte inducerede temperaturændringer inden for de undersøgte mikrobielle samfund uundgåelige. Som reaktion på den termiske evne af photosystem II og andre cellulære strukturer i psychrophiles22, laboratorieanalyser af smeltede is prøver vil altid føre til en forfalskning af in situ betingelser.
Ikke-destruktive in situ-målinger er den eneste fornuftige måde at opnå pålidelige data på. Dette mål kan opnås ved hjælp af fluorescens-baserede metoder. På grund af deres lette høst funktion er CHLa og b-phycoerythrin (b-PE) til stede i organismer, der bidrager til kulstofkredsløbet i supraglaciale miljøer, som det er bevist af anesio og andre11. Derfor er disse fluorescerende molekyler egnede biomarkører til kvantificering af mikrobielle medierede kulstof strømme i isøkosystemer.
I denne undersøgelse præsenterer vi udvikling, kalibrering og anvendelighed af et nyt ikke-invasivt værktøj til in situ-kvantificering af CHLa -og B-PE-molekyler i terrestriske og isøkosystemer. Prototypen enhed er baseret på Laser-induceret fluorescerende emission, også kendt som L.I.F.E. Det optiske instrument (figur 1) indfanger fluorescerende biomarkør-signaturer efter Laser induceret fluorescens excitation. Proceduren er ikke-destruktiv og kan udføres på forsøgsstedet eller i et laboratorium.
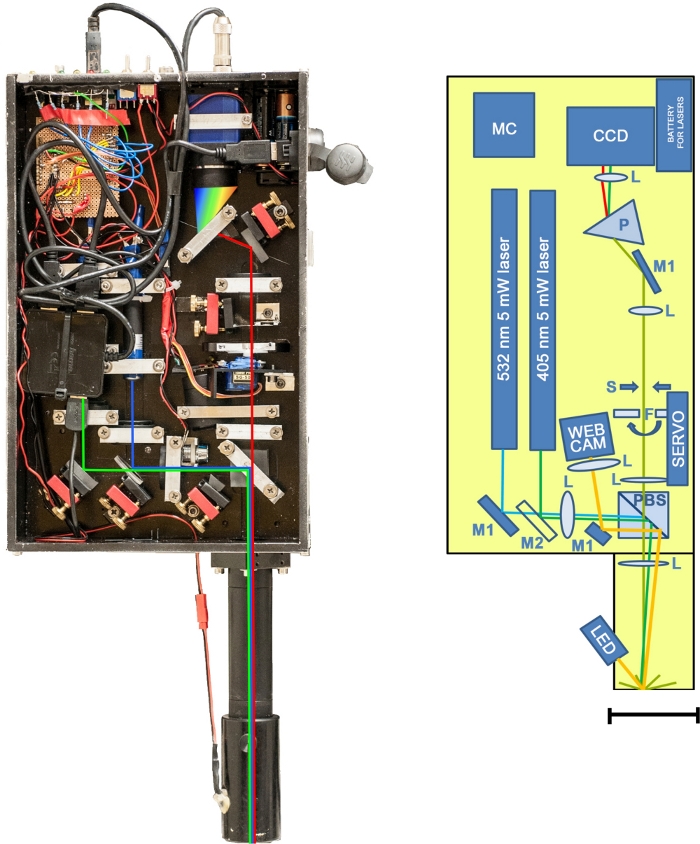
Figur 1: L.I.F.E. prototype. Venstre: Billede af instrumentet uden beskyttende låg. Højre: Skematisk illustration af instrumentet. Total masse = 5,4 kg (laser og optik = 4,025 kg, laptop = 1,37 kg). Aluminiumsstel = 32,5 cm x 20,3 cm x 6,5 cm. optisk rør: 18,4 cm x 4 cm (diameter). CCD: Bluefox mv220g sensor; F: servo-styrede lang-pass filtre (450 Nm og 550 nm); L: optiske linser; M1: spejle; M2: koldtlysreflektorlamper spejl; MC: microcontroller; P: prisme; PBS: polariserende stråle splitter; S: slids blænde lavet af justerbare barberblade. Scale bar = 70 mm. Klik her for at se en større version af dette tal.
Det bærbare Dual-bølgelængde kit vejer 4,5 kg og bruges på et stativ i kombination med en ekstern computer. Felt opsætningen er hurtig og nem. Instrumentet er fastgjort til stativet, og objektiv røret er fastgjort til enheden sammen med et USB-kabel og kamerakablet. Den eksterne computer er sluttet til instrumentet ved hjælp af et USB-kabel. Stativ benene justeres på en sådan måde, at linse røret er rettet mod og dækker prøven. Derefter rammer en 5 mW grøn laser prøven efter at have passeret en polariserende stråle splitter, der omdirigerer polariseret lys mod spektrometrets optiske akse. Præparatet udviser et fluorescerende lys, illustreret med rødt i figur 1. Halvdelen af det kollimerede lys passerer polariserende stråle splitter og er fokuseret gennem et servostyret langpasfilter, der fjerner laser signalerne. Dernæst rammer signalet en blænde spalte, der består af to justerbare barberblade. En prisme adskiller den fine linje af lys retvinklede til spalteåbningen, før signalet optages af sensoren. Proceduren gentages med en blå laser. De rå data overføres automatisk til en bærbar computer, der også bruges til software drift.
Instrumentet styres af en ekstern computer ved hjælp af et LabVIEW-miljø, der synkroniserer billed-tage med CCD-kameraet, tænde/slukke lasere, og rotere Long-pass filter hjulet. Den grafiske brugergrænseflade (GUI) er inddelt i tre hovedsektioner. Eksponerings justeringen udføres manuelt. Selv om korrektionen mellem eksponeringstid og signalintensitet er lineær (figur 2b), er den maksimale eksponeringstid begrænset til 10 s, fordi længere integrationstider fører til et signifikant fald i signal-til-støj-forholdet. Feltet bemærkning bruges til beskrivelsen af eksemplet (figur 2a). I højre sektion vises RAW-billeder, så snart målingerne er færdige. Denne funktion er afgørende for øjeblikkelig dataevaluering i marken (figur 2C – E). Røde områder indikerer overeksponerede pixels, hvilket kan undgås ved at reducere eksponeringstiden.
Den efterfølgende rå data reduktion proces er afkoblet fra billedet erhvervelse procedure og kan gøres på ethvert tidspunkt efter billed erhvervelse.
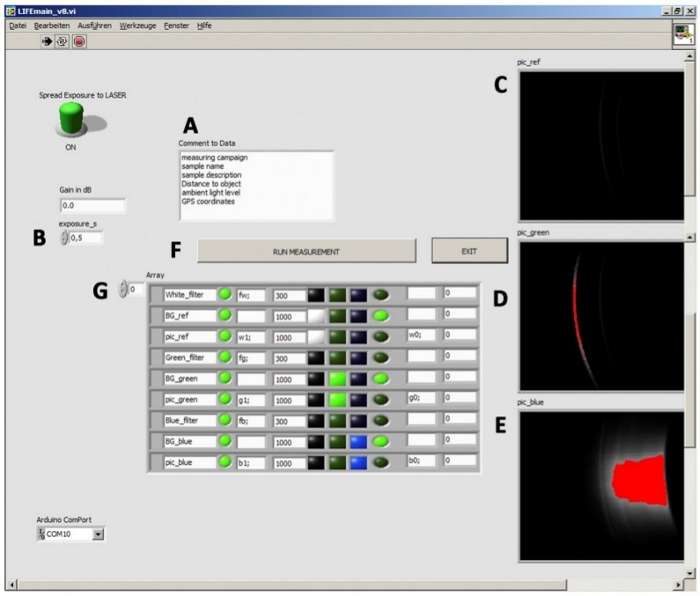
Figur 2: L.I.F.E. grafisk brugergrænseflade til dataindsamling og rå dataevaluering. (A) softwaren muliggør manuel tekstindtastning for eksempel beskrivelser. B) eksponeringstiden kan justeres før målingen. (C − E) De rå billeder vises i højre side af grænsefladen. (E) røde farver indikerer en mætning af sensoren. (F) aktiveringen af knappen Run-måling udløser dataindsamlings processen. I matrixen (G) vises alle kommandoer, der udføres automatisk under dataindsamlingen. Venligst klik her for at se en større version af dette tal.

Figur 3: eksempel på et RAW-billede. Venstre: Rå data af CHLen standard i acetone opløsning, indspillet med L. I. F. E instrumentet. På grund af enhedens optiske egenskaber vises signalet som en skæv linje. Højre: Fortolkning af RAW-billedet pr. pixel (px). Spektral aksen (5 nm/px opløsning) afbildes mod den rumlige akse (30 μm/px opløsning). Venligst klik her for at se en større version af dette tal.
De 12-bit gråskala-RAW-billeder viser en rumlig komponent på grund af den endimensionale blænde spalte og en spektral komponent på grund af prisme foran CCD (figur 3). Som reaktion på optiske begrænsninger er de rå billeder forvrænget. Derfor, de har brug for at blive beskåret og genoprettet ved at anvende en kode, der anerkender graden af forvrængning. Dette gøres med en software Wizard (figur 4). Dernæst er bølgelængden kalibrering udført med 532 nm laser. Det grønne lys er produceret ved frekvens fordobling af en 1.064 nm infrarød laser. Begge bølgelængder kan påvises ved CCD, og derfor kan den spektral position af hver pixel beregnes automatisk i genoprettet billeder (figur 4).
Billedet beskæres derefter ned til et givet bølgelængde område (550 – 1000 nm for grønne laser målinger og 400 – 1000 for blå laser målinger). Grå værdier fra hver pixel i en valgt pixel linje tælles og opsummeres. En grå værdi kan være mellem 0 – 255. Derefter tegner hver pixel linje sig for ét tal. Yderligere skærm software instruktioner fører til generering af et plot, der viser den grå værdi tæller fra hver pixel linje plottet mod de rumlige koordinater. Dette giver mulighed for en kvantitativ geografisk forskelsbehandling af CHLa og B-PE samtidig i stikprøven. Desuden kan de spektrale egenskaber for en prøve afbildes fra udvalgte pixel linjer automatisk.
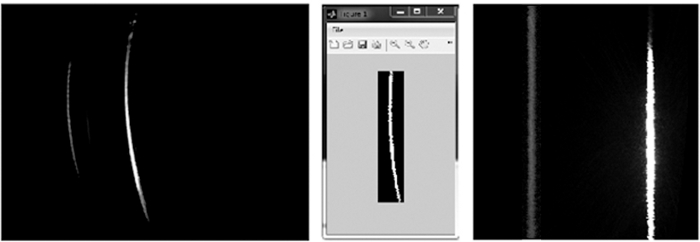
Figur 4: Dewarping RAW-billeder. Venstre: RAW-billede taget med en grøn laser. Der blev ikke brugt noget filter. Signalerne vises ved 532 nm og 1.064 nm. Eksponeringstid = 0,015 s. Center: det beskårne 532 nm-signal bruges som referencelinje til at dewarp et sæt billeder. Højre: Det genoprettet billede fra RAW-billedkilden. Venligst klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Kalibrering
Der var en lineær korrelation mellem pigment koncentrationen og fluorescens intensiteten efter normalisering af foton tællinger til en eksponeringstid på 1 s. prøver med lav kolonne højde og lave pigment koncentrationer førte til en overvurdering af målpigmenterne, sammenlignet med højere kolonne højder med samme pigment koncentration. Yderligere svage fluorescens signaler krævede lange eksponeringstider for tilstrækkelig foton tæller på sensoren. Men lange integrationstider øgede også mængden af omstrejfende lys på sensoren, hvilket resulterede i et fald i signal-til-støj-forholdet. I sin nuværende version kan softwaren ikke skelne mellem støj og signal under data reduktions processen. Derfor førte lave målinger af fluorescens intensitet til en pigment overvurdering, fordi støj blev regnet som et signal, der stammer fra målpigmenterne. Desuden viste fluorescens intensiteter fra mere koncentrerede pigment opløsninger en større variation end lavkoncentrations opløsninger. Denne effekt kan forklares ved absorptions processer inden for de pigment opløsninger, der blev anvendt til kalibreringskurven.
Data validering for klorofylen kvantificering
Efter filtrering af is-og sneprøver optrådte de tredimensionale prøver næsten som en todimensionel prøve på filteret. Dette begrundede en direkte sammenligning mellem L. I. F. E (areal tæthed) og spektrofotometriske data (volumetrisk måling).
Datasættet (figur 8) indikerede, at høj pigment koncentration fører til en undervurdering, hvorimod lav pigment koncentration fører til en overvurdering af den faktiske værdi. Denne effekt kan forklares ved tykkelsen af filterkagen og dermed den volumetriske karakter af prøven. Laser indtrængnings dybden afhang af prøvens optiske tæthed og tykkelse. Højt pigment indhold blev undervurderet, fordi laseren ikke kunne fremkalde pigment fluorescens i dybere lag. Men i tynde filterkager, lav fluorescens signaler blev fanget på grund af lav areal tætheder af pigmenter. Tilsyneladende, filteret selv viste Laser-induceret signaler efter passerer 450 Nm lang-pass filter (figur 12). Dette signal blev fejlagtigt talt som fluorescens signal afledt af CHLa. Derfor er tynde og for tykke filterkager svære at måle med L.I.F.E. instrumentet.
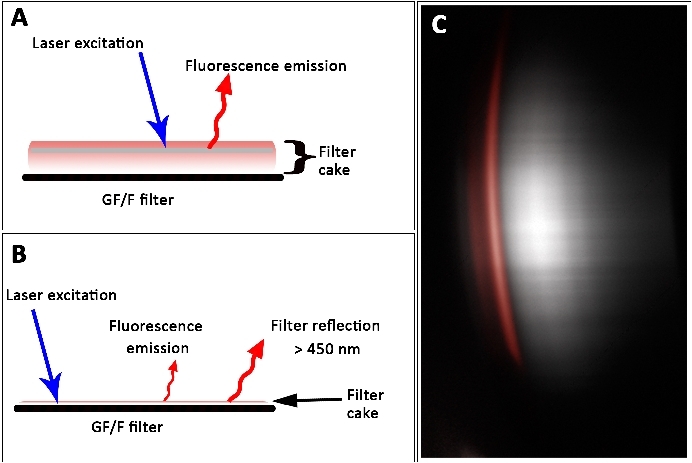
Figur 12: fluorescens signaler fra tykke (A) og tynde (B) filterkager på et GF/F-filter. (A) selv-skygger forhindrer Laser-induceret fluorescens fra dybere lag, hvilket resulterer i en undervurdering af den faktiske pigment koncentration. B) Fluorescens emission fra filterkage med overlay ved filter refleksioner. (C) rå data viser filter refleksion (grå). Den spektral egenskab af et laboratorium afledt CHLet fluorescens mønster er illustreret med rødt. Scale bar = 45 mm. Klik her for at se en større version af dette tal.
Begrænsninger af L.I.F.E. prototype
Under data reduktion fortolkede MATLAB-kodet software de rå billeder ved at opsummere pixel linjer inden for et givet bølgelængde område. Den nuværende version af softwaren skelner ikke mellem organiske og uorganiske afledte signaler. Tilstedeværelsen af flere signaler kan føre til en overvurdering af det faktiske pigment indhold. Lange eksponeringstider på grund af lave fluorescens intensiteter medførte et fald i signal-støj-forholdet, hvilket fremmer effekten som beskrevet ovenfor (Se figur 8 og figur 12).
En Geode klippe vist i Figur 13 udviste rødt fluorescerende lys, når den blev eksponeret med grønt og blåt lys. I øjeblikket er det ikke klart, om fluorescensen skyldes mineraler eller fra Porphyrin-baserede molekyler. En overlejring af biologiske og ikke-biologiske signaler kan derfor begrænse anvendelsen af denne metode og kræve, at der oprettes en fluorescens database, der er specielt fremstillet til L.I.F.E. prototypen.
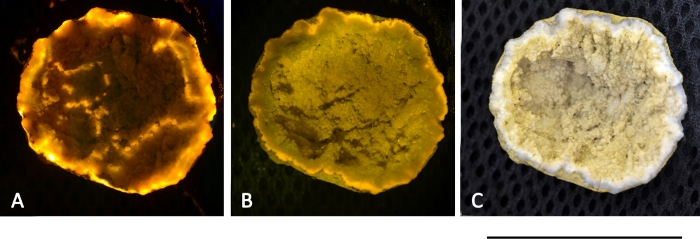
Figur 13: mineralsk fluorescens fra en Geode klippe, fundet i ny-Ålesund. Klippen var spændt med en 532 nm 50 mW Laser (a) og en 405 nm 50 mW Laser (B). Begge billeder blev taget med et polariseringsfilter, der var fastgjort på objektivet, hvilket førte til en forfalskning af de faktiske fluorescens farver. (C) ægte farvebillede uden brug af et polariseringsfilter under dagslysforhold. Scale bar = 40 mm. Klik her for at se en større version af dette tal.
Beutler og andre29 konkluderede, at karakteristiske emissions spektre for cyanobakterier i marine økosystemer afhænger af miljøforholdene. Metaboliseringstilstanden har også indvirkning på fluorescens egenskaberne i fototrofiske organismer30. Instrumentet L. i. F. E kan skelne mellem det alge-og cyanobakteriale fluorescens mønster ved at anvende bio-fingeraftryks biblioteker, der indeholder spektral information af præparatet, som er korreleret med miljøforhold.
I mørke-tilpassede CHLa -molekyler er alle reaktions Centre fuldt oxideret og tilgængelige for fotokemi, og intet fluorescens udbytte slukkes31. Ved hjælp af L.I.F.E. procedure, en prøve er først ophidset af en 532 nm laser (grøn) og derefter med en 405 nm laser (blå). Under den anden excitation af den blå laser, kan CHLa vise en nedsat fluorescens respons på grund af tidligere excitation af den grønne laser. CHLa absorberer energi ved 532 nm bølgelængde, på trods af sin afstand fra sin absorption maksimale bølgelængde32. Før den faktiske CHLa måling ved 405 nm, kan den grønne laser forårsage foto kemiske reaktioner, aktivere dæmpning mekanismer i målpigmenter. Desuden førte præ-belysning af marine fototrofiske organismer ikke til en ændring i spektral norm kurver mellem 450 Nm – 600 nm, mens standardafvigelsen i fluorescens intensiteter steg med 25%29. Afhængigt af arten, fluorescens intensiteter endda steget som reaktion på tidligere excitation. Dette emne kræver yderligere undersøgelser.
Anvendelighed
Vi testede L.I.F.E. instrumentet i forskellige habitater med vægt på cryoconite huller. Laseren blev anvendt med succes i jord og biofilm habitater på grund af fraværet af omgivende lys under målingen. Kryoconitgranulat kunne måles, når sediment lagene blokerede lys under hullet (figur 14a,C). Tynde sediment kryoconite huller var gennemtrængelig for Stray lys nedefra (figur 14b). Omstrejfende lys interfererer med målingen. Således er pigment koncentrationen i nøgne isoverflader ikke målbare under dagslysforhold endnu. Signal behandling indsats er i øjeblikket undervejs for at muliggøre driften af systemet i høj omgivende lysforhold.

Figur 14: Cryoconite hul med flydende vand på toppen. A) kryoconite på gletscher med L.I.F.E. linse slange. Scale bar = 70 mm. (B) sediment laget (rødt) er meget tyndt. Stray lys blødes gennem cryoconite lag. (C) sediment laget er tykt nok til at blokere det omstrejfende lys nedefra. Denne type cryoconite hul er målelige med L.I.F.E. instrumentet. Venligst klik her for at se en større version af dette tal.
Afslutningsvis, vores L.I.F.E. instrument detekterede fotoautotrofe organismer i terrestriske habitater såsom jord, bakterielle måtter, biofilms, og i cryoconite huller på glaciale overflader. Målmolekylerne var CHLa og B-PE. Den rumlige opløsning var 30 μm/px. Detektionsgrænsen for CHLa var 250 pg/ml og 2 ng/ml for B-PE. Efter en laboratorie kalibrering var vi i stand til at kvantificere pigment indholdet i prøver, der blev indsamlet på vores studiested i Arktis. Vi anvendte selv programmeret software til en automatiseret data reduktion proces. Virkningerne af tilstedeværelsen af mineraler og skiftende lysforhold under målingerne kræver yderligere undersøgelse.
Med klimaopvarmningen fører stigende temperaturer til øget tilgængelighed af flydende vand, hvilket resulterer i højere biologisk aktivitet på iskolde overflader af autotrofisk og heterotrofisk natur. Der bør gøres en energisk indsats for at påvise heterotrofisk organismer på stedet for at give et fuldstændigt billede af det aktive liv i kryosfæren. Dette kunne testes med andre målpigmenter og passende laser excitation bølgelængder. Derfor giver L.I.F.E. et passende overvågningssystem, der giver høj tidsmæssig og rumlig opløsning til supraglaciale forhold i sammenhæng med globale forandringer samt mulige astrobiologiske applikationer.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne takker taknemmeligt oberst (IL) J.N. Pritzker, Tawani Foundation, USA, det østrigske Forbundsministerium for videnskab, forskning og økonomi (funklende videnskab SPA04_149 og SPA05_201), alpine Forschungsstelle Obergurgl (AFO), det østrigske rumfarts forum ( ÖWF), romersk Erler fra Hintertuxer natur EIS Palast, den østrigske Forbunds skov-og base Manager Nick Cox fra Arktisk Station i ny Alesund (Svalbard). Vi er også i gæld til Sabrina obwegeser, Carina Rofner, og Fabian Drewes for deres hjælp under optagelserne. Endelig vil vi gerne takke James Bradley for at give stemmen til den samtidige video.
Materials
| aceton | Merck | 67-64-1 | |
| B-Phycoerythrin | Invirtrogen | P6305 | |
| Chlorophyll a standard | Sigma-Aldrich | C6144-1MG | |
| formaline | Merck | HT501128 | 36% |
| GF/C filters | Whatman | WHA1822025 | 25mm diameter |
| HCl | Merck | H1758 | 36,5-38% |
| L.I.F.E. Prototype | University of Innsbruck | built on demand | |
| LabView | National Instruments | Software, Laboratory Virtual Instrumentation Engineering Workbench | |
| Leucine, L-[4,5-3H], 1 mCi | Perkin Elmer | NET1166001MC | radioactive |
| Liquid scintillation cocktail Beckman Ready Use | Beckman | not more available, can be compensated by Ultra Gold, Packard | |
| liquid scintillation counter | Beckman | out of stock | LSC 6000 IC |
| NaH14CO3 (4 µCi/ml) | DHI Denmark | 4 μCi/ml, 1 ml | radioactive |
| Osmonics polycarbonate filters | DHI Denmark | PCTE | 25mm diameter, 0,2µm pore size |
| Polyscintillation vials | Perkin Elmer | WHA1825047 | 20ml |
| sample tubes | Sigma Aldrich | T2318-500EA | Greiner centrifuge tubes, 50ml |
| Spectrophotometer | Hitachi | NA | Model U2001, any photometer for absorption spectroscopy measuring at 664nm and 750nm would be appropriate |
| trichloric acetic acid (TCA) | Merck | T6399 | 100% |
| ultrasonic probe | nano lab | QS1T-2 |
References
- Boyd, E. S., Skidmore, M., Mitchell, A. C., Bakermans, C., Peters, J. W. Methanogenesis in subglacial sediments. Environmental Microbiology Reports. 2, 685-692 (2010).
- Sattler, B., Puxbaum, H., Psenner, R. Bacterial growth in supercooled cloud droplets. Geophysical Research Letters. 28, 239-242 (2001).
- Good, P., et al. A review of recent developments in climate change science. Part I: Understanding of future change in the large-scale climate system. Progress in Physical Geography. 35, 281-296 (2011).
- Fountain, A. G., et al. The Disappearing Cryosphere: Impacts and Ecosystem Responses to Rapid Cryosphere Loss. BioScience. 62, 405-415 (2012).
- Rignot, E., Mouginot, J., Morlighem, M., Seroussi, H., Scheuchl, B. Widespread, rapid grounding line retreat of Pine Island, Thwaites, Smith, and Kohler glaciers, West Antarctica, from 1992 to 2011. Geophysical Research Letters. 41, 3502-3509 (2014).
- McMillan, M., et al. Increased ice losses from Antarctica detected by CryoSat-2. Geophysical Research Letters. 41, 3899-3905 (2014).
- Barletta, V. R., et al. Glacier shrinkage and modeled uplift of the Alps. Geophysical Research Letters. 33, 14307 (2006).
- Nuth, C., et al. Decadal changes from a multi-temporal glacier inventory of Svalbard. The Cryosphere. 7, 1603-1621 (2013).
- Takeuchi, N., Kohshima, S., Seko, K. Structure, formation, and darkening process of albedo-reducing material (cryoconite) on a Himalayan glacier: A granular algal mat growing on the glacier. Arctic Antarctic and Alpine Research. 33, 115-122 (2001).
- Takeuchi, N. Optical characteristics of cryoconite (surface dust) on glaciers: the relationship between light absorbency and the property of organic matter contained in the cryoconite. Annals of Glaciology. 34, 409-414 (2002).
- Anesio, A. M., Hodson, A. J., Fritz, A., Psenner, R., Sattler, B. High microbial activity on glaciers: importance to the global carbon cycle. Global Change Biology. 15, 955-960 (2009).
- Anesio, A. M., et al. Carbon fluxes through bacterial communities on glacier surfaces. Annals of Glaciology. 51, 32-40 (2010).
- Storrie-Lombardi, M. C., Sattler, B. Laser-Induced Fluorescence Emission (L.I.F.E): In Situ Nondestructive Detection of Microbial Life in the Ice Covers of Antarctic Lakes. Astrobiology. 9, 659-672 (2009).
- Murray, A. E., et al. Microbial life at -13 °C in the brine of an ice-sealed Antarctic lake. Proceedings of the National Academy of Sciences of the United States of America. 109, 20626-20631 (2012).
- Edwards, A., et al. A distinctive fungal community inhabiting cryoconite holes on glaciers in Svalbard. Fungal Ecology. 6, 168-176 (2013).
- Miteva, V., Margesin, R., Schinner, F., Marx, J. C., Gerday, C. Bacteria in Snow and Glacier Ice. Psychrophiles: from Biodiversity to Biotechnology. , 31-50 (2008).
- Yallop, M. L., et al. Photophysiology and albedo-changing potential of the ice algal community on the surface of the Greenland ice sheet. The ISME Journal. 6, 2302-2313 (2012).
- Edwards, A., et al. A metagenomic snapshot of taxonomic and functional diversity in an alpine glacier cryoconite ecosystem. Environmental Research Letters. 8, 035003 (2013).
- Remias, D., et al. Characterization of an UV-and VIS-absorbing, purpurogallin-derived secondary pigment new to algae and highly abundant in Mesotaenium berggrenii (Zygnematophyceae, Chlorophyta), an extremophyte living on glaciers. FEMS Microbiology Ecology. 79, 638-648 (2012).
- Cook, J., et al. An improved estimate of microbially mediated carbon fluxes from the Greenland ice sheet. Journal of Glaciology. 58, 1098-1108 (2012).
- Mueller, D. R., Vincent, W. F., Pollard, W. H., Fritsen, C. H. Glacial cryoconite ecosystems: a bipolar comparison of algal communities and habitats. Nova Hedwigia Beiheft. 123, 173-198 (2001).
- Morgan-Kiss, R. M., Priscu, J. C., Pocock, T., Gudynaite-Savitch, L., Huner, N. P. A. Adaptation and Acclimation of Photosynthetic Microorganisms to Permanently Cold Environments. Microbiology and Molecular Biology Reviews. 70, 222-252 (2006).
- Hodson, A., et al. The cryoconite ecosystem on the Greenland ice sheet. Annals of Glaciology. 51, 123-129 (2010).
- Tilg, M., et al. L.I.F.E.: laser induced fluorescence emission, a non-invasive tool to detect photosynthetic pigments in glacial ecosystems. Proceedings SPIE. 8152, Instruments, Methods, and Missions for Astrobiology XIV, 81520I. , (2011).
- Lorenzen, C. J. Determination of chlorophyll and pheo-pigments: spectrophotometric equations. Limnology & Oceanography. 12, 343-346 (1967).
- Kirchman, D. Measuring bacterial biomass production and growth rates from leucine incorporation in natural aquatic environments. Methods in Microbiology. , 227-238 (2001).
- Bell, R. T., Kemp, P. F., Cole, J. J., Sherr, B. F., Sherr, E. B. Estimating production of heterotrophic bacterioplankton via incorporation of tritiated thymidine. Handbook of methods in aquatic microbial ecology. Edited by. , 495-503 (1993).
- Groemer, G., et al. Field trial of a dual-wavelength fluorescent emission (L.I.F.E.) instrument and the Magma White rover during the MARS2013 Mars analog mission. Astrobiology. 14, 391-405 (2014).
- Beutler, M. . Spectral fluorescence of chlorophyll and phycobilins as an in situ tool of phytoplankton analysis-models, algorithms and instruments. , (2003).
- Krogmann, K. D. Discoveries in Oxygenic Photosynthesis (1727-2003): A Perspective. Photosynthesis Research. 80, 15-57 (2004).
- Corrêa, D. S., et al. Reverse saturable absorption in chlorophyll A solutions. Journal of Applied Physics B. 74, 559-561 (2002).
- Kaňa, R., et al. The slow S to M fluorescence rise in cyanobacteria is due to a state 2 to state 1 transition. Biochimica et Biophysica Acta. 1817, 1237-1247 (2012).

