Høy nøyaktighet korreksjon av 3D kromatiske skift i en alder av super-oppløsning biologisk bildebehandling ved hjelp av chromagnon
Summary
Korrigering av kromatiske skift i tredimensjonale (3D) flerfarget fluorescensmikroskopibilder er avgjørende for kvantitative dataanalyser. Denne protokollen er utviklet for å måle og korrigere kromatiske endringer i biologiske prøver gjennom oppkjøp av egnede referansebilder og behandling med åpen kildekode-programvaren Chromagnon.
Abstract
Kvantitativ flerfarget fluorescensmikroskopi er avhengig av forsiktig romlig matching av fargekanaler som er anskaffet ved forskjellige bølgelengder. På grunn av kromatisk avvik og ufullkommen justering av kameraer, kan bilder som er anskaffet i hver kanal, forskyves, og forstørres, samt roteres i forhold til hverandre i noen av de tre dimensjonene. Med den klassiske kalibreringsmetoden måles kromatiske skift av flerfarget perler festet til overflaten av en coverslip, og en rekke programvare er tilgjengelige for å måle de kromatiske skiftene fra slike kalibreringsprøver. Kromatisk avvik kan imidlertid variere med dybde, endre med observasjonsforhold og bli indusert av selve den biologiske prøven, og dermed hindre fastsettelse av den sanne mengden kromatisk skifte i utvalget av interesse og på tvers av volumet. Korrigering av kromatiske skift med høyere nøyaktighet er spesielt relevant for superoppløselig mikroskopi der bare små kromatiske skift kan påvirke kvantitative analyser og endre tolkningen av flerfargebilder. Vi har utviklet en åpen kildekode-programvare Chromagnon og tilhørende metoder for å måle og korrigere 3D kromatiske skift i biologiske prøver. Her gir vi en detaljert programprotokoll som inneholder spesielle krav til prøveforberedelse, datainnsamling og programvarebehandling for å måle kromatiske endringer i biologiske prøver av interesse.
Introduction
Flerfarget bildebehandling er en av de grunnleggende aspektene ved biologisk fluorescensmikroskopi, i tilfeller der det romlige forholdet mellom forskjellige molekyler eller strukturer er av stor interesse. Kromatisk aberrasjon, et optisk avvik av polykromatisk lys forårsaket av spredning, endrer den tilsynelatende posisjonen til de fargede objektene av interesse. På samme måte har mikroskoper utstyrt med flere kameraer viet til å anskaffe hver farge mer komplekse kromatiske skift på grunn av forskjeller i optiske elementer og ufullkommen justering blant kanalene. Dermed kan slike kromatiske skift føre til en falsk konklusjon med mindre det er uttrykkelig korrigert av brukeren. Selv om kromatiske skift ikke har vært et stort problem så lenge oppløsningen av mikroskopi er begrenset av den klassiske oppløsningsgrensen, har den siste utviklingen av superoppløsningsmikroskopi1 ført til behovet for mer nøyaktig korreksjon av kromatiske skift.
Det har vært en vanlig praksis å måle kromatiske skift av mikroskopsystemer ved hjelp av en flerfarget perle kalibrering lysbilde2. Den perlebaserte kalibreringsmetoden passer for måling av kromatiske skift fra hele optikken til mikroskopet mot overflaten av dekkslippen2. Denne metoden er imidlertid ikke i stand til å måle kromatiske endringer i de biologiske prøver av interesse. Det er viktig å merke seg at mange biologiske prøver er tredimensjonale (3D), og de kromatiske skiftene til slike prøver er forskjellige fra de på overflaten av dekklip. Videre endres kromatiske skift med bildeforhold2,3. Vi har målt de kromatiske endringene i 3D biologiske prøver og funnet at usikkerheten i kromatiske skift var ofte så mye som 350 nm av den klassiske flerfarget perle kalibreringsmetode3. Derfor må kromatiske skift måles i biologiske prøver på dybden av interesse og under bildebehandlingsforholdene som brukes.
Her beskriver vi prosedyrer for å måle kromatiske endringer i biologiske prøver og korrigere disse skiftene ved hjelp av vår programvare, Chromagnon3. For å måle kromatiske skift i biologiske prøver, bruker vår metode to typer datasett, et “mål” bilde og et “referanse” bilde. “Målet” bildet er et flerfarget bilde av interesse, for eksempel bilder farget for DNA, kjernefysisk konvolutt og mikrotubuli. Det er ofte umulig å måle kromatiske skift i et slikt bilde. Derfor trenger vi et “referanse” bilde som er dedikert til å måle de kromatiske skiftene i prøven. Den eneste definisjonen av et “referanse” bilde er et flerfarget bilde av samme objekt. I denne forstand er et flerfarget perler bilde også en type referansebilde. Her beskriver vi tre forskjellige typer referansebilde som brukes til å måle kromatiske skift i de biologiske prøvene: “krysstalereferansebilder”, “lysfeltreferansebilder” og “biologiske kalibreringsreferansebilder”. Typen referansebilde avhenger av hvilken type mikroskop som brukes eller korrigeringsnøyaktigheten som kreves som summert i tabell 1.
| Krysstale | Lys-feltet | Biologisk kalibrering (på et annet lysbilde) | Biologisk kalibrering (på samme lysbilde) | |
| Nøyaktigheten | +++ | + | ++b (++ b) | +++ |
| Enkelhet | ++ | +++ | ++ | ++ |
| Gjeldende mikroskopi | Bredt felt | Bredt felt | Alle | Alle |
| Tilgjengelighet av lokal justering | + | + | –C | –C |
|
a:Antall “+” indikerer økende vurdering. Enkelt pluss er ca 50 nm og tre pluss er ca 15 nm i 3D. b: Nøyaktigheten avhenger av hvor mye de variable bildeforholdene holdes konstante. c: Lokal kalibrering målt ved flerfarget perleprøver kan kombineres som beskrevet i protokollseksjon 4. |
||||
Tabell 1: Parametere når du velger typen referansebilder.
“Crosstalk referansebilder” har den høyeste korreksjonsnøyaktigheten og er relativt enkle å oppnå3,4 (Tabell 1). Ulempen er deres begrensning i mikroskopiapplikasjoner på grunn av deres manglende evne til å måle kromatiske skift i eksitasjonsbaner. Også for å få slike bilder, bør mikroskopet være utstyrt med multiband dichroic speil, og utslippsfiltre som er uavhengig kontrollert fra eksitasjonsfiltre eller lyskilder. Egnet mikroskopi inkluderer konvensjonell bredfelts mikroskopi, enkeltmolekyl lokalisering mikroskopi (SMLM) som fotoaktivert lokalisering mikroskopi / stokastisk optisk rekonstruksjon mikroskopi (PALM / STORM)5,,6 og ekspansjon mikroskopi7 observert med bredfelt mikroskopi. Et krysstalereferansebilde er hentet fra selve målprøven. Det er et bilde av crosstalk (blø-gjennom) fluorescens av et fargestoff oppnådd i alle nødvendige kanaler. Fluorescensutslippet ekspanderer alltid mot de lengre bølgelengdene, derfor er fargestoffer med den korteste utslippsbølgelengden glade for å oppnå krysstalefluorescens i kanaler med lengre bølgelengder. For eksempel, når prøven er farget med blå, grønn og rød, er bare det blå fargestoffet spent, og utslippslyset oppnås i de blå, grønne og røde kanalene. I denne protokollen ble DNA farget med 4′,6-diamidino-2-fenylindol (DAPI) brukt til å oppnå crosstalk fluorescens.
“Bright-field reference images” er et enklere og mindre fototoksisk alternativ til “crosstalk referansebilder”, men er den minst nøyaktige3 (Tabell 1). Dette er lyse feltbilder av måleksemplet, som er anskaffet i alle fargekanalene som brukes i målbildet.
“Biologisk kalibrering referansebilder” har fordelen av å være aktuelt for alle typer mikroskopi på grunn av deres evne til å måle kromatiske skift både i eksitasjon og utslipp stier3,8 (Tabell 1). Egnet mikroskopi inkluderer wide-field mikroskopi, konfiskert mikroskopi, lysarkmikroskopi, stimulert utslipp uttømming ()9,strukturert belysning mikroskopi (SIM)10,Airyscan / SORA11,12, SMLM observert med den totale interne refleksjon fluorescens (TIRF) modus, Olympus super oppløsning (OSR)13, og så videre. Et biologisk kalibreringsreferansebilde er hentet fra en kalibreringsprøve som på samme måte er utarbeidet som målprøven, men med farging av en enkelt struktur med flere farger. Korrigeringsnøyaktigheten utmerker seg oppløsningen av de fleste superoppløselige mikroskopi og forbereder en biologisk kalibreringsprøve kan være relativt enkel. En annen fordel er tilgjengeligheten til “gjennomsnittlig” flere referansebilder. Derfor, selv om de enkelte bildene inneholder dårlig informasjon for måling av kromatiske skift, kan informasjonsinnholdet økes ved å snitte flere bilder. Nøyaktigheten avhenger av hvor mye bildebehandlingsforholdene holdes konstante. I denne forbindelse oppnås den beste ytelsen når både mål- og referanseprøver er på samme lysbilde, ved hjelp av for eksempel 8-brønns kamret dekkglass (Tabell 1, høyre-mest). I denne protokollen ble actin farget med tre farger av phalloidin brukt som en biologisk kalibrering.
Når et referansebilde er oppnådd, måles og korrigeres kromatisk skift av vår programvare Chromagnon. Det er ingen begrensning på antall kanaler, Z-seksjoner og tidsrammer som Chromagnon kan måle og korrigere kromatiske skift for. Kroromagnonen måler kromatiske skift i to trinn. Det første trinnet får de “globale” eller “affine” justeringsparameterne for oversettelse i X- og Y-, Z-aksene, forstørrelsen langs X-, Y-, Z-aksene og rotasjonen rundt Z-aksen. Beregningsnøyaktigheten for den globale justeringen er ~16 nm i 3D og ~8 nm i 2D. Det andre trinnet er en valgfri 2D iterativ “lokal justering” på projiserte bilder for å oppnå en høyere nøyaktighet. I den lokale justeringsprosessen måles bildene i flere områder, og kromatiske skift i disse lokale områdene måles. Deretter blir regionene videre delt og kromatiske skift i underregionene måles iterativt til antall piksler i regionen når minimum antall piksler (vanligvis 60 x 60 piksler). Det resulterende lokale justeringskartet kombineres med den globale justeringsparameteren og brukes på målbildet av en elastisk transformasjon. Etter dette trinnet er beregningsnøyaktigheten forbedret til ~ 14 nm i 3D og ~6 nm i 2D. Den lokale justeringen er ikke egnet for biologiske kalibreringsreferansebilder fordi biologisk struktur i referansen er forskjellig fra den i målet (tabell 1). Derfor brukes bare global justering for biologiske kalibreringsreferansebilder.
De lokale kromatiske skiftene stammer fra to kilder; mikroskop instrumental lokal forvrengning og biologisk strukturell inhomogenitet. Fordi mikroskopinstrumental lokal forvrengning er konstant, kan dette måles fra flerfarget perler referanseprøve og korrigeres som en fast parameter. Chromagnon kan kombinere mikroskopets instrumentelle lokale forvrengningskart og de globale justeringsparametrene fra de biologiske kalibreringene (tabell 1). Ved hjelp av denne metoden forventes det at den gjennomsnittlige nøyaktigheten av biologisk kalibrering vil bli forbedret med ytterligere 1-2 nm.
Her beskriver vi en protokoll for å korrigere kromatiske skift av 3D fluorescensbilder ved hjelp av vår programvare Chromagnon, fra den enkleste lave enden til den høyeste nøyaktigheten. Vi bruker immunostaining av HeLa-celler som et eksempel og observerte dem ved hjelp av 3D wide-field mikroskopi og 3D-SIM. I den første delen beskriver vi hvordan vi kan forberede målprøver og biologiske kalibreringsprøver. Denne delen av protokollen bør optimaliseres for de spesifikke målene for forskningen. I den andre delen beskriver vi oppkjøpsmetodene for tre typer referansebilder med mikroskoper. Forutsetningen var å få blå, grønne og røde kanaler, men kanalsammensetning bør endres av de spesifikke målene for forskningen og av oppsettene av mikroskopet. Det spiller ingen rolle om mikroskopet er utstyrt med et enkelt kamera eller flere kameraer. I den tredje delen beskriver vi hvordan man kan bruke programvaren vår til å måle og korrigere kromatiske skift av målbildet ved hjelp av referansebilder. Til slutt, i den fjerde delen, beskriver vi en metode for å utfylle de biologiske kalibreringsreferansebildene ved hjelp av et mikroskops instrumentelle lokale kalibrering.
Protocol
Representative Results
Discussion
Prosedyren for kromatisk korreksjon er en avveining mellom nøyaktighet og innsats. For å spare unødvendig innsats, er det bedre å vite hvor mye nøyaktighet som kreves for studien din. Den høyeste nøyaktigheten er kanskje ikke nødvendig for konvensjonell bredfelt (live) bildebehandling, og dermed er lyse feltreferansebilder ofte tilstrekkelige til å korrigere kromatisk skift. På samme måte, når bildetilstanden og miljøet er konstant, vil gjentatt bruk av en biologisk kalibrering spare tid. På den annen side, hvis en svært nøyaktig registrering er ønsket, er det nødvendig med krysstale av høy kvalitet eller biologiske kalibreringsreferansebilder. For best mulig ytelse bør referansebilder oppnås med så like vilkår og tidspunkter som målbildene som mulig. Så lenge både referanse- og målbilder oppnås av samme mikroskopi, vil høyere romlig oppløsning forbedre korrigeringsnøyaktigheten. Hvis dekonvolutsjon er tilgjengelig for både referanse- og målbilder, kan implementering av dette før korrigering forbedre korrigeringsnøyaktigheten. For best mulig ytelse bør prøvetakingsteoremet for den optiske aksen (Z) oppfylles i både referanse- og målfilen for nøyaktig subpixel interpolering (protokolltrinn 2.1.3).
Unnlatelse av å korrigere kromatisk skift fører til feil konklusjoner. Videre kan bruk av feil kalibrering til og med forverre kromatiske skift i stedet for å korrigere dem, og dette må derfor unngås. Vi har oppsummert mulige årsaker til feil, og deres felles løsninger, i tabell 2. For å undersøke årsaken til en feil, er det i første omgang nødvendig å visuelt kontrollere om det kromatiske skiftet i referansebildet er nøyaktig korrigert (protokolltrinn 3.12). De fleste feil skyldes kvaliteten på referansebildene og er lett utbedret i henhold til beskrivelsene i tabell 2. Når det gjelder kvaliteten på referansebilder, er det viktig å merke seg at nøyaktigheten av global justering reduseres hvis hele synsfeltet ikke er fylt med prøven (Figur 7, Tabell 2). Sammenlignet med det gode eksemplet som vises i figur 7A,inneholder det dårlige eksempelet vist i figur 7B bare tre kjernefysiske konvolutter i øvre venstre region, og Chromagnon klarte ikke å justere en del av dette bildet. Dette er fordi den globale justeringsmetoden for Chromagnon deler synsfeltet i fire regioner (Figur 7C) for å måle forskjellene i rotasjon og forstørrelse med høy nøyaktighet3. Denne metoden, hvis den er riktig drevet, er en ordre mer nøyaktig enn andre lineære metoder som loggpolpolering og simplex-metoder3. Hvis noen av de fire regionene ikke er tilgjengelige, vil Chromagnon bytte til mindre effektive lineære metoder. Derfor, for best ytelse, eksemplene vist i figur 7B og figur 7C er uønsket, og de fire regionene skal fylles med objekter. Brukere kan sjekke om et kvadratisk område i synsfeltet ikke er tilgjengelig for måling ved å se på loggfilen (“Chromagnon.log”; se protokolltrinn 3.10). Heldigvis kan dette problemet lett overvinnes ved å snitte flere biologiske kalibreringsbilder eller bruke lokal justering for krysstale- eller lysfeltreferansebilder (tabell 2). I motsetning til tilfelle av unnlatelse av å korrigere referansebilder, er det vanskeligere å identifisere å ikke korrigere målbilder. Fordi slike feil oppstår på grunn av forskjeller i filformater, bildebehandlingsforhold, bildebehandlingstid, bildebehandlings-/justeringsmetoder mellom referanse- og målbildene(tabell 2),bør brukerne alltid være forsiktige når de bruker referansebilder som er oppnådd under forskjellige forhold/tidspunkter fra målbildene. Noen eksempelbilder er tilgjengelige for testing (https://github.com/macronucleus/Chromagnon) for å få konkrete ide om de gode og dårlige eksempelbildene.
| Problem | Forårsake | Løsning |
| Kan ikke rette opp referansebildet | Lav kontrast | Få et høyere kontrastbilde hvis mulig. Hvis et referansebilde for lysfelt brukes, må du hente bildet i en vannbasert løsning for å oppnå høyere kontrast av cellen. Alternativt kan du prøve å bruke beregningsstøyreduksjon (f.eks. gaussisk filtrering). Slå av lokal justering, som er mer følsom for støy. |
| Kontaminering av ikke-relaterte bilder | Fjern kilden til de ikke-relaterte bildene i eksemplet hvis mulig. For krysstalereferansebilder, sjekk eksitasjonsspektraen på fargestoffene som brukes til målbildene. Hvis fargestoffene er begeistret under oppkjøpet av et crosstalk-bilde (f.eks. Alexa Fluor 568 eller 594), bør du vurdere andre fargestoffer (f.eks. Alexa Fluor 555). Hvis støv på kamerabrikken skaper en åpenbar kanalforskjell, rengjør du kamerabrikken eller bruker en beregningsmessig flatfeltmetode. | |
| Et ekstremt lyspunkt laget av en kosmisk stråle | Få bildet igjen hvis mulig. Alternativt kan du prøve å bruke beregningsstøyreduksjon (f.eks. median eller gaussisk filtrering). | |
| Dekonvolutasjonsartefakter (kunstige signaler på aksiale og laterale kanter) | Trim kantpikslene eller Z-delene etter dekonvolusjon. Hvis den ene siden er trimmet, bør den andre siden også trimmes for å opprettholde bildesenteret. | |
| Z-trinnstørrelsen er for sparsomme | En Z-stabel bør anskaffes for å oppfylle Nyquist-kriteriet som skrevet i protokoll 2.1.3. | |
| Optisk avvik | Sfærisk avvik er det store avviket forårsaket av brukere. Velg riktig objektiv for prøven og bruk en dekksliptykkelse på 170 μm. Hvis objektivet er utstyrt med en korreksjonsring, justerer du den for å finne posisjonen der det høyeste fluorescensantallet er hentet fra fokuset. Når det gjelder et oljenedsenkingsmål uten korreksjonsring, juster brytningsindeksen for nedsenkingsoljen som øker fluorescenstellingen i fokus. | |
| Synsfeltet er ikke fylt opp (fig. 7) | Når det gjelder biologiske kalibreringsreferansebilder, gjennomsnittlig mange bilder. I tilfelle av krysstale eller lysfeltreferansebilder, bruk lokal justering. | |
| En uidentifisert programvarefeil | Rapporter problemet via GitHub (https://github.com/macronucleus/Chromagnon/issues) | |
| Kunne ikke rette målbildet | Metadata for bildefilen går tapt | Bruk det opprinnelige mikroskopfilformatet som inneholder fullstendige metadata, og unngå å konvertere til en tiff-fil med flere sider før behandling. Bruk samme rekkefølge av kanaler som skrevet i protokoll 3.3. |
| Feil justeringsmetoder for den gitte mikroskopien | Ikke bruk den lokale justeringsmetoden når du måler fra biologiske kalibreringsreferansebilder til målbilder. Ikke bruk andre krysstalereferansebilder enn wide-field mikroskopi. | |
| Forskjeller i bildebehandlingsforhold | Hold bildeforholdene konstant mellom referansen og målbildene som skrevet i protokoll 2.3.3. | |
| Forskjeller i prøve (inkludert coverslip) | Bruk alltid samme monteringsmedium, dekkslip (f.eks. 1,5H) og en lignende fokusdybde. | |
| Mikroskopdrift siden kalibreringen sist ble gjort | Lag en kalibrering så ofte som annenhver uke. Hold temperaturen konstant, og bruk et flytende bord for å unngå maskinvaredrift av mikroskopet. |
Tabell 2: Feilsøking for kromatisk korrigering.
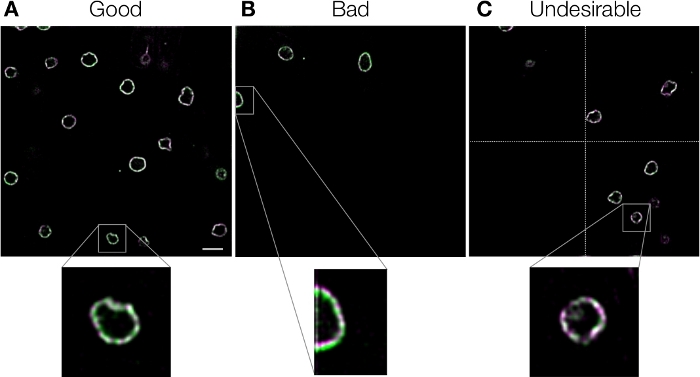
Figur 7: Eksempler på referansebilder. Kjernefysisk konvolutt i fisjon gjær celler merket med GFP og mCherry. Bilder ble anskaffet med konvensjonell bredfelts mikroskopi. Kromatiske skift ble korrigert ved hjelp av Chromagnon uten lokal justering ved hjelp av bildene selv som referansebilder. Bilder ble deretter dekonvolvert for å vise detaljene. (A)Et godt eksempel med mange objekter i synsfeltet. (B)Et dårlig eksempel med objekter bare øverst til venstre. Feiljustering er åpenbar på en bestemt region av bildet. (C)Et uønsket eksempel der en av kvarsjonen (atskilt med stiplede krysslinjer) er tomt. Skalalinje i panel A indikerer 5 μm for full feltvisning og 1,25 μm for forstørret visning og gjelder for alle paneler. Vennligst klikk her for å se en større versjon av dette tallet.
I denne protokollen beskrev vi tre forskjellige referansetyper (tabell 1). Blant dem trenger krysstale referansebilder og biologiske kalibreringsreferansebilder ytterligere nøye diskusjon. For krysstalereferansebilder kan prøver farget med DAPI eller Hoechst 33342, og montert i glyserol eller kommersielle monteringsmedier effektivt brukes til å justere de blå, grønne og røde kanalene. På samme måte kan Alexa Fluor 488 brukes til å justere de grønne og røde kanalene. Men å skaffe crosstalk fluorescens er ofte vanskelig siden mange blå fargestoffer unntatt DAPI og Hoechst er dimmer og forfall raskere enn de fleste grønne og røde fargestoffer. Videre er utslippsspektraen av moderne fargestoffer smalere, noe som gjør justeringen av mer enn tre kanaler ved denne metoden utfordrende. Det bør også tas hensyn til noen vanlige røde fargestoffer (f.eks. Alexa Flour 568 og 594, men ikke Alexa Fluor 555) som kan være begeistret av fiolett lys, som forhindrer å få høykontrast krysstalebilder fra blå fargestoffer. En annen ulempe er at denne metoden ikke kan måle kromatisk aberrasjon av eksitasjon lysbaner i flerfarget eksitasjon, fordi bare en enkelt eksitasjon bølgelengde brukes til eksitasjon (Tabell 1). Som de fleste avanserte mikroskopi bruker endret belysning optikk, er anvendelsen av denne metoden begrenset. Likevel er den høyere korreksjonsnøyaktigheten tilstrekkelig fordelaktig for at den skal beskrives i denne protokollen. Generelt bør et krysstalebilde tas etter et målbilde for å forhindre bleking eller fototoksiske effekter. For SMLM observert med bredfeltsmodus, bør et referansebilde anskaffes før du anskaffer et målbilde, da fluorescensfarger kan blekes mens bildebehandling.
Biologiske kalibreringsreferansebilder gjør det enkelt for brukere å justere et ønsket antall kanaler på bekostning av ekstra prøveklargjøring. En annen fordel med biologiske kalibreringsreferansebilder er tilgjengeligheten av “snitt” flere referanser som bidrar til å fylle alle synsfelt. Denne metoden kan lide av forskjeller i bildeforhold hvis kalibreringsprøven er klargjort på et annet lysbilde. Det meste av dette problemet kan løses hvis både mål og referanser er utarbeidet på samme lysbilde ved hjelp av kommersielle kamret coverbriller (Tabell 1), og andre bildebehandlingsforhold holdes konstant som i protokolltrinn 2.3.3. I dette tilfellet kan en korrigeringsnøyaktighet som ligner på krysstalereferansebilder forventes3. Protokollen for å bruke phalloidin som vist her er en av de enkleste måtene å flekke en enkelt cellulær struktur med flere farger. Det er mange mulige scenarier for å forberede biologiske kalibreringsprøver. For immunstoppnåelse kan en prøve merkes med et enkelt primært antistoff etterfulgt av farging med sekundære antistoffer i flere farger. På denne måten kan en enkelt målstruktur merkes med flere farger. Alternativt, 5-ethynyl-2′-deoxyuridine, oppdaget av “klikk” kjemi etiketter nylig syntetisert DNA i flere farger med høy tetthet, som beskrevet i detalj tidligere8. For levende celler er det nyttig å forberede en transgen stamme som skjuler to kopier av et gen som er smeltet sammen til GFP eller mCherry for å merke samme struktur med to farger. Hvis kopinummeret til genet er kritisk som ofte observert for membranproteiner, kan en enkelt kopi av genet smeltes sammen til GFP og mCherry (figur 7). Fotokonverterbare fluorescerende proteiner, som mEOS218,kan også brukes ved å belyse et moderat nivå av fiolett lys for å oppnå både proteinarter med eller uten fotokonvertering. Under lave oksygenforhold kan GFP også brukes som et fotokonverterbart protein fra grønt til rødt19,,20. Hvis du velger riktig kalibreringsprøve, blir eksperimentet mer robust.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Denne studien ble støttet av JSPS KAKENHI Grant Numbers JP19H03202 til A.M., JP18H05528 og JP17H03636 til T.H., og JP17H01444 og JP18H05533 til H.Y. L.S. anerkjenner støtten fra Welcome Trust Strategic Awards 091911 og 107457/Z/15/Z finansiering avansert bildebehandling på Micron Oxford.
Materials
| 16% formaldehyde solution | Polyscience | 18814-10 | |
| 35 mm glass-bottom dish | MatTek | P35G-1.5-10-C | |
| Alexa Fluor 405 phalloidin | Thermo Fisher Scientific | A30104 | |
| Alexa Fluor 488 phalloidin | Thermo Fisher Scientific | A12379 | |
| Alexa Fluor 594 phalloidin | Thermo Fisher Scientific | A12381 | |
| Bovine Serum | Thermo Fisher Scientific | 16170078 | |
| Coverslip | Matsunami | No. 1S HT | |
| DAPI (4',6-Diamidino-2-Phenylindole, Dihydrochloride) | Thermo Fisher Scientific | D1306 | |
| Dulbecco’s Modified Eagle Medium with L-Gln and sodium pyruvate | Nacalai Tesque | 08458-16 | |
| Mounting medium (VECTASHIELD) | Vector Laboratories | H-1000 | |
| Mouse anti-tubulin monoclonal antibody (TAT1) | Described in Ref 15. | ||
| Nunc Lab-Tek II chambered coverglass (8 well) | Thermo Fisher Scientific | 155409 | |
| Rabbit anti-emerin polyclonal antibody (ED1) | A gift from Hiroshi Yorifuji, Gunma University, Gunma, Japan and Kiichi Arahata, National Center of Neurology and Psychiatry, Tokyo, Japan; deceased. | ||
| Secondary antibody with Alexa Fluor 488 | Thermo Fisher Scientific | A-11034 | |
| Secondary antibody with Alexa Fluor 555 | Thermo Fisher Scientific | A-21424 | |
| Secondary antibody with Alexa Fluor 594 | Thermo Fisher Scientific | A-11032 | |
| TetraSpeck Microspheres, 0.2 µm | Thermo Fisher Scientific | T7280 |
References
- Schermelleh, L., et al. Super-resolution microscopy demystified. Nature Cell Biology. 21 (1), 72-84 (2019).
- Manders, E. M. M. Chromatic shift in multicolour confocal microscopy. Journal of Microscopy. 185 (3), 321-328 (1997).
- Matsuda, A., Schermelleh, L., Hirano, Y., Haraguchi, T., Hiraoka, Y. Accurate and fiducial-marker-free correction for three-dimensional chromatic shift in biological fluorescence microscopy. Scientific Reports. 8 (1), 7583 (2018).
- Grünwald, D., Singer, R. H. In vivo imaging of labelled endogenous β-actin mRNA during nucleocytoplasmic transport. Nature. 467 (7315), 604-607 (2010).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313 (5793), 1642-1645 (2006).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM). Nature Methods. 3 (10), 793-795 (2006).
- Chen, F., Tillberg, P. W., Boyden, E. S. Expansion microscopy. Science. 347 (6221), 543-548 (2015).
- Kraus, F., et al. Quantitative 3D structured illumination microscopy of nuclear structures. Nature Protocols. 2, 1011-1028 (2017).
- Hell, S. W. Far-Field Optical Nanoscopy. Science. 316 (5828), 1153-1158 (2007).
- Gustafsson, M. G. L. Surpassing the lateral resolution limit by a factor of two using structured illumination microscopy. Journal of Microscopy. 198 (2), 82-87 (2000).
- Schulz, O., et al. Resolution doubling in fluorescence microscopy with confocal spinning-disk image scanning microscopy. Proceedings of the National Academy of Sciences of United States of America. 110 (52), 21000-21005 (2013).
- Müller, C. B., Enderlein, J. Image Scanning Microscopy. Physical Review Letters. 104 (19), 198101 (1981).
- Hayashi, S., Okada, Y. Ultrafast superresolution fluorescence imaging with spinning disk confocal microscope optics. Molecular Biology of the Cell. 26 (9), 1743-1751 (2015).
- Yorifuji, H., et al. Emerin, deficiency of which causes Emery-Dreifuss muscular dystrophy, is localized at the inner nuclear membrane. Neurogenetics. 1 (2), 135-140 (1997).
- Woods, A., Sherwin, T., Sasse, R., MacRae, T. H., Baines, A. J., Gull, K. Definition of individual components within the cytoskeleton of Trypanosoma brucei by a library of monoclonal antibodies. Journal of Cell Science. 93 (3), 491-500 (1989).
- Tokunaga, M., Imamoto, N., Sakata-Sogawa, K. Highly inclined thin illumination enables clear single-molecule imaging in cells. Nature Methods. 5 (2), 159-161 (2008).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529 (2017).
- McKinney, S. A., Murphy, C. S., Hazelwood, K. L., Davidson, M. W., Looger, L. L. A bright and photostable photoconvertible fluorescent protein for fusion tags. Nature Methods. 6 (2), 131-133 (2009).
- Sawin, K. E., Nurse, P. Photoactivation of green fluorescent protein. Current Biology. 7 (10), 606-607 (1997).
- Elowitz, M. B., Surette, M. G., Wolf, P. E., Stock, J., Leibler, S. Photoactivation turns green fluorescent protein red. Current Biology. 7 (10), 809-812 (1997).

