Karakterisering av intra-brusk transport egenskaper av kationiske peptid bærere
Summary
Denne protokollen bestemmer likevektopptak, dybde av penetrasjon og ikke-likevekt diffusjonshastighet for kationiske peptid bærere i brusk. Karakterisering av transportegenskaper er avgjørende for å sikre en effektiv biologisk respons. Disse metodene kan brukes for å designe en optimalt ladet narkotika bærere for målretting negativt ladet vev.
Abstract
Flere negativt ladede vev i kroppen, som brusk, presenterer en barriere for målrettet legemiddellevering på grunn av deres høye tetthet av negativt ladede aggrekaner og krever derfor forbedrede målrettingsmetoder for å øke deres terapeutiske respons. Fordi brusk har en høy negativ fast ladningstetthet, kan legemidler endres med positivt ladede legemiddelbærere for å dra nytte av elektrostatiske interaksjoner, noe som åpner for forbedret intrabrusk narkotikatransport. Å studere transport av legemiddelbærere er derfor avgjørende for å forutsi effekten av legemidler for å indusere en biologisk respons. Vi viser utformingen av tre eksperimenter som kan kvantifisere likevektsopptaket, dybden av penetrasjon og ikke-likevektsdiffusjonshastighet av kationiske peptidbærere i bruskekplanter. Likevektopptakseksperimenter gir et mål på den løse konsentrasjonen i brusk i forhold til det omkringliggende badet, noe som er nyttig for å forutsi potensialet til en legemiddelbærer for å øke terapeutisk konsentrasjon av legemidler i brusk. Dybde av penetrasjonsstudier ved hjelp av konfokal mikroskopi gir mulighet for visuell representasjon av 1D-solute diffusjon fra overfladisk til dyp sone av brusk, noe som er viktig for å vurdere om solutes når sine matrise- og cellulære målsteder. Ikke-likevektsdiffusjonshastighetsstudier ved hjelp av et spesialdesignet transportkammer gjør det mulig å måle styrken av bindende interaksjoner med vevsmatrisen ved å karakterisere diffusjonshastigheten til fluorescerende merkede solutes over vevet; Dette er gunstig for å designe bærere med optimal bindingsstyrke med brusk. Sammen gir resultatene fra de tre transporteksperimentene en retningslinje for å utforme optimalt belastede legemiddelbærere som drar nytte av svake og reversible ladeinteraksjoner for søknader om legemiddellevering. Disse eksperimentelle metodene kan også brukes til å evaluere transport av narkotika og narkotika-narkotika bærer konjugater. Videre kan disse metodene tilpasses for bruk i målretting mot andre negativt ladede vev som menisk, hornhinnen og glasslegemet humor.
Introduction
Legemiddellevering til negativt ladet vev i kroppen er fortsatt en utfordring på grunn av manglende evne til narkotika å trenge dypt inn i vevet for å nå celle og matrise mål nettsteder1. Flere av disse vevene består av tettpakkede, negativt ladede aggrekaner som skaper en høy negativ fast ladningstetthet (FCD)2 i vevet og fungerer som en barriere for levering av de flestemakromolekyler 3,4. Men med hjelp av positivt ladede legemiddelbærere, kan denne negativt ladede vevsbarrieren faktisk konverteres til et legemiddeldepot via elektrostatiske ladeinteraksjoner for vedvarende legemiddellevering1,,5,,6,7( figur1).
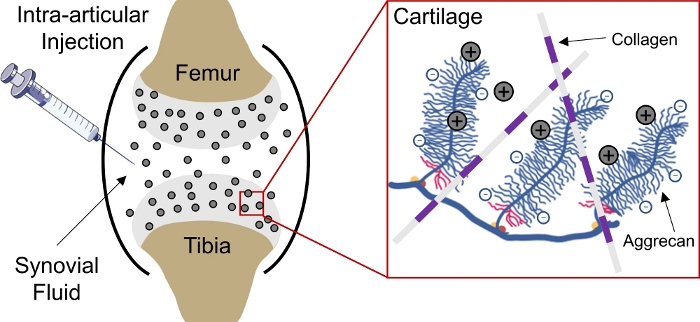
Figur 1: Ladebasert intrabrusklevering av CPC-er. Intraartikulær injeksjon av CPC-er i kneleddet. Elektrostatiske interaksjoner mellom positivt ladede CPC-er og negativt ladede aggrekanske grupper muliggjør rask og full dybdegjennomtrengning gjennom brusk. Dette tallet er endret fra Vedadghavami et al4. Vennligst klikk her for å se en større versjon av denne figuren.
Nylig ble kationiske peptidbærere (CPC) designet med sikte på å skape små kationiske domener som er i stand til å bære større størrelse terapeutiske midler for levering til negativt ladetbrusk 4. For effektiv legemiddellevering til brusk for behandling avutbredte 8,,9 og degenerative sykdommer som slitasjegikt (OA)10, er det avgjørende at terapeutiske konsentrasjoner av legemidler trenger dypt inn i vevet, hvor et flertall av bruskcellene (kondrocytter)ligger 11. Selv om det er flere potensielle sykdomsmodifiserende legemidler tilgjengelig, ingen har fått FDA godkjenning fordi disse ikke er i stand til effektivt å målrettebrusk 12,13. Derfor er evaluering av transportegenskapene til legemiddelbærere nødvendig for å forutsi effektiviteten av legemidler for å indusere en terapeutisk respons. Her har vi designet tre separate eksperimenter som kan benyttes for å vurdere likevektsopptaket, dybden av penetrasjon og ikke-likevektsdiffusjonshastighet av CPC4.
For å sikre at det er en tilstrekkelig legemiddelkonsentrasjon i brusk som kan gi en optimal terapeutisk respons, ble opptakseksperimenter designet for å kvantifisere likevekt CPC konsentrasjon ibrusk 4. I denne designen, etter en likevekt mellom brusk og det omkringliggende badet, kan den totale mengden solutgående inne i brusk (enten bundet til matrisen eller gratis) bestemmes ved hjelp av et opptaksforhold. Dette forholdet beregnes ved å normalisere konsentrasjonen av solutes inne i brusk til likevektbadet. I prinsippet ville nøytrale solutes, hvis diffusjon gjennom brusk ikke er assistert av ladeinteraksjoner, ha et opptaksforhold på mindre enn 1. Omvendt viser kationiske solutes, hvis transport er forbedret via elektrostatiske interaksjoner, et opptaksforhold som er større enn 1. Men, som vist med CPC, bruk av en optimal positiv ladning kan resultere i mye høyere opptaksforhold (større enn 300)4.
Selv om høy legemiddelkonsentrasjon i brusk er viktig for å oppnå terapeutisk nytte, er det også avgjørende at legemidler sprer seg gjennom bruskens fulle tykkelse. Derfor er studier som viser dybden av penetrasjon nødvendig for å sikre at legemidler når dypt inne i brusk slik at matrisen og cellulære målsteder kan nås, og dermed gi en mer effektiv terapi. Dette eksperimentet ble designet for å vurdere enveis diffusjon av solutes gjennom brusk, simulere diffusjon av narkotika i brusk etter intra-ledd injeksjon in vivo. Fluorescensavbildning ved hjelp av konfokal mikroskopi gjør det mulig å evaluering av dybden av penetrasjon i brusk. Netto partikkelladning spiller en nøkkelrolle i å moderere hvordan dype legemidler kan spre seg gjennom matrisen. En optimal nettoladning basert på et vev FCD er nødvendig for å tillate svake reversible bindende interaksjoner mellom kationiske partikler og anionisk vevmatrise. Dette innebærer at enhver interaksjon er svak nok slik at partikler kan kobles fra matrisen, men reversibel i naturen slik at den kan binde seg til et annet matrisebindende sted dypere ivevet 4. Omvendt kan overdreven positiv nettoladning av en partikkel være skadelig mot diffusjon, da for sterk matrisebinding forhindrer løsrivelse av partikler fra det opprinnelige bindingsstedet i brusksonen. Dette ville resultere i en utilstrekkelig biologisk respons som et flertall av målstedene ligger dypt inne ivevet 11.
For ytterligere å kvantifisere styrken av de bindende interaksjonene, er analyse av narkotikadiffusjonshastigheter gjennom brusk en fordel. Ikke-likevektsdiffusjonsstudier tillater sammenligning av sanntidsdiffusjonshastigheter mellom forskjellige solutes. Som narkotika diffuse gjennom overfladiske, midtre og dype soner av brusk, kan tilstedeværelsen av bindende interaksjoner i stor grad endre diffusjonshastigheten. Når bindende interaksjoner er tilstede mellom legemidler og bruskmatrisen, er det definert som effektiv diffusivitet (DEFF). I dette tilfellet, når alle bindende steder har blitt okkupert, er diffusjonsraten av legemidler styrt av steady-state diffusjon (DSS). Sammenligning mellom DEFF av forskjellig solute bestemmer den relative bindende styrken til solutes med matrisen. For en gitt solute, hvis DEFF og DSS er innenfor samme størrelsesorden, innebærer det at det er minimal binding tilstede mellom stoffet og matrisen under diffusjon. Men hvis DEFF er større enn DSS, finnes det betydelig binding av partikler til matrise.
De utformede eksperimentene tillater individuelt karakterisering av solute transport gjennom brusk, men en helhetlig analyse inkludert alle resultater er nødvendig for å designe en optimalt ladet legemiddelbærer. Den svake og reversible karakteren av ladeinteraksjoner styrer partikkeldiffusjonshastigheten og gir høy likevektsopptak og rask full dybdegjennomtrengning gjennom brusk. Gjennom likevektsopptakseksperimenter bør vi se etter bærere som viser høyt opptak som følge av ladeinteraksjoner som kan verifiseres ved hjelp av ikke-likevektsdiffusjonshastighetsstudier. Disse bindingsinteraksjonene bør imidlertid være svake og reversible i naturen for å tillate full tykkelsesinntrengning av det løse gjennom brusk. En ideell legemiddelbærer ville ha en optimal ladning som muliggjør sterk nok binding for opptak og høye intra-brusk narkotikakonsentrasjoner, men ikke for sterk som å hindre full tykkelse diffusjon4. De presenterte eksperimentene vil bistå i designegenskapene for ladebaserte vev rettet mot legemiddelbærere. Disse protokollene ble brukt til å karakterisere CPC transport gjennom brusk4, men disse kan også brukes på en rekke narkotika og narkotika bærere gjennom brusk og andre negativt ladet vev.
Protocol
Representative Results
Discussion
Metodene og protokollene som er beskrevet her, er signifikante for feltet målrettet legemiddellevering til negativt ladet vev. På grunn av den høye tettheten av negativt ladede aggrekaner tilstede i disse vevene, opprettes det en barriere, og dermed hindrer narkotika i å nå sine cellulære målsteder som ligger dypt inne i matrisen. For å løse denne enestående utfordringen, kan narkotika endres for å innlemme positivt ladede legemiddelbærere som kan forbedre transporthastigheten, opptaket og bindingen av narkot…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble finansiert av USAs forsvarsdepartement gjennom Congressionally Directed Medical Research Programs (CDMRP) under kontrakt W81XWH-17-1-0085, og National Institute of Health R03 EB025903-1. AV ble finansiert av College of Engineering Dean’s Fellowship ved Northeastern University.
Materials
| 316 Stainless Steel SAE Washer | McMaster-Carr | 91950A044 | For number 5 screw size, 0.14" ID, 0.312" OD |
| 96-Well Polystyrene Plate | Fisherbrand | 12566620 | Black |
| Acrylic Thick Gauge Sheet | Reynolds Polymer | N/A | For non-equilibrium diffusion and 1-D diffusion transport chamber |
| Antibiotic-Antimycotic | Gibco | 15240062 | 100x |
| Bovine Cartilage | Research 87 | N/A | 2-3 weeks old, femoropatellar groove |
| Bovine Serum Albumin | Fisher BioReagents | BP671-1 | |
| CPC+14 | LifeTein | LT1524 | Custom designed peptide |
| CPC+20 | LifeTein | LT1525 | Custom designed peptide |
| CPC+8 | LifeTein | LT1523 | Custom designed peptide |
| Delicate Task Wipers | Kimberly-Clark Professional | 34155 | |
| Dermal Punch | MedBlades | MB5-1 | 3, 4 and 6 mm |
| Economy Plain Glass Microscope Slides | Fisherbrand | 12550A3 | |
| Flat Bottom Cell Culture Plates | Corning Costar | 3595 | Clear, 96 well |
| Flexible Wrapping Film | Bemis Parafilm M Laboratory | 1337412 | |
| Gold Seal Cover Glass | Electron Microscopy Sciences | 6378701 | # 1.5, 18×18 mm |
| Hammer-Driven Hole Punch | McMaster-Carr | 3427A15 | 1/2" Diameter |
| Hammer-Driven Hole Punch | McMaster-Carr | 3427A19 | 3/4" Diameter |
| Laser | Chroma Technology | AT480/30m | Spectrophotometer Laser Light |
| Low-Strength Steel Hex Nut | McMaster-Carr | 90480A007 | 6-32 Thread size |
| LSM 700 Confocal Microscope | Zeiss | LSM 700 | |
| Micro Magnetic Stirring Bars | Bel-Art Spinbar | F37119-0007 | 7×2 mm |
| Multipurpose Neoprene Rubber Sheet | McMaster-Carr | 1370N12 | 1/32" Thickness |
| Non-Fat Dried Bovine Milk | Sigma Aldrich | M7409 | |
| Petri Dish | Chemglass Life Sciences | CGN1802145 | 150 mm diameter |
| Phosphate-Buffered Saline | Corning | 21-040-CMR | 1x |
| Plate Shaker | VWR | 89032-088 | |
| Protease Inhibitors | Thermo Scientific | A32953 | |
| Razor Blades | Fisherbrand | 12640 | |
| R-Cast Acrylic Thin Gauge Sheet | Reynolds Polymer | N/A | Black transport chamber inserts |
| RTV Silicone | Loctite | 234323 | Epoxy, Non-corrosive, clear |
| Scalpel | TedPella | 549-3 | #10, #11 blades |
| Signal Receiver | Chroma Technology | ET515lp | Spectrophotometer Laser Signal Receiver |
| Snap-Cap Microcentrifuge Tubes | Eppendorf | 22363204 | 1.5 mL |
| Spatula | TedPella | 13508 | |
| Synergy H1 Microplate Reader | Biotek | H1M | |
| Zinc-Plated Alloy Steel Socket Head Screw | McMaster-Carr | 90128A153 | 6-32 Thread size, 1" Long |
References
- Bajpayee, A. G., Grodzinsky, A. J. Cartilage-targeting drug delivery: can electrostatic interactions help. Nature Reviews Rheumatology. 13 (3), 183-193 (2017).
- Maroudas, A. Transport of solutes through cartilage: permeability to large molecules. Journal of Anatomy. 122, 335-347 (1976).
- Bajpayee, A. G., Wong, C. R., Bawendi, M. G., Frank, E. H., Grodzinsky, A. J. Avidin as a model for charge driven transport into cartilage and drug delivery for treating early stage post-traumatic osteoarthritis. Biomaterials. 35 (1), 538-549 (2014).
- Vedadghavami, A., et al. Cartilage penetrating cationic peptide carriers for applications in drug delivery to avascular negatively charged tissues. Acta Biomaterialia. 93, 258-269 (2019).
- Mehta, S., Akhtar, S., Porter, R. M., Önnerfjord, P., Bajpayee, A. G. Interleukin-1 receptor antagonist (IL-1Ra) is more effective in suppressing cytokine-induced catabolism in cartilage-synovium co-culture than in cartilage monoculture. Arthritis Research & Therapy. 21 (1), 238 (2019).
- Vedadghavami, A., Zhang, C., Bajpayee, A. G. Overcoming negatively charged tissue barriers: Drug delivery using cationic peptides and proteins. Nano Today. 34, 100898 (2020).
- Young, C. C., Vedadghavami, A., Bajpayee, A. G. Bioelectricity for Drug Delivery: The Promise of Cationic Therapeutics. Bioelectricity. , (2020).
- Felson, D. T. Osteoarthritis of the knee. New England Journal of Medicine. 354 (8), 841-848 (2006).
- Wieland, H. A., Michaelis, M., Kirschbaum, B. J., Rudolphi, K. A. Osteoarthritis – An untreatable disease. Nature Reviews Drug Discovery. 4 (4), 331-344 (2005).
- Martel-Pelletier, J. Pathophysiology of osteoarthritis. Osteoarthritis and Cartilage. 7 (4), 371-373 (1999).
- Sophia Fox, A. J., Bedi, A., Rodeo, S. A. The basic science of articular cartilage: Structure, composition, and function. Sports Health. 1 (6), 461-468 (2009).
- Chevalier, X., et al. Intraarticular injection of anakinra in osteoarthritis of the knee: A multicenter, randomized, double-blind, placebo-controlled study. Arthritis Care and Research. 61 (3), 344-352 (2009).
- Cohen, S. B., et al. A randomized, double-blind study of AMG 108 (a fully human monoclonal antibody to IL-1R1) in patients with osteoarthritis of the knee. Arthritis Research and Therapy. 13 (4), 125 (2011).
- Evans, C. H., Kraus, V. B., Setton, L. A. Progress in intra-articular therapy. Nature Reviews Rheumatology. 10 (1), 11-22 (2014).
- He, T., et al. Multi-arm Avidin nano-construct for intra-cartilage delivery of small molecule drugs. Journal of Controlled Release. 318, 109-123 (2020).
- Bajpayee, A. G., Scheu, M., Grodzinsky, A. J., Porter, R. M. A rabbit model demonstrates the influence of cartilage thickness on intra-articular drug delivery and retention within cartilage. Journal of Orthopaedic Research. 33 (5), 660-667 (2015).
- Bajpayee, A. G., Quadir, M. A., Hammond, P. T., Grodzinsky, A. J. Charge based intra-cartilage delivery of single dose dexamethasone using Avidin nano-carriers suppresses cytokine-induced catabolism long term. Osteoarthritis and Cartilage. 24 (1), 71-81 (2016).
- Zhang, C., et al. Avidin-biotin technology to synthesize multi-arm nano-construct for drug delivery. MethodsX. , 100882 (2020).
- Wagner, E. K., et al. Avidin grafted dextran nanostructure enables a month-long intra-discal retention. Scientific Reports. 10.1, 1-14 (2020).
- Troeberg, L., Nagase, H. Proteases involved in cartilage matrix degradation in osteoarthritis. Biochimica et Biophysica Acta – Proteins and Proteomics. 1824 (1), 133-145 (2012).
- Kirk, T. B., Wilson, A. S., Stachowiak, G. The effects of dehydration on the surface morphology of articular cartilage. Journal of Orthopaedic Rheumatology. 6 (2-3), 75-80 (1993).
- Ateshian, G. A., Maas, S., Weiss, J. A. Solute transport across a contact interface in deformable porous media. Journal of Biomechanics. 45 (6), 1023-1027 (2012).
- Arbabi, V., Pouran, B., Weinans, H., Zadpoor, A. A. Multiphasic modeling of charged solute transport across articular cartilage: Application of multi-zone finite-bath model. Journal of Biomechanics. 49 (9), 1510-1517 (2016).
- Arbabi, V., Pouran, B., Zadpoor, A. A., Weinans, H. An experimental and finite element protocol to investigate the transport of neutral and charged solutes across articular cartilage. Journal of Visualized Experiments. 2017 (122), (2017).
- Sampson, S. L., Sylvia, M., Fields, A. J. Effects of dynamic loading on solute transport through the human cartilage endplate. Journal of Biomechanics. 83, 273-279 (2019).
- Bajpayee, A. G., Scheu, M., Grodzinsky, A. J., Porter, R. M. Electrostatic interactions enable rapid penetration, enhanced uptake and retention of intra-articular injected avidin in rat knee joints. Journal of Orthopaedic Research : Official Publication of the Orthopaedic Research Society. 32 (8), 1044-1051 (2014).
- Bajpayee, A. G., et al. Sustained intra-cartilage delivery of low dose dexamethasone using a cationic carrier for treatment of post traumatic osteoarthritis. European Cells & Materials. 34, 341-364 (2017).
- Malda, J., et al. Of Mice, Men and Elephants: The Relation between Articular Cartilage Thickness and Body Mass. PLoS One. 8 (2), 57683 (2013).
- Frisbie, D. D., Cross, M. W., McIlwraith, C. W. A comparative study of articular cartilage thickness in the stifle of animal species used in human pre-clinical studies compared to articular cartilage thickness in the human knee. Veterinary and Comparative Orthopaedics and Traumatology. 19 (3), 142-146 (2006).

