تحريض التدفق الدقيق بواسطة تذبذبات الفقاعات غير الكروية في نظام الرفع الصوتي
Summary
تم اقتراح تقنية سريعة وموثوقة للتحكم في تذبذبات شكل فقاعة صوتية واحدة محاصرة تعتمد على تقنية الالتحام بين فقاعتين. تسمح تذبذبات شكل الفقاعة المستقرة التي يتم التحكم فيها بالتماثل بتحليل تدفق السوائل المتولد بالقرب من واجهة الفقاعة.
Abstract
عندما تقع بالقرب من الحواجز البيولوجية ، قد تزيد الفقاعات الدقيقة المتذبذبة من نفاذية غشاء الخلية ، مما يسمح باستيعاب الأدوية والجينات. تشير الملاحظات التجريبية إلى أن الاختراق المؤقت لهذه الحواجز قد يكون بسبب إجهاد القص الذي يمارس على أنسجة الخلايا عن طريق التجويف المجهري. التدفق الدقيق للتجويف هو توليد تدفقات دوامة تنشأ حول الفقاعات الدقيقة المتذبذبة بالموجات فوق الصوتية. لإنتاج مثل هذه التدفقات السائلة ، يجب أن تنحرف تذبذبات الفقاعات عن التذبذبات الكروية البحتة وتتضمن إما عدم استقرار انتقالي أو أوضاع شكل. غالبا ما تكون الدراسات التجريبية للتدفقات التي تسببها الفقاعات وإجهاد القص على الأسطح القريبة مقيدة في نطاقها بسبب صعوبة التقاط تشوهات شكل الفقاعات الدقيقة بطريقة مستقرة ويمكن التحكم فيها. وصفنا تصميم غرفة الرفع الصوتية لدراسة التذبذبات غير الكروية التي يتم التحكم فيها بالتماثل. يتم إجراء هذا التحكم باستخدام تقنية الالتحام بين فقاعتين تقتربان في مجال الموجات فوق الصوتية المكثف بدرجة كافية. يفتح التحكم في التذبذبات غير الكروية الطريق أمام التدفق الدقيق للتجويف المتحكم فيه لفقاعة دقيقة متذبذبة سطحيا حرة. تسمح الكاميرات ذات معدل الإطارات العالي بالتحقيق في ديناميكيات الفقاعات غير الكروية في وقت واحد تقريبا على مقياس زمني صوتي وتدفق السائل في نطاق زمني أقل. يتبين أنه يمكن الحصول على مجموعة كبيرة ومتنوعة من أنماط السوائل وأنها مرتبطة بالمحتوى المشروط لواجهة الفقاعة. لقد أثبتنا أنه حتى أوضاع الشكل عالية الترتيب يمكن أن تخلق أنماطا للسوائل لمسافات كبيرة إذا كانت ديناميكيات الواجهة تحتوي على عدة أوضاع ، مما يسلط الضوء على إمكانات التذبذبات غير الكروية لتوصيل الدواء المستهدف والموضعي.
Introduction
في الطب ، يجب أن يخترق الدواء المدار العديد من العقبات في النظام الحي قبل الوصول إلى الأهداف المرجوة. ومع ذلك ، يتم تنظيف معظم الأدوية بسرعة بعيدا عن مجرى الدم. كفاءة الاستهداف منخفضة ولا يمكنها عبور أغشية الخلايا بسهولة ، مما يؤدي إلى توصيل الدواء بشكل غير فعال. حاليا ، تم اقتراح استخدام الفقاعات الدقيقة مع الموجات فوق الصوتية كطريقة مبتكرة للتوصيل غير الجراحي والدقيق والمستهدف للأدوية والجينات إلى الأنسجة والخلايا المرضية1. في هذا النهج ، يمكن أن تلعب الفقاعات الدقيقة دورا كناقلات حيث يتم حقن الأدوية المجانية إما بتعليق فقاعة الغاز أو تحميلها على سطحها. يمكن أن تعمل الفقاعات الدقيقة أيضا كناقل محلي لإعادة تركيز طاقة الموجات فوق الصوتية من أجل التفاعل مع الخلايا. في الأساس ، تحت التعرض للموجات فوق الصوتية ، تضغط الفقاعات وتتوسع بثبات ، وهو نظام يسمى التجويف المستقر الذي يولد تدفقات سائلة وبالتالي إجهاد القص على الأشياء القريبة. قد تتذبذب الفقاعات الدقيقة أيضا بشكل غير خطي وتتوسع حتى الانهيار ، في نظام التجويف بالقصور الذاتي ، مما ينتج عنه موجات صدمة تنتشر شعاعيا من موقع الانهيار2. لقد ثبت أن التجويف ، سواء كان مستقرا أو بالقصور الذاتي ، يعزز نفاذية أغشية الخلايا ، وبالتالي يعزز استيعاب الأدوية في الخلية3.
في التطبيقات العلاجية ، يعد فهم آلية تفاعل خلية الفقاعة أمرا مهما للغاية ، ولكن هناك العديد من الحواجز ، من الجانبين العلمي والتقني ، التي تمنع معرفتنا من التقدم. أولا ، من الصعب للغاية التقاط ديناميكيات الخلايا استجابة للمحفزات الميكانيكية التي تسببها الفقاعات4. في النطاق الزمني الصوتي ، يمكن أن تؤدي تذبذبات الفقاعات الدقيقة من الدرجة الأولى إلى تنشيط قنوات الغشاء ، مما يسهل المرور الجزيئي عبر الواجهات البيولوجية. يحدث هذا من خلال التذبذب المباشر لغشاء الخلية ، ويسمى أيضا “التدليك الخلوي”5. تم إثبات تنشيط القناة بعد الإجهاد الميكانيكي المباشر باستخدام تقنيات المشبك الرقعي التي تقيس الخصائص الفيزيولوجية الكهربية لأغشية الخلايا أثناء وبعد التعرض للموجات فوق الصوتية6. إن قياس ديناميكيات الخلايا التي تسببها الفقاعات (بمعنى المجال الكامل لتشوه غشاء الخلية) على النطاق الزمني الصوتي ، سيوفر أيضا رؤى حول عتبة توسع منطقة الغشاء Δ A/ A المطلوبة لحث المسام في غشاء الخلية7. الحاجز الثاني هو التحكم في نظام الفقاعة المنهارة لتجنب تحلل الخلايا الناجم عن الفقاعات الدقيقة. تم تحديد انهيار الفقاعات والنفاثات الدقيقة المستحثة كآلية يحدث من خلالها ثقب الغشاء 8,9. بمجرد أن يتخلل ، يتم إصلاح غشاء الخلية من خلال الختم الذاتي للكالسيوم للطبقات الثنائية الدهنية واندماج الحويصلات داخل الخلايا9. قد يتسبب حدوث انهيارات الفقاعات أيضا في حدوث أضرار قاتلة للخلية وإحداث آثار جانبية غير ضرورية في الخلايا المحيطة. في التطبيقات الحساسة مثل فتح الحاجز الدموي الدماغي بوساطة الموجات فوق الصوتية ، من المقبول عموما أنه يجب تجنب انهيار الفقاعات بالقصور الذاتي10.
لذلك ، يتم حاليا تكريس جهود ضخمة لتصميم تسلسل انبعاثات الموجات فوق الصوتية ، إلى جانب مراقبة التجويف السلبي والتحكم فيه ، من أجل ضمان تذبذبات مستقرة للفقاعات الدقيقة11. في هذا النظام المستقر ، تم افتراض أن الفقاعات المتذبذبة بشكل ثابت تلعب دورا قويا في تحفيز نفاذية الغشاء من خلال تعزيز إجهاد القص المستهدف مكانيا على غشاء الخلية7. ينتج إجهاد القص عن تدفقات السائل الناتجة بالقرب من الفقاعات المتذبذبة. تسمى هذه التدفقات السائلة microstreaming التجويف ، وكما ذكر أعلاه ، فهي واحدة من العديد من الآليات الممكنة المسؤولة عن تعزيز امتصاص الجزيئات خارج الخلية. عند التعامل مع تعليق الفقاعات أو الخلايا مثل فحوصات النقل البيولوجي في المختبر12 ، قد تكون النفاذية عن طريق البث الدقيق أكثر كفاءة من النفاذية عن طريق انهيار الفقاعة. يمكن إظهار ذلك من خلال اعتبار هندسي بسيط. في تعليق الخلية ، سيكون sonoporation فعالا إذا تم تقديم غالبية الخلايا المعلقة لتأثيرات ميكانيكية كبيرة بما فيه الكفاية (مما يؤدي إلى نفاذية الغشاء). من المعروف أن انهيارات الفقاعات يتم توجيهها على طول اتجاه كسر التماثل الخواص ، مثل محور جدار الفقاعة13 أو خط الفقاعة وخلية الفقاعة الذي ينضم إلى مركز الكتلة14. وبالتالي فإن النفاثة الصغيرة المنتجة هي ظاهرة موضعية مكانيا على طول عدد محدود من الخطوط التي تربط مراكز الخلية والفقاعات. اعتمادا على تركيز الخلية والفقاعة ، وكذلك المسافة بين خلية الفقاعة ، قد لا يكون هذا التأثير هو الأكثر كفاءة لاختراق العدد الكامل للخلايا العالقة. في المقابل ، يعد التدفق الدقيق للتجويف ظاهرة تحدث في نطاق زمني بطيء ، مع توسع مكاني كبير مقارنة بنصف قطر الفقاعة. أيضا ، يتم توزيع تدفق السائل في جميع أنحاء الفقاعة ، وبالتالي قد يؤثر على عدد أكبر من الخلايا ، على مدى طويل جدا. لذلك ، فإن فهم التدفق الدقيق للتجويف المتولد حول فقاعة متذبذبة هو شرط أساسي للتحكم في إجهاد القص الناجم عن الفقاعة الذي يتم تطبيقه على الخلايا وتحديده.
للقيام بذلك ، تتمثل الخطوة الأولية في التحكم في التذبذبات الكروية وغير الكروية للفقاعة التي تحركها الموجات فوق الصوتية ، حيث يتم تحفيز تدفقات السائل المتولدة بواسطة حركة واجهة الفقاعة15,16. على وجه الخصوص ، يجب تشغيل تذبذبات شكل الفقاعات الدقيقة والحفاظ على استقرارها. علاوة على ذلك ، يجب التحكم في اتجاه تذبذبات شكل الفقاعة لتحليل العلاقة بين ديناميكيات واجهة الفقاعة ونمط التدفق الدقيق المستحث بشكل صحيح. عند تلخيص الأدبيات الموجودة ، من الواضح أن النتائج التجريبية التفصيلية للتدفق الدقيق الناجم عن التجويف متاحة فقط للفقاعات المرتبطة بالسطح. تستخدم الفقاعات الدقيقة المتصلة بالجدار بشكل شائع لتقييم ديناميكيات الواجهة الدقيقة وتفاعلات الخلايا على مقياس الميكرومتر تحت نظام الفحص المجهري فائق السرعة. هذا التكوين مناسب علاجيا عند التفكير في الفقاعات الدقيقة المهتزة الموجودة على غشاء الخلية17،18،19. ومع ذلك ، فإن دراسة الفقاعة المرتبطة بالركيزة قد تجعل تحليل ديناميكيات الفقاعات أكثر تعقيدا ، ويرجع ذلك جزئيا إلى الطبيعة المعقدة لديناميكيات خط الاتصال20 ، وتشغيل أوضاع الشكل غير المتماثل21. في التطبيقات الطبية والبيولوجية ، توجد الفقاعات غير المتصلة بالجدار بشكل شائع في الأشكال الهندسية المحصورة مثل الأوعية الصغيرة. هذا يؤثر بشكل كبير على ديناميكيات الفقاعة وعدم استقرار الشكل. على وجه الخصوص ، يؤدي وجود جدار قريب إلى تحويل عتبة الضغط لوضع الشكل مما يؤدي إلى انخفاض قيم الضغط اعتمادا على رقم وضع الشكل وحجم الفقاعة22. يؤثر الجدار أيضا على التدفق الدقيق الناجم عن الفقاعة مع احتمال كثافة أعلى للتدفق المنتج23.
من بين جميع السيناريوهات المحتملة التي قد تواجهها الفقاعات الدقيقة (حرة أو متصلة ، قريبة من جدار ، تنهار أو تتأرجح بثبات) ، نقترح التحقيق في الديناميكيات غير الكروية لفقاعة واحدة بعيدة عن أي حدود. يعتمد الإعداد التجريبي على نظام الرفع الصوتي24 حيث يتم استخدام موجة الموجات فوق الصوتية الدائمة لاحتجاز الفقاعة. يتوافق هذا السيناريو مع التطبيقات الطبية التي تتعايش فيها مجموعة من الفقاعات والخلايا العالقة في غرفة نقل الصوت ، على سبيل المثال. بقدر ما تكون الفقاعات والخلايا ليست قريبة جدا ، فمن المفترض أن وجود خلية لا يؤثر على ديناميكيات واجهة الفقاعة. عندما تتبع الخلايا المسارات الشبيهة بالحلقة للتدفق الدقيق الناجم عن التجويف ، فإنها تقترب بشكل دوري وتتنافر من موقع الفقاعة ويمكننا أن نفترض أن وجود الخلية لا يؤثر على نمط التدفق ولا سرعته المتوسطة. بالإضافة إلى ذلك ، فإن الديناميكيات غير الكروية والتدفق الدقيق المستحث من فقاعات مفردة بعيدة عن الحدود معروفة جيدا من وجهة نظر نظرية. من أجل ربط تدفق السائل الناجم عن الفقاعة بديناميكيات كفاف الفقاعة ، يلزم توصيف ديناميكيات واجهة الفقاعة بدقة. للقيام بذلك ، من الأفضل تكييف النطاق الزماني المكاني في الدراسات التجريبية فيما يتعلق بتلك المستخدمة في العلاجات بحيث يكون الحصول على كاميرات عالية السرعة شائعة (أقل من 1 مليون إطار / ثانية) ممكنا باستخدام فقاعات كبيرة متحمسة عند ترددات منخفضة. عند النظر في الفقاعات غير المطلية ، يرتبط التردد الذاتي ω n لنمط معين n بحجم الفقاعة مثل 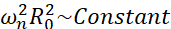 25. يتم تعديل علاقة نصف القطر والتردد الذاتي هذه بشكل طفيف عند النظر في الفقاعات المقشرة26 ، لكن ترتيب حجم التردد الذاتي ωn يظل كما هو. وبالتالي ، فإن فحص الفقاعات ذات أنصاف أقطار التوازن ~ 50 ميكرومتر في مجال الموجات فوق الصوتية 30 كيلو هرتز يشبه دراسة الفقاعات المغلفة من أنصاف الأقطار ~ 3 ميكرومتر في مجال 1.7 ميجاهرتز ، على النحو الذي اقترحه Dollet et al.27. لذلك من المتوقع أن تكون أرقام وضع الشكل مماثلة وبالتالي أنماط البث المصغر.
25. يتم تعديل علاقة نصف القطر والتردد الذاتي هذه بشكل طفيف عند النظر في الفقاعات المقشرة26 ، لكن ترتيب حجم التردد الذاتي ωn يظل كما هو. وبالتالي ، فإن فحص الفقاعات ذات أنصاف أقطار التوازن ~ 50 ميكرومتر في مجال الموجات فوق الصوتية 30 كيلو هرتز يشبه دراسة الفقاعات المغلفة من أنصاف الأقطار ~ 3 ميكرومتر في مجال 1.7 ميجاهرتز ، على النحو الذي اقترحه Dollet et al.27. لذلك من المتوقع أن تكون أرقام وضع الشكل مماثلة وبالتالي أنماط البث المصغر.
من أجل تشغيل تذبذبات غير كروية لواجهة الفقاعة ، من الضروري تجاوز عتبة ضغط معينة تعتمد على نصف القطر ، كما هو موضح في الشكل 1. تعتمد التقنيات التجريبية الحالية على زيادة الضغط الصوتي لتحريك الأنماط السطحية (الموضحة بالمسار (1) في الشكل 1) ، إما عن طريق زيادة الضغط خطوة بخطوة28 أو عن طريق إثارة السعة المعدلة المسؤولة عن البداية الدورية وانقراض أوضاع السطح29. العيوب الرئيسية لهذه التقنيات هي (i) الاتجاه العشوائي لمحور التماثل للتذبذبات السطحية التي لا يمكن التحكم فيها لتكون في مستوى التصوير ، (ii) عمر قصير لتذبذبات شكل الفقاعة التي تجعل تحليل تدفقات السائل المستحثة صعبا في نطاقات زمنية أكبر ، و (iii) التشغيل المتكرر لأوضاع الشكل غير المستقرة. نقترح تقنية بديلة لعبور عتبة الضغط عند ضغط صوتي ثابت في خريطة نصف القطر / الضغط ، كما هو موضح في المسار (2) في الشكل 1. للقيام بذلك ، يلزم زيادة حجم الفقاعة بحيث تكون في منطقة عدم الاستقرار. يتم تنفيذ هذه الزيادة بواسطة تقنية اندماج الفقاعة. يتم استغلال اندماج فقاعتين صغيرتين ، متذبذبتين كرويا في البداية ، لإنشاء فقاعة واحدة مشوهة. إذا كان الضغط الصوتي وحجم الفقاعة للفقاعة المدمجة في منطقة عدم الاستقرار ، يتم تشغيل أوضاع السطح. لقد أثبتنا أيضا أن تقنية الالتحام تحفز تذبذبات الشكل المستقر في نظام الحالة المستقرة ، بالإضافة إلى محور تناظر متحكم فيه تحدده الحركة المستقيمة للفقاعتين المقتربتين. نظرا لأن تذبذب الشكل المستقر مضمون على مدار دقائق ، فإن تحليل تدفق السوائل الناجم عن الفقاعات ممكن عن طريق بذر الوسط السائل بجزيئات دقيقة فلورية مضاءة بواسطة ورقة ليزر رقيقة. يسمح تسجيل حركة الجسيمات الدقيقة الصلبة بالقرب من واجهة الفقاعة بتحديد نمط تدفق السائل المستحث30. يوضح الشكل 2 المبدأ العام لتحفيز تذبذبات شكل الفقاعة ، مما يؤدي إلى تدفق سائل مستقر زمنيا.
في البروتوكول التالي ، نوضح الخطوات المطلوبة لإنشاء تذبذبات مستقرة على شكل فقاعة عبر تقنية الالتحام ونصف قياسات تدفق السوائل. يتضمن ذلك تصميم نظام الرفع الصوتي ، والمعايرة الصوتية ، ونواة الفقاعات وتقنية الالتحام ، وقياس ديناميكيات واجهة الفقاعة وتدفق السوائل المحيطة ، ومعالجة الصور.
Protocol
Representative Results
Discussion
يتكون الإجراء المقدم من استخدام اندماج الفقاعات من أجل تحفيز تذبذبات شكل الفقاعة المستقرة التي يتم التحكم فيها بالتماثل ، مما يسمح بدراسة تدفق السوائل على المدى الطويل الناجم عن هذه التذبذبات. التحدي الرئيسي في هذه التقنية هو التحكم في التذبذبات غير الكروية للفقاعة المحاصرة ، بعيدا عن أ?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
تم دعم هذا العمل من قبل LabEx CeLyA من جامعة ليون (ANR-10-LABX-0060 / ANR-11-IDEX-0007).
Materials
| Aspherical lens | Thorlabs | AL4050 | Lens of focus 40 mm |
| Continuous wave laser source | CNI | MLL6FN | DPSS laser of wavelength 532nm, energy 400 mW |
| Cylindrical plano-concave lens | Thorlabs | LJ1277L1-A | lens of focus -25?4mm |
| Cylindrical plano-concave lens | Thorlabs | LK1900L1 | lens of focus 250 mm |
| Fluorescent particles | Duke Scientific | R700 | Red polymer fluorescent microspheres |
| Function generator | Agilent | HP33120 | Generator of function feeding the ultrasound transducer |
| High-speed camera | Vision Research | Phantom v12.0 | High-speed recording up to 1 Mfps |
| Liquid medium | Carlo Erba | Water for analysis | Demineralized, undegassed water |
| Multiphysics software | Comsol | None | Softwate for simulating the acoustic field of the levitation chamber |
| Nd:Yag pulsed laser | New Wave Research | Solo III-15 | 5 ns pulse duration, λ=532 nm, 3.5 mm beam diameter, up to 50 mJ |
| Plano-concave lens | Thorlabs | N-BK7 | lens of focus 125 mm |
| Spherical concave lens | Thorlabs | N-SF11 | Bi-concave lens of focus -25mm |
| Ultrasound transducer | SinapTec | Custom-made | Nominal frequency 31kHz, active area 35mm diameter |
| Visualization software | NIH | ImageJ | Software for image processing and analysis in Java |
| XY Linear stage | Newport | M-406 | Displacement stage with micrometric screw |
| Z-axis linear stage | Edmund Optics | 62-299 | Vertical displacement stage with micrometric screw |
References
- Roovers, S., et al. The role of ultrasound-driven microbubble dynamics in drug delivery: from microbubble fundamentals to clinical translation. Langmuir. 35 (31), 10173-10191 (2019).
- Liu, H. L., Fan, C. H., Ting, C. Y., Yeh, C. K. Combining microbubbles and ultrasound for drug delivery to brain tumors: current progress and overview. Theranostics. 4 (4), 432-444 (2014).
- Lammertink, B. H. A., et al. Sonochemotherapy: from bench to bedside. Frontiers in Pharmacology. 6, 138 (2015).
- Lajoinie, G., et al. In vitro methods to study bubble-cell interactions: fundamentals and therapeutic applications. Biomicrofluidics. 10, 011501 (2016).
- Van Wamel, A., Bouakaz, A., Versluis, M., de Jong, N. Micromanipulation of endothelial cells: ultrasound-microbubble-cell interaction. Ultrasound in Medicine and Biology. 30, 1255-1258 (2004).
- Tran, T. A., Roger, S., Le Guennec, J. Y., Tranquart, F., Bouakaz, A. Effect of ultrasound-activated microbubbles on the cell electrophysiological properties. Ultrasound in Medicine and Biology. 33, 158-163 (2007).
- Marmottant, P., Hilgenfeldt, S. Controlled vesicle deformation and lysis by single oscillating bubbles. Nature. 423 (6936), 153-156 (2003).
- Prentice, P. A., Cuschieri, K., Dholakia, K., Prausnitz, M., Campbell, P. Membrane disruption by optically controlled microbubble cavitation. Nature Physics. 1, 107-110 (2005).
- Kudo, N., Okada, K., Yamamoto, K. Sonoporation by single-shot pulsed ultrasound with microbubbles adjacent to cells. Biophysical Journal. 96, 4866-4876 (2009).
- Novell, A., et al. A new safety index based on intrapulse monitoring of ultra-harmonic cavitation during ultrasound-induced blood-brain barrier opening procedures. Scientific Reports. 10, 10088 (2020).
- Cornu, C., et al. Ultrafast monitoring and control of subharmonic emissions of an unseeded bubble cloud during pulsed sonication. Ultrasonics Sonochemistry. 42, 697-703 (2018).
- Reslan, L., Mestas, J. L., Herveau, S., Béra, J. C., Dumontet, C. Transfection of cells in suspension by ultrasound cavitation. Journal of Controlled Release. 142 (2), 251-258 (2010).
- Reuter, F., Gonzalez-Avila, S. R., Mettin, R., Ohl, C. D. Flow fields and vortex dynamics of bubbles collapsing near a solid boundary. Physical Review Fluids. 2, 064202 (2017).
- Chew, L. W., Klaseboer, E., Ohl, S. W., Khoo, B. C. Interaction of two differently sized oscillating bubbles in a free field. Physical Review E. 84, 066307 (2011).
- Doinikov, A. A., Bouakaz, A. Acoustic microstreaming around a gas bubble. The Journal of the Acoustical Society of America. 127 (2), 703-709 (2010).
- Tho, P., Manasseh, R., Ooi, A. Cavitation microstreaming patterns in single and multiple bubble systems. Journal of Fluid Mechanics. 576, 191-233 (2007).
- Van Wamel, A., et al. Vibrating microbubbles poking individual cells: Drug transfer into cells via sonoporation. Journal of Controlled Release. 112, 149-155 (2006).
- Helfield, B., Chen, X., Watkins, S. C., Villanueva, F. S. Biophysical insight into mechanisms of sonoporation. PNAS. 113 (36), 9983-9988 (2016).
- Pereno, V., et al. Layered acoustofluidic resonators for the simultaneous optical and acoustic characterization of cavitation dynamics, microstreaming, and biological effects. Biomicrofluidics. 12, 034109 (2018).
- Shklyaev, S., Straube, A. V. Linear oscillations of a compressible hemispherical bubble on a solid substrate. Physics of Fluids. 20, 052102 (2008).
- Fauconnier, M., Bera, J. C., Inserra, C. Nonspherical modes non-degeneracy of a tethered bubble. Physical Review E. 102, 033108 (2020).
- Xi, X., Cegla, F., Mettin, R., Holsteyns, F., Lippert, A. Study of non-spherical bubble oscillations near a surface in a weak acoustic standing wave field. The Journal of the Acoustical Society of America. 135, 1731 (2014).
- Doinikov, A. A., Bouakaz, A. Effect of a distant rigid wall on microstreaming generated by an acoustically driven gas bubble. Journal of Fluid Mechanics. 742, 425-445 (2014).
- Cleve, S., Guédra, M., Inserra, C., Mauger, C., Blanc-Benon, P. Surface modes with controlled axisymmetry triggered by bubble coalescence in a high-amplitude acoustic field. Physical Review E. 98, 033115 (2018).
- Lamb, H. . Hydrodynamics. 6th ed. , (1932).
- Liu, Y., Wang, Q. Stability and natural frequency of nonspherical mode of an encapsulated microbubble in a viscous liquid. Physics of Fluids. 28, 062102 (2016).
- Dollet, B., et al. Nonspherical oscillations of ultrasound contrast agent microbubbles. Ultrasound in Medicine and Biology. 34 (9), 1465-1473 (2008).
- Versluis, M., et al. Microbubble shape oscillations excited through ultrasonic parametric driving. Physical Review E. 82, 026321 (2010).
- Guédra, M., Cleve, S., Mauger, C., Blanc-Benon, P., Inserra, C. Dynamics of nonspherical microbubble oscillations above instability threshold. Physical Review E. 96, 063104 (2017).
- Cleve, S., Guédra, M., Mauger, C., Inserra, C., Blanc-Benon, P. Microstreaming induced by acoustically trapped, non-spherically oscillating microbubbles. Journal of Fluid Mechanics. 875, 597-621 (2019).
- Doinikov, A. A., Cleve, S., Regnault, G., Mauger, C., Inserra, C. Acoustic microstreaming produced by nonspherical oscillations of a gas bubble. I. Case of modes 0 and m. Physical Review E. 100, 033104 (2019).
- Inserra, C., Regnault, G., Cleve, S., Mauger, C., Doinikov, A. A. Acoustic microstreaming produced by nonspherical oscillations of a gas bubble. III. Case of self-interacting modes n-n. Physical Review E. 101, 013111 (2020).
- Prabowo, F., Ohl, C. D. Surface oscillations and jetting from surface attached acoustic driven bubbles. Ultrasonics Sonochemistry. 18 (1), 431-435 (2011).
- Garbin, V., et al. Changes in microbubble dynamics near a boundary revealed by combined; optical micromanipulation and high-speed imaging. Applied Physics Letters. 90, 114103 (2007).
- Collis, J., et al. Cavitation microstreaming and stress fields created by microbubbles. Ultrasonics. 50, 273-279 (2010).
- Loughran, J., Eckersley, R. J., Tang, M. X. Modeling non-spherical oscillations and stability of acoustically driven shelled microbubbles. The Journal of the Acoustical Society of America. 131 (6), 4349-4357 (2012).
- Vos, H. J., Dollet, B., Bosch, J. G., Versluis, M., de Jong, N. Nonspherical vibrations of microbubbles in contact with a wall – a pilot study at low mechanical index. Ultrasound in Medicine and Biology. 34 (4), 685-688 (2008).
- Regnault, G., Mauger, C., Blanc-Benon, P., Inserra, C. Secondary radiation force between two closely spaced acoustic bubbles. Physical Review E. 102, 031101 (2020).

