En 3D kartografisk beskrivelse av cellen av Cryo Soft X-ray Tomography
Summary
Her presenteres en protokoll som beskriver prøveforberedelsen og datainnsamlingstrinnene som kreves i cryo soft X-ray tomografi (SXT) for å avbilde ultrastrukturen til hele kryobevarte celler med en oppløsning på 25 nm halv tonehøyde.
Abstract
Avbildningsteknikker er grunnleggende for å forstå celleorganisasjon og maskineri i biologisk forskning og relaterte felt. Blant disse teknikkene tillater kryo myk røntgentomografi (SXT) avbildning av hele kryokonserverte celler i vannvinduets røntgenenergiområde (284-543 eV), der karbonstrukturer har iboende høyere absorpsjon enn vann, slik at 3D-rekonstruksjonen av absorpsjons lineær koeffisient av materialet som finnes i hver voksel. Kvantitativ strukturell informasjon på nivået av hele celler opp til 10 μm tykk er da oppnåelig på denne måten, med høy gjennomstrømning og romlig oppløsning ned til 25-30 nm halv pitch. Cryo-SXT har vist seg relevant for dagens biomedisinske forskning, og gir 3D-informasjon om cellulære infeksjonsprosesser (virus, bakterier eller parasitter), morfologiske endringer på grunn av sykdommer (som recessive genetiske sykdommer) og hjelper oss med å forstå narkotikavirkning på cellenivå, eller lokalisere spesifikke strukturer i 3D-cellemiljøet. I tillegg, ved å dra nytte av den justerbare bølgelengden på synkrotronanlegg, spektroskopi eller dens 3D-motstykke, kan spektrotomografi også brukes til å avbilde og kvantifisere spesifikke elementer i cellen, for eksempel kalsium i biomineraliseringsprosesser. Cryo-SXT gir komplementær informasjon til andre biologiske avbildningsteknikker som elektronmikroskopi, røntgenfluorescens eller synlig lysfluorescens, og brukes vanligvis som partnermetode for 2D- eller 3D-korrelativ avbildning ved kryogeniske forhold for å koble funksjon, plassering og morfologi.
Introduction
Cryo-SXT kan spille en sentral rolle i biologisk bildeforskning, da det gir 3D-middels oppløsning (25-30 nm halv tonehøyde) volumer av hydrerte hele celler 1,2,3,4,5,6. I vannvinduets energiområde, mellom karbon og oksygenabsorpsjon K kanter (4,4-2,3 nm), absorberer karbonrike cellulære strukturer 10 ganger mer enn det oksygenrike mediet som gjennomsyrer og omgir dem. I dette energiområdet kan vitrifiserte celler opp til 10 μm tykkelse avbildes uten behov for seksjonering eller farging, noe som fører til kvantitative høyabsorpsjonskontrastprojeksjoner, som, kombinert med prøverotasjonsevner, tillater tomografisk rekonstruksjon av cellulær struktur. Cryo-SXT fyller en nisje når det gjelder prøvedimensjoner og romlig oppløsning som ikke er lett tilgjengelig av noen annen bildeteknikk.
Kort sagt, absorpsjonskontrasten til cryo-SXT er kvantitativ, da dempingen av fotonene gjennom prøven av tykkelse t adlyder Beer-Lambert-loven som følger: 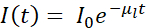 , hvor jeg0 representerer hendelsesintensiteten og μl den lineære absorpsjonskoeffisienten, som avhenger av bølgelengden λ og den imaginære delen β av den brytningsindeksen til prøven (
, hvor jeg0 representerer hendelsesintensiteten og μl den lineære absorpsjonskoeffisienten, som avhenger av bølgelengden λ og den imaginære delen β av den brytningsindeksen til prøven (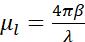 ). Dempingen er en funksjon av den biokjemiske sammensetningen og tykkelsen på strukturene som blir avbildet, med hver biokjemiske komponent som har en bestemt røntgen lineær absorpsjonskoeffisient μl (LAC). Dette betyr at hver tomografi voxel verdi avhenger av de kjemiske elementene og deres konsentrasjon i den voxel7. Dette muliggjør naturlig diskriminering av forskjellige organeller som nuklei, nukleoli, lipidlegemer eller mitokondrier, eller forskjellige komprimeringstilstander av kromatin utelukkende basert på deres iboende LAC-verdier rekonstruert 2,8,9.
). Dempingen er en funksjon av den biokjemiske sammensetningen og tykkelsen på strukturene som blir avbildet, med hver biokjemiske komponent som har en bestemt røntgen lineær absorpsjonskoeffisient μl (LAC). Dette betyr at hver tomografi voxel verdi avhenger av de kjemiske elementene og deres konsentrasjon i den voxel7. Dette muliggjør naturlig diskriminering av forskjellige organeller som nuklei, nukleoli, lipidlegemer eller mitokondrier, eller forskjellige komprimeringstilstander av kromatin utelukkende basert på deres iboende LAC-verdier rekonstruert 2,8,9.
I tillegg er cryo-SXT en høy gjennomstrømningsteknikk med tomogrammer som samles inn på få minutter. Dette muliggjør spesielt mesoskala avbildning av cellepopulasjoner som kan fanges på viktige tidspunkter som divisjon, differensiering og apoptose, men også ved forskjellige responstilstander som de som er indusert av kjemisk eksponering for spesifikke medikamentterapier eller til patogene infeksjoner. Data samlet inn på disse viktige punktene vil levere 3D-beskrivelse av systemet med en trofast oversikt over den romlige organiseringen av de forskjellige cellulære organellene på de spesifikke øyeblikkene.
Vanligvis brukes cryo-SXT i kombinasjon med andre teknikker som følger korrelative tilnærminger som gjør det mulig å finne spesifikke egenskaper, hendelser eller makromolekyler i 3D-cellemiljøet 4,10,11,12,13,14,15,16, eller harde røntgenfluorescensdata 17,18 . Korrelative tilnærminger ved kryogeniske forhold er av avgjørende betydning for å oppnå det mest komplette og verdifulle bildet av interessesystemet. Et kortfattet sammendrag av den typiske arbeidsflyten ved strålelinjene Mistral (Alba) og B24 (Diamond) cryo-SXT er skissert i figur 1.
Videre, ved å dra nytte av bølgelengdejusteringsevnen på synkrotronanlegg, kan spektroskopisk informasjon fås i tillegg til den strukturelle ved hjelp av den spesifikke differensialabsorpsjonen av bestemte elementer som finnes i prøven. Et eksempel på dette ville være plasseringen av kalsium i studiet av biomineraliseringsprosesser i cellene 19,20,21. Ved å ta 2D-bilder på forskjellige fotonenergier (spektra) eller tomogrammer under og ved røntgenabsorpsjonskanten av interesse, kan pikslene eller voxlene som inneholder det valgte elementet identifiseres. Spectra tillater også differensiering av kjemiske tilstander (dvs. utviklingen av amorf kalsium til hydroksyapatitt som i forrige biomineraliseringseksempel20). Kvantifisering av ulike elementer er mulig i 2D og 3D. Spektroskopisk avbildning av vitrifiserte celler gjøres vanligvis i vannvinduet, men er også mulig ved andre energiområder hvis vanninnholdet er lavt nok, eller hvis andre prøveprepareringsprotokoller, inkludert dehydrering, brukes22. En detaljert spektroskopi trinnvis protokoll er utenfor fokuset til protokollen heri.
I det følgende fokuserer protokollen på å kort oppsummere de viktigste prøveforberedelsestrinnene, selv om hvert system kanskje trenger individuell raffinement, etterfulgt av en detaljert trinnvis datainnsamlingsprosedyre for cryo myk røntgentomografi.
Protocol
Representative Results
Discussion
Prøvepreparering er et kritisk skritt for å oppnå myke røntgentomogrammer av høy kvalitet, da kvaliteten deres direkte avhenger av kvaliteten på prøvevistrifiseringen og islagtykkelsen der cellen er innebygd. Projeksjoner med høyt signal-til-støy-forhold vil bli samlet inn i regioner med tynt islag, noe som gjør det mulig å minimere strålingsdosen som kreves for å oppnå høyest mulig oppløsning. I tillegg vil cellesamstrømningen også påvirke den endelige tomogramkvaliteten, siden man bør unngå å ha nærliggende celler som kommer inn i FoV ved rotasjon. Til slutt vil riktig spredning av Au-fiducial markører bestemme nøyaktigheten av projeksjonsjusteringen og deretter til slutt bestemme kvaliteten på det endelige 3D-rekonstruerte volumet. Merk at en riktig spredning av Au-fiducials på rutenettet muliggjør automatisering av projeksjonsjusteringstrinnet, uten hvilken en høy kompetanse er nødvendig for et så kritisk trinn.
Protokollen heri skildrer bare en mulig prøveforberedelsesstrategi, som har likheter med de som brukes i kryoelektrontomografi (cryo-ET). I begge tilfeller vil protokoller som forbedrer den krevende prøveforberedelsen for bedre reproduserbarhet være grunnleggende for suksessen til disse teknikkene, og det arbeides mot dette målet29. Det er verdt å nevne at i tillegg til å avbilde isolerte celler, kan deler av vev også visualiseres forutsatt at overføringssignalet gjennom seksjonen vil være nok i høye vippevinkler. Vanligvis vil dette innebære deler av få mikron (under 10 μm).
Hvis du vil vise en bestemt struktur eller hendelse i en celle, må man kontrollere at denne funksjonen er inne i FoV-en i vippeserien. Siden FoV i cryo-SXT er begrenset til 10 x 10 μm2 til 15 x 15 μm2, avhengig av linsen og står for en pikseloversampling av oppløsningen til minst en faktor på 2, er den ofte mindre enn hele celleutvidelsen (se de røde firkantene angitt i figur 5). Derfor må avkastningen bli funnet og riktig merket. Dette gjøres vanligvis ved hjelp av fluorescerende koder og synlige lyskorrelative tilnærminger. 2D-strategier som kombinerer epifluorescens er enkle ettersom det myke røntgenoverføringsmikroskopet har et integrert on-line synlig lysfluorescensmikroskop, men andre tilnærminger for høyoppløselig 2D- eller 3D-fluorescenssignal er også tilgjengelige 4,12,13,15,16 . I slike tilfeller må nettet først avbildes i spesifikke instrumenter som mikroskoper med superoppløsning. Vær oppmerksom på at de mest effektive korrelative tilnærmingene er de som involverer datainnsamling ved kryogene forhold. Dette er fordi tidsforløpet mellom romtemperatur (RT), synlig lysfluorescensavbildning og prøvevistrifisering, for eksempel, vil hindre å fange riktig cellulær hendelse i tide; I tillegg kan vitrifiseringsprosedyren løsne den interessecellen som er avbildet ved RT fra rutenettet. Selv om de fleste korrelative avbildningsmetoder kan innebære at prøvenettene må manipuleres og transporteres fra det ene instrumentet til det andre, og til tross for den økte risikoen for nettkontaminering eller skade dette utgjør, er belønningen klar: å kunne finne spesifikke hendelser eller molekyler i det cellulære landskapet.
Når hele celleavbildning er nødvendig, er det mulig å sy forskjellige tomogrammer forutsatt at den totale dosen som påføres ikke overstiger strålingsskadegrensen. Vanligvis er den avsatte dosen for å samle få tomogrammer på samme celle godt under grensen ved oppnåelig oppløsning (109 Gy), og derfor er det ikke nødvendig med noen spesifikk strategi for å senke dosen, selv om dette er prøve- og eksperimentavhengig. Ved intensiv datainnsamling som spektrotomografi, vil det faktisk være nødvendig å minimere dosen, og praktisk datainnsamling og spesifikke behandlingsstrategier må brukes.
Cryo-SXT har flere begrensninger, som bør nevnes her. Den første er den velkjente manglende kilen, som er iboende til å bruke flate prøvestøtter. Kapillærprøvestøtter som tillater 180-graders rotasjon har blitt brukt tidligere og brukes fortsatt på noen anlegg, men de presenterer også ulemper som en fattig kontrast på grunn av glassabsorpsjon og begrensningen av å bruke celler i suspensjon. En måte å redusere effekten av den manglende kilen er ved å utføre dobbel tilt tomografi. Dette er faktisk mulig på Mistral-strålelinjen i dag. Den andre begrensningen er satt av Fresnel soneplatelinse som brukes i slike mikroskoper. Denne linsen setter den ultimate oppløsningen oppnåelig og dybdeskarpheten (DoF), som begge er tett beslektet. Dette innebærer at å øke oppløsningen vil redusere DoF mens tykkelsen på cellen ofte vil være større. For eksempel vil en 40 nm linse i teorien ha en DoF på 3 μm og en oppløsning på 24,4 nm halv pitch. Kompromisset mellom oppløsning og DoF er derfor strategisk, og valget av linsen vil avhenge av typen celle30,31. Til slutt er operasjonelle TXMer over hele verden langt fra ideelle mikroskoper, og det arbeides for å forbedre de optiske systemene for å nå de teoretiske forventningene. Til slutt kan visualiseringen og segmenteringen av de rekonstruerte volumene utføres med spesifikke programvareverktøy 25,32,33,34.
Oppsummert tillater cryo-SXT bildeceller kvantitativt ved middels oppløsning (25-30 nm halv tonehøyde) og i statistiske tall (få titalls tomogrammer per dag). Dette gjør det mulig å oppnå organisering, distribusjon og dimensjon av organeller ved bestemte forhold, for eksempel under patogeninfeksjon eller sykdommer, på nøyaktige tidspunkter eller etter bestemte behandlinger. Det er derfor en nyttig komplementær biologisk bildeteknikk til de mer vanlige elektron- og synlige lysmikroskopiene, hver av dem takler et bestemt utvalg av prøvedimensjoner og oppløsning. Cryo-SXT brukes ofte i korrelative tilnærminger som involverer synlig lysfluorescens, men andre kryokorrelative strategier er også mulige.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette prosjektet har fått støtte fra EU-kommisjonens Horisont 2020 iNEXT-Discovery-prosjekt og EUs forsknings- og innovasjonsprogram Horizon 2020 under Marie Skłodowska-Curie-tilskuddsavtalen No 75439.
Materials
| Amira | Thermo Fisher | Software for segmentation | |
| Au Holey Carbon Films finder grids | (Quantifoil Micro Tools Gmb | R 2/2 Au G200F1 | Au Holey Carbon Films finder grids |
| Au nanoparticles | BBI Group, Cardiff, UK | Au nanoparticles 100nm | 100 nm Au nanoparticles (NPs) at Mistral (Alba) |
| Au nanoparticles | BBI Group, Cardiff, UK | Au nanoparticles 250nm | 250 nm Au nanoparticles (NPs) at B24 (Diamond) |
| Axio Scope A1 | Zeiss | 430035 9060 | Fluorescence microscope |
| Blotting No.1 filter paper | Whatman | WHA10010155 | Blotting filter |
| Bsoft | Software for projection alignment, reconstruction and visualization (Heymann et al., 2008) | ||
| Chimera | Software for segmentation (Pettersen et al. 2004) | ||
| Cryo-EM Glow Discharge Set | PELCO easiGlow | 91000S | Glow Discharge Cleaning System |
| Cu Holey Carbon Films finder grids | (Quantifoil Micro Tools Gmb | R 2/2Cu G200F1 | Cu Holey Carbon Films finder grids |
| Fetal calf serum | Sigma | F9665 | Heat Inactivated, sterile-filtered, suitable for cell culture |
| ImageJ | Software for image processing and analysis in Java (NIH & LOCI University of Wisconsin) | ||
| IMOD | Software for projection alignment, reconstruction and visualization (Kremer et al., 1996) | ||
| Leica EM GP Grid Plunger | Leica | 16706401 | Automatic Plunge Freezer EM |
| LINKAM cryo-stage | Linkam Scientific Instruments | CMS 196 | Cryo-Correlative Microscopy Stage |
| MIB | Software for segmentation (Belevich et al. 2016) | ||
| P100 Petri dish | Sigma | P6106 | Treated for cell culture and sterile |
| P60 Petri dish | Sigma | D8054 | Treated for cell culture and sterile |
| Polylysin | Sigma | P4707 | Poly-L-lysine solution 0.01%, sterile-filtered |
| Soft X-Ray microscope 0.25-1.2keV | Xradia | NCT-SB | Transmission soft X-Ray microscope |
| SURVOS | Software for segmentation (Luengo et al. 2017) | ||
| Tomo3d | Software for reconstruction (SIRT, WBP) (Agulleiro et al. 2011) | ||
| TomoJ | Software for reconstruction (ART) (Messaoudi et al., 2007) | ||
| XM Data Explorer | Zeiss | TXM software |
References
- Carrascosa, J. L., et al. Cryo X-ray tomography of vaccinia virus membranes and inner compartments. Journal of Structural Biology. 168, 234-239 (2009).
- Uchida, M., et al. Soft X-ray tomography of phenotypic switching and the cellular response to antifungal peptoids in Candida albicans. PNAS. 106, 19375-19380 (2009).
- Schneider, G., et al. Three-dimensional cellular ultrastructure resolved by X-ray microscopy. Nature Methods. 10, 1-3 (2010).
- Chichón, F. J., et al. Cryo nano-tomography of vaccinia virus infected cells. Journal of Structural Biology. 177, 202-211 (2012).
- Groen, J., Conesa, J. J., Valcárcel, R., Pereiro, E. The cellular landscape by soft X-ray tomography. Biophysical Reviews. 11, 611-619 (2019).
- Kepsutlu, B., et al. Cells undergo major changes in the quantity of cytoplasmic organelles after uptake of gold nanoparticles with biologically relevant surface coatings. ACS Nano. 14, 2248-2264 (2020).
- Natterer, F. . The mathematics of computerized tomography. , (1986).
- Weiss, D., et al. Computed tomography of cryogenic biological specimens based on X-ray microscopic images. Ultramicroscopy. 84, 185-197 (2000).
- Clowney, E. J., et al. Nuclear aggregation of olfactory receptor genes governs their monogenic expression. Cell. 151, 724-737 (2012).
- Duke, E. M. H., et al. Imaging endosomes and autophagosomes in whole mammalian cells using correlative cryo-fluorescence and cryo-soft X-ray microscopy (cryo-CLXM). Ultramicroscopy. 143, 77-87 (2014).
- Cinquin, B., et al. Putting molecules in their place. Journal of Cellular Biochemistry. 115, 209-216 (2014).
- Hagen, C., et al. Multimodal nanoparticles as alignment and correlation markers in fluorescence/soft X-ray cryo-microscopy/tomography of nucleoplasmic reticulum and apoptosis in mammalian cells. Ultramicroscopy. 146, 46-54 (2014).
- Pérez-Berná, A. J., et al. Structural changes in cells images by soft X-ray cryo-tomography during Hepatitis C virus infection. ACS Nano. 10, 6597-6611 (2016).
- Chiappi, M., et al. Cryo-soft X-ray tomography as a quantitative three-dimensional tool to model nanoparticle:cell interaction. Journal of Nanobiotechnology. 14, 15 (2016).
- Varsano, N., et al. Development of correlative cryo-soft X-ray tomography and stochastic reconstruction microscopy. A study of cholesterol crystal early formation in cells. Journal of the American Chemical Society. 138, 14931-14940 (2016).
- Kounatidis, I., et al. Correlative cryo-structured illumination fluorescence microscopy and soft X-ray tomography elucidates reovirus intracellular release pathway. Cell. 182, 1-16 (2020).
- Kapishnikov, S., et al. Mode of action of quinoline antimalarial drugs in red blood cells infected by Plasmodium falciparum revealed in vivo. PNAS. 116 (46), 22946-22952 (2019).
- Conesa, J. J., et al. Unambiguous intracellular localization and quantification of a potent iridium anticancer compound by correlative 3D cryo X-ray imaging. Angewandte Chemie International Edition. 59, 1270-1278 (2020).
- Gal, A., et al. Native-state imaging of calcifying and noncalcifying microalgae reveals similarities in their calcium storage organelles. PNAS. 115 (43), 11000-11005 (2018).
- Procopio, A., et al. Chemical fingerprint of Zn-hydroxyapatite in the early stages of osteogenic differentiation. ACS Central Science. 5, 1449-1460 (2019).
- Kahil, K., et al. Cellular pathways of calcium transport and concentration toward mineral formation in sea urchin larvae. PNAS. 117 (49), 30957-30965 (2020).
- Conesa, J. J., et al. Intracellular nanoparticles mass quantification by near-edge absorption soft X-ray nanotomography. Scientific Reports. 6, 22354 (2016).
- Otón, J., Sorzano, C. O. S., Maribini, R., Pereiro, E., Carazo, J. M. Measurement of the modulation transfer function of an X-ray microscope based on multiple Fourier orders analysis of a Siemens star. Optics Express. 23 (8), 9567-9572 (2015).
- Otón, J., et al. Characterization of transfer function, resolution and depth of field of a soft X-ray microscope applied to tomography enhancement by Wiener deconvolution. Biomedical Optics Express. 7, 5092-5103 (2016).
- Kremer, J. R., Mastronarde, D. N., McIntosh, J. R. Computer visualization of three-dimensional image data using IMOD. Journal of Structural Biology. 116, 71-76 (1996).
- Heymann, J. B., Cardone, G., Winkler, D. C., Steven, A. C. Computational resources for cryo-electron tomography in Bsoft. Journal of Structural Biology. 161, 232-242 (2008).
- Messaoudi, C., et al. Three-dimensional chemical mapping by EFTEM-TomoJ including improvement of SNR by PCA and ART reconstruction of volume by noise supression. Microscopy Microanalysis. 19, 1669-1677 (2013).
- Agulleiro, J. I., Fernández, J. J. Fast tomographic reconstruction on multicore computers. Bioinformatics. 27, 582-583 (2011).
- Toro-Nahuelpan, M., et al. Tailoring cryo-electron microscopy grids by photo-micropatterning for in-cell structural studies. Nature Methods. 17, 50-54 (2020).
- Attwood, D. . Soft X-rays and Extreme Ultraviolet Radiation. Principles and Applications. , (2000).
- Howells, M., Jacobsen, C., Warwick, T. . Principles and Applications of Zone Plate X-ray. Microscopes. Science of Microscopy. , (2007).
- Pettersen, E. F., et al. UCSF Chimera–a visualization system for exploratory research and analysis. Journal of Computational Chemistry. 25, 1605-1612 (2004).
- Belevich, I., Joensuu, M., Kumar, D., Vihinen, H., Jokitalo, E. Microscopy image browser: a platform for segmentation and analysis of multidimensional datasets. PLOS Biology. 14 (1), 1002340 (2016).
- Luengo, I., et al. SuRVoS: Super-region volume segmentation workbench. Journal of Structural Biology. 198, 43-53 (2017).

