Kvantitativa bildanalys in vitro för faragocytos av döda neuroblastomceller av iPSC-makrofager
Summary
Neurodegenerativa sjukdomar är associerade med dysreglerade mikroglia funktioner. Denna artikel beskriver en in vitro-analys av fagocytos av neuroblastomceller av iPSC-makrofager. Kvantitativa mikroskopiavläsningar beskrivs för både livecellig timelapse-avbildning och avbildning med högt innehåll med fast cell.
Abstract
Microglia orkestrera neuroimmuna svar i flera neurodegenerativa sjukdomar, inklusive Parkinsons sjukdom och Alzheimers sjukdom. Microglia rensa upp döda och döende nervceller genom processen av efferocytos, en specialiserad form av fagocytos. Faagocytosfunktionen kan störas av miljömässiga eller genetiska riskfaktorer som påverkar mikroglia. Detta dokument presenterar en snabb och enkel in vitro mikroskopi protokoll för att studera microglial efferocytosis i en inducerad pluripotent stamcell (iPSC) modell av microglia, med hjälp av en mänsklig neuroblastom cellinje (SH-SY5Y) märkt med en pH-känsliga färgämne för phagocytic last. Förfarandet resulterar i ett högt utbyte av döda neuroblastomceller, som visar ytan fosfatidylserin, erkänd som en “äta-mig” signal av fostrater. 96-brunnsplattans analys är lämplig för live-cell time-lapse-avbildning, eller så kan plattan fixas framgångsrikt före vidare bearbetning och kvantifieras genom högkvalitativ mikroskopi. Mikroskopi med högt innehåll med fast cell gör det möjligt att skala upp analysen för screening av små molekylhämmare eller bedöma den fagocytiska funktionen hos genetiska varianter iPSC-linjer. Medan denna analys utvecklades för att studera faagocytos av hela döda neuroblastomceller av iPSC-makrofager, kan analysen enkelt anpassas för andra laster som är relevanta för neurodegenerativa sjukdomar, såsom synaptosomer och myelin, och andra fagocytiska celltyper.
Introduction
Microglia är hjärnvävnad-bosatta makrofager, och deras funktioner inkluderar immunövervakning, samordna inflammatoriska svar på skada / infektion, synaptisk ombyggnad och faagocytos av döda celler, myelin, proteinaggregat och patogener. Faagocytos är den process genom vilken mikroglia känner igen last med ytreceptorer och omorganiserar sitt cytoskeleton för att uppsluka objektet till en fagosom, som sedan smälter samman med lysosomer för nedbrytning av lasten. Friska microglia phagocytose apoptotiska hjärnceller för att ta bort dem innan de blir nekrotiska1. Foscytosen hos apoptotiska celler är också känd som efferocytos, och kräver visning av en fosfatidylserin “äta-mig” signal av den döendecellen 2. Många mikrogliareceptorer binder direkt till fosfatidylserin, inklusive TIM-4, BAI1, Stabilin-2 och TREM2. Mikroglialla TAM-receptorer (t.ex. MERTK) och integrins binder indirekt till fosfatidylserin, med hjälp av tillbehörsproteinerna GAS6 respektive MFG-E8. Andra “eat-me”-signaler kan vara nödvändiga för erkännande av döende celler, dessa inkluderar förändringar i glykosylering eller laddning av ytproteiner; Uttryck av intracellulära proteiner ICAM3, calreticulin, annexin-I vid cellytan. oxiderad LDL; eller beläggning av apoptotisk cell med mikrogliaproducerat komplement C1q1,2.
Neurodegenerativa sjukdomar, inklusive Parkinsons sjukdom, Alzheimers sjukdom, frontotemporal demens och amyotrofisk lateral skleros har associerats med försämring av mikroglia funktion, inklusive en ackumulering av hjärnan avfall produkter såsom döda celler, myelin fragment och protein aggregat, och överdrivna inflammatoriska svar på dessa stimuli3. Faagocytos kan försämras vid neurodegenerativa sjukdomar och bidra till patologin, på grund av en kombination av åldrande, inflammation eller specifika genetiska riskvarianter4,5. Å andra sidan finns det också bevis från djurmodeller av neurodegenerativa sjukdomar att mikroglia kan olämpligt faagocytose livskraftiga nervceller eller synapser6,7,8. Mekanismen kommer sannolikt att initieras av fosfatidylserindisplay av skadade neuriter, som direkt avkänns av mikrogliafostosreceptorer TREM2 eller GPR56, eller indirekt avkäns genom lösligt komplement C1q beläggning fosfatidylserinberikat membran, vilket leder till CR3-medierad fosagocytos9,10,11.
In vitro-analyser av fagocytosfunktion,t.ex.för att bedöma den fenotypiska effekten av en genetisk riskvariant i mikroglia, utförs ofta med icke-fysiologiska laster såsom latexpärlor 4 . Fluorescerande märkta bakterier och zymosan används också, som är fysiologiska men inte relevanta för neurodegenerativa sjukdomar. Icke-fysiologiska farocytiska laster kan användas för att upptäcka defekter i de grundläggande maskinerna för fagocytisk uppslukling men misslyckas med att noggrant modellera det första “erkännande” steget i fagocytos av apoptotiska nervceller. Storleken, formen, styvheten och typen av last dikterar också de intracellulära signalvägarna som aktiveras, vilket leder till olika resultat av mikrogliaaktiveringstillstånd. Till exempel är E.coli-bakterier små och styva, till skillnad från mänskliga celler, och lipopolysackariderna på deras yta känns igen av Toll-liknande receptor 4 (TLR4) som aktiverar faagocytos och proinflammatoriska signalvägar2,12.
I samband med neurodegenerativa sjukdomsstudier skulle en mer relevant fosfacytisk last ha fosfatidylserindisplay på däggdjursplasmamembran, och skulle helst vara mänskliga och neuronala, för att inkludera signaler som mikroglia sannolikt kommer att stöta på. För detta faagocytosprotokoll valdes den mänskliga neuroblastomcelllinjen SH-SY5Y som en neuronmodell som är lätt att odla. Permanent yta fosfatidylserin display inducerades artificiellt av paraformaldehyd, som tidigare har visat sig orsaka fosfatidylserin display av trombocyter13. För mikroglia cell modell mänskliga iPSC-makrofager användes, som efterliknar ontogeny och transkriptionell profil av mänskliga microglia, och är faagocyticallykompetenta 14,15,16,17. iPSC-makrofager är inte den mest autentiska mikrogliamodellen som finns tillgänglig, t.ex. Man kan dock ersätta den med en mer autentisk monokultur iPSC-modell av mikroglia om så önskas, såsom Haenseler et al.15. Mänskliga iPSC-modeller är att föredra framför primära gnagare microglia för att studera neurodegeneration, på grund av oro för den begränsade överlappningen av mikroglia transkriptionsmoduler observeras i mänskliga kontra mus neurodegenerativa sjukdom vävnader18. De döda SH-SY5Ys är färgade med ett syrakänsligt färgämne som fluorescerar svagt vid neutralt pH och starkare inuti fagolysosomerna hos iPSC-makrofager efter fagocytos. Att använda ett syrakänsligt färgämne förbättrar noggrannheten i att upptäcka fagocytiska händelser, med mångsidighet för olika avläsningar av levande och fasta makrofager19. Detta protokoll beskriver både live-cell time-lapse imaging av fagocytos och en fast höginnehåll imaging analys för fagocytos, med samma cell förberedelse steg före avläsning (Figur 1).
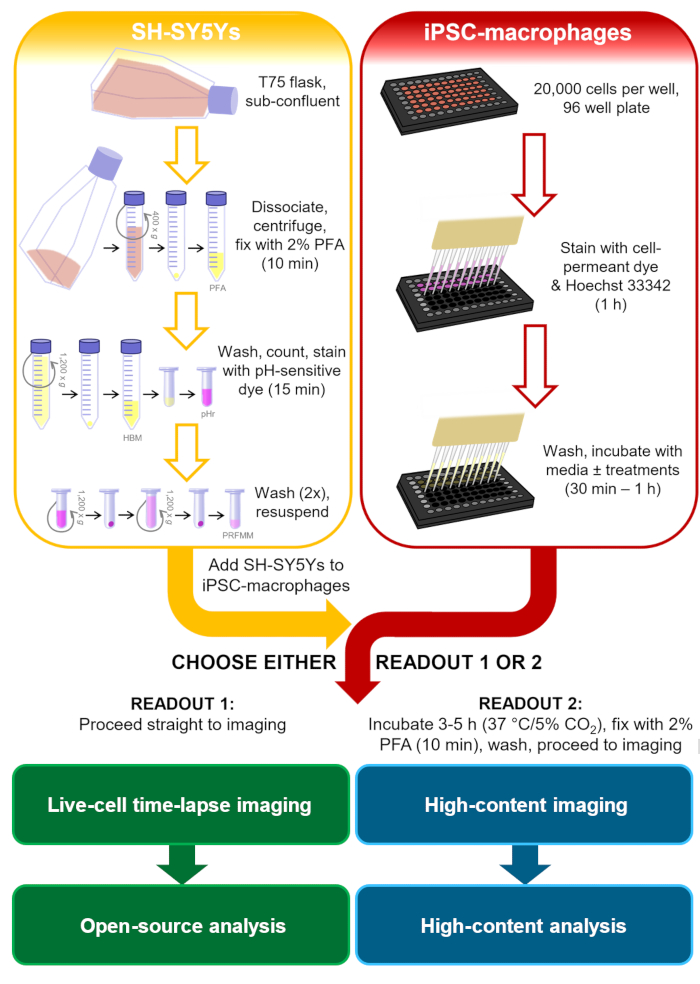
Figur 1: Schematiskt metoddiagram. Kontur av fagocytosanalysen, där beredning av SH-SY5Ys och färgning av iPSC-makrofager utförs parallellt, och sedan SH-SY5Ys pipetted på iPSC-makrofager. Antingen utförs live-cell time-lapse imaging omedelbart, eller cellerna inkuberas vid 37 °C/5% CO2 under den erforderliga varaktigheten och fixeras innan höginnehållsmikroskopi utförs. PFA: paraformaldehyd, HBM: fenol röd-fria HEPES-buffrade medier, pHr: pH-känsliga röda fluorescerande färgämne STP Ester lösning, PRFMM: fenol röd-fria makrofagen massmedia. Klicka här om du vill visa en större version av den här figuren.
Protocol
Representative Results
Discussion
Microglia har viktiga funktioner som påverkar initiering och progression av neurodegenerativa sjukdomar, inklusive fagocytos av apoptotiska nervceller. Nedsatt mikroglial fagocytos och olämplig faagocytos av synapser har båda associerats med neurodegenerativa sjukdomar, även om de underliggande mekanismerna och orsakssambandet inte är väl förstådda4,23. Detta dokument beskriver en faagocytosanalys för att mäta fagocytos av apoptotiska celler med iPSC-makrofager, med antingen en levande cell tid-förfall avbildning av avläsning eller fast-cell höginnehåll mikroskopi, eller en kombination av båda på en enda analys. Denna mångsidighet innebär att analysen kan användas för att studera enskilda farocytiska händelser över tid i några brunnar eller användas för screening med högt innehåll med flera tillstånd eller behandlingar. Eftersom analysen med hög halt är fixerad vid en enda tidpunkt kan flera analysplattor beredas samtidigt. Analysen med högt innehåll har potentiellt nytta för att karakterisera makrofager/mikroglia med sjukdomsrelaterade genetiska varianter eller screening av små molekylhämmare för förändringar i fagocytos. Analysen kan också enkelt anpassas för att studera fagocytos av andra mikrogliamodeller, eller potentiellt astrocyter. Phagocytosis analys kan potentiellt multiplexeras med levande-cell imaging fläckar, t.ex. mitokondrier, kalcium eller ROS indikatorer, och post-fixation immunofluorescent färgning för proteiner av intresse kan utföras. Jämfört med befintliga phagocytosis analyser som använder apoptotiska neuronal celler, de främsta fördelarna som detta protokoll ger är att förberedelse av den phagocytic lasten är relativt enkel och snabb, och resulterar i en enhetlig produkt. Andra analyser inducerar apoptos av nervceller eller SH-SY5Ys med S-nitroso-L-cystein i 2 h25, okadasyra i 3 h22, staurospor för 4-16 h26,27,28,29 eller UV-bestrålning i 24 h30, och kan resultera i celler i olika stadier av apoptos. Dessutom har live-cell imaging och hög innehåll imaging avläsningar inte tidigare beskrivits, såvitt författarna är medvetna om. Den huvudsakliga begränsningen av att använda paraformaldehydfixering för att förbereda den farocytiska lasten är att den inte helt rekapitulerar apoptosprocessen, eftersom fixering förhindrar att cellerna delas upp i apoptotiska kroppar, som sannolikt kommer att faagocytoseras snabbare på grund av deras mindre storlek. Det är inte känt vilken effekt fixering har på utsöndring av nukleotid “hitta mig” signaler (t.ex. ATP, UDP) från målcellen som lockar fagocyter. I likhet med apoptotiska celler uppvisar de fasta SH-SY5Ys vissa membranpermeabilitet till propidiumididid. Membranpermeabilitet är förknippad med frisättningen av “hitta mig” signaler; Detta har dock inte studerats i de fasta SH-SY5Ys, och om nukleotid frigörs för snabbt, skulle de tvättas bort innan SH-SY5Ys läggs till iPSC-makrofager.
Det första kritiska steget i protokollet är färgning av döda SH-SY5Ys med en STP ester av en pH-känslig röd fluorescerande färgämne. Detta färgämne reagerar snabbt och kovaly med fria primära aminer på ytan av de döda SH-SY5Ys. Färgningens varaktighet behöver inte optimeras; Försiktighet måste dock vidtas vid hantering av färgämnet innan märkning. Märkningsreaktionen får inte utföras i buffertar som innehåller fria aminer. Dessutom finns det risk för nederbörd om DMSO-beståndet späds ut i kall vattenbuffert eller vid hög slutlig koncentration. Fällningar visas som täta mörka föremål under mikroskopet. Dessutom fastnar den pH-känsliga färglösningen på vanliga centrifugrör av plast och tvättas långsamt bort; Därför rekommenderas lågbindande rör för märkningssteget. Användning av ett pH-känsligt färgämne, istället för ett permanent fluorescerande färgämne, hjälper identifiering av uppslukade partiklar, jämfört med partiklar som granne plasmamembranet. Eftersom det finns viss fluorescens vid neutralt pH, måste densiteten hos fagocytisk last och iPSC-makrofager hållas tillräckligt låg för noggrann segmentering, även om den är tillräckligt hög för att många phagocytiska händelser fångas. Höginnehåll mikroskopi kunde exakt identifiera faagocytos med en medelhög densitet av last i brunnen (mer än 2 SH-SY5Ys per iPSC-makrofag). Omvänt, på grund av svagare känslighet för mikroskopet i det djupa röda spektrumet, var segmentering av iPSC-makrofager i live-cell time-lapse imaging data mindre säker och det var nödvändigt att använda en mycket låg densitet av last för att minska sannolikheten för falska positiva (1 SH-SY5Y för varannan iPSC-makrofager). Validering av korrekt segmentering och lasttäthet bör utföras med jämförelser mellan obehandlade och cytochalasin D-behandlade brunnar. I en väloptimerad analys bör cytochalasin D minska det genomsnittliga antalet fläckar per cell med 90% i förhållande till obehandlade prover.
Ett annat kritiskt steg i protokollet är iPSC-makrofen färgning, vilket gör att cellen kan identifieras och segmenteras i bild analys så att alla externa SH-SY5Ys utesluts från räkningen. Det rekommenderade färgämnet är cellpermeant, omvandlat till en olöslig fluorescerande produkt i cytoplasman, fixerbar och giftfri (se Materialförteckning ). Färgningssteget optimerades för användning av iPSC-makrofager med den höginnehållsbildande phagocytosanalysen, och vi föreslår att den ska optimeras om andra celltyper används. Varaktigheten av cellfärgning kan ökas för att förbättra nedfallet av den olösliga fluorescerande produkten i celler. Om färgkoncentrationen optimeras bör man vara försiktig så att toxiska halter av det organiska lösningsmedelsfordonet undviks.
Den tredje kritiska faktorn för analysens framgång är dataanalysen. De analyspipeliner som tillhandahålls är avsedda att vara vägledande snarare än normativa, eftersom skillnader i färgningsintensitet eller cellmorfologi kan minska effektiviteten av segmentering av rörledningarna som skrivna. Vissa optimeringar kommer därför att krävas, med testning av pipelinen på lämpliga positiva och negativa kontroller, och de parametrar som ska optimeras anges i protokolltexten. Negativa kontroller bör omfatta ett tillstånd där iPSC-makrofager förbehandlas med en potent fagocytoshämmare såsom cytochalasin D före tillsats av SH-SY5Ys. En annan möjlig negativ kontroll är tillägg av SH-SY5Ys till tidigare obehandlade brunnar av iPSC-makrofager i slutet av analysen, 10 min före fixering, vilket gör det möjligt att lösa lasten men är för kort för att en märkbar mängd fagocytos ska uppstå. En fagocytoshändelse definieras som ett rödfluorescerande objekt inom gränserna för en iPSC-makrofag, definierad av programvarualgoritmen med hjälp av den djupröda fluorescenskanalen. Om segmenteringen av cellerna är dålig (figur 2),kan många icke-faagocytosed SH-SY5Ys i närheten av iPSC-makrofager felaktigt inkluderas i analysen, dvs. falska positiva. Den viktigaste faktorn för att uppnå god segmentering är strikt avgränsning av iPSC-makrofager. Segmentering för båda analyserna är automatiserad, så det är inte möjligt att få perfekt segmentering för varje cell; Några parametrar kan dock justeras för att göra segmenteringen mer optimal, med några testbilder som referens. Cytochalasin D kontroll är viktigt för att bedöma optimal segmentering eftersom ett stort antal phagocytic händelser som detekteras i detta villkor indikerar att segmenteringen är suboptimal. Optimering av dataanalyspipelinen bör helst upprepas tills antalet fagocytiska händelser per cell är 80-90% lägre i cytochalasin D-tillståndet jämfört med ingen hämmare.
De problem med fagocytosanalysen som mest sannolikt uppstår är: (1) svag pH-känslig fluorescens i positiva kontroller, (2) sparse eller ojämn fördelning av makrofager i slutet av analysen, eller (3) högt antal falska positiva i analysen från icke-faagocytosed SH-SY5Ys. Felsökning av svag pH-känslig fluorescens bör först kontrollera att färgning av SH-SY5Ys resulterade i en cellpellets med en stark magentafärg. Om färgen är svag, se till att ett färskt färgämneslager används, se till att märkningsbufferten är amningsfri, tillsätt en extra tvätt till SH-SY5Ys före färgning, kontrollera om rätt antal SH-SY5Ys var färgat, se till att inga färgutfällningar är i bevis och optimera färgämnets märkningskoncentration. Om SH-SY5Ys är starkt färgade, kontrollera om koncentrationen som tillsätts analysplattan är korrekt och se till att iPSC-makrofager är friska och inte för gamla. Den andra typen av problem, ojämn makrofagfördelning, kan bero på förlust av celler under pipetting och åtgärder bör vidtas för att minska de pipettingkrafter som cellerna upplevr, vilket undviker smalborrningsspetsar. Om problemet kvarstår, minska inkubationstiden för att ladda iPSC-makrofager med cellpermeantfärgämne. Det tredje problemet, när det gäller felaktigt införande av icke-faagocytosed partiklar i analysen, indikerar att mer optimering av analyspipelinen krävs. Felsökning bör först fokusera på cellsegmentering och om programvaran innehåller intilliggande objekt. Specifika parametrar som kan justeras föreslås i noterna nedan de relevanta stegen (steg 6.1.11-6.1.15 för livecellsanalysen och steg 6.2.4-6.2.8 för analysen av höginnehåll). Om cellsegmenteringen inte kan förbättras ytterligare har analysen med högt innehåll ett extra steg (steg 6.2.8) som utesluter felaktigt segmenterade iPSC-makrofager. Dessutom kan modulen som filtrerar accepterade fläckar av pH-känslig fluorescens inom iPSC-makrofager optimeras, vilket ökar tröskelvärdets intensitet för accepterade objekt, vilket bör bidra till att utesluta icke-phagocytosed SH-SY5Ys (steg 6.1.17 för live-cell timelapse-analysen och steg 6.2.11 för analysen med högt innehåll).
Vi utvecklade två typer av mikroskopi avläsning för phagocytosis analys att var och en har fördelar och begränsningar. Live-cells timelapse-avbildning har fördelarna med att ge extra information om phagocytos kinetik och är mer allmänt tillgänglig än avbildningsplattformar med högt innehåll. Den rekommenderade programvaran med öppen källkod är agnostisk för mikroskopkällan och kan användas med alla fluorescerande mikroskop av god kvalitet, med eller utan live-cell time-lapse-kapacitet. Den huvudsakliga begränsningen av live-cell imaging är begränsad känslighet och optik, vilket gör det mer utmanande att upptäcka och utföra bra segmentering av iPSC-makrofager. Denna begränsning kan mildras antingen genom att öka varaktigheten för iPSC-makrofingringsfärgning eller genom att växla till ett känsligare mikroskop, om tillgängligt. Den högkvalitativa avbildningsfasen är den rekommenderade avläsningen om ett bildsystem med högt innehåll är tillgängligt. Avbildningssystem med högt innehåll möjliggör högre dataflöde och mer tillförlitliga data, vilket gör det möjligt att använda denna analys för screening, där ett robust Z på ≥0,7 förväntas för “antal fläckar per cell”-utgång 20. Jämfört med livecells timelapse-metoden har den högupplösta mikroskopiavläsningen högre känslighet, högre grad av automatisering och hastighet, fler brunnar och bildfält kan bearbetas och högupplösta konfokala bilder produceras. Cellsegmentering är effektivare med bra bilder, och segmentering underlättas dessutom av programvaran för analys av avbildning med högt innehåll som ger fler cellsegmenteringsmetoder som lämpar sig för mycket oregelbundet formade celler. Programvaran för avbildningsanalys med högt innehåll beräknade också fler parametrar för faagocytos, jämfört med programvaran med öppen källkod, till exempel andelen fagocytiska celler. Den huvudsakliga begränsningen av phagocytostestet med högt innehåll är kostnad och tillgänglighet för bildsystemet och analysprogramvaran.
Sammanfattningsvis är den kvantitativa faagocytosanalysen som presenteras i detta dokument ett användbart verktyg för modellering av mikroglia faagocytos av döda nervceller in vitro. Mikroglia modelleras av iPSC-makrofager och de döda nervcellerna modelleras av paraformaldehyd-fasta SH-SY5Ys. Även om inte de mest autentiska mikroglia och döda / apoptotiska neuronmodeller publicerade, är dessa lätta att förbereda och skalbara. Själva analysen är mycket mångsidig, med två typer av avläsning av avbildningar detaljerade, och den har potential att anpassas för användning med olika mikroglia / makrofag monokulturmodeller, eller en annan celltyp för att fungera som den fagocytiska lasten. Avläsningen med hög innehåll är fördelaktig för att erhålla kvantitativa data och kan skalas upp för att analysera små molekylmodulatorer av fagocytos eller screengenetiska varianter i iPSC-makrofager. Men eftersom avbildningssystem med högt innehåll är dyra och datatunga, har en alternativ avläsning av avbildning inkluderats i protokollet med hjälp av ett live-cells tidsfördröjningsmikroskop, som skulle kunna ersätta alla konventionella fluorescensmikroskop av god kvalitet, om det behövs.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna tackar Dr. Val Millar och Dr. Sohaib Nizami för deras hjälp med högkvalitativ mikroskopi och Dr Daniel Ebner för tillgång till de höginnehållsmikroskopen. Dessutom tackar författarna Dr. Emma Mead för analysutvecklingsråd och Mrs. Cathy Browne för iPSC-stöd. Detta arbete stöddes av Alzheimer’s Research UK Oxford Drug Discovery Institute (ARUK ODDI, grant reference ARUK-2020DDI-OX), med ytterligare stöd till James Martin Stem Cell Facility Oxford (S.A.C.) från Oxford Martin School LC0910-004; Monument Trust Discovery Award från Parkinsons Storbritannien (J-1403); MRC Dementias Platform UK Stem Cell Network Capital Equipment MC_EX_MR/N50192X/1, Partnership MR/N013255/1 och Momentum MC_PC_16034 Awards.
Materials
| 15 mL conical centrifuge tube | Falcon | 352096 | For centrifugation of cells |
| 2-20 µL, 20-200 µL, 100-1000 µL single-channel micropipettes | |||
| 2-mercaptoethanol 50 mM | Gibco | 31350010 | Component of Factory media |
| 4% paraformaldehyde in PBS | Alfa Aesar | J61899 | For fixation of cells |
| 6-well plate, tissue culture treated | |||
| AggreWell-800 24-well plate | STEMCELL Technologies | 34815 | Microwell low-adherence 24-well plate for formation of embryoid bodies |
| Annexin V-FITC Apoptosis Staining / Detection Kit | Abcam | ab14085 | Kit for annexin V-FITC staining , as an assay for quality control of fixed SH-SY5Ys. Kit contains annexin binding buffer, annexin V-FITC, and propidium iodide. |
| Automated cell counter | |||
| Benchtop centrifuge | |||
| Benchtop microcentrifuge | |||
| CellCarrier-96 Ultra Microplates, tissue culture treated, black, 96-well with lid | Perkin Elmer | 6055302 | 96-well tissue culture (TC)-treated microplate with black well walls and an optically-clear bottom, for phagocytosis assay |
| CellProfiler software | Open-source software for analysis of phagocytosis images obtained by live-cell time-lapse microscope. Download for free from website (http://cellprofiler.org/), this protocol used version 2.2.0. | ||
| CellTracker Deep Red dye | Thermo Fisher | C34565 | Deep red-fluorescent, cell-permeant, succinimidyl ester-reactive dye for staining cytoplasm of iPS-macrophages. Dissolve CellTracker Deep Red dye in DMSO to 2 mM (1.4 mg/mL). Use at 1 μM, by dilution of DMSO stock with Macrophage media. |
| Class 2 laminar air flow safety cabinet | |||
| CO2 gas bottle | Accessory for EVOS FL Auto | ||
| CO2 incubator, set to 37°C and 5 % CO2 | |||
| Columbus Image Data Storage and Analysis System | Perkin Elmer | Columbus | Data storage and analysis platform for Opera Phenix. Supports all major high content screening instruments. |
| Cytochalasin D | Cayman | 11330 | Negative control treatment for phagocytosis assay. Reconstitute in DMSO to 10 mM and store aliquots at -20°C, avoid further freeze-thaw cycles. Use at final concentration 10 µM. |
| DMEM/F12 | Gibco | 11320074 | Component of SH-SY5Y media |
| DMSO | Sigma | D8418 | Solvent for CellTracker and pHrodo dyes |
| EVOS FL Auto Imaging System | Thermo Fisher | AMF4300 | Live-cell time-lapse imaging microscope |
| EVOS Light Cube CY5 | Thermo Fisher | AMEP4656 | Accessory for EVOS FL Auto |
| EVOS Light Cube DAPI | Thermo Fisher | AMEP4650 | Accessory for EVOS FL Auto |
| EVOS Light Cube RFP | Thermo Fisher | AMEP4652 | Accessory for EVOS FL Auto |
| EVOS Onstage Incubator | Thermo Fisher | AMC1000 | Accessory for EVOS FL Auto |
| Fetal Bovine Serum | Sigma | F4135 | Component of SH-SY5Y media |
| Flow cytometer | |||
| Flow cytometry analysis software | |||
| Geltrex LDEV-Free, hESC-Qualified, Reduced Growth Factor Basement Membrane Matrix | Invitrogen | A1413302 | hESC-qualified basement membrane matrix for iPSC culture |
| GlutaMAX Supplement | Gibco | 35050-038 | Component of both Factory and Macrophage media |
| HBSS | Lonza | BE 10-547F | Hank’s balanced salt solution for washing steps |
| Human recombinant BMP4 | Gibco | PHC9534 | Component of Embryoid Body media |
| Human recombinant IL-3 | Gibco | PHC0033 | Component of both Factory and Macrophage media |
| Human recombinant SCF | Miltenyi Biotech | 130-096-695 | Component of Embryoid Body media |
| Human recombinant VEGF | Gibco | PHC9394 | Component of Embryoid Body media |
| Live Cell Imaging Solution | Thermo Fisher | A14291DJ | Phenol red-free HEPES-buffered media for labelling dead SH-SY5Ys |
| Low protein binding 2 mL tubes | Eppendorf | 30108.132 | For staining SH-SY5Ys |
| M-CSF | Thermo Fisher | PHC9501 | Component of both Factory and Macrophage media |
| mTeSR1 Medium | STEMCELL Technologies | 85850 | iPSC media |
| Multichannel 20-200 uL pipette | For liquid handling of 96-well plate | ||
| NucBlue Live ReadyProbes Reagent | Thermo Fisher | R37605 | Hoechst 33342 formulation in a dropper bottle for staining nuclei of iPS-macrophages, use 0.5 drops/mL in Macrophage media. |
| Opera Phenix High-Content Screening System | Perkin Elmer | HH14000000 | High-content imaging microscope, used with Harmony software version 4.9. |
| Penicillin-Streptomycin | Gibco | 15140-122 | Component of Factory, Macrophage, and SH-SY5Y media |
| pHrodo iFL Red STP-Ester | Thermo Fisher | P36011 | pH-sensitive red fluorescent dye for labelling dead SH-SY5Ys. Reconstitute pHrodo iFL Red STP Ester powder in DMSO to a 5 mg/mL concentration. For each 1 million SH-SY5Ys, add 2.5 μL (12.5 μg) of pHrodo iFL Red STP Ester stock to pre-warmed cells suspended in Live Cell Imaging Solution. |
| Serological pipette filler | |||
| T175 flask, tissue culture treated | Vessel for differentiations of iPSC-macrophage precursors, known as "Factories" | ||
| T75 flask | Vessel for SH-SY5Y culture | ||
| Transparent plate sealers | Greiner Bio-One | 676001 | For assay plate storage and transportation |
| TrypLE Express (1X), no phenol red | Gibco | 12604013 | Cell dissociation buffer containing recombinant trypsin-like enzymes and 1.1 mM EDTA, use neat. |
| Water bath, set to 37°C | |||
| X-VIVO 15 Medium with L-glutamine, gentamicin, and phenol red | Lonza | BE04-418F | Component of Factory and Macrophage media |
| X-VIVO 15 Medium with L-glutamine; without gentamicin or phenol red | Lonza | 04-744Q | Phenol red-free macrophage media, for use in phagocytosis without additives or growth factors |
References
- Hochreiter-Hufford, A., Ravichandran, K. S. Clearing the dead: apoptotic cell sensing, recognition, engulfment, and digestion. Cold Spring Harbour Perspectives in Biology. 5, 008748 (2013).
- Freeman, S. A., Grinstein, S. Phagocytosis: receptors, signal integration, and the cytoskeleton. Immunological Reviews. 2262, 193-215 (2014).
- Hickman, S., Izzy, S., Sen, P., Morsett, L., El Khoury, J. Microglia in neurodegeneration. Nature Neuroscience. 21 (10), 1359-1369 (2018).
- Galloway, D. A., Phillips, A. E. M., Owen, D. R. J., Moore, C. S. Phagocytosis in the brain: Homeostasis and disease. Frontiers in Immunology. 10, 790 (2019).
- Nizami, S., Hall-Roberts, H., Warrier, S., Cowley, S. A., Di Daniel, E. Microglial inflammation and phagocytosis in Alzheimer’s disease: potential therapeutic targets. British Journal of Pharmacology. 176 (18), 3515-3532 (2019).
- Hong, S., et al. Complement and microglia mediate early synapse loss in Alzheimer mouse models. Science. 352 (6286), 712-716 (2016).
- Neher, J. J., et al. Inhibition of microglial phagocytosis is sufficient to prevent inflammatory neuronal death. The Journal of Immunology. 186 (8), 4973-4983 (2011).
- Brown, G. C., Neher, J. J. Microglial phagocytosis of live neurons. Nature Reviews Neuroscience. 15 (4), 209-216 (2014).
- Scott-Hewitt, N., et al. Local externalization of phosphatidylserine mediates developmental synaptic pruning by microglia. The EMBO Journal. 39 (16), 105380 (2020).
- Li, T., et al. A splicing isoform of GPR56 mediates microglial synaptic refinement via phosphatidylserine binding. The EMBO Journal. 39 (16), 104136 (2020).
- Sapar, M. L., et al. Phosphatidylserine externalization results from and causes neurite degeneration in Drosophila. Cell Reports. 24 (9), 2273-2286 (2018).
- Skjesol, A., et al. The TLR4 adaptor TRAM controls the phagocytosis of Gram-negative bacteria by interacting with the Rab11-family interacting protein 2. PLOS Pathogens. 15 (3), 1007684 (2019).
- Wong, K., Li, X., Ma, Y. Paraformaldehyde induces elevation of intracellular calcium and phosphatidylserine externalization in platelets. Thrombosis Research. 117 (5), 537-542 (2006).
- van Wilgenburg, B., Browne, C., Vowles, J., Cowley, S. A. Efficient, long term production of monocyte-derived macrophages from human pluripotent stem cells under partly-defined and fully-defined conditions. PLoS One. 8 (8), (2013).
- Haenseler, W., et al. A highly efficient human pluripotent stem cell microglia model displays a neuronal-co-culture-specific expression profile and inflammatory response. Stem Cell Reports. 8 (6), 1727-1742 (2017).
- Buchrieser, J., James, W., Moore, M. D. Human induced pluripotent stem cell-derived macrophages share ontogeny with MYB-independent tissue-resident macrophages. Stem Cell Reports. 8 (2), 334-345 (2017).
- Hall-Roberts, H., et al. TREM2 Alzheimer’s variant R47H causes similar transcriptional dysregulation to knockout, yet only subtle functional phenotypes in human iPSC-derived macrophages. Alzheimer’s Research & Therapy. 12, 151 (2020).
- Friedman, B. A., et al. Diverse brain myeloid expression profiles reveal distinct microglial activation states and aspects of Alzheimer’s disease not evident in mouse models. Cell Reports. 22 (3), 832-847 (2018).
- Aziz, M., Yang, W. L., Wang, P. Measurement of phagocytic engulfment of apoptotic cells by macrophages using pHrodo succinimidyl ester. Current Protocols in Immunology. 100, 1-8 (2013).
- Atmaramani, R., Pancrazio, J. J., Black, B. J. Adaptation of robust Z’ factor for assay quality assessment in microelectrode array based screening using adult dorsal root ganglion neurons. Journal of Neuroscience Methods. 339, 108699 (2020).
- Fernandes, H. J. R., et al. ER Stress and Autophagic Perturbations Lead to Elevated Extracellular α-Synuclein in GBA-N370S Parkinson’s iPSC-Derived Dopamine Neurons. Stem Cell Reports. 6 (3), 342-356 (2016).
- Takahashi, K., Rochford, C. D. P., Neumann, H. Clearance of apoptotic neurons without inflammation by microglial triggering receptor expressed on myeloid cells-2. Journal of Experimental Medicine. 201 (4), 647-657 (2005).
- Kober, D. L., Brett, T. J. TREM2-ligand interactions in health and disease. Journal of Molecular Biology. 429 (11), 1607-1629 (2017).
- Hong, S., et al. Complement and microglia mediate early synapse loss in Alzheimer mouse models. Science. 352 (6286), 712-716 (2016).
- Witting, A., Müller, P., Herrmann, A., Kettenmann, H., Nolte, C. Phagocytic clearance of apoptotic neurons by microglia/brain macrophages in vitro: Involvement of lectin-, integrin-, and phosphatidylserine-mediated recognition. Journal of Neurochemistry. 75 (3), 1060-1070 (2000).
- Hsieh, C. L., et al. A role for TREM2 ligands in the phagocytosis of apoptotic neuronal cells by microglia. Journal of Neurochemistry. 109 (4), 1144-1156 (2009).
- Beccari, S., Diaz-Aparicio, I., Sierra, A. Quantifying microglial phagocytosis of apoptotic cells in the brain in health and disease. Current Protocols in Immunology. 122 (1), 49 (2018).
- Diaz-Aparicio, I., et al. Microglia actively remodel adult hippocampal neurogenesis through the phagocytosis secretome. Journal of Neuroscience. 40 (7), 1453-1482 (2020).
- Shirotani, K., et al. Aminophospholipids are signal-transducing TREM2 ligands on apoptotic cells. Scientific Reports. 9 (1), 1-9 (2019).
- Garcia-Reitboeck, P., et al. Human induced pluripotent stem cell-derived microglia-like cells harboring TREM2 missense mutations show specific deficits in phagocytosis. Cell Reports. 24 (9), 2300-2311 (2018).

