Enkelt partikel kryo-elektronmikroskopi: Fra prøve til struktur
Summary
Strukturbestemmelse af makromolekylære komplekser ved hjælp af kryoEM er blevet rutine for visse klasser af proteiner og komplekser. Her opsummeres denne pipeline (prøveforberedelse, screening, dataindsamling og -behandling), og læserne er rettet mod yderligere detaljerede ressourcer og variabler, der kan ændres i tilfælde af mere udfordrende prøver.
Abstract
Kryo-elektronmikroskopi (cryoEM) er en kraftfuld teknik til strukturbestemmelse af makromolekylære komplekser via enkelt partikelanalyse (SPA). Den samlede proces indebærer i) vitrifying prøven i en tynd film understøttes på en cryoEM gitter; ii) screening af prøven for at vurdere partikelfordelingen og iskvaliteten iii) hvis nettet er egnet, indsamling af et enkelt partikeldatasæt til analyse og iv) billedbehandling for at give et EM-tæthedskort. I denne protokol findes der en oversigt over hvert af disse trin med fokus på de variabler, som en bruger kan ændre under arbejdsprocessen, og fejlfinding af almindelige problemer. Med fjernmikroskopdrift, der bliver standard i mange faciliteter, vil variationer på billeddiagnostiske protokoller for at hjælpe brugerne med effektiv drift og billeddannelse, når den fysiske adgang til mikroskopet er begrænset, blive beskrevet.
Introduction
Enkelt partikel CryoEM
For at undersøge livet på molekylært niveau må vi forstå struktur. Mange teknikker til sondeproteinstruktur er tilgængelige, såsom NMR, røntgenkrystallografi, massespektrometri og elektronmikroskopi (EM). Til dato er de fleste strukturer deponeret til Protein Databank (FBF) blevet løst ved hjælp af røntgenkrystallografi. Men fra ~ 2012 og fremefter blev kryo-elektronmikroskopi (cryoEM) en mainstream-teknik til bestemmelse af proteinstruktur, og brugen af den steg dramatisk. Det samlede antal EM-kort, der blev deponeret i Electron Microscopy Databank (EMDB) (pr. december 2020), var 13.421 sammenlignet med 1.566 i 2012 (figur 1, www.ebi.co.uk). I 2012 var antallet af atomkoordinater modelleret i kryoEM-tæthedskort, deponeret til FBF, kun 67, men fra december 2020 er der indtil videre deponeret 2.309 strukturer, en 35-dobling. Denne underliggende vækst i kvaliteten og kvantiteten af de producerede kryoEM-tæthedskort, undertiden benævnt »resolutionsrevolutionen«1, skyldtes en sammenkrødning af fremskridt på flere områder: udvikling af nye kameraer til billedbehandling, såkaldte direkte elektrondetektorer; ny software; og mere stabile mikroskoper2,3,4.
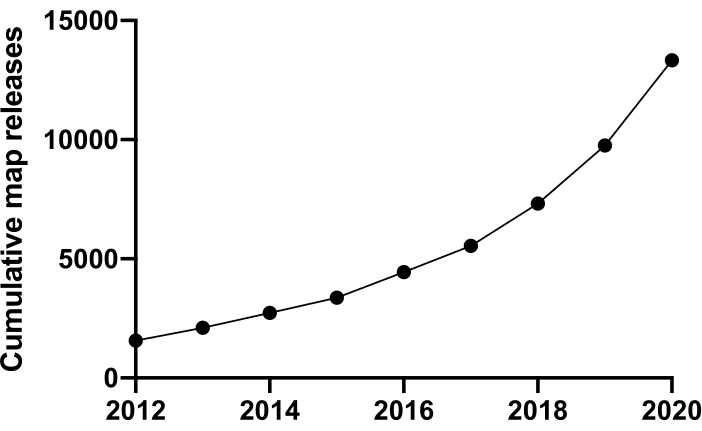
Figur 1: Kumulative indsendelser til EMDB fra 2012 til december 2020. Klik her for at se en større version af dette tal.
Enkelt partikelanalyse (SPA) er et kraftfuldt værktøj til at generere biologisk indsigt i en lang række prøvetyper ved at belyse strukturer med høj opløsning af isolerede komplekser5,6, herunder vira7,8, membranproteiner9,10, spiralformede samlinger11 og andre dynamiske og heterogene makromolekskulære komplekser12,13, hvis størrelser varierer efter størrelsesordener (fra 39 kDa 14,15 til snesevis af megadaltons). Her beskrives en protokol for en standardrørledning til cryoEM SPA fra prøve til struktur.
Inden denne rørledning påbegyndes, bør en renset prøve underkastes biokemisk analyse for at vurdere dens chancer for downstream-succes. Forberedelse af en egnet prøve er uden tvivl den største hindring for SBO, især for forbigående og heterogene (både kompositoriske og kropslige) komplekser. Det makromolekylære komplekse præparat skal indeholde så få forurenende stoffer som muligt, i tilstrækkelig koncentration til at give mange partikler i hver kryoEM-mikrograf og i en buffersammensætning, der er velegnet til kryoEM-analyse. Visse bufferkomponenter, herunder saccharose, glycerol og høje (~> 350 mM saltkoncentrationer, afhængigt af prøvestørrelse, egenskaber og andre bufferkomponenter), kan forstyrre vitrificeringsprocessen eller reducere signal-til-støj-forholdet i billeder, hvilket hindrer strukturbestemmelse16.
Typisk, som et minimum, størrelse udelukkelse kromatografi (SEC) og SDS-PAGE gel analyse bør anvendes til at vurdere prøve renhed17,18, men cirkulær dichroisme, funktionelle assays, SEC kombineret med multi-vinkel lys spredning, og termisk stabilitet assays er alle nyttige værktøjer til kvalitativ analyse af makromolektære komplekse præparater forud for kryoEM analyse. Resultaterne fra disse biokemiske analyser giver dog kun ringe indsigt i prøvens strukturelle heterogenitet og dens adfærd på et kryoemgitter. Af denne grund bruges negativ plet EM rutinemæssigt som et hurtigt, billigt og kraftfuldt værktøj til vurdering af kompositorisk og kropslig heterogenitet, og derfor er en god måde at fastslå, hvilken elutionsfraktion fra en rensning der er mest lovende, eller screening af forskellige buffersammensætninger19,20. Når en lovende prøve er blevet identificeret, kan vi gå videre til SPA cryoEM rørledningen. Negativ plet er ikke altid i overensstemmelse med de efterfølgende resultater, der ses i cryoEM; nogle gange ser en prøve dårlig ud af negativ plet, men forbedres, når den ses i glasagtig is i kryoEM. I modsætning hertil ser nogle gange prøver fremragende ud under negative plettrin, men kræver betydelig yderligere optimering, når de udvikler sig til cryoEM. Men i de fleste tilfælde giver negativ plet et nyttigt kvalitetskontroltrin.
Forglasning
Det barske miljø i elektronmikroskopets vakuumsystem forårsager både dehydrering og strålingsskader på faste biologiske prøver21. For at afbilde prøven i en oprindelig tilstand skal den biologiske prøve derfor bevares før billeddannelse. For rensede præparater af makromolekylære komplekser er vitrificering den foretrukne metode til at muliggøre dens visualisering ved cryoEM, samtidig med at kompleksets atomdetaljer bevares. Opdagelsen af vitrifikation som en metode til prøvepræparat var et grundlæggende fremskridt inden for elektronmikroskopi af biologiske prøver, for hvilken Dubochet blev anerkendt i Nobelprisen i kemi i 2017. Prøve vitrifikation indebærer at skabe et tyndt lag af opløsning, der indeholder prøven af interesse, typisk snesevis af nm tyk, suspenderet på en cryoEM gitter støtte. Den tynde film fryses derefter ekstremt hurtigt i en cryogen som flydende ethan ved ~ -175 °C. Frysehastigheden er ~ 106 ° C / s, hurtig nok til, at amorf eller glasøs is dannes, suspendere prøven i en tynd, solid film22.
Den oprindelige variabel til at overveje, er cryoEM gitter støtte valgt23. Et EM-gitter består typisk af en amorf carbonfilm med perforeringer (enten almindelige eller uregelmæssige) over en støttestruktur. Støttestrukturen er typisk et cirkulært metalgitter med en diameter på 3,05 mm, normalt fremstillet af kobber, men andre metaller som guld eller molybdæn (som har foretrukket termiske ekspansionsegenskaber24) kan anvendes. Nogle gange påføres en ekstra tynd, kontinuerlig støtte på tværs af gitteret, såsom grafen, grafenoxid eller et tyndt (~ 1-2 nm) amorf kulstoflag. Mens standard kryoEM gitre (oftest 400-200 mesh kobber med en perforeret (1,2 μm runde huller adskilt af 1,3 μm (r1.2/1.3), eller 2 μm adskilt af 2 μm kulstof (r2/2)) kulstof støtte- selv om mange forskellige mønstre er tilgængelige) er blevet anvendt i langt de fleste strukturer rapporteret til dato, nettet nye teknologier med forbedret ledningsevne og reduceret prøvebevægelse er blevet rapporteret25 . Udvalgte gitre udsættes for en glow-udledning/plasmarensningsbehandling for at gøre dem hydrofile og modtagelige for prøveudbringning26.
Efter glød-udledning, den næste fase er tynd film dannelse. Denne tynde film er mest almindeligt dannet ved hjælp af filterpapir til at fjerne overskydende væske fra nettet. Mens dette kan udføres manuelt, en række springet frysning enheder er kommercielt tilgængelige, herunder Vitrobot Mk IV (Thermo Fisher Scientific), EM GP II (Leica) og CP3 (Gatan). Med disse enheder påføres ~3-5 μL prøve i opløsning på EM-gitteret, efterfulgt af blotting væk overskydende opløsning ved hjælp af filterpapir. Gitteret, med en tynd film suspenderet på tværs af det, er derefter kastet i flydende ethan afkølet af flydende nitrogen (LN2) til ~ -175 °C. Når nettet er frosset, holdes det ved en temperatur under devitrifikationspunktet (-137 °C) før og under billeddannelse.
Prøvescreening og dataindsamling
Efter vitrificering af et kryoEM-gitter er næste fase at screene nettet for at vurdere dets kvalitet og afgøre, om nettet er egnet til at fortsætte med dataindsamling i høj opløsning. Et ideelt kryoEM gitter har glasagtig is (i modsætning til krystallinsk is) med istykkelsen lige tilstrækkelig til at rumme den længste dimension af prøven, hvilket sikrer, at den omgivende is bidrager med så lidt støj til det resulterende billede som muligt. Partiklerne i isen skal have en størrelse og (hvis kendt) form i overensstemmelse med biokemi, og ideelt set være monodisperse med en tilfældig fordeling af partikel orienteringer. Endelig bør nettet have tilstrækkeligt mange områder af tilstrækkelig kvalitet til at opfylde den ønskede dataindsamlingslængde. Afhængigt af prøven kan dette tage mange gentagelser af vitrifikation og screening, indtil der produceres optimale gitre. Både heldigvis og desværre er der et stort udvalg af variabler, der kan empirisk testes for at ændre partikelfordelingen på kryoEM-gitre (gennemgået i16,27). I dette manuskript vises repræsentative resultater for et membranproteinprojekt10.
Når et passende gitter er blevet identificeret, kan dataindsamlingen fortsætte. Flere modeller af kryo-transmission elektronmikroskoper til biologiske prøver er optimeret til at indsamle data med høj opløsning på en automatiseret måde. Typisk indsamles data på 300 kV- eller 200 kV-systemer. Automatiseret dataindsamling kan opnås ved hjælp af software, herunder EPU (Thermo Fisher Scientific)28, Leginon29, JADAS30 og SerialEM31,32. En automatiseret dataindsamling med moderne detektorer resulterer typisk i terabyte (TB) af rå data i en 24 timers periode (gennemsnitlige datasæt er ~ 4 TB i størrelse).
På grund af covid-19-restriktionerne i store dele af verden (skrivetid december 2020) er mange mikroskopifaciliteter flyttet til at tilbyde fjernadgang. Når gitrene er blevet indlæst i autoloaderen af et mikroskop, kan dataindsamling udføres eksternt.
Billedbehandling og modelbygning
Hvis en dataindsamlingssession typisk kan være 0,5-4 dage, kan efterfølgende billedbehandling tage mange uger og måneder, afhængigt af tilgængeligheden af computerressourcer. Det er standard for indledende billedbehandling trin, nemlig bevægelse korrektion og kontrast overførsel funktion (CTF) skøn til at finde sted ‘on the fly’ 33,34. Til downstream-behandling er der en overflod af softwarepakker til rådighed. Partikler ‘plukkes’ og udvindes af mikrografer35,36. Når partikler er ekstraheret, en standard protokol ville være at behandle partiklerne gennem flere runder af klassificering (i begge to dimensioner (2D) og tre dimensioner (3D) og / eller fokuseret på specifikke regioner af interesse) for at nå en homogen delmængde af partikler. Denne homogene delmængde af partikler er derefter gennemsnit sammen for at producere en 3D-rekonstruktion. På dette tidspunkt korrigeres data ofte yderligere for at producere det højest mulige kvalitetskort, for eksempel gennem CTF-raffinement, distortionkorrektioner37 og bayesisk polering38 . Resultatet af denne billedbehandling er et 3D cryoEM-kort over den biologiske prøve af interesse. Opløsningsområdet, der nås i et ‘standard’ automatiseret enkeltpartikeleksperiment fra et gitter af tilstrækkelig kvalitet, med data indsamlet på et 300 kV mikroskopsystem er typisk mellem 10 Å og 2 Å afhængigt af proteinkompleksets størrelse og fleksibilitet. Med en ideel prøve er opløsninger på ~ 1,2 Å nu nået ved hjælp af SPA-arbejdsgange5. Mens denne protokol detaljer skridt i retning af at opnå en EM tæthed kort, når dette er i hånden det kan fortolkes yderligere ved montering og raffinering af en protein model (hvis opløsningen er < 3,5 Å) eller building de novo39. Data i forbindelse med strukturbestemmelseseksperimenter kan deponeres i online offentlige depoter, herunder EM-tæthedskort (Electron Microscopy Data Bank)40, deraf følgende atomkoordinater (Protein Data Bank)41 og rå datasæt (Electron Microscopy Public Image Archive)42.
I denne protokol bruges det ydre membranproteinkompleks RagAB (~340 kDa) fra Porphyromonas gingivalis som et eksempel på makromolekylær kompleks10 (EMPIAR-10543). For de nye til cryoEM, støtte til prøver gennem denne rørledning fra prøve til struktur er tilgængelig, med forbehold for peer review, gennem finansierede adgangsordninger såsom iNEXT Discovery og Instruct.
Protocol
Representative Results
Discussion
I denne protokol har vi beskrevet en grundlæggende rørledning, der gælder for prøver, der kan bruges til rutinemæssige SBO’er. Mens dette filter papir blotting metode til tynd film dannelse og vitrification er utvivlsomt en succes i betragtning af dens anvendelse i langt de fleste SPA-projekter til dato, det kommer med en række ulemper. Disse omfatter prøvespild, de langsomme tidsskalaer (sekunder), der kræves for at danne den tynde film og fryse prøven, rapporterede uudholdelighed27 og rapporterede negative virkninger af at bruge filterpapir til at fjerne overskydende væske50. For nylig er der udviklet nye teknologier for at forbedre reproducerbarheden af tyndfilmsproduktion51,52. Der er udviklet andre teknologier, som reducerer tiden mellem prøveudbringning og vitrificering53,54,55. Mens filter papir-baserede metoder til tynd film dannelse fortsat mest allestedsnærværende metode til SPA cryoEM prøve forberedelse i skrivende stund, kan disse nye teknologier bringe en række fordele med hensyn til effektivitet og reproducerbarhed af nettet vitrification, samt skabe nye muligheder for at bringe i yderligere eksperimentelle dimensioner, såsom tidsopløsning og hurtig blanding forud for vitrification.
Processen med netscreening for de fleste brugere er i øjeblikket en kvalitativ proces, der indebærer erhvervelse af lave forstørrelsesatlaser efterfulgt af at tage billeder med høj forstørrelse på tværs af nettet for at vurdere partikelfordelingen. Selv om dette er en tilstrækkelig robust tilgang til nogle typer af prøve, kan det være svært at vurdere med øjet, hvis prøven er faktisk, hvad forskeren håber at billede eller har en foretrukken orientering, for eksempel med små (<200 kDa) prøver, eller hvor lav opløsning morfologi gør det svært at identificere ved øjet, hvis en række partikelfordelinger er til stede. For nogle projekter er det umuligt at afgøre, om prøven er som ønsket, f.eks. når en ligand er bundet, eller hvor prøven screenes for at vurdere, om en lille (f.eks. 10 kDa) underenhed stadig er til stede i forbindelse med et kompleks. For disse projekter vil fuldautomatiske pipelines til dataanalyse kombineret med en "kort" 0,5 – 1-h samlinger, der kan fortsætte gennem billedbehandling trin til 2D-klassificering eller endda 3D-klassificering og raffinement hjælpe effektivt med at afgøre, om en længere samling er berettiget. Disse rørledninger er stadig under udvikling og er ikke almindeligt implementeret i øjeblikket, men de har potentiale til at forbedre effektiviteten af cryoEM-netscreening, især for udfordrende prøver.
Forbedringer i direkte elektrondetektorer samt ændringer i mikroskopi kombineret med fremskridt inden for billedbehandling såsom indsamling af billedskiftdata har øget gennemløbet og kvaliteten af billeder, der produceres under dataindsamling. Denne stigning i antallet af data, der indsamles, understreger behovet for en grundig screening af kryoEM-net forud for mange TB data, der indsamles.
CryoEM SPA er blevet en virkelig mainstream strukturel biologi teknik, og i mange tilfælde ‘gå til’ tilgang for nogle klasser af prøver, såsom heterogene og labile makromolekylær komplekser. Mens protokollen her beskriver en grundlæggende oversigt over SPA-rørledningen, er hvert afsnit, der er dækket her (gittervitrificering og screening, cryoEM og billedbehandling) et emne i sig selv og værd at udforske under udviklingen af et SPA-projekt. Efterhånden som prøveforberedelses- og mikroskopiteknologier skrider frem, og nye algoritmer og tilgange til billedbehandling kommer online, vil SPA fortsætte med at udvikle sig som en pipeline, der hjælper forskere med at få indsigt i komplekse biologiske systemer.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbejde blev støttet af iNEXT-Discovery (Grant 871037), der blev finansieret af Horizon 2020-programmet fra Europa-Kommissionen. J B. R. White er finansieret af Wellcome Trust (215064/Z/18/Z). FEI Titan Krios mikroskoper blev finansieret af University of Leeds (UoL ABSL award) og Wellcome Trust (108466 / Z / 15 / Z). Vi takker M Iadanza for brugen af hans mikrograf analyse script. Vi anerkender Diamond Light Source for adgang til og støtte af cryo-EM faciliteter på Storbritanniens nationale Electron Bio-imaging Center (eBIC) finansieret af Wellcome Trust, MRC og BBRSC.
Materials
| Blunt tweezers | Agar Scientific | AGT5022 | |
| Cryo EM round storage box | Agar Scientific | AGG3736 | |
| CryoEM autogrid boxes | ThermoFisher Scientific | 1084591 | |
| CryoEM grids | Quantifoil | N1-C14nCu30-01 | |
| Ethane gas | Boc | 270595-F | |
| LN2 foam dewar | Agar Scientific | AG81760-500 | |
| LN2 storage dewar | Worthington industries | HC 34 | |
| Pipette | Gilson | 10082012 | |
| Pipette tips | Star labs | s1111-1706 | |
| Syringe | BD | BD 300869 | |
| Type II lab water | Suez | select fusion | |
| Vitrobot | ThermoFisher Scientific | 1086439 | |
| Vitrobot filter paper | Whatman | 1001-055 | |
| Vitrobot styrophome container assembly | ThermoFisher Scientific | 1086439 | |
| Vitrobot tweesers | ThermoFisher Scientific | 72882-D | |
| Software | |||
| EPU | ThermoFisher Scientific | 2.8.1.10REL | |
| TEM server | ThermoFisher Scientific | 6.15.3.22415REL | |
| Tia | ThermoFisher Scientific | 5.0.0.2896REL | |
| Titan krios microscope | ThermoFisher Scientific | Titan Krios G2 |
References
- Kuehlbrandt, W. The Resolution Revolution. Science. 343 (6178), 1443-1444 (2014).
- McMullan, G., Faruqi, A. R., Henderson, R. Direct Electron Detectors. Methods in Enzymology. , (2016).
- Elmlund, D., Le, S. N., Elmlund, H. High-resolution cryo-EM: the nuts and bolts. Current Opinion in Structural Biology. , (2017).
- Lyumkis, D. Challenges and opportunities in cryo-EM single-particle analysis. Journal of Biological Chemistry. , (2019).
- Nakane, T., et al. Single-particle cryo-EM at atomic resolution. Nature. , (2020).
- Yip, K. M., Fischer, N., Paknia, E., Chari, A., Stark, H. Atomic-resolution protein structure determination by cryo-EM. Nature. , (2020).
- Conley, M. J., et al. Calicivirus VP2 forms a portal-like assembly following receptor engagement. Nature. 565 (7739), 377-381 (2019).
- Hesketh, E. L., et al. The 3.3 Å structure of a plant geminivirus using cryo-EM. Nature communications. 9 (1), 2369 (2018).
- Malone, L. A., et al. Cryo-EM structure of the spinach cytochrome b6 f complex at 3.6 A resolution. Nature. 575 (7783), 535-539 (2019).
- Madej, M., et al. Structural and functional insights into oligopeptide acquisition by the RagAB transporter from Porphyromonas gingivalis. Nature Microbiology. , (2020).
- Gallardo, R., et al. Fibril structures of diabetes-related amylin variants reveal a basis for surface-templated assembly. Nature Structural and Molecular Biology. , (2020).
- Scarff, C., et al. Structure of the shutdown state of myosin-2. Nature. , (2020).
- Scarff, C. A., et al. Structure of the protective nematode protease complex H-gal-GP and its conservation across roundworm parasites. PLoS Pathogens. 16 (4), 1008465 (2020).
- Wu, M., Lander, G. C. How low can we go? Structure determination of small biological complexes using single-particle cryo-EM. Current Opinion in Structural Biology. , (2020).
- Khoshouei, M., Radjainia, M., Baumeister, W., Danev, R. Cryo-EM structure of haemoglobin at 3.2 Å determined with the Volta phase plate. Nature Communications. , (2017).
- Drulyte, I., et al. Approaches to altering particle distributions in cryo-electron microscopy sample preparation. Acta crystallographica. Section D, Structural biology. 74, 560-571 (2018).
- Thompson, R. F., Walker, M., Siebert, C. A., Muench, S. P., Ranson, N. A. An introduction to sample preparation and imaging by cryo-electron microscopy for structural biology. Methods. 100, 3-15 (2016).
- Cheng, Y., Grigorieff, N., Penczek, P. A., Walz, T. A primer to single-particle cryo-electron microscopy. Cell. 161 (3), 438-449 (2015).
- Scarff, C. A., Fuller, M. J. G., Thompson, R. F., Iadanza, M. G. Variations on negative stain electron microscopy methods: tools for tackling challenging systems. Journal of Visualized Experiments. (132), e57199 (2018).
- Ohi, M., Li, Y., Cheng, Y., Walz, T. Negative Staining and Image Classification – Powerful Tools in Modern Electron Microscopy. Biological procedures online. 6, 23-34 (2004).
- Baker, L. A., Rubinstein, J. L. Radiation Damage in Electron Cryomicroscopy. Methods in enzymology. 481, 371-388 (2010).
- Dubochet, J., et al. Cryo-electron microscopy of vitrified specimens. Quarterly Reviews of Biophysics. 21 (02), 129-228 (1988).
- Passmore, L. A., Russo, C. J. Specimen Preparation for High-Resolution Cryo-EM. Methods in enzymology. 579, 51-86 (2016).
- Carragher, B., et al. Current outcomes when optimizing ‘standard’ sample preparation for single-particle cryo-EM. Journal of Microscopy. , (2019).
- Naydenova, K., Jia, P., Russo, C. J. Cryo-EM with sub-1 Å specimen movement. Science. , (2020).
- Passmore, L. A., Russo, C. J. Specimen Preparation for High-Resolution Cryo-EM. Methods in Enzymology. , (2016).
- Thompson, R. F., Iadanza, M. G., Hesketh, E. L., Rawson, S., Ranson, N. A. Collection, pre-processing and on-the-fly analysis of data for high-resolution, single-particle cryo-electron microscopy. Nature protocols. 14 (1), 100-118 (2019).
- Suloway, C., et al. Automated molecular microscopy: the new Leginon system. Journal of Structural Biology. 151 (1), 41-60 (2005).
- Zhang, J., et al. JADAS: A customizable automated data acquisition system and its application to ice-embedded single particles. Journal of Structural Biology. , (2009).
- Mastronarde, D. N. SerialEM: A program for automated tilt series acquisition on Tecnai microscopes using prediction of specimen position. Microscopy and Microanalysis. , (2003).
- Schorb, M., Haberbosch, I., Hagen, W. J. H., Schwab, Y., Mastronarde, D. N. Software tools for automated transmission electron microscopy. Nature Methods. , (2019).
- Fernandez-Leiro, R., Scheres, S. H. W. A pipeline approach to single-particle processing in RELION. Acta crystallographica. Section D, Structural biology. 73, 496-502 (2017).
- Gómez-Blanco, J., et al. Using Scipion for stream image processing at Cryo-EM facilities. Journal of Structural Biology. , (2018).
- Wagner, T., et al. SPHIRE-crYOLO is a fast and accurate fully automated particle picker for cryo-EM. Communications biology. 2 (1), 213-218 (2019).
- Bepler, T., et al. TOPAZ: A Positive-Unlabeled Convolutional Neural Network CryoEM Particle Picker that can Pick Any Size and Shape Particle. Microscopy and Microanalysis. , (2019).
- Zivanov, J., et al. New tools for automated high-resolution cryo-EM structure determination in RELION-3. eLife. 7, 163 (2018).
- Zivanov, J., Nakane, T., Scheres, S. H. W. A Bayesian approach to beam-induced motion correction in cryo-EM single-particle analysis. IUCrJ. , (2019).
- Cianfrocco, M. A., Kellogg, E. H. What Could Go Wrong? A Practical Guide to Single-Particle Cryo-EM: From Biochemistry to Atomic Models. Journal of Chemical Information and Modeling. , (2020).
- Tagari, M., Newman, R., Chagoyen, M., Carazo, J. M., Henrick, K. New electron microscopy database and deposition system. Trends in Biochemical Sciences. , (2002).
- Berman, H. M., et al. The Protein Data Bank. Nucleic Acids Research. , (2000).
- Iudin, A., Korir, P. K., Salavert-Torres, J., Kleywegt, G. J., Patwardhan, A. EMPIAR: A public archive for raw electron microscopy image data. Nature Methods. , (2016).
- Punjani, A., Rubinstein, J. L., Fleet, D. J., Brubaker, M. A. CryoSPARC: Algorithms for rapid unsupervised cryo-EM structure determination. Nature Methods. , (2017).
- Tegunov, D., Cramer, P. Real-time cryo-electron microscopy data preprocessing with Warp. Nature Methods. , (2019).
- Goddard, T. D., et al. UCSF ChimeraX: Meeting modern challenges in visualization and analysis. Protein Science. 27 (1), 14-25 (2018).
- Klebl, D. P., et al. Need for Speed: Examining Protein Behavior during CryoEM Grid Preparation at Different Timescales. Structure. , (2020).
- Noble, A. J., et al. Routine single particle CryoEM sample and grid characterization by tomography. eLife. 7, 32 (2018).
- Danev, R., Buijsse, B., Khoshouei, M., Plitzko, J. M., Baumeister, W. Volta potential phase plate for in-focus phase contrast transmission electron microscopy. Proceedings of the National Academy of Sciences. , (2014).
- Zi Tan, Y., et al. Addressing preferred specimen orientation in single-particle cryo-EMthrough tilting. Nature Methods. , (2017).
- Armstrong, M., Han, B. -. G., Gomez, S., Turner, J., Fletcher, D. A., Glaeser, R. M. Microscale Fluid Behavior during Cryo-EM Sample Blotting. Biophysical Journal. 118 (3), 708-719 (2020).
- Arnold, S. A., et al. Blotting-free and lossless cryo-electron microscopy grid preparation from nanoliter-sized protein samples and single-cell extracts. Journal of Structural Biology. , (2017).
- Dandey, V. P., et al. Spotiton: New Features and Applications. Journal of Structural Biology. , (2018).
- Rubinstein, J. L., et al. Shake-it-off: a simple ultrasonic cryo-EM specimen-preparation device. Acta crystallographica. Section D, Structural biology. 75, 1063-1070 (2019).
- Tan, Y. Z., Rubinstein, J. L. Through-grid wicking enables high-speed cryoEM specimen preparation. bioRxiv. , (2020).
- Klebl, D. P., et al. Sample deposition onto cryo-EM grids: From sprays to jets and back. Acta Crystallographica Section D: Structural Biology. , (2020).

