Single Particle Cryo-Electron Mikroskopi: Från prov till struktur
Summary
Strukturbestämning av makromolekylära komplex med cryoEM har blivit rutin för vissa klasser av proteiner och komplex. Här sammanfattas denna pipeline (provberedning, screening, datainsamling och bearbetning) och läsarna riktas mot ytterligare detaljerade resurser och variabler som kan ändras vid mer utmanande exemplar.
Abstract
Cryo-elektronmikroskopi (cryoEM) är en kraftfull teknik för strukturbestämning av makromolekylära komplex, via enstaka partikelanalys (SPA). Den övergripande processen innebär i) vitrifiera exemplaret i en tunn film som stöds på ett kryoEM-rutnät; ii) Screening av provexemplaret för att bedöma partikelfördelning och iskvalitet, iii) Om gallret är lämpligt, samla in en enda partikeldatauppsättning för analys. och iv) bildbehandling för att ge en EM-densitetskarta. I det här protokollet ges en översikt för vart och ett av dessa steg, med fokus på de variabler som en användare kan ändra under arbetsflödet och felsökning av vanliga problem. I och med att fjärrmikroskopdrift blir standard i många anläggningar kommer variationer på bildprotokoll för att hjälpa användare att effektivt använda och avbilda när den fysiska tillgången till mikroskopet är begränsad att beskrivas.
Introduction
En partikel CryoEM
För att undersöka livet på molekylär nivå måste vi förstå struktur. Många tekniker för att undersöka proteinstruktur finns tillgängliga, såsom NMR, röntgenkristallografi, masspektrometri och elektronmikroskopi (EM). Hittills har de flesta strukturer som deponerats på Protein Databank (PDB) lösts med hjälp av röntgenkristallografi. Men från ~ 2012 och framåt blev kryoelektronmikroskopi (cryoEM) en mainstream-teknik för proteinstrukturbestämning och dess användning ökade dramatiskt. Det totala antalet EM-kartor som deponerades på Electron Microscopy Databank (EMDB) (i december 2020) var 13 421 jämfört med 1 566 år 2012 (figur 1, www.ebi.co.uk). År 2012 var antalet atomkoordinater modellerade i kryoEM-densitetskartor, deponerade på PDB bara 67 men i december 2020 har 2 309 strukturer deponerats hittills, en 35-faldig ökning. Denna underliggande ökning av kvaliteten och kvantiteten av kryoEM-densitetskartor som producerades, ibland kallad “upplösningsrevolutionen”1, orsakades av en sammanslagning av framsteg på flera områden: utveckling av nya kameror för avbildning som kallas direkta elektrondetektorer; Ny programvara. och stabilare mikroskop2,3,4.
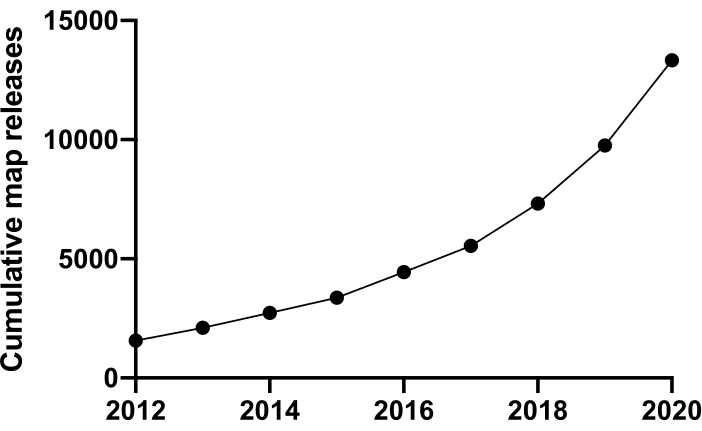
Figur 1: Kumulativa inlagor till EMDB från 2012 till december 2020. Klicka här för att se en större version av denna siffra.
Single particle analysis (SPA) är ett kraftfullt verktyg för att generera biologisk insikt i en mängd olika provtyper genom att belysa högupplösta strukturer av isolerade komplex5,6 inklusive virus7,8, membranproteiner9,10, spiralformade sammansättningar11 och andra dynamiska och heterogena makromolekylära komplex12,13, vars storlek varierar beroende på storleksordning (från 39 kDa 14,15 till tiotals megadalton). Här beskrivs ett protokoll för en standardpipeline för cryoEM SPA från exempel till struktur.
Innan detta rörledning påbörjas bör ett renat prov genomgå biokemisk analys för att bedöma dess chanser att lyckas nedströms. Beredning av ett lämpligt prov är utan tvekan det största hindret för SPA, särskilt för övergående och heterogena (både sammansättnings- och konformationella) komplex. Makromolekylära komplexa preparatet bör innehålla så få föroreningar som möjligt, vid tillräcklig koncentration för att ge många partiklar i varje cryoEM-mikrograf och i en buffertkomposition som är väl lämpad för kryoEM-analys. Vissa buffertbeståndsdelar, inklusive sackaros, glycerol och hög (~> 350 mM koncentrationer av salter, beroende på provstorlek, egenskaper och andra buffertbeståndsdelar) kan störa processen för vitrifikation eller minska signal-till-brus-förhållandet i bilder, vilket hindrar strukturbestämning16.
Vanligtvis bör storleksuteslutningskromatografi (SEC) och SDS- PAGE gelanalys användas för att bedöma provrenhet17,18, men cirkulär dichroism, funktionella analyser, SEC i kombination med flervinkelljusspridning och termiska stabilitetsanalyser är alla användbara verktyg för kvalitativ analys av makromolekylära komplexa preparat före kryoEM-analys. Resultaten från dessa biokemiska analyser kan dock ge liten insikt i provets strukturella heterogenitet och dess beteende på ett kryoEM-rutnät. Av denna anledning används negativ fläck EM rutinmässigt som ett snabbt, billigt och kraftfullt verktyg för att bedöma kompositionell och konformationell heterogenitet, och därför ett bra sätt att fastställa vilken elutionsfraktion från en rening som är mest lovande, eller screening av olika buffertkompositioner19,20. När ett lovande prov har identifierats kan vi gå vidare till SPA cryoEM-pipelinen. Negativ fläck överensstämmer inte alltid med de efterföljande resultaten som ses i cryoEM; ibland ser ett prov dåligt ut av negativ fläck men förbättras när det ses i glasaktig is i cryoEM. Däremot ser ibland prover utmärkta ut under negativa fläcksteg men kräver betydande ytterligare optimering när du går vidare till cryoEM. Men i de flesta fall ger negativ fläck ett användbart kvalitetskontrollsteg.
Förglasning
Den hårda miljön i elektronmikroskopets vakuumsystem orsakar både uttorkning och strålningsskador på ofixerade biologiska exemplar21. För att avbilda provet i ett inhemskt tillstånd måste därför det biologiska provet bevaras före avbildning. För renade preparat av makromolekylära komplex är vitrifikation den metod som valts för att möjliggöra dess visualisering genom cryoEM samtidigt som de atomiska detaljerna i komplexet bevaras. Upptäckten av vitrifikation som en metod för provberedning var ett grundläggande framsteg inom elektronmikroskopi av biologiska exemplar, för vilket Dubochet uppmärksammades i Nobelpriset i kemi 2017. Provvitrifiering innebär att skapa ett tunt lager av lösning som innehåller det prov av intresse, vanligtvis tiotals nm tjockt, upphängt på ett kryoEM-rutnätsstöd. Den tunna filmen fryses sedan extremt snabbt i en kryogen som flytande etan vid ~-175 °C. Fryshastigheten är ~106 °C/s, tillräckligt snabb för att amorf eller glasaktig is bildas, vilket suspenderar provet i en tunn, fast film22.
Den första variabeln att tänka på är kryoEM-rutnätsstödet som valts23. Ett EM-rutnät består vanligtvis av en amorf kolfilm med perforeringar (antingen regelbundna eller oregelbundna) över en stödstruktur. Stödstrukturen är vanligtvis ett cirkulärt metallnät med en diameter på 3,05 mm, vanligtvis tillverkad av koppar, men andra metaller som guld eller molybden (som har föredragna termiska expansionsegenskaper24) kan användas. Ibland appliceras ytterligare ett tunt, kontinuerligt stöd över nätet, såsom grafen, grafenoxid eller ett tunt (~ 1-2 nm) amorft kolskikt. Medan standard cryoEM-galler (oftast 400-200 mesh koppar med perforerad (1,2 μm runda hål åtskilda av 1,3 μm (r1,2/1,3), eller 2 μm åtskilda av 2 μm kol (r2/2)) har kolstöd – även om många olika mönster finns tillgängliga) använts i de allra flesta strukturer som rapporterats hittills, har ny nätteknik med förbättrad ledningsförmåga . Utvalda galler utsätts för en behandling för rengöring av glöd-urladdning/plasma för att göra dem hydrofila och mottagliga för provtillämpning26.
Efter glödurladdning är nästa steg tunnfilmsbildning. Denna tunna film bildas oftast med filterpapper för att avlägsna överflödig vätska från gallret. Även om detta kan utföras manuellt finns ett antal dykfrysningsanordningar kommersiellt tillgängliga, inklusive Vitrobot Mk IV (Thermo Fisher Scientific), EM GP II (Leica) och CP3 (Gatan). Med dessa enheter appliceras ~3-5 μL prov i lösning på EM-nätet, följt av att man blottar bort överflödig lösning med filterpapper. Gallret, med en tunn film upphängd över sig, kastas sedan i flytande etan som kyls av flytande kväve (LN2) till ~-175 °C. När gallret har frusits hålls det vid en temperatur under devitrifieringspunkten (-137 °C) före och under avbildningen.
Screening och datainsamling av prov
Efter vitrifikation av ett kryoEM-rutnät är nästa steg att screena rutnätet för att bedöma dess kvalitet och avgöra om rutnätet är lämpligt för att gå vidare till högupplöst datainsamling. Ett idealiskt kryoEM-galler har glasaktig is (i motsats till kristallin is) med istjockleken precis tillräcklig för att rymma den längsta dimensionen av provet, vilket säkerställer att den omgivande isen bidrar med så lite ljud till den resulterande bilden som möjligt. Partiklarna i isen ska ha en storlek och (om känd) form som överensstämmer med biokemin, och helst vara monodisperse med en slumpmässig fördelning av partikelorienteringar. Slutligen bör nätet ha tillräckligt med områden av tillräcklig kvalitet för att uppfylla önskad datainsamlingslängd. Beroende på exemplaret kan detta ta många iterationer av vitrifikation och screening tills optimala galler produceras. Både lyckligtvis och tyvärr finns det ett stort antal variabler som kan testas empiriskt för att ändra partikelfördelningen på kryoEM-rutnät (granskas 16,27). I detta manuskript visas representativa resultat för ett membranproteinprojekt10.
När ett lämpligt rutnät har identifierats kan datainsamlingen fortsätta. Flera modeller av kryotransitiva elektronmikroskop för biologiska exemplar är optimerade för att samla in högupplösta data på ett automatiserat sätt. Vanligtvis samlas data in på 300 kV- eller 200 kV-system. Automatiserad datainsamling kan uppnås med hjälp av programvara som EPU (Thermo Fisher Scientific)28, Leginon29, JADAS30 och SerialEM31,32. En automatiserad datainsamling med moderna detektorer resulterar vanligtvis i terabyte (TB) rådata under en 24-timmarsperiod (genomsnittliga datamängder är ~ 4 TB i storlek).
På grund av covid-19-restriktionerna på stora delar av världen (i skrivande stund december 2020) har många mikroskopianläggningar flyttat till att erbjuda fjärråtkomst. När näten har laddats in i en mikroskops autoloader kan datainsamlingen utföras på distans.
Bildbehandling och modellbyggnad
Om en datainsamlingssession vanligtvis kan vara 0,5-4 dagar kan efterföljande bildbehandling ta många veckor och månader, beroende på tillgängligheten av datorresurser. Det är standard för inledande bildbehandlingssteg, nämligen uppskattning av rörelsekorrigering och kontrastöverföringsfunktion (CTF) som ska äga rum “i farten” 33,34. För bearbetning nedströms finns det en mängd programvarusviter tillgängliga. Partiklar “plockas” och extraheras från mikrografer35,36. När partiklarna har extraherats skulle ett standardprotokoll vara att bearbeta partiklarna genom flera omgångar av klassificering (i båda dimensionerna (2D) och tre dimensioner (3D) och/eller fokuserade på specifika områden av intresse) för att nå en homogen delmängd av partiklar. Denna homogena delmängd av partiklarna beräknas sedan tillsammans för att producera en 3D-rekonstruktion. Vid denna tidpunkt korrigeras ofta data ytterligare för att producera högsta möjliga kvalitetskarta, till exempel genom CTF-förfining, förvrängningskorrigeringar37 och Bayesian polering38 . Resultatet av denna bildbehandling är en 3D cryoEM karta över det biologiska exemplaret av intresse. Upplösningsområdet som uppnås i ett “standard” automatiserat enpartikelexperiment från ett rutnät av tillräcklig kvalitet, med data som samlas in på ett 300 kV mikroskopsystem är vanligtvis mellan 10 Å och 2 Å beroende på proteinkomplexets storlek och flexibilitet. Med ett idealiskt exemplar har upplösningar på ~1,2 Å nu uppnåtts med hjälp av SPA-arbetsflöden5. Även om detta protokoll beskriver steg mot att få en EM-densitetskarta, kan den när den är i handen tolkas ytterligare genom montering och raffinering av en proteinmodell (om upplösningen är < 3,5 Å) eller bygga de novo39. Data som är associerade med experiment för strukturbestämning kan deponeras i offentliga online-databaser, inklusive EM-densitetskartor (Electron Microscopy Data Bank)40, resulterande atomkoordinater (Protein Data Bank)41 och råa datamängder (Electron Microscopy Public Image Archive)42.
I detta protokoll används det yttre membranproteinkomplexet RagAB (~ 340 kDa) från Porphyromonas gingivalis som ett exempel makromolekylärt komplex10 (EMPIAR-10543). För dem som är nya inom cryoEM är stöd för prover via denna pipeline från exempel till struktur tillgängligt, föremål för inbördes granskning, genom finansierade åtkomst system som iNEXT Discovery och Instruct.
Protocol
Representative Results
Discussion
I detta protokoll har vi beskrivit en grundläggande pipeline som är tillämplig på exemplar som är mottagliga för rutinmässiga SPA. Även om denna filterpapper blottningsmetod för tunnfilmsbildning och vitrifikation utan tvekan är framgångsrik med tanke på dess användning i de allra flesta SPA-projekt hittills, kommer det med ett antal nackdelar. Dessa inkluderar provsvinn, de långsamma tidsskalor (sekunder) som krävs för att bilda den tunna filmen och frysa provet, rapporterad irreproduktivitet27 och rapporterade negativa effekter av att använda filterpapper för att utplåna överflödig vätska50. Nyligen har ny teknik utvecklats för att förbättra reproducerbarheten av tunnfilmsproduktion51,52. Annan teknik har utvecklats som minskar tiden mellan provtillämpning och vitrifikation53,54,55. Även om filterpappersbaserade metoder för tunnfilmsbildning fortfarande är den mest allestädes närvarande metoden för SPA cryoEM-provberedning i skrivande stund, kan dessa nya tekniker medföra en rad fördelar när det gäller effektivitet och reproducerbarhet av nätvitrifiering, samt skapa nya möjligheter att få in ytterligare experimentella dimensioner, såsom tidsupplösning och snabb blandning före vitrifikation.
Processen med nätscreening för de flesta användare är för närvarande en kvalitativ process som innebär förvärv av atlaser med låg förstoring följt av att ta bilder med hög förstoring över nätet för att bedöma partikelfördelningen. Även om detta är ett tillräckligt robust tillvägagångssätt för vissa typer av prov, kan det vara svårt att bedöma med ögat om provet verkligen är vad forskaren hoppas kunna avbilda eller har en föredragen orientering, till exempel med små (<200 kDa) prover eller där den lågupplösta morfologin gör det svårt att identifiera med ögat om det finns en rad partikelfördelningar. För vissa projekt är det omöjligt att avgöra om exemplaret är som önskat, till exempel var en ligand är bunden eller var provet screenas för att bedöma om en liten (t.ex. 10 kDa) underenhet fortfarande finns i samband med ett komplex. För dessa projekt skulle helautomatiska pipelines för dataanalys i kombination med en "kort" 0,5- 1-h-samlingar, som kan fortsätta genom bildbehandlingssteg till 2D-klassificering eller till och med 3D-klassificering och förfining, hjälpa till att effektivt avgöra om en längre samling är berättigad. Dessa rörledningar är fortfarande under utveckling och är inte allmänt genomförda för närvarande, men de har potential att förbättra effektiviteten i cryoEM-nätscreening, särskilt för utmanande exemplar.
Förbättringar av direkta elektrondetektorer, liksom modifieringar inom mikroskopi i kombination med framsteg inom bildbehandling såsom insamling av bildskiftsdata, har ökat genomströmningen och kvaliteten på de bilder som produceras vid datainsamling. Denna ökning av den datahastighet som samlas in belyser behovet av noggrann screening av kryoEM-nät innan många TB data förvärvas.
CryoEM SPA har blivit en verkligt mainstream strukturell biologi teknik, och i många fall “gå till” strategi för vissa klasser av exemplar, såsom heterogena och labila makromolekylära komplex. Protokollet här beskriver en grundläggande översikt över SPA-pipelinen, men varje avsnitt som behandlas här (nätvitrifiering och screening, cryoEM och bildbehandling) är ett ämne i sig och värt att utforska under utvecklingen av ett SPA-projekt. I takt med att provberednings- och mikroskopitekniken utvecklas och nya algoritmer och metoder för bildbehandling kommer online kommer SPA att fortsätta att utvecklas som en pipeline, vilket hjälper forskare att få insikt i komplexa biologiska system.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Detta arbete stöddes av iNEXT-Discovery (Grant 871037) som finansierades av Europeiska kommissionens Horisont 2020-program. J B. R. White finansieras av Wellcome Trust (215064/Z/18/Z). FEI Titan Krios mikroskop finansierades av University of Leeds (UoL ABSL award) och Wellcome Trust (108466/Z/15/Z). Vi tackar M Iadanza för användningen av hans mikrografanalysskript. Vi bekräftar Diamond Light Source för åtkomst och stöd till kryo-EM-anläggningarna vid Storbritanniens nationella Electron Bio-imaging Centre (eBIC) som finansieras av Wellcome Trust, MRC och BBRSC.
Materials
| Blunt tweezers | Agar Scientific | AGT5022 | |
| Cryo EM round storage box | Agar Scientific | AGG3736 | |
| CryoEM autogrid boxes | ThermoFisher Scientific | 1084591 | |
| CryoEM grids | Quantifoil | N1-C14nCu30-01 | |
| Ethane gas | Boc | 270595-F | |
| LN2 foam dewar | Agar Scientific | AG81760-500 | |
| LN2 storage dewar | Worthington industries | HC 34 | |
| Pipette | Gilson | 10082012 | |
| Pipette tips | Star labs | s1111-1706 | |
| Syringe | BD | BD 300869 | |
| Type II lab water | Suez | select fusion | |
| Vitrobot | ThermoFisher Scientific | 1086439 | |
| Vitrobot filter paper | Whatman | 1001-055 | |
| Vitrobot styrophome container assembly | ThermoFisher Scientific | 1086439 | |
| Vitrobot tweesers | ThermoFisher Scientific | 72882-D | |
| Software | |||
| EPU | ThermoFisher Scientific | 2.8.1.10REL | |
| TEM server | ThermoFisher Scientific | 6.15.3.22415REL | |
| Tia | ThermoFisher Scientific | 5.0.0.2896REL | |
| Titan krios microscope | ThermoFisher Scientific | Titan Krios G2 |
References
- Kuehlbrandt, W. The Resolution Revolution. Science. 343 (6178), 1443-1444 (2014).
- McMullan, G., Faruqi, A. R., Henderson, R. Direct Electron Detectors. Methods in Enzymology. , (2016).
- Elmlund, D., Le, S. N., Elmlund, H. High-resolution cryo-EM: the nuts and bolts. Current Opinion in Structural Biology. , (2017).
- Lyumkis, D. Challenges and opportunities in cryo-EM single-particle analysis. Journal of Biological Chemistry. , (2019).
- Nakane, T., et al. Single-particle cryo-EM at atomic resolution. Nature. , (2020).
- Yip, K. M., Fischer, N., Paknia, E., Chari, A., Stark, H. Atomic-resolution protein structure determination by cryo-EM. Nature. , (2020).
- Conley, M. J., et al. Calicivirus VP2 forms a portal-like assembly following receptor engagement. Nature. 565 (7739), 377-381 (2019).
- Hesketh, E. L., et al. The 3.3 Å structure of a plant geminivirus using cryo-EM. Nature communications. 9 (1), 2369 (2018).
- Malone, L. A., et al. Cryo-EM structure of the spinach cytochrome b6 f complex at 3.6 A resolution. Nature. 575 (7783), 535-539 (2019).
- Madej, M., et al. Structural and functional insights into oligopeptide acquisition by the RagAB transporter from Porphyromonas gingivalis. Nature Microbiology. , (2020).
- Gallardo, R., et al. Fibril structures of diabetes-related amylin variants reveal a basis for surface-templated assembly. Nature Structural and Molecular Biology. , (2020).
- Scarff, C., et al. Structure of the shutdown state of myosin-2. Nature. , (2020).
- Scarff, C. A., et al. Structure of the protective nematode protease complex H-gal-GP and its conservation across roundworm parasites. PLoS Pathogens. 16 (4), 1008465 (2020).
- Wu, M., Lander, G. C. How low can we go? Structure determination of small biological complexes using single-particle cryo-EM. Current Opinion in Structural Biology. , (2020).
- Khoshouei, M., Radjainia, M., Baumeister, W., Danev, R. Cryo-EM structure of haemoglobin at 3.2 Å determined with the Volta phase plate. Nature Communications. , (2017).
- Drulyte, I., et al. Approaches to altering particle distributions in cryo-electron microscopy sample preparation. Acta crystallographica. Section D, Structural biology. 74, 560-571 (2018).
- Thompson, R. F., Walker, M., Siebert, C. A., Muench, S. P., Ranson, N. A. An introduction to sample preparation and imaging by cryo-electron microscopy for structural biology. Methods. 100, 3-15 (2016).
- Cheng, Y., Grigorieff, N., Penczek, P. A., Walz, T. A primer to single-particle cryo-electron microscopy. Cell. 161 (3), 438-449 (2015).
- Scarff, C. A., Fuller, M. J. G., Thompson, R. F., Iadanza, M. G. Variations on negative stain electron microscopy methods: tools for tackling challenging systems. Journal of Visualized Experiments. (132), e57199 (2018).
- Ohi, M., Li, Y., Cheng, Y., Walz, T. Negative Staining and Image Classification – Powerful Tools in Modern Electron Microscopy. Biological procedures online. 6, 23-34 (2004).
- Baker, L. A., Rubinstein, J. L. Radiation Damage in Electron Cryomicroscopy. Methods in enzymology. 481, 371-388 (2010).
- Dubochet, J., et al. Cryo-electron microscopy of vitrified specimens. Quarterly Reviews of Biophysics. 21 (02), 129-228 (1988).
- Passmore, L. A., Russo, C. J. Specimen Preparation for High-Resolution Cryo-EM. Methods in enzymology. 579, 51-86 (2016).
- Carragher, B., et al. Current outcomes when optimizing ‘standard’ sample preparation for single-particle cryo-EM. Journal of Microscopy. , (2019).
- Naydenova, K., Jia, P., Russo, C. J. Cryo-EM with sub-1 Å specimen movement. Science. , (2020).
- Passmore, L. A., Russo, C. J. Specimen Preparation for High-Resolution Cryo-EM. Methods in Enzymology. , (2016).
- Thompson, R. F., Iadanza, M. G., Hesketh, E. L., Rawson, S., Ranson, N. A. Collection, pre-processing and on-the-fly analysis of data for high-resolution, single-particle cryo-electron microscopy. Nature protocols. 14 (1), 100-118 (2019).
- Suloway, C., et al. Automated molecular microscopy: the new Leginon system. Journal of Structural Biology. 151 (1), 41-60 (2005).
- Zhang, J., et al. JADAS: A customizable automated data acquisition system and its application to ice-embedded single particles. Journal of Structural Biology. , (2009).
- Mastronarde, D. N. SerialEM: A program for automated tilt series acquisition on Tecnai microscopes using prediction of specimen position. Microscopy and Microanalysis. , (2003).
- Schorb, M., Haberbosch, I., Hagen, W. J. H., Schwab, Y., Mastronarde, D. N. Software tools for automated transmission electron microscopy. Nature Methods. , (2019).
- Fernandez-Leiro, R., Scheres, S. H. W. A pipeline approach to single-particle processing in RELION. Acta crystallographica. Section D, Structural biology. 73, 496-502 (2017).
- Gómez-Blanco, J., et al. Using Scipion for stream image processing at Cryo-EM facilities. Journal of Structural Biology. , (2018).
- Wagner, T., et al. SPHIRE-crYOLO is a fast and accurate fully automated particle picker for cryo-EM. Communications biology. 2 (1), 213-218 (2019).
- Bepler, T., et al. TOPAZ: A Positive-Unlabeled Convolutional Neural Network CryoEM Particle Picker that can Pick Any Size and Shape Particle. Microscopy and Microanalysis. , (2019).
- Zivanov, J., et al. New tools for automated high-resolution cryo-EM structure determination in RELION-3. eLife. 7, 163 (2018).
- Zivanov, J., Nakane, T., Scheres, S. H. W. A Bayesian approach to beam-induced motion correction in cryo-EM single-particle analysis. IUCrJ. , (2019).
- Cianfrocco, M. A., Kellogg, E. H. What Could Go Wrong? A Practical Guide to Single-Particle Cryo-EM: From Biochemistry to Atomic Models. Journal of Chemical Information and Modeling. , (2020).
- Tagari, M., Newman, R., Chagoyen, M., Carazo, J. M., Henrick, K. New electron microscopy database and deposition system. Trends in Biochemical Sciences. , (2002).
- Berman, H. M., et al. The Protein Data Bank. Nucleic Acids Research. , (2000).
- Iudin, A., Korir, P. K., Salavert-Torres, J., Kleywegt, G. J., Patwardhan, A. EMPIAR: A public archive for raw electron microscopy image data. Nature Methods. , (2016).
- Punjani, A., Rubinstein, J. L., Fleet, D. J., Brubaker, M. A. CryoSPARC: Algorithms for rapid unsupervised cryo-EM structure determination. Nature Methods. , (2017).
- Tegunov, D., Cramer, P. Real-time cryo-electron microscopy data preprocessing with Warp. Nature Methods. , (2019).
- Goddard, T. D., et al. UCSF ChimeraX: Meeting modern challenges in visualization and analysis. Protein Science. 27 (1), 14-25 (2018).
- Klebl, D. P., et al. Need for Speed: Examining Protein Behavior during CryoEM Grid Preparation at Different Timescales. Structure. , (2020).
- Noble, A. J., et al. Routine single particle CryoEM sample and grid characterization by tomography. eLife. 7, 32 (2018).
- Danev, R., Buijsse, B., Khoshouei, M., Plitzko, J. M., Baumeister, W. Volta potential phase plate for in-focus phase contrast transmission electron microscopy. Proceedings of the National Academy of Sciences. , (2014).
- Zi Tan, Y., et al. Addressing preferred specimen orientation in single-particle cryo-EMthrough tilting. Nature Methods. , (2017).
- Armstrong, M., Han, B. -. G., Gomez, S., Turner, J., Fletcher, D. A., Glaeser, R. M. Microscale Fluid Behavior during Cryo-EM Sample Blotting. Biophysical Journal. 118 (3), 708-719 (2020).
- Arnold, S. A., et al. Blotting-free and lossless cryo-electron microscopy grid preparation from nanoliter-sized protein samples and single-cell extracts. Journal of Structural Biology. , (2017).
- Dandey, V. P., et al. Spotiton: New Features and Applications. Journal of Structural Biology. , (2018).
- Rubinstein, J. L., et al. Shake-it-off: a simple ultrasonic cryo-EM specimen-preparation device. Acta crystallographica. Section D, Structural biology. 75, 1063-1070 (2019).
- Tan, Y. Z., Rubinstein, J. L. Through-grid wicking enables high-speed cryoEM specimen preparation. bioRxiv. , (2020).
- Klebl, D. P., et al. Sample deposition onto cryo-EM grids: From sprays to jets and back. Acta Crystallographica Section D: Structural Biology. , (2020).

