Praktiska aspekter av provberedning och installation av 1H R 1ρ avslappningsdispersionsexperiment av RNA
Summary
Vi presenterar ett protokoll för att mäta mikro- till millisekekunder dynamik på 13C /15N-märkta och omärkta RNA med 1H R1ρ avslappning dispersion kärnmagnetisk resonans (NMR) spektroskopi. Fokus för detta protokoll ligger i hög renhetsprovberedning och installation av NMR-experiment.
Abstract
RNA är en mycket flexibel biomolekyl, där förändringar i strukturer spelar avgörande roller i de funktioner som RNA-molekyler utför som cellulära budbärare och modulatorer. Medan dessa dynamiska tillstånd förblir dolda för de flesta strukturella metoder, R1ρ avslappning dispersion (RD) spektroskopi gör det möjligt att studera konformationsdynamik i mikro-till millisekunder regim vid atomupplösning. Användningen av 1H som observerad kärna utökar ytterligare den tidsordning som omfattas och ger direkt tillgång till vätebindningar och basparning.
De utmanande stegen i en sådan studie är hög renhet och hög avkastning provberedning, potentiellt 13C- och 15N-märkta, samt installation av experiment och montering av data för att extrahera befolkning, växelkurs och sekundär struktur i det tidigare osynliga tillståndet. Detta protokoll ger viktiga praktiska steg i provberedning för att säkerställa beredning av ett lämpligt RNA-prov och installation av 1H R1ρ experiment med både isotopiskt märkta och omärkta RNA-prover.
Introduction
RNAs utför en mängdreglerande 1,katalytiska2, och strukturella3 funktioner i cellen, varav många är korrelerade till en flexibel molekylär struktur och invecklade förändringar av dessa strukturer4,5,6,7. Lågbefolkade tillstånd förblir osynliga för de flesta metoder för strukturbestämning eller tillåter inte studier av dessa dolda tillstånd med hög atomupplösning. Lösningstillstånd kärnmagnetisk resonansspektroskopi (NMR) kombinerar båda aspekterna genom att ge tillgång till enskilda atomkärnor samt erbjuda en stor verktygslåda med experiment som riktar sig mot dynamik genom alla tidsregimer8. RD NMR-experiment ger tillgång till konformationsutbyte i mellantidsskalan, där förändringar i basparningsmönster och lokala strukturella omorganiseringar kan förväntas5,9,10,11,12,13,14. RD-experiment utförs som långa R2-mätningar i form av ett Carr-Purcell-Meiboom-Gill pulståg15 eller som avslappningsmätningar i den roterande ramen, kallade R1ρ RD-experiment16.
Även om båda kan användas för att extrahera population av och växelkurs och kemisk skiftskillnad till det mindre tillståndet, ger R1ρ RD-experiment också tecknet på den kemiska skiftskillnaden i det upphetsade tillståndet. Detta möjliggör en slutsats om sekundär struktur, vilket starkt korrelerar till kemisk förändring i RNA-strukturer17. Det kemiska skiftet är en bra indikator på helicitet när det gäller aromatiska protoner och kol på kärnkärnorna, basparningspartners för iminoprotoner och sockerpuckers på C4′ och C1′ atomer18,19. Det bör noteras att nyligen ett experiment för överföring av kemiska utbytesmättnad (CEST) med högre spinnlåskraft (SL), vilket flyttade tillämpligheten av CEST-experimentet till snabbare växelkurstidsskalor, publicerades som ett alternativ till R1ρ RD-experimentet för system med ett upphetsad tillstånd.
Även om 13C och 15N isotoper ofta har använts för att få tillgång till strukturellt utbyte, använde nyligen arbete från detta laboratorium aromatiska och imino protoner som sonder för konformationsutbyte9,10. Användningen av 1H som observerad kärna ger flera fördelar, till exempel tillgång till utbyte på snabbare och långsammare tidsskalor, högre känslighet och kortare mättider. Detta underlättas ytterligare av SELective Optimized Proton Experiment (SELOPE) strategi, ger tillgång till aromatiska protoner genom dekrowding av det endimensionella (1D) spektrumet med hjälp av homonukleära skalär kopplingar, istället för en heteronukleär magnetisering överföring, och eliminera behovet av isotop etiketter20. Detta protokoll behandlar mätningen i 1H R1ρ RD-experiment med enhetliga 13C/15N-märkta och omärkta prover. Därför presenterar detta dokument en provberedningsmetod som konstaterades vara den mest mångsidiga för olika provberedningsbehov21 och diskuterar alternativ i det sista avsnittet i denna artikel (figur 1).
Vid denna tidpunkt bör läsaren notera att andra provberedningsmetoder är godtagbara för 1H R1ρ RD-experiment och att andra metoder för strukturell och funktionell analys kan utföras med proverna syntetiserade med den presenterade tekniken. 1 (på 1) H R1ρ RD-experiment kräver höga RNA-koncentrationer (helst >1 mM) samt hög homogenitet, både i RNA-längd och strukturell konformation för att säkerställa tillförlitlig karakterisering av molekylär dynamik. In vitro-transkription (IVT) är den metod som många forskare väljer för att producera 13C/15N-märkta RNA-prover på grund av tillgången på märkta nukleosid triphosphates (NTPs) och underlätta införlivande i den enzymatiska reaktionen22. Emellertid lider den allmänt använda T7 RNA-polymerasen (T7RNAP)23,24,25 från låg 5′ homogenitet vid vissa initieringssekvenser26,27 och ofta också 3′ homogenitet under transkriptionavrinning 28. Rening av mål RNA-arten blir dyrare och mödosam på grund av behovet av stora mängder ~ 200 nmol. Metoden som används här har presenterats tidigare där fördelar diskuterades i stort21. Kort sagt löser det beskrivna problem genom att transkribera en större tandemavskrift som sedan specifikt klyvs av Escherichia coli RNase H, vägledd av en chimerisk oligonukleotid29,30 (se figur 2 för detaljer).
Införlivande av en distanssekvens i tandemavskriftens ändar på 5′ respektive 3″ gör det möjligt att använda en initieringssekvens med hög avkastning och avlägsnande av terminalöverhäng nära linjäriseringsplatsen för plasmidmallen (figur 2B). Metoden visade sig förbättra avkastningen avsevärt, samtidigt som kostnaderna och arbetet minskade, med förbehållet för en mer komplex mallsyntes och behovet av ett ytterligare enzym och oligonukleotid. Den höga specificiteten hos RNase H klyvning underlättar rening på grund av bristen på RNA arter i ett liknande storleksintervall. Det nuvarande protokollet använder ett jonutbyte högpresterande vätskekromatografi (HPLC) steg som har publicerats av detta laboratorium nyligen31, även om andra metoder är möjliga alternativ. 1 (på 1) H R1ρ RD kan i allmänhet förvärvas på märkta eller omärkta prover med två respektive pulssekvenser, det “märkta” 1H R1ρ heteronukleära enskilda kvantkorrelationsprovet (HSQC)-baserat experiment med en indirekt dimension på 13C10 och det “omärkta“ 1H R1ρ SELOPE-baserade experimentet med en indirekt dimension20på 1H.
Dessa tvådimensionella (2D) experiment kan fungera som en första kontroll, oavsett om dynamiken på R1ρ-tidsskalan finns i provet. En översikt över rd för alla lösta toppar i spektra kan erhållas, och toppar av intresse för en mer grundlig RD-analys kan identifieras. Detta innebär att även omärkta prover kan kontrolleras innan ett beslut om att ta fram ett dyrare, märkt prov görs. När en topp med konformationsutbytesbidrag har valts ut för att studeras mer noggrant är det bäst att byta till 1D-versionerna av ovanstående experiment (om toppen fortfarande kan lösas) för att utföra så kallade off-resonansexperiment. För den märkta versionen HSQC-överföringen till 13C ersätts med ett selektivt heteronukleärt korspolariseringssteg (HCP) som används i 13C R1ρ experiment32,33,34,35, medan experimentet i fallet med SELOPE-experimentet helt enkelt körs som en 1D, vilket är särskilt användbart för H8- och H2-signaler som ligger på diagonalen i 2D ändå. Ett kriterium för vilken sekvens som ska användas, förutsatt att både ett märkt och omärkt prov finns tillgängligt, är hur väl isolerad toppen av intresset är i de två experimenten.
I allmänhet rekommenderas SELOPE-experimentet för RNA-prover på upp till 50 nukleotider. För större RNAs kommer överlappningen att vara större; Strukturellt intressanta nukleotider förekommer dock ofta i kemiska skiftregioner som är mindre överlappande och fortfarande kan vara tillgängliga i ännu större RNAs. Ett annat argument skulle vara att i omärkta prover sker ingen J-koppling mellan 1H och 12C. Eftersom minsta spinnlåseffekt definieras av den minsta effekt som används för att frikoppla dessa två spinn (~1 kHz) i det märkta experimentet, tillåter det omärkta experimentet användningen av ett bredare utbud av spinnlås (SL) styrkor och därmed tillgång till en bredare tidsskala för utbyte. Dessa off-resonans experiment ger ytterligare information till kex, såsom populationen av det upphetsade tillståndet (alternativ konformator), pES, liksom mycket värdefull kemisk skiftinformation i form av Δω (den kemiska skiftskillnaden mellan marktillståndet och det upphetsade tillståndet).
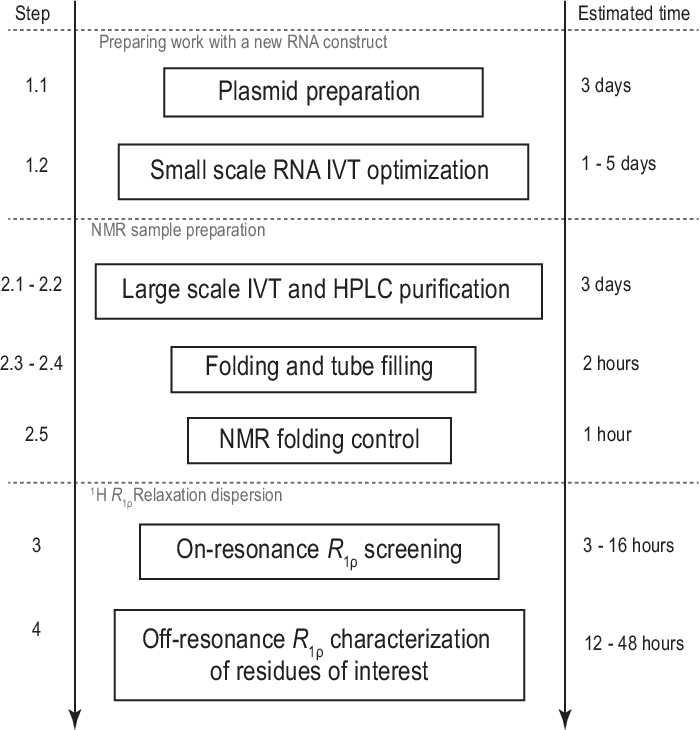
Figur 1: Arbetsflöde för det presenterade protokollet. Förberedelse före den faktiska storskaliga provproduktionen, bestående av mallberedning och bekräftelse av framgångsrik in vitro-transkription och RNase H-klyvning. Storskalig produktion inklusive HPLC-rening, fyllning av NMR-rör och bekräftelse av RNA-vikning. Vid isotopmärkt syntes bör en omärkt rening utföras för gradientoptimering samma dag. NMR karakterisering av konformationsdynamik med R1ρ experiment. Varje steg kan utföras självständigt, t.ex. 1H R1ρ RD-analysen kan tillämpas på alla lämpliga RNA-prov som produceras med en annan metod. Förkortningar: IVT = in vitro-transkription; HPLC = högpresterande vätskekromatografi; NMR = kärnmagnetisk resonans; RD = avslappningsspridning. Klicka här om du vill visa en större version av den här figuren.
Syftet med detta protokoll är att ge praktiska detaljer och kritiska parametrar för studier av konformationsdynamik med 1H R1ρ avslappningsdispersion i RNA-hårnålsmolekyler. Efter att ha tillhandahållit ett detaljerat protokoll över design, syntes och jonutbyte HPLC-rening av ett mål-RNA som kan utföras med alla, vissa eller inga NTPs som 13C /15N-märkta versioner, har arbetsflödet för att slutföra NMR-provet och bekräfta konformationsutbytet med NMR-spektroskopi beskrivits. Slutligen beskrivs detaljerna för installationen av 1H R1ρ RD-experiment på en Bruker NMR-spektrometer (figur 1). Protokollet ger varje steg för att ställa in 1D-versionen för märkta prover och ytterligare kommentarer och en tabell för att justera för inställningen av SELOPE-versionen (tabell 2). Efter protokollet diskuteras kritiska steg och alternativa vägar till prov förberedelse och 1H R1ρ RD setup.
Protocol
Representative Results
Discussion
Protokollet som presenteras häri är en syntes av flera protokoll som publicerats tidigare i form av forskningsartiklar10,20,21,31. Därför kan segment av protokollet tillämpas, medan andra kan bytas till läsarens önskemål. Till exempel kan R1ρ-mätningarna utföras på ett RNA-prov som produceras med vilken metod som helst, med tanke på att vikning och homogenitet av längden antas. Dessutom innehåller protokollet inte information om resonanstilldelning av RNA-sekvensen -ett steg som krävs för RD-experiment – eftersom detta har täckts mycket i tidigarelitteratur 19,37,38. Partiella, segmentala eller platsspecifika märkningssystem36,41,42,43,44 är metoder för att underlätta resonanstilldelning eller minska överlappningen av resonanser som är av intresse för RD-experiment och har beskrivits länge i litteraturen. Denna metod tillåter användning av enhetlig märkning av alla nukleotididentiteter, vilket redan kan förenkla resonanstilldelningen avsevärt.
IVT-metoden som presenteras här övervinner kända problem med sekvenser och märkning, ökar avkastningen och minskar kostnader och arbetstid jämfört med andra metoder. Användningen av den virala initieringssekvensen minskar behovet av reaktionsoptimering, vilket är ett känt problem inom området som kan vara tidskrävande att utföra och ger bara några kopior av avskriften vid icke-G-initiering. Tandemavskriftens T7 IVT- och RNase H-klyvning kan utföras samtidigt i samma kärl. Ett mönster av multimeriska tandemrepetitioner kan ses på en denaturerande PAGE-gel under reaktionen, som sammanförs till ett enda band på mål-RNA efter slutförandet av RNase H-reaktionen (Figur 3A, körfält 1 och 2b). Typiska utbyten med denna metod varierar mellan 30 och 70 nmol RNA per 1 ml IVT. Ändå kommer metoden baserad på RNase H klyvning av tandemrepetitioner inte utan vissa egna problem. RNase H-klyvningsreaktionen slutförs ofta inte när den körs samtidigt med T7-transkription (Figur 3A, körfält 2a).
Separationen av tandemenheter kan slutföras genom att klyvningsguiden glödgas till avskriften och lägga till fler RNase H (Figur 3A, körfält 2b, steg 2.1.2). Eftersom uppvärmningen av stora volymer är långsam och leder till Mg2 +-katalyserad hydrolys av RNA användes en konventionell mikrovågsugn, vilket värmer provet till >95 °C på 10-15 s. Negativa effekter på de producerade proverna har hittills inte observerats. Vissa konstruktioner visar ett mindre andra band som inte kunde elimineras genom optimering av reaktionsförhållandena (Figur 3A, körfält 4). Vanligtvis är dessa ganska tydligt synliga som en axel i HPLC-kromatogrammet, om en väloptimerad elueringsgradient används och kan tas bort (steg 2.2.5). Följande diskussion syftar till att belysa kritiska steg i protokollet, särskilt när det gäller att erhålla högkvalitativa data som möjliggör en tolkning av konformationsdynamiken.
RNase förorening
Extracellulära RNases är allestädes närvarande, mycket stabila och utgör det största hotet för långsiktig stabilitet hos NMR-prover. Därför är det viktigt att arbeta i en RNase-fri miljö och hålla alla reagenser och plastartiklar RNase-fria. Användningen av filterspetsar och kanske till och med ansiktsmasker rekommenderas. Detta är särskilt viktigt efter HPLC-rening. NMR-prover som är förorenade med RNases uppvisar vanligtvis smala toppar synliga i 1H-1D-spektra efter dagar eller veckor på grund av enkärniga nedbrytningsprodukter. Ett sådant prov är inte lämpligt för R1ρ-mätningar.
NMR-prov
På grund av sin mycket laddade natur kan RNA användas i höga koncentrationer utan nederbörd jämfört med de flesta proteiner. Användningen av Shigemi NMR-rör (se materialtabellen)är fördelaktig eftersom de tillåter centrering av det högkoncentrerade provet i mitten av spolen samtidigt som det ger idealiska shimming- och låsförhållanden på grund av den känslighetsmatchade glasbotten och kolven. På så sätt reduceras B1-inhomogenitet, vilket ger upphov till smalare linjer. Den typiska provvolymen i ett NMR-rör är 250 μL och den typiska koncentrationen är 1-2 mM. Prover under 500 μM rekommenderas inte för RD-experiment eftersom experimentet skulle ta för lång tid och en bra shim. På samma sätt rekommenderas inte provvolym under 200 μL eftersom en god shim och fältstabilitet (lås) krävs. Vid insättning av kolven är det viktigt att undvika bildandet av bubblor i provet (steg 2.4.5). Om kolven inte är korrekt fastsatt kan den glida ner i provet, vilket minskar den detekterbara volymen. Dessutom kan snabba temperaturförändringar leda till bildandet av nya bubblor i provet. Därför bör försiktighet vidtas vid transport av provet och vid ändring av sondtemperaturen i NMR-spektrometern. Kontrollera provet för bubblor när du mäter igen efter en längre period.
RNA-vikning
Dynamiska RNA-molekyler kan finnas i flera konformationer när de inte viks ordentligt. Även om smälttemperaturer i sekundära strukturer endast kan vara något över rumstemperaturen, rekommenderas ett grundligt uppvärmnings- och snäppkylningsförfarande före mätning. Högkoncentrerade hårnålsprover som viks under kinetisk kontroll (uppvärmning och snapkylning) kan bilda homodimers över tid, vilket kräver rigorös kontroll av RNA-vikning före varje NMR-mätning. Om det uppmätta RNA inte är en hårnålsstruktur utan en RNA-duplex, bör långsam vikning under termodynamisk kontroll appliceras.
I detta fall bör kylprocessen efter uppvärmning vara inom intervallet timmar, medan RNA används vid sin slutliga volym och koncentration i NMR-provet. En första räkning av förväntade imino och aromatiska resonanser kan ge insikt om provets homogenitet. Om provet inte ser ut som förväntat bör det vikas om. Mg2+ (tillsatt som kloridsalt) kan hjälpa till med vikbara RNA-strukturer45. I praktiken fungerar vikningskontrollen som en jämförelse med ett prov som har använts för att åtminstone delvis tilldela NMR-resonanserna och för att lösa den sekundära strukturen experimentellt.
Spinnlåskraft och värmeöverväganden
Vid körning av 1H R1ρ RD-experiment som 2D-översiktsexperiment bör SL-kraften inte vara lägre än 1,2 kHz. Radiofrekvensen ska placeras i mitten av ppm-området i de bästa topparna (t.ex. 7,5ppm för aromatiska protoner). Bandbredden på 1,2 kHz kommer då att vara tillräckligt stor för att spinna dessa protoner utan några större off-resonanseffekter. Sådana effekter kan identifieras i RD-profilen. Om de inträffar ökar R2+REX-värden istället för att minska med ökande SL-effektvärden, särskilt för låg SL-effekt. Kontrollera om de beräknade SL-effektvärdena motsvarar den effekt som levereras till provet. I praktiken kan beräknad SL-effekt användas om 1H 90° hårdpulsen kalibrerades noggrant på nyare spektrometrar; Detta kan dock kontrolleras genom att kalibrera SL-ström för varje önskad bandbredd.
Utbudet av SL-effekt, som kan användas i 1H R1ρ RD-experiment, är mycket brett, vilket leder till varierande provuppvärmning (1,2 kHz till 15 kHz för HSQC för HCP-baserade sekvenser och 50 Hz till 15 kHz för SELOPE-experiment). Ojämn provuppvärmning kan detekteras som en liten förändring i kemiskt skifte när man jämför 1D:er som erhållits för lågeffekts-SLs jämfört med. hög effekt SLs. Denna effekt beaktas vanligtvis inte i värmekompensationer i R1ρ experiment på heteronuclei. Värmekompensation i dessa experiment ställs vanligtvis in för att korrigera för olika uppvärmning på grund av de olika spinnlåslängder som anges i vd-listan för varje spinnlåskraftserie. Speciellt för SELOPE-experimentet bör en andra värmekompensation användas över alla tillämpade SL-styrkor enligt beskrivningen i20.
vd-lista överväganden
Som nämnts tidigare bör vd-listan innehålla en tidspunkt som är tillräckligt lång för att erhålla ett betydande förfall av intensitet (helst ner till 30% av den ursprungliga signalen eller så låg som möjligt om det inte är möjligt att nå ett 70% förfall inom sondens specifikationer). Även om vd-listan var optimerad för en låg SL-effekt (1,2 kHz), bör denna vd-lista också testas med den högstaSL-effektsom ska användas ( t.ex. 15 kHz). Detta beror på att för toppar med betydande REX-bidrag kommer förfallet att vara mycket långsammare vid hög SL-effekt. Så ett tillräckligt förfall bör också verifieras vid hög SL-effekt. Detsamma måste övervägas för förfall vid höga förskjutningar i off-resonans experiment. Den idealiska maximala tidspunkten för vd-listan kan vara betydligt annorlunda för de olika regionerna i spridningsexperimentet. I så fall kan fler punkter ingå i vd-listan, och ju längre vd-listpunkter för högre SL-effekt eller högre förskjutningar under analysen, baserat på den låga SINO de kommer att leda till, kan kasseras. I allmänhet bör 5-8 vd-listpunkter anses kunna upptäcka potentiella artefakter som leder till icke-exponentiella förfall som J-koppling (se nedan).
1D–HCP selektivitet överväganden
Särskild försiktighet måste vidtas när du kör den HCP-baserade 1D-versionen om det finns en annan topp som överlappar med toppen av intresset för 1H-dimensionen i det 2D HSQC-baserade experimentet. HCP-baserade överföringar är mycket, men aldrig 100% selektiva, och det kan därför hända att en annan topp bidrar till intensiteten och förfallsbeteendet hos toppen av intresset för 1D. En indikation på detta skulle vara en skillnad i värdena R1ρ som erhålls med hjälp av 1D- och 2D-versionerna av det märkta experimentet.
ROE överväganden:
För off-resonanskurvor av atomer med långsam mellanliggande utbyte, ROE artefakter kan identifieras baserat på en jämförelse av den erhållna Δω med en NOESY eller ROESY spektrum. Om en korstopp kan identifieras vid en kemisk skiftskillnad motsvarande Δω, kan det observerade upphetsade tillståndet i själva verket vara en ROE-artefakt (t.ex.hittades ROEs mellan aromatiska protoner, som alla ligger i samma kemiska skiftområde och därför omfattas av dessa off-resonanskurvor20). Av erfarenhet ledde detta alltid också till dåliga anfall med stora fel, möjligen på grund av att ROE inte följer samma mönster som REX med ökande SL-kraft. Situationen blir svårare för mellansnabbt utbyte. Medan resonanskurvan är (från jämförelse med 13C-data som erhållits på grannkärnan) fortfarande representativ för utbytesprocessen mellan GS och ES, påverkas off-resonanskurvan av flera ROE-artefakter.
I så fall är SL-kraften för att upptäcka utbytesprocessen större (>1,5 kHz) och sträcker sig därför över ett större antal protoner eftersom off-resonanskurvor sträcker sig över kemiska skiftskillnader mellan olika ROE-kandidater (för H8 skulle dessa vara: aminoprotoner vid ca. ±1000 Hz, H5/H1 är på ca -1200 Hz, imino protoner vid ca 3500 Hz). Hittills har det inte visat sig att någon metod för att undertrycka dessa ROE-artefakter (annat än att använda delvis avuteröjda nukleotider46),och data från annan än resonans bör inte registreras för snabb mellanliggande utbyte, eftersom ingen tillförlitlig information om den faktiska Δω kan extraheras med denna metod, om NOE/ROE-bidraget inte kan uteslutas via NOESY-spektra.
J-Koppling (Hartmann-Hahn) överväganden
Även om on-resonanskurvor för homonukleära J-kopplade protoner, såsom H6, framgångsrikt registrerades10,20, måste särskild försiktighet tas för off-resonansmätningar, särskilt för låg SL-kraft eftersom Hartmann-Hahn matchande villkor kan sträcka sig över ett brett spektrum av de undersökta förskjutningarna. Hartmann-Hahn artefakter kan identifieras som svängningar på det exponentiella förfallet eller ökande R2+REX-värden med ökande SL-styrkor i on-resonans RD-tomter20.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi tackar proteinvetenskapsanläggningen (PSF) vid Karolinska Institutet för uttryck och rening av T7 RNA-polymeras och E. coli RNase H, Martin Hällberg för den oorganiska fosfatasens generösa gåva och hela Petzoldlab för värdefulla diskussioner. Vi tackar Luca Retattino för förberedelserna av U-bulge-konstruktionerna och Emilie Steiner och Carolina Fontana för deras bidrag till makron och passande manus. Vi bekräftar Karolinska Institutet och Institutionen för medicinsk biokemi och biofysik för att stödja inköp av en 600 MHz spektrometer- och positionsfinansiering (KI FoAss och KID 2-3707/2013). Vi är tacksamma för ekonomiska bidrag från Vetenskapsrådet (#2014-4303), Stiftelsen för strategisk Forskning (ICA14-0023 och FFL15-0178) och Ragnar Söderberg Stiftelse (M91-14), Harald och Greta Jeansson Stiftelse (JS201400 09), Carl Tryggers stiftelse (CTS14-383 och 15-383), Eva och Oscar Ahréns Stiftelse, Åke Wiberg Stiftelse (467080968 och M14-0109), Cancerfonden (CAN 2015/388), J.S. erkänner finansiering genom en Marie Skłodowska-Curie IF (EU H2020, MSCA-IF projekt nr 747446).
Materials
| 40% Acrylamide/Bis Solution | Bio-Rad | 161-0144 | |
| 5-alpha Competent E. coli | NEB | C2987I | |
| Acetic Acid | Sigma-Aldrich | 49199 | |
| Acetonitrile | Sigma-Aldrich | 34851 | |
| AFC-3000, HPLC Fraction collector | Thermo Scientific | 5702.1 | |
| Agarose | Sigma-Aldrich | A9414 | |
| Amersham ImageQuant 800 UV | GE Healthcare | 29399482 | Replacing LAS-4000 or equivalent |
| Amicon ultra centrifugal filter unit | Sigma-Aldrich | UFC900324 | |
| Ammonium persulfate | Sigma-Aldrich | A3678 | |
| Ampicillin | Sigma-Aldrich | A9518 | |
| ATP | Sigma-Aldrich | A2383 | |
| ATP-13C10/15N5 | Sigma-Aldrich | 645702 | |
| BamHI restriction enzyme | NEB | R0136L | |
| Bottle top filter | VWR | 514-1019 | |
| Bromophenol Blue | Sigma-Aldrich | 1081220005 | |
| Cleavage guide | IDT | N/A | or equivalent |
| CTP | Sigma-Aldrich | C1506 | |
| CTP-13C10/15N5 | Sigma-Aldrich | 645699 | |
| D2O | Sigma-Aldrich | 151882 | |
| Dionex Ultimate 3000 UHPLC system | Thermo Scientific | N/A | |
| DL-Dithiotreitol | Sigma-Aldrich | 43815 | |
| DMSO | Sigma-Aldrich | D8418 | |
| DNAPac PA200 22×250 Semi-Prep column | Thermo Scientific | SP6734 | |
| DNAPac PA200 22×50 guard column | Thermo Scientific | SP6731 | |
| E.coli RNase H | NEB | M0297L | or made in-house uniprot ref. P0A7Y4 |
| EDTA | Sigma-Aldrich | E6758 | |
| Eppendorf centrifuge, rotor: A-4-44 | Eppendorf | 5804R | |
| Ethanol 95% | Fisher scientific | 11574139 | |
| Ethanol 95% denatured | VWR | 85829.29 | |
| Formamide | Sigma-Aldrich | 47671 | |
| GelRed | VWR | 41003 | |
| GeneRuler 1kbp Plus | Fisher Scientific | SM1333 | Optional |
| GMP | Sigma-Aldrich | G8377 | |
| GMP-13C10/15N5 | Sigma-Aldrich | 650684 | |
| GTP | Sigma-Aldrich | G8877 | |
| GTP-13C10/15N5 | Sigma-Aldrich | 645680 | |
| Hydrochloric Acid | Sigma-Aldrich | H1758 | |
| Inorganic pyrophosphatase | Sigma-Aldrich | I1643-100UN | or made in-house uniprot ref. P0A7A9 |
| Invitrogen UltraPure 10X TBE-buffer | Sigma-Aldrich | T4415 | |
| Julabo TW8 Water bath | VWR | 461-3117 | |
| kuroGEL Midi 13 Horizontal gel electrophoresis | VWR | 700-0056 | or comparable |
| LB broth (Lennox) | Sigma-Aldrich | L3022 | |
| LB broth with agar (Lennox) | Sigma-Aldrich | L2897 | |
| Low Range ssRNA Ladder | NEB | N0364S | Optional |
| LPG-3400RS Pump | Thermo Scientific | 5040.0036 | |
| Magnesium chloride hexahydrate | Sigma-Aldrich | 63068 | |
| microRNA Marker | NEB | N2102S | |
| Microwave oven | Samsung | MS23F301EAW | |
| Mini-PROTEAN electrophoresis equipment | Bio-Rad | 1658004 | |
| NucleoBond Xtra Maxi | Machinery-Nagel | 740414.10M | |
| pUC19 plasmid containing tandem insert | Genscript | N/A | or equivalent |
| RNaseZAP | Sigma-Aldrich | R2020 | |
| Shigemi tube 5mm | Sigma-Aldrich | Z529427 | |
| Single-use syringe, Luer lock tip | VWR | 613-2008 | |
| Sodium acetate | Sigma-Aldrich | S2889 | |
| Sodium chloride | Sigma-Aldrich | 730-1470 | |
| Sodium perchlorate | Sigma-Aldrich | 71853 | |
| Sodium phosphate dibasic | Sigma-Aldrich | S3264 | |
| Sodium phosphate monobasic | Sigma-Aldrich | S3139 | |
| Spermidine trihydrochloride | Sigma-Aldrich | 85578 | |
| SYBR Gold | ThermoFisher | S11494 | |
| Syringe filters | VWR | 514-0061 | |
| T7 RNA polymerase | Sigma-Aldrich | 10881767001 | or made in-house uniprot ref. P00573 |
| TCC-3000RS Column thermostat | Thermo Scientific | 5730 | |
| Tetramethylethylenediamine | Sigma-Aldrich | T9281 | |
| Tris Base | Fisher Scientific | 10103203 | |
| UMP | Sigma-Aldrich | U6375 | |
| UMP-13C9/15N2 | Sigma-Aldrich | 651370 | |
| Urea | Sigma-Aldrich | U5378 | |
| UTP | Sigma-Aldrich | U6625 | |
| UTP-13C10/15N5 | Sigma-Aldrich | 645672 | |
| VWD-3100 Detector | Thermo Scientific | 5074.0005 |
References
- Djebali, S., et al. Landscape of transcription in human cells. Nature. 489 (7414), 101-108 (2012).
- Doudna, J. A., Cech, T. R. The chemical repertoire of natural ribozymes. Nature. 418 (6894), 222-228 (2002).
- Sehgal, P. B., Westley, J., Lerea, K. M., DiSenso-Browne, S., Etlinger, J. D. Biomolecular condensates in cell biology and virology: phase-separated membraneless organelles (MLOs). Analytical Biochemistry. , 597 (2020).
- Herschlag, D., Allred, B. E., Gowrishankar, S. From static to dynamic: the need for structural ensembles and a predictive model of RNA folding and function. Current Opinion Structural Biology. 30, 125-133 (2015).
- Kimsey, I. J., Petzold, K., Sathyamoorthy, B., Stein, Z. W., Al-Hashimi, H. M. Visualizing transient Watson-Crick-like mispairs in DNA and RNA duplexes. Nature. 519 (7543), 315-320 (2015).
- Dethoff, E. A., Petzold, K., Chugh, J., Casiano-Negroni, A., Al-Hashimi, H. M. Visualizing transient low-populated structures of RNA. Nature. 491 (7426), 724-728 (2012).
- Baisden, J. T., Boyer, J. A., Zhao, B., Hammond, S. M., Zhang, Q. Visualizing a protonated RNA state that modulates microRNA-21 maturation. Nature Chemical Biology. 17 (1), 80-88 (2021).
- Marušič, M., Schlagnitweit, J., Petzold, K. RNA dynamics by NMR spectroscopy. Chembiochem. 20 (21), 2685-2710 (2019).
- Baronti, L., et al. Base-pair conformational switch modulates miR-34a targeting of Sirt1 mRNA. Nature. 583 (7814), 139-144 (2020).
- Steiner, E., Schlagnitweit, J., Lundström, P., Petzold, K. Capturing excited states in the fast-intermediate exchange limit in biological systems using 1H spectroscopy. Angewandte Chemie International Edition. 55 (51), 15869-15872 (2016).
- Moschen, T., et al. Ligand-detected relaxation dispersion NMR spectroscopy: dynamics of preQ1-RNA binding. Angewandte Chemie International Edition. 54 (2), 560-563 (2015).
- LeBlanc, R. M., Longhini, A. P., Tugarinov, V., Dayie, T. K. NMR probing of invisible excited states using selectively labeled RNAs. Journal of Biomolecular NMR. 71 (3), 165-172 (2018).
- Strebitzer, E., Nußbaumer, F., Kremser, J., Tollinger, M., Kreutz, C. Studying sparsely populated conformational states in RNA combining chemical synthesis and solution NMR spectroscopy. Methods. 1148, 39-47 (2018).
- Rangadurai, A., Shi, H., Al-Hashimi, H. M. Extending the sensitivity of CEST NMR spectroscopy to micro-to-millisecond dynamics in nucleic acids using high-power radio-frequency fields. Angewandte Chemie International Edition. 59 (28), 11262-11266 (2020).
- Hansen, D. F., Vallurupalli, P., Kay, L. E. Using relaxation dispersion NMR spectroscopy to determine structures of excited, invisible protein states. Journal of Biomolecular NMR. 41 (3), 113-120 (2008).
- Lundström, P., Akke, M. Off-resonance rotating-frame amide proton spin relaxation experiments measuring microsecond chemical exchange in proteins. Journal of Biomolecular NMR. 32 (2), 163-173 (2005).
- Lee, J., Dethoff, E. A., Al-Hashimi, H. M. Invisible RNA state dynamically couples distant motifs. Proceedings of the National Academy of Sciences of the United States of America. 111 (26), 9485-9490 (2014).
- Schnieders, R., Keyhani, S., Schwalbe, H., Fürtig, B. More than proton detection- new avenues for NMR spectroscopy of RNA. Chemistry. 26 (1), 102-113 (2020).
- Fürtig, B., Richter, C., Wöhnert, J., Schwalbe, H. NMR spectroscopy of RNA. Chembiochem. 4 (10), 936-962 (2003).
- Schlagnitweit, J., Steiner, E., Karlsson, H., Petzold, K. Efficient detection of structure and dynamics in unlabeled RNAs: The SELOPE approach. Chemistry. 24 (23), 6067-6070 (2018).
- Feyrer, H., Munteanu, R., Baronti, L., Petzold, K. One-pot production of RNA in high yield and purity through cleaving tandem transcripts. Molecules. 25 (5), 1142 (2020).
- Baronti, L., Karlsson, H., Marušič, M., Petzold, K. A guide to large-scale RNA sample preparation. Analytical and Bioanalytical Chemistry. 410 (14), 3239-3252 (2018).
- Brunelle, J. L., Green, R. In vitro transcription from plasmid or PCR-amplified DNA. Methods in Enzymology. 530, 101-114 (2013).
- Borkotoky, S., Murali, A. The highly efficient T7 RNA polymerase: A wonder macromolecule in biological realm. International Journal of Biological Macromolecules. 118, 49-56 (2018).
- Arnaud-Barbe, N., Cheynet-Sauvion, V., Oriol, G., Mandrand, B., Mallet, F. Transcription of RNA templates by T7 RNA polymerase. Nucleic Acids Research. 26 (15), 3550-3554 (1998).
- Guillerez, J., Lopez, P. J., Proux, F., Launay, H., Dreyfus, M. A mutation in T7 RNA polymerase that facilitates promoter clearance. Proceedings of the National Academy of Sciences of the United States of America. 102 (17), 5958-5963 (2005).
- Kuzmine, I., Gottlieb, P. A., Martin, C. T. Binding of the priming nucleotide in the initiation of transcription by T7 RNA polymerase. Journal of Biological Chemistry. 278 (5), 2819-2823 (2003).
- Gholamalipour, Y., Karunanayake Mudiyanselage, A., Martin, C. T. 3′ end additions by T7 RNA polymerase are RNA self-templated, distributive and diverse in character – RNA-Seq analyses. Nucleic Acids Research. 46 (18), 9253-9263 (2018).
- Inoue, H., Hayase, Y., Iwai, S., Ohtsuka, E. Sequence-dependent hydrolysis of RNA using modified oligonucleotide splints and RNase H. FEBS Letters. 215 (2), 327-330 (1987).
- Wang, X., Li, C., Gao, X., Wang, J., Liang, X. Preparation of small RNAs using rolling circle transcription and site-specific RNA disconnection. Molecular Therapy – Nucleic Acids. 4, 215 (2015).
- Karlsson, H., Baronti, L., Petzold, K. A robust and versatile method for production and purification of large-scale RNA samples for structural biology. RNA. 26 (8), 1023-1037 (2020).
- Hartmann, S. R., Hahn, E. L. Nuclear double resonance in the rotating frame. Physical Review. 128 (5), 2042-2053 (1962).
- Chiarparin, E., Pelupessy, I., Bodenhausen, G. Selective cross-polarization in solution state NMR. Molecular Physics. 95 (5), 759-767 (1998).
- Korzhnev, D. M., Orekhov, V. Y., Kay, L. E. Off-resonance R 1ρ NMR studies of exchange dynamics in proteins with low spin-lock fields: an application to a Fyn SH3 domain. Journal of the American Chemical Society. 127 (2), 713-721 (2005).
- Hansen, A. L., Nikolova, E. N., Casiano-Negroni, A., Al-Hashimi, H. M. Extending the range of microsecond-to-millisecond chemical exchange detected in labeled and unlabeled nucleic acids by selective carbon R 1ρ NMR spectroscopy. Journal of the American Chemical Society. 131 (11), 3818-3819 (2009).
- Duss, O., Maris, C., von Schroetter, C., Allain, F. H. -. T. A fast, efficient and sequence-independent method for flexible multiple segmental isotope labeling of RNA using ribozyme and RNase H cleavage. Nucleic Acids Research. 38 (20), 188 (2010).
- Krähenbühl, B., Lukavsky, P., Wider, G. Strategy for automated NMR resonance assignment of RNA: application to 48-nucleotide K10. Journal of Biomolecular NMR. 59 (4), 231-240 (2014).
- LeBlanc, R. M., Longhini, A. P., Le Grice, S. F. J., Johnson, B. A., Dayie, T. K. Combining asymmetric 13C-labeling and isotopic filter/edit NOESY: a novel strategy for rapid and logical RNA resonance assignment. Nucleic Acids Research. 45 (16), 146 (2017).
- Parisien, M., Major, F. The MC-Fold and MC-Sym pipeline infers RNA structure from sequence data. Nature. 452 (7183), 51-55 (2008).
- Fürtig, B., Richter, C., Bermel, W., Schwalbe, H. New NMR experiments for RNA nucleobase resonance assignment and chemical shift analysis of an RNA UUCG tetraloop. Journal of Biomolecular NMR. 28 (1), 69-79 (2004).
- Keyhani, S., Goldau, T., Blümler, A., Heckel, A., Schwalbe, H. Chemo-enzymatic synthesis of position-specifically modified RNA for biophysical studies including light control and NMR spectroscopy. Angewandte Chemie International Edition. 57 (37), 12017-12021 (2018).
- Marchanka, A., Kreutz, C., Carlomagno, T. Isotope labeling for studying RNA by solid-state NMR spectroscopy. Journal of Biomolecular NMR. 71, 151-164 (2018).
- Becette, O., Olenginski, L. T., Dayie, T. K. Solid-phase chemical synthesis of stable isotope-labeled RNA to aid structure and dynamics studies by NMR spectroscopy. Molecules. 24 (19), 3476 (2019).
- Zhang, X., Li, M., Liu, Y. Optimization and characterization of position-selective labelling of RNA (PLOR) for diverse RNA and DNA sequences. RNA Biology. 17 (7), 1009-1017 (2020).
- Roh, J. H., et al. Effects of preferential counterion interactions on the specificity of RNA folding. The Journal of Physical Chemistry Letters. 9 (19), 5726-5732 (2018).
- Juen, M. A., et al. Excited states of nucleic acids probed by proton relaxation dispersion NMR spectroscopy. Angewandte Chemie German Edition. 55 (39), 12008-12012 (2016).

