Reconstitutie van membraangebonden minimale actinecorticosterces op ondersteunde lipidebilagen
Summary
Dit protocol beschrijft de vorming van ondersteunde lipide bilayers en de toevoeging van cytoskeletale filamenten en motoreiwitten om de dynamiek van gereconstitueerde, membraangebonden cytoskeletale netwerken te bestuderen met behulp van fluorescentiemicroscopie.
Abstract
Het oppervlak van een levende cel biedt een veelzijdig actief platform voor tal van cellulaire processen, die voortkomen uit het samenspel van het plasmamembraan met de onderliggende actine cortex. In de afgelopen decennia hebben gereconstitueerde, minimale systemen op basis van ondersteunde lipide bilayers in combinatie met actinefilamentnetwerken bewezen zeer instrumenteel te zijn bij het ontrafelen van basismechanismen en gevolgen van membraangebonden actinenetwerken, evenals bij het bestuderen van de functies van individuele membraan-geassocieerde eiwitten. Hier beschrijven we hoe dergelijke actieve composietsystemen in vitro kunnen worden gereconstitueerd die bestaan uit vloeistofondersteunde lipide bilayers gekoppeld via membraan-geassocieerde actine-bindende eiwitten aan dynamische actinefilamenten en myosinemotoren die gemakkelijk kunnen worden waargenomen via totale interne reflectie fluorescentiemicroscopie. Een open-kamer ontwerp maakt het mogelijk om het systeem stap voor stap samen te stellen en systematisch vele parameters te regelen, zoals linker eiwitconcentratie, actineconcentratie, actinefilamentlengte, actine / myosineverhouding en ATP-niveaus. Ten slotte bespreken we hoe we de kwaliteit van het systeem kunnen controleren, hoe we veelvoorkomende problemen kunnen detecteren en oplossen en enkele beperkingen van dit systeem in vergelijking met het oppervlak van de levende cel.
Introduction
Het plasmamembraan van een levende dierlijke cel interageert voortdurend met het aangrenzende actinecytoskelet en samen vormen ze een actief composietmateriaal dat een veelheid aan cellulaire functies vervult 1,2. Om processen op deze lipidemembraan-actine-interface te bestuderen, is de reconstitutie van cytoskeletale netwerken bovenop ondersteunde lipide bilayers (SLBs) zeer nuttig gebleken. Deze minimale systeembenadering maakt de nauwkeurige controle van cytoskeletnetwerkcomponenten en lipidensamenstelling mogelijk. Vergeleken met de vrijstaande lipidemembranen van gigantische unilamellaire blaasjes, maakt de vlakke geometrie van SLB’s efficiënt gebruik mogelijk van state-of-the-art microscopietechnieken zoals superresolutie 3,4, totale interne reflectiefluorescentie (TIRF)5,6,7 of interferometrische verstrooiing8 het bestuderen van de ruimtelijke organisatie en dynamiek van cytoskeletale netwerken. TIRF biedt het hoogste contrast voor fluorescerend gelabelde componenten, omdat het signaal van ongebonden gelabelde moleculen in de oplossing die bijdragen aan het achtergrondsignaal minimaal is.
Hier beschrijven we een basisprotocol voor de vorming van actomyosinenetwerken die zijn gekoppeld aan ondersteunde lipidebilagen, die op grote schaal in het veld worden gebruikt om de fysica van actieve, quasi-2D-netwerken 9,10,11 en hun effect op membraanorganisatie 3,5,12,13,14,15,16 te bestuderen (figuur 11 ). Deze aanpak is niet beperkt tot op actine gebaseerde netwerken, maar kan ook gemakkelijk worden aangepast om microtubuli, intermediaire filamenten of samengestelde netwerken van gemengde aard te verkennen en om een verscheidenheid aan interacties tussen lipidemembraaneiwitten en cytoskeletale componenten te bestuderen met behulp van oppervlaktegevoelige microscopiemethoden.
Om dit protocol gefocust te houden, hebben we een gedetailleerde beschrijving van de zuivering en etikettering van actine- en myosine-eiwitten uitgesloten of details over hoe de contractiliteit en organisatie van actomyosinenetwerken kunnen worden afgestemd en gecontroleerd. Men moet verwijzen naar andere protocollen die naast deze zijn gepubliceerd in de JoVE Methods Collection, In Vitro Reconstitution of Cytoskeleton Networks for Biomaterials, Biophysics and Active Matter Research17.
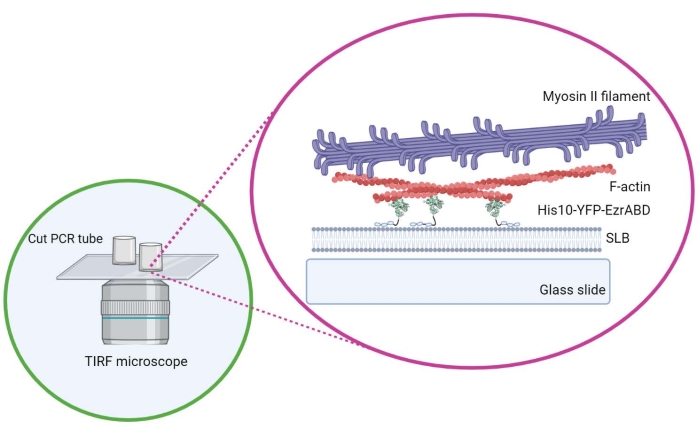
Figuur 1: Schema van het in vitro actine-membraan actieve composietsysteem. Gemaakt met Biorender. Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
Dit protocol biedt een veelzijdig platform en een startpunt om experimenten te ontwerpen om de membraan-cortex interface van cellen te bestuderen. Kritieke stappen zijn de voorbereiding van schone glazen dia’s, met behulp van verse lipiden voor efficiënte SUV-vorming (beide van invloed op de kwaliteit van SLB’s), en het gebruik van vers gerecyclede myosine II-eiwitten voor dynamische actinefilamentreorganisatie. Bij beeldvormingsdynamiek over een lange tijd is het erg belangrijk om een zuurstofvangersysteem op te nemen (bijv. protocatechuïnezuur en protocatechuaat 3 4-dioxygenase 5,31).
Het ontwerp met open kamer maakt de sequentiële toevoeging van componenten aan een bestaand systeem mogelijk zonder lipidenstromen te induceren. Dit kan een belangrijk voordeel zijn ten opzichte van veelgebruikte benaderingen met gesloten kamers of werken met ingekapselde eiwitten binnen liposomen36. Tegengestelde effecten zoals eiwit-geïnduceerde membraanvervorming kunnen niet worden bestudeerd met glas-geadsorbeerde lipide bilayers.
De lipide bilayers kunnen worden gevormd met een breed scala aan lipidesamenstellingen. Het begint met adsorptie van de lipideblaasjes aan het hydrofiele glasoppervlak, gevolgd door spontane blaasjesruptuur als gevolg van oppervlakte-blaasje en directe vesikel-vesikelinteracties of de geadsorbeerde blaasjes die een kritische dekking bereiken waarna een klein deel van de blaasjes scheurt, actieve randen vormt, wat uiteindelijk leidt tot de bilayer-vorming32 . Naast glas kunnen verschillende substraten worden gebruikt om ondersteunde lipide-bilayers te vormen, zoals Mica (bijvoorbeeld voor atoomkrachtmicroscopie), zachte substraten (bijv. Poly-di-methyl-siloxaan), polymeerkussens33,34,35, verspreid tussen gaten van elektronenmicroscopierasters14. Droplet interface bilayers zijn een andere interessante methode om stabiele, vrijstaande lipide bilayers te creëren36. Het opnemen van acto-myosinenetwerken in blaasjes of emulsies is een zeer krachtige methode om dit minimale systeem te bestuderen in een celachtige geometrie37,38, en die elders in detail wordt beschreven39.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dit werk werd ondersteund door het AXA-onderzoeksfonds en het Warwick-Wellcome Quantitative Biomedicine Programme (Wellcome ISSF, RMRCB0058) voor DVK, NCBS-TIFR voor AB en ST, en de Wellcome-DBT Margdarshi fellowship (IA/M/15/1/502018) voor SM. DVK wil ook de Biophysical Society bedanken voor het mogelijk maken van het virtuele netwerkevenement “Challenges in understanding multi-component cytoskeletal networks from the molecular to the meso-scale”, die heeft bijgedragen aan de totstandkoming van deze protocolcollectie.
Materials
| 1,2 dipalmitoyl-sn-glycero-3-phosphoethanolamine-N- (lissamine rhodamine B sulfonyl) | Avanti Polar Lipids | 810158 | 16:0 RhoPE |
| 1,2-dioleoyl-sn-glycero-3- [(N-(5-amino-1 carboxypentyl) iminodiacetic acid) succinyl] (nickel salt) | Avanti Polar Lipids | 790404 | DGS-NTA-Ni2+ |
| 1,2-dioleoyl-sn-glycero-3-phosphocholine | Avanti Polar Lipids | 850375 | DOPC |
| 1,2-dipalmitoyl-sn-glycero-3-phosphocholine | Avanti Polar Lipids | 850355 | DPPC |
| Amber glass vials | ThermoFisher | B7990-2A | |
| ATP disodium salt | Sigma Aldrich | A26209 | |
| Attofluor cell chamber | ThermoFisher | A7816 | |
| Bath sonicator | GT Sonic | 1860QTS | |
| beta-casein | Sigma Aldrich | C6905 | |
| CaCl2 | ThermoFisher | 12135 | |
| chloroform | Sigma Aldrich | 650471 | alternatively from Electron Microscopy Sciences, 50980296 |
| Cover slips, #1, 25 mm diameter, Gold Seal | Harvard Apparatus | 64-0705B | |
| Cover slips, #1, 40×22 mm, Gold Seal | ThermoFisher | 48404-031 | |
| EDTA | ThermoFisher | G12635 | |
| EGTA | Himedia | MB130 | |
| Gas tight glass syringes, with removebla needle, blunt, volumes 10 µL, 100 µL, 500 µL | Hammilton | 1700 series | |
| Hellmanex III | Hellma Analytics | Z805939 | cleaning solution |
| HEPES | Himedia | RM380 | |
| KaH2PO4 | ThermoFisher | G13405 | |
| KCl | ThermoFisher | G13305 | |
| KOH | ThermoFisher | G26708 | |
| Lipid extruder | Avanti Polar Lipids | 61000-1EA | |
| MgCl2 | ThermoFisher | G15535 | |
| Microtip sonicator | Sonics | VC750 | 3 mm Tip diameter |
| Na2CO3 | ThermoFisher | G15955 | |
| NaCl | Himedia | GRM853 | |
| NaH2PO4 | ThermoFisher | G15825 | |
| NaOH | ThermoFisher | G27815 | |
| Nikon Ti Eclipse TIRF microscope | Nikon | With a TIRF unit connected through a polarization-conserving optical fibre to an Agilent monolithic laser combiner MLC400 with multiple laser lines with a 100X, 1.45 NA Nikon Oil Objective with two 512 x 512-pixel EMCCD cameras (Photometrics Evolve 512) with a 100X, 1.45 NA Nikon Oil Objective with two 512 x 512-pixel EMCCD cameras (Photometrics Evolve 512) | |
| NOA88 | Norland Products | 8801 | |
| PTFE Coated Tweezer Style #2A | Structure Probe | 0S2AT-XD | |
| Refrigerated microcentrifuge | Eppendorf | 5424R | |
| Sucrose | ThermoFisher | G15925 | |
| UV-illuminator | Novascan | PSD PRO-UV | needs vacuum and O2 supply |
References
- Köster, D. V., Mayor, S. Cortical actin and the plasma membrane: Inextricably intertwined. Current Opinion in Cell Biology. 38, 81-89 (2016).
- Rao, M., Mayor, S. Active organization of membrane constituents in living cells. Current Opinion in Cell Biology. 29, 126-132 (2014).
- Honigmann, A., et al. A lipid bound actin meshwork organizes liquid phase separation in model membranes. eLife. 3, 01671 (2014).
- Das, A., et al. Stratification relieves constraints from steric hindrance in the generation of compact actomyosin asters at the membrane cortex. Science Advances. 6 (11), (2020).
- Köster, D. V., et al. Actomyosin dynamics drive local membrane component organization in an in vitro active composite layer. Proceedings of the National Academy of Sciences. 113 (12), 1645-1654 (2016).
- Vogel, S. K., Heinemann, F., Chwastek, G., Schwille, P. The design of MACs (minimal actin cortices). Cytoskeleton. 70 (11), 706-717 (2013).
- Murrell, M., Thoresen, T., Gardel, M. Reconstitution of contractile actomyosin arrays. Methods in Enzymology. 540, 265-282 (2014).
- Mosby, L. S., et al. Myosin II filament dynamics in actin networks revealed with interferometric scattering microscopy. Biophysical Journal. 118 (8), 1946-1957 (2020).
- Seara, D. S., et al. Entropy production rate is maximized in non-contractile actomyosin. Nature Communications. 9 (1), 4948 (2018).
- Linsmeier, I., et al. Disordered actomyosin networks are sufficient to produce cooperative and telescopic contractility. Nature Communications. 7, 12615 (2016).
- Vogel, S. K., Petrasek, Z., Heinemann, F., Schwille, P. Myosin motors fragment and compact membrane-bound actin filaments. eLife. 2, 00116 (2013).
- Ditlev, J. A., et al. A composition-dependent molecular clutch between T cell signaling condensates and actin. eLife. 8, 42695 (2019).
- Banjade, S., Rosen, M. K. Phase transitions of multivalent proteins can promote clustering of membrane receptors. eLife. 3, 04123 (2014).
- Heinemann, F., Vogel, S. K., Schwille, P. Lateral membrane diffusion modulated by a minimal actin cortex. Biophysical Journal. 104 (7), 1465-1475 (2013).
- Vogel, S. K., Greiss, F., Khmelinskaia, A., Schwille, P. Control of lipid domain organization by a biomimetic contractile actomyosin cortex. eLife. 6, 24350 (2017).
- Block, S. Brownian motion at lipid membranes: A comparison of hydrodynamic models describing and experiments quantifying diffusion within lipid bilayers. Biomolecules. 8 (2), 30 (2018).
- JoVE, JoVE Methods Collection. In vitro reconstitution of cytoskeleton networks for biomaterials, biophysics and active matter research. Journal of Visualized Experiments. , (2022).
- Pardee, J. D., Spudich, J. A. Purification of muscle actin. Methods in Enzymology. 85, 164-181 (1982).
- Spudich, J. A., Watt, S. The regulation of rabbit skeletal muscle contraction. I. Biochemical studies of the interaction of the tropomyosin-troponin complex with actin and the proteolytic fragments of myosin. Journal of Biological Chemistry. 246 (15), 4866-4871 (1971).
- Pollard, T. D. Myosin purification and characterization. Methods in Cell Biology. 24, 331-371 (1982).
- JoVE Science Education Database. Separating protein with SDS-PAGE. Journal of Visualized Experiments. , (2022).
- Bieling, P., et al. WH2 and proline-rich domains of WASP-family proteins collaborate to accelerate actin filament elongation. The EMBO Journal. 37 (1), 102-121 (2018).
- Shrivastava, R., Köster, D., Kalme, S., Mayor, S., Neerathilingam, M. Tailor-made ezrin actin binding domain to probe its interaction with actin in-vitro. PLoS One. 10 (4), 0123428 (2015).
- Nye, J. A., Groves, J. T. Kinetic control of histidine-tagged protein surface density on supported lipid bilayers. Langmuir. 24 (8), 4145-4149 (2008).
- Honigmann, A., et al. Scanning STED-FCS reveals spatiotemporal heterogeneity of lipid interaction in the plasma membrane of living cells. Nature Communications. 5, 5412 (2014).
- Selden, N. S., et al. Chemically programmed cell adhesion with membrane-anchored oligonucleotides. Journal of the American Chemical Society. 134 (2), 765-768 (2012).
- Seu, K. J., et al. Effect of surface treatment on diffusion and domain formation in supported lipid bilayers. Biophysical Journal. 92 (7), 2445-2450 (2007).
- Kang, M., Day, C. A., Kenworthy, A. K., DiBenedetto, E. Simplified equation to extract diffusion coefficients from confocal FRAP data. Traffic. 13 (12), 1589-1600 (2012).
- Kang, M., Day, C. A., Kenworthy, A. K. A novel computational framework for D(t) from Fluorescence Recovery after Photobleaching data reveals various anomalous diffusion types in live cell membranes. Traffic. 20 (11), 867-880 (2019).
- Lorén, N., et al. Fluorescence recovery after photobleaching in material and life sciences: Putting theory into practice. Quarterly Reviews of Biophysics. 48 (3), 323-387 (2015).
- Alvarado, J., Sheinman, M., Sharma, A., MacKintosh, F. C., Koenderink, G. H. Molecular motors robustly drive active gels to a critically connected state. Nature Physics. 9 (7), 1-7 (2013).
- Andrecka, J., Spillane, K. M., Ortega-Arroyo, J., Kukura, P. Direct observation and control of Supported lipid bilayer formation with interferometric scattering microscopy. ACS Nano. 7 (12), 10662-10670 (2013).
- Lin, W. -. C., et al. Supported membrane formation, characterization, functionalization, and patterning for application in biological science and technology. Current Protocols in Chemical Biology. 2 (4), 235-269 (2010).
- Richter, R. P., Bérat, R., Brisson, A. R. Formation of solid-supported lipid bilayers: An integrated view. Langmuir. 22 (8), 3497-3505 (2006).
- Sapuri-Butti, A. R., Butti, R. C., Parikh, A. N. Characterization of supported membranes on topographically patterned polymeric elastomers and their applications to microcontact printing. Langmuir. 23 (25), 12645-12654 (2007).
- Leptihn, S., et al. Constructing droplet interface bilayers from the contact of aqueous droplets in oil. Nature Protocols. 8 (6), 1048-1057 (2013).
- Bashirzadeh, Y., Moghimianavval, H., Liu, A. P. Encapsulated actomyosin patterns drive cell-like membrane shape changes. iScience. 25 (5), 104236 (2022).
- Bashirzadeh, Y., Wubshet, N., Litschel, T., Schwille, P., Liu, A. P. Rapid encapsulation of reconstituted cytoskeleton inside giant unilamellar vesicles. Journal of Visualized Experiments. (177), e63332 (2021).
- Murrell, M., Chen, S., Sun, Z. G. In vitro reconstitution of actin cytoskeleton inside giant unilamellar vesicles. Journal of Visualized Experiments. , (2022).

