लंबाई के पैमाने पर क्रोमोसोम रचना कैप्चर करना
Summary
हाई-सी 3.0 एक बेहतर हाई-सी प्रोटोकॉल है जो सिग्नल-टू-शोर अनुपात और क्रोमैटिन इंटरैक्शन डिटेक्शन के रिज़ॉल्यूशन को बढ़ाने के लिए डीपीएनआई और डीडीईआई प्रतिबंध एंजाइमों के कॉकटेल के साथ फॉर्मलाडेहाइड और डिसुसिनिमिडिल ग्लूटारेट क्रॉसलिंकर को जोड़ता है।
Abstract
क्रोमोसोम अनुरूपता कैप्चर (3 सी) का उपयोग त्रि-आयामी क्रोमैटिन इंटरैक्शन का पता लगाने के लिए किया जाता है। आमतौर पर, फॉर्मलाडेहाइड (एफए) के साथ रासायनिक क्रॉसलिंकिंग का उपयोग क्रोमैटिन इंटरैक्शन को ठीक करने के लिए किया जाता है। फिर, एक प्रतिबंध एंजाइम के साथ क्रोमैटिन पाचन और बाद में टुकड़े के सिरों का पुन: बंधाव तीन आयामी (3 डी) निकटता को अद्वितीय बंधाव उत्पादों में परिवर्तित करता है। अंत में, क्रॉसलिंक, प्रोटीन हटाने और डीएनए अलगाव के उलट के बाद, डीएनए को कतरनी किया जाता है और उच्च-थ्रूपुट अनुक्रमण के लिए तैयार किया जाता है। लोकी के जोड़े की निकटता बंधाव की आवृत्ति एक सेल आबादी में त्रि-आयामी अंतरिक्ष में उनके सह-स्थानीयकरण की आवृत्ति का एक उपाय है।
एक अनुक्रमित हाई-सी लाइब्रेरी लोकी के सभी जोड़े के बीच बातचीत आवृत्तियों पर जीनोम-व्यापक जानकारी प्रदान करती है। हाई-सी का संकल्प और परिशुद्धता कुशल क्रॉसलिंकिंग पर निर्भर करती है जो क्रोमैटिन संपर्कों और क्रोमैटिन के लगातार और समान विखंडन को बनाए रखती है। यह पेपर एक बेहतर सीटू हाई-सी प्रोटोकॉल, हाई-सी 3.0 का वर्णन करता है, जो दो क्रॉसलिंकर (फॉर्मलाडेहाइड [एफए] और डिसुसिनिमिडिल ग्लूटारेट [डीएसजी]) के संयोजन से क्रॉसलिंकिंग की दक्षता को बढ़ाता है, इसके बाद दो प्रतिबंध एंजाइमों (डीपीएनआई और डीडीईआई) का उपयोग करके बेहतर पाचन होता है। हाई-सी 3.0 छोटे पैमानों जैसे लूप और टोपोलॉजिकल रूप से संबद्ध डोमेन (टीएडी) पर जीनोम फोल्डिंग सुविधाओं की सटीक मात्रा का ठहराव करने के लिए एक एकल प्रोटोकॉल है, साथ ही साथ डिब्बों जैसे बड़े नाभिक-व्यापक पैमाने पर विशेषताएं भी हैं।
Introduction
क्रोमोसोम अनुरूपता कैप्चर का उपयोग 2002 1 से किया गयाहै। मौलिक रूप से, प्रत्येक रचना कैप्चर संस्करण 3 डी क्रोमैटिन संगठन को संरक्षित करने के लिए डीएनए-प्रोटीन और प्रोटीन-प्रोटीन इंटरैक्शन के निर्धारण पर निर्भर करता है। इसके बाद डीएनए विखंडन होता है, आमतौर पर प्रतिबंध पाचन द्वारा, और अंत में, पास के डीएनए का पुनर्ग्रहण स्थानिक रूप से समीपस्थ लोकी को अद्वितीय सहसंयोजक डीएनए अनुक्रमों में परिवर्तित करने के लिए समाप्त होता है। प्रारंभिक 3 सी प्रोटोकॉल ने विशिष्ट, “वन-टू-वन” इंटरैक्शन का नमूना लेने के लिए पीसीआर का उपयोग किया। बाद के 4 सी परीक्षणों ने “वन-टू-ऑल” इंटरैक्शन2 का पता लगाने की अनुमति दी, जबकि 5 सी ने “कई-से-कई” इंटरैक्शन3 का पता लगाया। अगली पीढ़ी, उच्च-थ्रूपुट अनुक्रमण (एनजीएस) को लागू करने के बाद क्रोमोसोम रचना कैप्चर पूर्ण रूप से फलीभूत हुआ, जिसने जीनोम-वाइड हाई-सी4 और तुलनीय तकनीकों जैसे 3 सी-सेक5, टीसीसी6 और माइक्रो-सी 7,8 का उपयोग करके “ऑल-टू-ऑल” जीनोमिक इंटरैक्शन का पता लगाने की अनुमति दी (डेंकर और डी लाट9 द्वारा समीक्षा भी देखें)।
हाई-सी में, बायोटिनाइलेटेड न्यूक्लियोटाइड का उपयोग पाचन के बाद और बंधाव से पहले 5 ‘ ओवरहैंग को चिह्नित करने के लिए किया जाता है (चित्रा 1)। यह स्ट्रेप्टाविडिन-लेपित मोतियों का उपयोग करके ठीक से पचने वाले और पुनर्निर्मित टुकड़ों के चयन की अनुमति देता है, इसे जीसीसी10 से अलग करता है। हाई-सी प्रोटोकॉल के लिए एक महत्वपूर्ण अद्यतन राव एट अल .11 द्वारा लागू किया गया था, जिन्होंने नकली बंधाव उत्पादों को कम करने के लिए बरकरार नाभिक (यानी, सीटू में) में पाचन और पुनरावृत्ति का प्रदर्शन किया था। इसके अलावा, एमबीओआई (या डीपीएनआई) पाचन के साथ हिंद III पाचन को प्रतिस्थापित करने से टुकड़े का आकार कम हो गया और हाई-सी की संकल्प क्षमता में वृद्धि हुई। इस वृद्धि ने अपेक्षाकृत छोटे पैमाने पर संरचनाओं का पता लगाने और संपर्क के बिंदुओं के अधिक सटीक जीनोमिक स्थानीयकरण की अनुमति दी, जैसे कि छोटे सीआईएस-तत्वों के बीच डीएनए लूप, उदाहरण के लिए, लूप एक्सट्रूज़न11,12 द्वारा उत्पन्न सीटीसीएफ-बाध्य साइटों के बीच लूप। हालांकि, यह क्षमता एक कीमत पर आती है। सबसे पहले, रिज़ॉल्यूशन में दो गुना वृद्धि के लिए अनुक्रमण में चार गुना (22) वृद्धिकी आवश्यकता होती है। दूसरा, छोटे टुकड़े के आकार से पचे हुए और पुनर्निर्मित टुकड़ों के लिए बिना पचे हुए पड़ोसी टुकड़ों को गलत समझने की संभावना बढ़जाती है। जैसा कि उल्लेख किया गया है, हाई-सी में, पचा हुआ और पुनर्निर्मित टुकड़े बंधाव जंक्शन पर बायोटिन की उपस्थिति से बिना पचे हुए टुकड़ों से भिन्न होते हैं। हालांकि, यह सुनिश्चित करने के लिए कि केवल बंधाव जंक्शनों को14,15 से नीचे खींचा जाता है, अनलिगेटेड सिरों से उचित बायोटिन हटाने की आवश्यकता होती है।
एनजीएस की घटती लागत के साथ, क्रोमोसोम फोल्डिंग का अधिक विस्तार से अध्ययन करना संभव हो जाता है। डीएनए टुकड़ों के आकार को कम करने के लिए, और इस प्रकार रिज़ॉल्यूशन बढ़ाने के लिए, हाई-सी प्रोटोकॉल को प्रतिबंध एंजाइमों 16 को अधिक बार काटने या प्रतिबंध एंजाइम17,18,19 के संयोजन का उपयोग करने के लिए अनुकूलित किया जा सकता है। वैकल्पिक रूप से, माइक्रो-सी में एमनेस 7,8 और डीनेस हाई-सी20 में डीनेस को इष्टतम पाचन प्राप्त करने के लिए टाइटरेट किया जा सकता है।
3 सी विधियों के मूल सिद्धांतों के हालिया व्यवस्थित मूल्यांकन से पता चला है कि हर लंबाई के पैमाने पर क्रोमोसोम फोल्डिंग सुविधाओं का पता लगाने में 1% एफए के साथ अनुक्रमिक क्रॉसलिंकिंग के साथ बहुत सुधार हुआ, जिसके बाद 3 एमएम डीएसजी17 था। इसके अलावा, हिंद III पाचन के साथ हाई-सी बड़े पैमाने पर फोल्डिंग सुविधाओं का पता लगाने के लिए सबसे अच्छा विकल्प था, जैसे कि डिब्बे, और माइक्रो-सी डीएनए लूप जैसे छोटे पैमाने पर फोल्डिंग सुविधाओं का पता लगाने में बेहतर था। इन परिणामों ने एक एकल, उच्च-रिज़ॉल्यूशन “हाई-सी 3.0” रणनीति के विकास को जन्म दिया, जो एफए और डीएसजी क्रॉसलिंकर के संयोजन का उपयोग करता है, जिसके बाद डीपीएनआई और डीडीईआई एंडोन्यूक्लिज़21 के साथ डबल पाचन होता है। हाई-सी 3.0 सामान्य उपयोग के लिए एक प्रभावी रणनीति प्रदान करता है क्योंकि यह सभी लंबाई तराजू17 में फोल्डिंग सुविधाओं का सटीक रूप से पता लगाता है। हाई-सी 3.0 प्रोटोकॉल का प्रयोगात्मक भाग यहां विस्तृत है और अनुक्रमण के बाद अपेक्षित विशिष्ट परिणाम दिखाए जा सकते हैं।
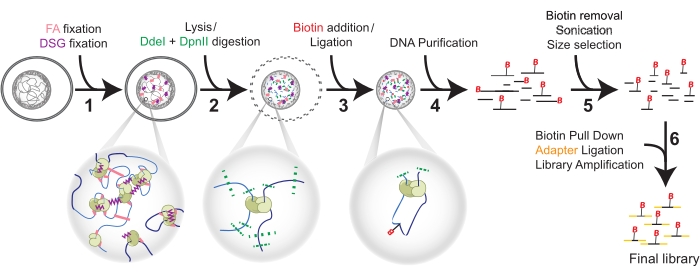
चित्रा 1: छह चरणों में हाई-सी प्रक्रिया। कोशिकाओं को पहले एफए के साथ तय किया जाता है, और फिर डीएसजी (1)। फिर, लाइसिस डीडीईआई और डीपीएनआई (2) के साथ दोहरे पाचन से पहले होता है। बायोटिन को ओवरहैंग फिल-इन द्वारा जोड़ा जाता है और समीपस्थ कुंद सिरों को डीएनए शुद्धिकरण (4) से पहले (3) किया जाता है। बायोटिन को सोनिकेशन और आकार चयन से पहले अनलिगेटेड सिरों से हटा दिया जाता है (5). अंत में, बायोटिन का पुल-डाउन पीसीआर द्वारा एडाप्टर लिगेशन और लाइब्रेरी प्रवर्धन की अनुमति देता है (6). संक्षेप: एफए = फॉर्मलाडेहाइड; डीएसजी = डिसुकिनिमिडिल ग्लूटारेट; बी = बायोटिन। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें।
Protocol
Representative Results
Discussion
सेल हैंडलिंग के लिए महत्वपूर्ण कदम
यद्यपि इनपुट कोशिकाओं की कम संख्या का उपयोग करना संभव है, इस प्रोटोकॉल को गहन अनुक्रमण के बाद उचित जटिलता सुनिश्चित करने के लिए ~ 5 × 106 कोशिकाओं प्रति अनुक्रमण लेन (~ 400 एम रीड) के लिए अनुकूलित किया गया है। निर्धारण से पहले कोशिकाओं को सबसे अच्छी तरह से गिना जाता है। अल्ट्राडीप पुस्तकालयों की पीढ़ी के लिए, हम आम तौर पर लेन (और कोशिकाओं) की संख्या को गुणा करते हैं जब तक कि वांछित पठन-गहराई तक नहीं पहुंच जाता है। इष्टतम निर्धारण के लिए, सीरम युक्त माध्यम को एफए निर्धारण से पहले पीबीएस के साथ बदल दिया जाना चाहिए, और फिक्सेटिव समाधानों को तुरंत और एकाग्रता ग्रेडिएंट15,22 के बिना जोड़ा जाना चाहिए। सेल कटाई के लिए, ट्रिप्सिनाइजेशन पर स्क्रैपिंग को प्राथमिकता दी जाती है, क्योंकि ट्रिप्सिनाइजेशन के बाद चापलूसी से गोलाकार आकार में संक्रमण परमाणु रचना को प्रभावित कर सकता है। डीएसजी को जोड़ने के बाद, ढीले और झुरमुट सेल छर्रों को आसानी से खो दिया जाता है। इस स्तर पर कोशिकाओं को संभालते समय सावधान रहें और झुरमुट को कम करने के लिए 0.05% बीएसए जोड़ें।
विधि में संशोधन
यह प्रोटोकॉल मानव कोशिकाओं17 का उपयोग करके विकसित किया गया था। फिर भी, क्रोमोसोम रचना कैप्चर के साथ अनुभव के आधार पर, यह प्रोटोकॉल अधिकांश यूकेरियोटिक कोशिकाओं के लिए काम करना चाहिए। काफी कम इनपुट (~ 1 × 106 कोशिकाओं) के लिए, हम लाइसिस और अनुरूपता कैप्चर प्रक्रियाओं [चरण 2.1-2.4] के लिए आधे वॉल्यूम का उपयोग करने की सलाह देते हैं। यह डीएनए अलगाव [चरण 2.5] को 1.7 एमएल ट्यूबों के साथ टेबलटॉप सेंट्रीफ्यूज में करने की अनुमति देगा, जो कम डीएनए सांद्रता के लिए पेलेटिंग में सुधार कर सकता है। डीएनए की मात्रा (चरण 2.6.6) इंगित करेगी कि कैसे आगे बढ़ना है। पृथक डीएनए (1-5 μg) की कम मात्रा के लिए, हम आकार चयन (चरण 3.3) को छोड़ने का सुझाव देते हैं और सीएफयू के साथ मात्रा को 130 μL से ~ 45 μL तक कम करने के बाद बायोटिन हटाने के साथ आगे बढ़ते हैं।
इस प्रोटोकॉल को विशेष रूप से एफए और डीएसजी के साथ क्रॉसलिंकिंग और डीपीएनआई और डीडीईआई के साथ पाचन के बाद उच्च गुणवत्ता वाले डेटा को सुनिश्चित करने के लिए विकसित किया गया था। हालांकि, वैकल्पिक क्रॉसलिंकिंग रणनीतियाँ जैसे कि एफए के बाद ईजीएस (एथिलीन ग्लाइकोल बिस (सक्सिनिमिडिल सक्सिनेट)), जिसका उपयोग CHIP-seq23 और CHIA-PET24 में भी किया जाता है, समान रूपसे अच्छी तरह से काम कर सकता है। इसी तरह, विभिन्न एंजाइम संयोजन, जैसे कि DpnII और HinfI18 या MBOI , MSEI, और NLAIII19 का उपयोग पाचन के लिए किया जा सकता है। एंजाइम संयोजनों को अपनाते समय, बायोटिनिलेटेड न्यूक्लियोटाइड का उपयोग करना सुनिश्चित करें जो विशिष्ट 5 ‘ओवरहैंग्स को भर सकते हैं और प्रत्येक कॉकटेल के लिए सबसे इष्टतम बफर का उपयोग कर सकते हैं। DpnII अपने स्वयं के बफर के साथ आता है और एंजाइम निर्माता डीडीईआई पाचन के लिए एक विशिष्ट बफर की सिफारिश करता है। फिर भी, इस प्रोटोकॉल में DpnII और DDEI के साथ डबल-पाचन के लिए, प्रतिबंध बफर की सिफारिश की जाती है क्योंकि यह दोनों एंजाइमों के लिए 100% गतिविधि पर रेट किया गया है।
समस्या निवारण रचना कैप्चर
क्रोमोसोम रचना कैप्चर में तीन प्रमुख चरण: जेल पर परिणामों की कल्पना करने से पहले क्रॉसलिंकिंग, पाचन और रिलिगेशन सभी किए गए हैं। इन तीन चरणों में से प्रत्येक की गुणवत्ता निर्धारित करने और यह समझने के लिए कि समस्याएं कहां उत्पन्न हो सकती हैं, पाचन से पहले (सीआई) और बाद में (डीसी) एलिकोट लिए जाते हैं और लिगेटेड हाई-सी नमूने (चित्रा 2) के साथ जेल पर लोड किए जाते हैं। इस जेल का उपयोग हाई-सी नमूने की गुणवत्ता निर्धारित करने के लिए किया जाता है और क्या यह प्रोटोकॉल जारी रखने के लायक होगा। सीआई और डीसी के बिना, संभावित उप-मानक चरण (ओं) को इंगित करना मुश्किल है। यह ध्यान देने योग्य है कि उप-बंधाव लिगेशन में समस्या, फिल-इन, या क्रॉसलिंकिंग के साथ समस्या के कारण हो सकता है। क्रॉसलिंकिंग की समस्या का निवारण करने के लिए, सुनिश्चित करें कि प्रति पुस्तकालय 107 कोशिकाओं × 1 से अधिक का उपयोग न करें और ताजा क्रॉसलिंकिंग अभिकर्मकों और स्वच्छ कोशिकाओं (यानी, पीबीएस से धोया गया) के साथ शुरू करें। बंधाव के लिए, सुनिश्चित करें कि कोशिकाओं और बंधाव मिश्रण को बर्फ पर रखा गया है। 4 घंटे से ठीक पहले टी 4 डीएनए लिगेज जोड़ें इनक्यूबेशन 16 डिग्री सेल्सियस पर और अच्छी तरह मिलाएं।
लायब्रेरी तैयारी में समस्या का निवारण
यदि पीसीआर अनुमापन (चित्रा 4) के बाद जेल पर 10 से अधिक पीसीआर चक्रों की आवश्यकता होती है या कोई पीसीआर उत्पाद नहीं देखा जा सकता है, तो हाई-सी नमूने को बचाने के लिए कुछ विकल्प हैं। पीसीआर अनुमापन से वापस काम करते हुए, पहला विकल्प पीसीआर को फिर से आज़माना है। यदि अभी भी पर्याप्त उत्पाद नहीं है, तो 1x TLE बफर के साथ दो बार मोतियों को धोने के बाद ए-टेलिंग और एडाप्टर लिगेशन (चरण 3.6) के एक और दौर का प्रयास करना संभव है। इस अतिरिक्त ए-टेलिंग और एडाप्टर लिगेशन के बाद, कोई भी पहले की तरह पीसीआर अनुमापन के लिए आगे बढ़ सकता है। यदि अभी भी कोई उत्पाद नहीं है, तो अंतिम विकल्प चरण 3.3 से 0.8x अंश को पुन: व्यवस्थित करना और वहां से आगे बढ़ना है।
हाई-C3.0 की सीमाएं और फायदे
यह महसूस करना महत्वपूर्ण है कि हाई-सी एक जनसंख्या-आधारित विधि है जो सेल आबादी में लोकी के जोड़े के बीच बातचीत की औसत आवृत्ति को पकड़ती है। कुछ कम्प्यूटेशनल विश्लेषण25 की आबादी से अनुरूपता के संयोजन को अलग करने के लिए डिज़ाइन किए गए हैं, लेकिन सिद्धांत रूप में, हाई-सी कोशिकाओं के बीच अंतर के लिए अंधा है। यद्यपि एकल-सेल हाई-सी26,27 करना संभव है और कम्प्यूटेशनल निष्कर्ष28 बनाए जा सकते हैं, एकल-सेल हाई-सी अल्ट्राहाई-रिज़ॉल्यूशन 3 सी जानकारी प्राप्त करने के लिए उपयुक्त नहीं है। हाई-सी की एक अतिरिक्त सीमा यह है कि यह केवल जोड़ीवार इंटरैक्शन का पता लगाता है। मल्टीकॉन्टैक्ट इंटरैक्शन का पता लगाने के लिए, कोई या तो शॉर्ट-रीड सीक्वेंसिंग (इलुमिना) 16 के साथ संयुक्त लगातार कटर का उपयोग कर सकता है या पैकबायो या ऑक्सफोर्ड नैनोपोर प्लेटफार्मों से लंबे समय तक पढ़े जाने वाले अनुक्रमण का उपयोग करके मल्टीकॉन्टैक्ट 3 सी29 या 4 सी30 कर सकता है। विशेष रूप से बहन क्रोमैटिड के बीच और उसके साथ संपर्कों का पता लगाने के लिए हाई-सी डेरिवेटिव भी31,32 विकसित किए गए हैं।
यद्यपि हाई-सी19 और माइक्रो-सी33 का उपयोग सबकिलोबेस रिज़ॉल्यूशन पर संपर्क मानचित्र उत्पन्न करने के लिए किया जा सकता है, दोनों को बड़ी मात्रा में अनुक्रमण पढ़ने की आवश्यकता होती है और यह एक महंगा उपक्रम बन सकता है। लागत के बिना समान या उच्च रिज़ॉल्यूशन प्राप्त करने के लिए, विशिष्ट जीनोमिक क्षेत्रों (कैप्चर-सी34) या विशिष्ट प्रोटीन इंटरैक्शन (चिया-पीईटी35, पीएलएसी-सेक36, हाई-सीएचआईपी37) के लिए संवर्धन लागू किया जा सकता है। इन संवर्धन अनुप्रयोगों की ताकत और नकारात्मक पक्ष यह है कि केवल सीमित संख्या में इंटरैक्शन का नमूना लिया जाता है। इस तरह के संवर्धन के साथ, हाई-सी का वैश्विक पहलू (और वैश्विक सामान्यीकरण का विकल्प) खो जाता है।
हाय-C3.0 का महत्व और संभावित अनुप्रयोग
इस प्रोटोकॉल को उच्च-रिज़ॉल्यूशन, अल्ट्राडीप 3 सी को सक्षम करने के लिए डिज़ाइन किया गया था, जबकि साथ ही टीएडी और डिब्बों17 (चित्रा 6) जैसे बड़े पैमाने पर फोल्डिंग सुविधाओं का पता लगाया गया था। यह प्रोटोकॉल प्रत्येक हाई-सी लाइब्रेरी के लिए प्रति ट्यूब 5 × 106 कोशिकाओं के साथ शुरू होता है, जो 1 बिलियन युग्मित-अंत पठन प्राप्त करने के लिए प्रवाह सेल पर एक या दो लेन अनुक्रमित करने के लिए पर्याप्त सामग्री से अधिक होना चाहिए। अल्ट्राडीप अनुक्रमण के लिए, मैप किए गए रीड और पीसीआर डुप्लिकेट की संख्या के आधार पर 5 × 106 कोशिकाओं के कई ट्यूब तैयार किए जाने चाहिए। उच्चतम रिज़ॉल्यूशन (<1 केबी) पर, लूपिंग इंटरैक्शन ज्यादातर सीटीसीएफ साइटों के बीच पाए जाते हैं, लेकिन प्रमोटर-एन्हांसर इंटरैक्शन का भी पता लगाया जा सकता है। पाठक डेटा विश्लेषण के विस्तृत विवरण के लिए एकगोल ओकसुज़ एट अल .17 का उल्लेख कर सकते हैं।
Disclosures
The authors have nothing to disclose.
Acknowledgements
हम प्रोटोकॉल विकास के लिए डेनिस लाफोंटेन और जैव सूचना विज्ञान सहायता के लिए सर्गेई वेनेव को धन्यवाद देना चाहते हैं। इस काम को नेशनल इंस्टीट्यूट ऑफ हेल्थ कॉमन फंड 4 डी न्यूक्लियोम प्रोग्राम से जेडी (यू 54-डीके 107980, यूएम 1-एचजी 011536) के अनुदान द्वारा समर्थित किया गया था। जेडी हॉवर्ड ह्यूजेस मेडिकल इंस्टीट्यूट के एक अन्वेषक हैं।
यह लेख HHMI की प्रकाशनों के लिए खुली पहुँच नीति के अधीन है। एचएचएमआई प्रयोगशाला प्रमुखों ने पहले अपने शोध लेखों में जनता को एक गैर-विशिष्ट सीसी बीवाई 4.0 लाइसेंस और एचएचएमआई को एक उप-लाइसेंस योग्य लाइसेंस दिया है। उन लाइसेंसों के अनुसार, इस लेख की लेखक-स्वीकृत पांडुलिपि को प्रकाशन के तुरंत बाद सीसी बीवाई 4.0 लाइसेंस के तहत स्वतंत्र रूप से उपलब्ध कराया जा सकता है।
Materials
| 1 kb Ladder | New England Biolabs | N3232L | |
| Agarose | Invitrogen | 16500100 | |
| Agencourt AMPure XP magnetic beads , 60 mL | Beckman Coulter | A63881 | |
| Amicon Ultra-0.5 Centrifugal Filter Unit (CFU) | EMD Millipore | UFC500396 | |
| Annealing Buffer (5x) | See recipe in supplemental materials | ||
| ATP 10 mM | ThermoFisher | R0441 | |
| Avanti J-25i High Speed Refrigerated ultra-centrifuge | Beckman Coulter | ||
| beckman ultracentrifuge tube 35 mL | Beckman Coulter | 357002 | |
| Binding Buffer (2x) | See recipe in supplemental materials | ||
| biotin-14-dATP 0.4 mM | Invitrogen | 19524-016 | |
| BSA 10 mg/mL | New England Biolabs | B9000S | dilute from 20 mg/mL |
| Cell scraper | Falcon | 353089 | |
| Cell scraper | Corning | 3008 | |
| Conical polypropylene tubes 50 mL | Denville | C1062-P | |
| Conical tube 15 mL | Denville | C1017-P | |
| Covaris micro tube AFA fiber with snap-cap 130 µL | Covaris | 520045/520077 | |
| Covaris Sonicator | Covaris | E220/E220evolution/M220 | |
| Culture flask 175 cm2 | Falcon | 353112 | |
| Culture plates 150 mm x 25 mm | Corning | 430599 | |
| dATP 1 mM | Invitrogen | 56172 | |
| dATP 10 mM | Invitrogen | 56172 | |
| dCTP 10 mM | Invitrogen | 56173 | |
| DdeI | New England Biolabs | R0175L | |
| dGTP 10 mM | Invitrogen | 56174 | |
| DMSO | Sigma | D2650-5x10ML | |
| dNTP mix 25 mM | Invitrogen | 10297117 | |
| Dounce homogenizer | DWK Life Sciences | 8853010002/8853030002 | |
| DPBS | Gibco | 14190-144 | |
| DpnII | New England Biolabs | R0543M | |
| DSG | ThermoScientific | 20593 | |
| dTTP 10 mM | Invitrogen | 56175 | |
| Ethanol 70% | Fisher | A409-4 | Diluted from 100% |
| Ethidium Bromide | Fisher | BP1302-10 | |
| Formaldehyde (37%) | Fisher | BP531-500 | |
| Gel loading dye (6x ) | New England Biolabs | B7024S | |
| Glycine in ultrapure water 2.5 M | Sigma | G8898-1KG | |
| HBSS | Gibco | 14025-092 | |
| Igepal CA-630 detergent | MP Biomedicals | 198596 | |
| Klenow DNA polymerase 5 U/µL | New England Biolabs | M0210L | |
| Klenow Fragment 3–>5’ exo-, 5 U/µL | New England Biolabs | M0212L | |
| ligation buffer (10x) | New England Biolabs | B7203S | |
| Liquid nitrogen | |||
| LoBind microcentrifuge tube 1.7 mL | Eppendorf | 22431021 | |
| Low Molecular Weight DNA Ladder | New England Biolabs | N3233L | |
| Lysis buffer | See recipe in supplemental materials | ||
| Magnetic Particle separator | ThermoFisher | 12321D | |
| Microfuge tubes 1.7 mL | Axygen | MCT-175-C | |
| MyOne Streptavidin C1 beads | Invitrogen | 65001 | |
| NEBuffer 2.1 (10x) | New England Biolabs | B7002S | |
| NEBuffer 3.1 (10x) | New England Biolabs | B7203S | |
| PBS | Gibco | 70013-032 | |
| PCR (strip) tubes | Biorad | TBS0201/ TCS0803 | |
| PCR thermocycler | Biorad | T100 | |
| Pfu Ultra II Buffer (10x) | Agilent | Comes with Pfu Ultra | |
| PfuUltra II Fusion HS DNA Polymerase | Agilent | 600674 | |
| Phase lock tube 15 mL | Qiagen | 129065 | |
| Phase lock tubes 2 mL | Qiagen | 129056 | |
| Phenol:chloroform:isoamyl alcohol | Invitrogen | 15593-049 | |
| Protease inhibitor cocktail | ThermoFisher | 78440 | |
| Proteinase K in ultrapure water 10 mg/mL | Invitrogen | 25530-031 | |
| Refrigerated Centrifuge | Eppendorf | 5810R | |
| RNase A, DNase and protease-free 10 mg/mL | Thermo Scientific | EN0531 | |
| Rotator | Argos technologies | EW-04397-40 or rocking platform | |
| SDS 1% | Fisher | BP13111 | |
| Sodium acetate pH = 5.2, 3 M | Sigma | ||
| Sub-Cell GT Horizontal Electrophoresis System | Biorad | 1704401 | |
| T4 DNA ligase 1 U/µL | Invitrogen | 100004817 | |
| T4 DNA polymerase | New England Biolabs | M0203L | |
| T4 DNA polymerase | New England Biolabs | M0203L | |
| T4 DNA polymerase 3 U/µL | New England Biolabs | M0203L | |
| T4 ligation buffer (5x) | Invitrogen | Y90001 | |
| T4 polynucleotide kinase 10 U/µL | New England Biolabs | M0201L | |
| Tabletop centrifuge | Eppendorf | 5425 | |
| TBE buffer | See recipe in supplemental materials | ||
| Tris Low EDTA Buffer (TLE) | See recipe in supplemental materials | ||
| Triton X-100 (10%) | Sigma | 93443 | |
| Truseq adapter oligos | Integrated DNA Technologies (IDT)) | https://www.idtdna.com/site/order/oligoentry | 250 nmole and HPLC purified |
| Tween 20 detergent | Fisher | 9005-64-5 | |
| Tween Wash Buffer | See recipe in supplemental materials | ||
| Vortex | Scientific Industries | (G560)SI-0236 |
References
- Dekker, J., Rippe, K., Dekker, M., Kleckner, N. Capturing chromosome conformation. Science. 295 (5558), 1306-1311 (2002).
- Simonis, M., et al. Nuclear organization of active and inactive chromatin domains uncovered by chromosome conformation capture-on-chip (4C). Nature Genetics. 38 (11), 1348-1354 (2006).
- Dostie, J., et al. Chromosome Conformation Capture Carbon Copy (5C): a massively parallel solution for mapping interactions between genomic elements. Genome Research. 16 (10), 1299-1309 (2006).
- Lieberman-Aiden, E., et al. Comprehensive mapping of long-range interactions reveals folding principles of the human genome. Science. 326 (5950), 289-293 (2009).
- Stadhouders, R., et al. Multiplexed chromosome conformation capture sequencing for rapid genome-scale high-resolution detection of long-range chromatin interactions. Nature Protocols. 8 (3), 509-524 (2013).
- Kalhor, R., Tjong, H., Jayathilaka, N., Alber, F., Chen, L. Genome architectures revealed by tethered chromosome conformation capture and population-based modeling. Nature Biotechnology. 30 (1), 90-98 (2012).
- Hsieh, T. H., et al. Mapping nucleosome resolution chromosome folding in yeast by micro-C. Cell. 162 (1), 108-119 (2015).
- Hsieh, T. -. H. S., Fudenberg, G., Goloborodko, A., Rando, O. J. Micro-C XL: assaying chromosome conformation from the nucleosome to the entire genome. Nature Methods. 13 (12), 1009-1011 (2016).
- Denker, A., de Laat, W. The second decade of 3C technologies: detailed insights into nuclear organization. Genes & Development. 30 (12), 1357-1382 (2016).
- Rodley, C. D., Bertels, F., Jones, B., O’Sullivan, J. M. Global identification of yeast chromosome interactions using Genome conformation capture. Fungal Genetics and Biology. 46 (11), 879-886 (2009).
- Rao, S. S., et al. A 3D map of the human genome at kilobase resolution reveals principles of chromatin looping. Cell. 159 (7), 1665-1680 (2014).
- Alipour, E., Marko, J. F. Self-organization of domain structures by DNA-loop-extruding enzymes. Nucleic Acids Research. 40 (22), 11202-11212 (2012).
- Lajoie, B. R., Dekker, J., Kaplan, N. The Hitchhiker’s guide to Hi-C analysis: Practical guidelines. Methods. 72, 65-75 (2015).
- Belaghzal, H., Dekker, J., Gibcus, J. H. Hi-C 2.0: An optimized Hi-C procedure for high-resolution genome-wide mapping of chromosome conformation. Methods. 123, 56-65 (2017).
- Golloshi, R., Sanders, J. T., McCord, R. P. Iteratively improving Hi-C experiments one step at a time. Methods. 142, 47-58 (2018).
- Darrow, E. M., et al. Deletion of DXZ4 on the human inactive X chromosome alters higher-order genome architecture. Proceedings of the National Academy of Sciences of the United States of America. 113 (31), 4504-4512 (2016).
- Akgol Oksuz, B., et al. Systematic evaluation of chromosome conformation capture assays. Nature Methods. 18 (9), 1046-1055 (2021).
- Ghuryeid, J., et al. Integrating Hi-C links with assembly graphs for chromosome-scale assembly. PLoS Computational Biology. 15 (8), 1007273 (2019).
- Gu, H., et al. Fine-mapping of nuclear compartments using ultra-deep Hi-C shows that active promoter and enhancer elements localize in the active A compartment even when adjacent sequences do not. bioRxiv. , (2021).
- Ramani, V., et al. Mapping 3D genome architecture through in situ DNase Hi-C. Nature Protocols. 11 (11), 2104-2121 (2016).
- Lafontaine, D. L., Yang, L., Dekker, J., Gibcus, J. H. Hi-C 3.0: Improved Protocol for Genome-Wide Chromosome Conformation Capture. Current Protocols. 1 (7), 198 (2021).
- Belton, J. -. M. M., et al. Hi-C: A comprehensive technique to capture the conformation of genomes. Methods. 58 (3), 268-276 (2012).
- Truch, J., Telenius, J., Higgs, D. R., Gibbons, R. J. How to tackle challenging ChIP-Seq, with long-range cross-linking, Using ATRX as an example. Methods in Molecular Biology. 1832, 105-130 (2018).
- Wang, P., et al. In situ chromatin interaction analysis using paired-end tag sequencing. Current Protocols. 1 (8), 174 (2021).
- Tjong, H., et al. Population-based 3D genome structure analysis reveals driving forces in spatial genome organization. Proceedings of the National Academy of Sciences of the United States of America. 113 (12), 1663-1672 (2016).
- Nagano, T., et al. Cell-cycle dynamics of chromosomal organization at single-cell resolution. Nature. 547 (7661), 61-67 (2017).
- Ramani, V., et al. Massively multiplex single-cell Hi-C. Nature Methods. 14 (3), 263-266 (2017).
- Meng, L., Wang, C., Shi, Y., Luo, Q. Si-C is a method for inferring super-resolution intact genome structure from single-cell Hi-C data. Nature Communications. 12 (1), 4369 (2021).
- Tavares-Cadete, F., Norouzi, D., Dekker, B., Liu, Y., Dekker, J. Multi-contact 3C reveals that the human genome during interphase is largely not entangled. Nature Structural & Molecular Biology. 27 (12), 1105-1114 (2020).
- Vermeulen, C., et al. Multi-contact 4C: long-molecule sequencing of complex proximity ligation products to uncover local cooperative and competitive chromatin topologies. Nature Protocols. 15 (2), 364-397 (2020).
- Oomen, M. E., Hedger, A. K., Watts, J. K., Dekker, J. Detecting chromatin interactions between and along sister chromatids with SisterC. Nature Methods. 17 (10), 1002-1009 (2020).
- Mitter, M., et al. Conformation of sister chromatids in the replicated human genome. Nature. 586 (7827), 139-144 (2020).
- Krietenstein, N., et al. Ultrastructural Details of Mammalian Chromosome Architecture. Molecular Cell. 78 (3), 554-565 (2020).
- Hughes, J. R., et al. Analysis of hundreds of cis-regulatory landscapes at high resolution in a single, high-throughput experiment. Nature Genetics. 46 (2), 205-212 (2014).
- Fullwood, M. J., et al. An oestrogen-receptor-alpha-bound human chromatin interactome. Nature. 462 (7269), 58-64 (2009).
- Fang, R., et al. Mapping of long-range chromatin interactions by proximity ligation-assisted ChIP-seq. Cell Research. 26 (12), 1345-1348 (2016).
- Mumbach, M. R., et al. HiChIP: efficient and sensitive analysis of protein-directed genome architecture. Nature Methods. 13 (11), 919-922 (2016).

