Förbättrade metoder för beredning av tvärsnitt och rullade hela fästen av majsbladsprimordia för fluorescens och konfokal avbildning
Summary
Majsblad primordia är djupt mantlade och rullade, vilket gör dem svåra att studera. Här presenterar vi metoder för att förbereda tvärsnitt och rullade ut hela fästen av majsbladprimordia för fluorescens och konfokal avbildning.
Abstract
I majs (Zea mays) och andra gräs (Poaceae) är bladprimordia djupt mantlade och rullade inuti bladvirveln, vilket gör det svårt att studera tidig bladutveckling. Här beskriver vi metoder för beredning av tvärsnitt och rullade ut hela fästen av majsbladprimordia för fluorescens och konfokal avbildning. Den första metoden använder en trådstrippare för att ta bort de övre delarna av äldre löv, exponera spetsen på bladprimordium och möjliggöra mätning för mer exakt tvärsnittsprovtagning. Den andra metoden använder klar, dubbelsidig nanotejp för att rulla ut och montera helbladiga primordier för avbildning. Vi visar nyttan av de två metoderna för att visualisera och analysera fluorescerande proteinreportrar i majs. Dessa metoder ger en lösning på de utmaningar som den distinkta morfologin hos majsbladprimordia presenterar och kommer att vara användbara för att visualisera och kvantifiera bladanatomiska och utvecklingsegenskaper hos majs och andra gräsarter.
Introduction
Gräsgrödor är en viktig källa till mat och biobränsle för den globala befolkningen1, och förbättrad bladanatomi har potential att öka deras produktivitet 2,3. Vår nuvarande förståelse för hur bladanatomi regleras i gräs är dock begränsad4 och kräver analys av bladprimordia, eftersom många anatomiska och fysiologiska egenskaper hos bladet är förutbestämda tidigt i utvecklingen 5,6,7. Cellulära avbildningstekniker, såsom fluorescens och konfokal avbildning, är oumbärliga för att studera gräsbladanatomi och cellulära egenskaper, men dessa tekniker är svåra att tillämpa på gräsbladprimordia eftersom de är djupt mantlade och rullade inuti bladvirveln. Vi tog itu med denna fråga genom att utveckla metoder för att förbereda tvärsnitt och orullade helbladsfästen för fluorescens och konfokalanalys av majsbladprimordia, ett modellsystem för att studera gräsbladens anatomi och utveckling 2,8.
Majsbladet, som alla gräsblad, består av ett bandliknande blad med en mantel som sveper runt stammen och utvecklar skott 9,10,11,12,13. Bladen utvecklas från skottapikal meristem (SAM) i ett distichous mönster, där varje nytt blad initierar i motsatt position som föregående blad, vilket resulterar i två rader av löv längs den vertikala axeln (Figur 1A)14 . Utvecklingsstadiet för varje bladprimordium identifieras genom dess position i förhållande till SAM, med det närmaste primordium betecknat som plastokron1 (P1) och följande primordia betecknat som P2, P3 och så vidare (figur 1B, C)2. Under utvecklingen (figur 1D) framträder bladprimordium först som en halvmåneformad strävpelare runt basen av SAM (P1) och växer sedan till ett huvformat primordium som sträcker sig över meristem (P2) 9,10,11. Huvens basala marginaler expanderar sedan i sidled och överlappar varandra när spetsen växer uppåt och bildar ett konformat primordium (P3-P5)10. Primordium växer sedan snabbt i längd, och mantelbladsgränsen vid basen blir mer framträdande med bildandet av ligulen, den fransliknande projektionen på bladets adaxiella sida (P6 / P7). Slutligen rullar bladet ut när det kommer ut ur virveln under steady-state-tillväxt, där delningscellerna är begränsade inom bladets lilla basala region och bildar en gradient med expanderande och differentierande celler längs den proximala-distala axeln (P7 / P8)15. Skotttoppen på en majsplanta innehåller flera primordia i olika utvecklingsstadier, vilket gör den till en utmärkt modell för att studera bladutveckling8.
Noggrann analys av tidig bladutveckling kräver iscensättning eller användning av standardiserade kriterier för att definiera distinkta stadier av primordiumutveckling i förhållande till andra tillväxt- eller morfologiska parametrar. Eftersom bladprimordia är dolda i grässkottet använder utredare vanligtvis parametrar som växtens ålder eller storleken på de framväxande bladen som prediktorer för stadierna och storlekarna på bladprimordia 9,16. I majs bestäms växtens kronologiska ålder antingen av antalet dagar efter plantering eller groning (DAP/DAG)17,18. Det vegetativa stadiet (V-steget) bestäms av det översta bladet med en synlig krage, en blek linje på den abaxiella sidan mellan bladet och manteln som motsvarar ligulens och auriklarnas position, ett par kilformade regioner vid bladets bas (figur 1A,B)17,19 . Mellan 20 och 25 DAG övergår SAM till en blomställning meristem och upphör att producera nya blad20. Tillväxthastigheten för majsbladprimordia kan variera beroende på miljön och växtens genotyp. Av denna anledning kan växtåldern och storleken på de framväxande bladen inte exakt förutsäga storleken på bladprimordia; Att använda dessa parametrar kan dock hjälpa till att förutsäga intervallet för Primordia-stadier och storlekar för experimentella ändamål.
Tvärsnittsanalys är en populär metod för att undersöka bladanatomi och utveckling i majs och andra gräs eftersom det möjliggör provtagning av flera plastokroner i en enda sektion över skottet21,22,23. Denna metod är också lämplig för cellulär avbildning av färska prover, eftersom de omgivande bladen fungerar som en byggnadsställning som håller bladprimordia på plats under sektionering och montering24. En nackdel med denna metod är dock att det kan vara utmanande att exakt lokalisera målplastokranen och regionen inom primordium vid snittning från en intakt skott. Eftersom bladtillväxten varierar mellan plastokroner och längs den proximala-distala axeln 2,5 kan dessutom inexakt provtagning leda till en felaktig tolkning av primordiumets utvecklingsstadium och region i ett givet avsnitt. Därför är det viktigt att utveckla en metod för exakt tvärsnittsprovtagning för att säkerställa noggrannheten och reproducerbarheten av anatomiska och utvecklingsanalyser av gräsbladprimordia.
Helbladsmonteringsanalys möjliggör omfattande och integrativ undersökning av vävnads- och cellulära processer som uppträder på helorganskalan, såsom proliferativ tillväxt25 och venmönstring26,27,28. Metoden ger en paradermal översikt över bladet, vilket möjliggör upptäckt av distinkta processer och mönster som annars skulle vara svåra att upptäcka med hjälp av tvärsnittsanalys24,27. Till skillnad från Arabidopsis, där det redan finns etablerade metoder för avbildning av helbladsfästen29,30, finns det för närvarande ingen standardmetod för avbildning av orullade helbladsfästen i gräs. Ett tidigare protokoll för utrullning av isolerat majsbladprimordia involverade ovanliga material och var inte lämpligt för cellulär avbildning31. Avancerade avbildningstekniker, såsom datortomografi (CT) och magnetisk resonanstomografi (MRT), kan förvärva 3D-anatomisk information utan att isolera och rulla ut primordia 11,32,33, men de är dyra och kräver specialutrustning. Att utveckla en teknik för att övervinna de begränsningar som den rullade och koniska morfologin hos bladprimordia i majs och andra gräs skulle främja undersökningar av deras anatomiska och utvecklingsegenskaper.
Här presenterar vi metoder för att förbereda tvärsnitt och rullade ut hela fästen av majsbladprimordia för fluorescens och konfokal avbildning. Vi använde dessa metoder för att kvantifiera venantal och kartlägga fördelningen av rumsligt-temporalt hormon i majsbladprimordia med fluorescerande proteiner (FPs)24. Den första metoden innebär att man tar bort den övre delen av äldre löv från majsplantor med en trådstrippare (figur 1E). Genom att exponera primordiumspetsen (P5-P7) blir det möjligt att bestämma dess längd utan att helt behöva ta bort de äldre omgivande bladen, vilket möjliggör enkel och exakt sektionering. Den andra metoden innefattar avrullning och montering av helbladig primordia (P3-P7) med klar, dubbelsidig nanotejp (figur 1F). Dessa metoder är lämpliga för att visualisera olika FP24 men behöver optimering för att använda fluorescerande färgämnen och clearingreagens. Dessutom beskriver vi några procedurer för att platta z-stackar, sy bilder och slå samman kanaler i ImageJ / FIJI34, som gäller för bilderna som produceras med de två metoderna. Dessa metoder är användbara för rutinmässig fluorescens eller konfokal avbildning av majsblad, men de kan också anpassas för andra modellgräsarter, såsom ris, setaria och brachypodium.
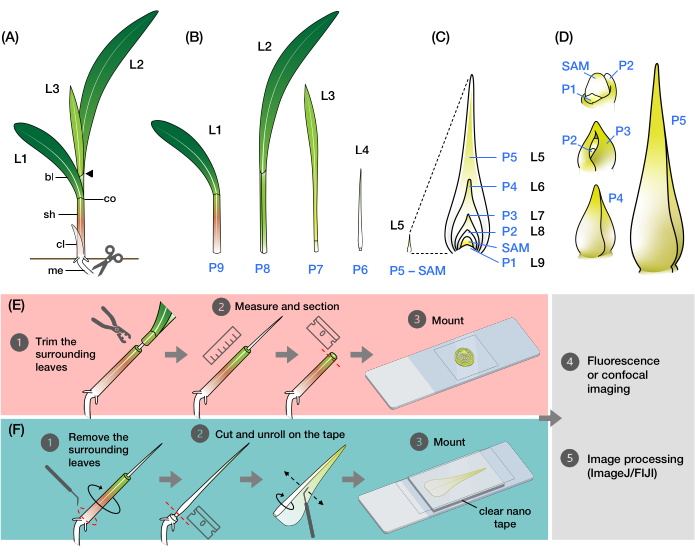
Figur 1: Organisation och morfologi av majsbladprimordia och översikt över metoderna . a) Schematisk framställning av en majsplanta. Majs har en distichous phyllotaxy, med det nya bladet som initierar i motsatt position som föregående blad. Bladnumret anger den kronologiska ordning i vilken bladen uppstod från groning (dvs. första bladet, L1; andra bladet, L2; tredje bladet, L3; etc.). Varje blad har ett distalt blad och en basalmantel avgränsad av en krage som motsvarar ligulen och öronen. Det översta bladet med kragen synlig betecknar det vegetativa stadiet. Plantan i detta exempel är i V2-steget, med L2-kragen (pilspetsen) synlig. Saxikonen anger platsen vid mesocotyl (mig) där plantan måste skäras för att kunna samlas in. (B) Schematisk representation av den dissekerade skottet som visar isolerad L1 till L4, med bladprimordia L5 till L9 som en förstorad bild i (C). Plastokrantalet anger primordiumets position i förhållande till SAM, med det yngsta bladprimordium (P1) närmast SAM och det äldre bladprimordia (P2, P3, P4 och så vidare) successivt längre bort2. D) Schematisk framställning av morfologin hos majsbladprimordia från P1 till P5. E) Schematisk översikt över metoden för tvärsnittsanalys av primordia av majsblad. (1) Trimma de äldre bladen med en trådstrippare. (2) Mät primordium och sektionera skottet. (3) Montera sektionen på ett objektglas för bildbehandling och bearbetning (4, 5). F) Schematisk översikt över metoden för helmonteringsanalys av majsbladets primordia. (1) Ta bort de omgivande bladen för att extrahera primordium. (2) Klipp och rulla ut primordium platt på nanotejpen. (3) Montera provet för bildbehandling och bearbetning (4, 5). Förkortningar: L = blad; bl = blad; sh = mantel; co = krage; mig = mesocotyl; V = vegetativ; P = plastokron; SAM = skjut apikalt meristem. Klicka här för att se en större version av denna figur.
Protocol
Representative Results
Discussion
Vi presenterar två metoder för beredning av majsbladprimordia för cellulär avbildning. Den första metoden (protokollavsnitt 2) möjliggör mätning av primordium för tvärsnittsanalys, medan den andra metoden (protokollavsnitt 3) möjliggör avrullning och utplattning av primordium för helmonteringsanalys. Dessa metoder underlättar cellulär avbildning av ramprogram i majsblad primordia24 (som visas i figur 4 och figur 5) och ger enkla lösningar på utmaningarna med att avbilda utveckling av majsblad. Protokoll avsnitt 2 minskar dissektionstiden och förbättrar provtagningsnoggrannheten genom att mäta primordia före sektionering snarare än att enbart förlita sig på mellanlagringsparametrarna 9,16. Med kommersiellt tillgänglig nanotejp löser protokollavsnitt 3 det långvariga problemet med att avbilda helbladiga primordier i majs. Detta protokoll förbättrar den tidigare metoden, som använde dialysslang 31, och är ett mycket billigare alternativ till CT och MR11,32,33. Men när det gäller att visualisera bladanatomiska egenskaper och producera optimala resultat har båda protokollen vissa begränsningar, som beskrivs i tabell 2 och diskuteras mer detaljerat nedan.
I protokollavsnitt 2 stötte vi på svårigheter att visualisera cellkonturer i tjocka tvärsnitt av bladprimordia, och motfärgning med cellväggs- eller plasmamembranbindande fluorescerande färgämnen gav inte tillfredsställande resultat. Till exempel gav FM 4-64 suboptimala resultat jämfört med plasmamembranets FP-markör, p Zm PIP2-1::ZmPIP2-1:CFP39 (PIP2-1-CFP; Figur 3A-D). För att övervinna denna begränsning rekommenderar vi att du använder ett vibratom för att producera tunnare vävnadssnitt (~ 0,1 mm)58 vilket möjliggör en levande ljusfältsavbildning av cellkonturer eller optimering av motfärgningsprotokollet 47,59.
I protokollavsnitt 3 är huvudbegränsningen svårigheten att montera bladet utan att riva, skada eller luftbubblor, vilket beskrivs i protokollstegen 3.2.5-3.2.6 (figur 3E-K). Eftersom majsbladet är bilateralt symmetriskt kan ett halvbladsfäste snarare än ett helbladsfäste vara tillräckligt för visualisering9. För att göra detta kan primordium skäras med ett rakblad längs längdaxeln efter att ha rullat upp det till mittribben, så att endast hälften av bladet kan monteras. En annan begränsning i protokollavsnitt 3 är att bladets tjocklek kan begränsa fluoroforsignalens optiska upplösning under djupavbildning. För att lösa detta problem är det möjligt att använda en vävnadsrensningsteknik60. Vi fann dock att ClearSee61, ett vanligt clearingreagens för avbildning av växtvävnader, inte är kompatibelt med protokollet eftersom det gör att provet och täckglaset lossnar från nanotejpen. En potentiell lösning på detta problem kan vara att applicera ett semipermeabelt membran31 över bladprovet, så att det kan behandlas med clearinglösningen medan det hålls på plats av nanotejpen. En sådan metod som gör det möjligt att applicera flytande lösningar på det orullade bladet kan också användas för helmonterade RNA in situ-hybridiserings– och immunlokaliseringstekniker, som tidigare har optimerats för att utveckla majsblomställningar men inte för helbladiga primordia62,63.
Vi beskrev protokoll för majs, som har stora bladprimordia även vid plantstadiet. Andra gräsarter med mycket mindre bladprimordia, såsom ris, korn, vete, setaria och Brachypodium 16,23,64,65,66, kan kräva användning av ytterligare precisionsverktyg för att effektivt tillämpa dessa protokoll. Dessutom var dessa protokoll inte avsedda för levande cellavbildning, som fångar dynamiska processer i realtid för vävnadsbildning och cellulära svar. Men eftersom fluorescerande sonder, bildteknik och datorkapacitet fortsätter att utvecklas inom levande cellavbildning för växter67, kan framtida forskning bygga på dessa protokoll för att utveckla levande cellavbildningsstrategier skräddarsydda för de unika egenskaperna hos gräsbladprimordia.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna vill tacka Maize Genetics Cooperation, Maize Cell Genomics Project, Dave Jackson (Cold Spring Harbor Laboratory, NY), Anne W. Sylvester (Marine Biological Laboratory, University of Chicago, IL), Andrea Gallavotti (Rutgers University, NJ) och Carolyn G. Rasmussen (University of California, Riverside) för att tillhandahålla mutanta och transgena bestånd, liksom Robert F. Baker och Alexander Jurkevich från Advanced Light Microscopy Core vid University of Missouri-Columbia för deras hjälp med konfokalmikroskopi. JMR stöddes av J. William Fulbright Fellowship, Diane P. och Robert E. Sharp Fund och National Science Foundation’s Plant Genome Research Program (IOS-1546873) till PM. CDTC, CMRV, EDCDP och RJRR stöds av Ateneo College Scholarship Program. CDTC, EDCDP och RJRR stöds av DOST-SEI S&T Undergraduate Scholarship. DODL stöds av Fr. Thomas Steinbugler SJ Academic Scholarship. RJRR stöds av Aiducation International – Pathways to Higher Education Scholarship. Detta arbete stöddes av School of Science and Engineering och Rizal Library, Ateneo de Manila University.
Materials
| Acrylic Gel Clear Double Sided Nano Tape 16.5 ft x 1.2 in, 2 mm thick | EZlifego Store (Amazon) | B07YB1ZXG6 | 1 roll |
| Bellucci Pick Curved micro probe 16.8 cm, 6.6 in | Bausch & Lomb | N1692 9 | 1 pc |
| Clayman guide microprobe Sinskey hook angled shaft, 11.6 cm, 4.6 in | Storz Opthalmic Instruments | E0542 | 1 pc |
| Dental Probe, Bent Needle, 14 cm (5.5 in) | Ted Pella | 13553 | 1 pc |
| DOWELL 10-22 AWG Wire Stripper | Dowell Store (Amazon) | 10-22 AWG | 1 pc |
| Feather Double Edge Carbon Steel Blades | Ted Pella | 121-9 | pkg/10; for fine sectioning |
| Frosted End Glass Microscope Slides, 75 mm x 25 mm x 1-1.2 mm | Ted Pella | 260442 | pkg/144 |
| GEM Single Edge, Stainless Steel Uncoated Blades | Ted Pella | 121-1 | box/200; for general cutting/sectioning |
| Glycerol | Thermo Scientific | PI17904 | 1 liter |
| ImageJ/FIJI with EDF plugin (version 17.05.2021) and Grid/Collection Stitching plugin | National Institutes of Health (NIH) USA | version 2.9.0/1.54s | The EDF plugin was developed by Alex Prudencio, Jesse Berent, and Daniel Sage for the Biomedical Imaging Group, École Polytechnique Fédérale de Lausanne (EPFL; http://bigwww.epfl.ch/demo/edf/). The grid/collection stitching software was developed by Stephan Preibisch for the Max Planck Institute of Molecular Cell Biology and Genetics (MPI-CBG). |
| Kimwipes Ex-L Small 111.76 mm x 213.36 mm | Kimtech Science | 34155 | box/280 ply |
| Micro Cover Glasses, 22 mm x 22 mm x 0.13 – 0.16 mm thick | Ted Pella | 260140 | 1 ounce |
| PU Gel Clear Double Sided Nano Tape 29.5 ft x 1.18 in, 1 mm thick | Yecaye Store (Amazon) | L354 W1.18 | 2 rolls |
| Superslip Cover Glasses, 24 mm x 50 mm x 0.13 – 0.16 mm thick | Ted Pella | 260166 | 1 ounce |
| Superslip Cover Glasses, 24 mm x 60 mm x 0.13 – 0.16 mm thick | Ted Pella | 260168 | 1 ounce |
| Tempered Glass Cutting Board | Hacaroa (Amazon) | B09XMXBT5S | 4 pc |
References
- McSteen, P., Kellogg, E. A. Molecular, cellular, and developmental foundations of grass diversity. Science. 377 (6606), 599-602 (2022).
- Wang, P., Vlad, D., Langdale, J. A. Finding the genes to build C4 rice. Current Opinion in Plant Biology. 31, 44-50 (2016).
- Wang, P., et al. Candidate regulators of early leaf development in maize perturb hormone signalling and secondary cell wall formation when constitutively expressed in rice. Scientific Reports. 7 (1), 4535 (2017).
- Perico, C., Tan, S., Langdale, J. A. Developmental regulation of leaf venation patterns: Monocot versus eudicots and the role of auxin. New Phytologist. 234 (3), 783-803 (2022).
- Wang, P., Kelly, S., Fouracre, J. P., Langdale, J. A. Genome-wide transcript analysis of early maize leaf development reveals gene cohorts associated with the differentiation of C4 Kranz anatomy. The Plant Journal. 75 (4), 656-670 (2013).
- Liu, W. Y., et al. Regulators of early maize leaf development inferred from transcriptomes of laser capture microdissection (LCM)-isolated embryonic leaf cells. Proceedings of the National Academy of Sciences. 119 (35), e2208795119 (2022).
- Liu, W. Y., et al. Anatomical and transcriptional dynamics of maize embryonic leaves during seed germination. Proceedings of the National Academy of Sciences. 110 (10), 3979-3984 (2013).
- Strable, J., Nelissen, H. The dynamics of maize leaf development: Patterned to grow while growing a pattern. Current Opinion in Plant Biology. 63, 102038 (2021).
- Reynolds, J. O., Eisses, J. F., Sylvester, A. W. Balancing division and expansion during maize leaf morphogenesis: Analysis of the mutant, warty-1. Development. 125 (2), 259-268 (1998).
- Richardson, A. E., et al. Evolution of the grass leaf by primordium extension and petiole-lamina remodeling. Science. 374 (6573), 1377-1381 (2021).
- Johnston, R., Leiboff, S., Scanlon, M. J. Ontogeny of the sheathing leaf base in maize (Zea mays). New Phytologist. 205 (1), 306-315 (2015).
- Sharman, B. C. Developmental anatomy of the shoot of Zea mays L. Annals of Botany. 6 (22), 245-282 (1942).
- Johnston, R., et al. Transcriptomic analyses indicate that maize ligule development recapitulates gene expression patterns that occur during lateral organ initiation. The Plant Cell. 26 (12), 4718-4732 (2014).
- Sharman, B. C. Leaf and bud initiation in the Gramineae. Botanical Gazette. 106 (3), 269-289 (1945).
- Nelissen, H., et al. A local maximum in gibberellin levels regulates maize leaf growth by spatial control of cell division. Current Biology. 22 (13), 1183-1187 (2012).
- Itoh, J., et al. Rice plant development: From zygote to spikelet. Plant and Cell Physiology. 46 (1), 23-47 (2005).
- Ritchie, S. W., Hanway, J. J., Benson, G. O. How a corn plant develops. Iowa State University of Science and Technology. , (1986).
- Freeling, M., Walbot, V. . The Maize Handbook. , (2013).
- Freeling, M., Hake, S. Developmental genetics of mutants that specify knotted leaves in maize. Genetics. 111 (3), 617-634 (1985).
- Durbak, A. R., et al. Transport of boron by the tassel-less1 aquaporin is critical for vegetative and reproductive development in maize. The Plant Cell. 26 (7), 2978-2995 (2014).
- Langdale, J. A., Lane, B., Freeling, M., Nelson, T. Cell lineage analysis of maize bundle sheath and mesophyll cells. Developmental Biology. 133 (1), 128-139 (1989).
- Bosabalidis, A. M., Evert, R. F., Russin, W. A. Ontogeny of the vascular bundles and contiguous tissues in the maize leaf blade. American Journal of Botany. 81 (6), 745-752 (1994).
- Junqueira, N. E. G., et al. Anatomy and ultrastructure of embryonic leaves of the C4 species Setaria viridis. Annals of Botany. 121 (6), 1163-1172 (2018).
- Robil, J. M., McSteen, P. Hormonal control of medial-lateral growth and vein formation in the maize leaf. New Phytologist. 238 (1), 125-141 (2023).
- Donnelly, P. M., Bonetta, D., Tsukaya, H., Dengler, R. E., Dengler, N. G. Cell cycling and cell enlargement in developing leaves of Arabidopsis. Developmental Biology. 215 (2), 407-419 (1999).
- Govindaraju, P., Verna, C., Zhu, T., Scarpella, E. Vein patterning by tissue-specific auxin transport. Development. 147 (13), (2020).
- Linh, N. M., Scarpella, E. Leaf vein patterning is regulated by the aperture of plasmodesmata intercellular channels. PLoS Biology. 20 (9), e3001781 (2022).
- Verna, C., Ravichandran, S. J., Sawchuk, M. G., Linh, N. M., Scarpella, E. Coordination of tissue cell polarity by auxin transport and signaling. eLife. 8, e51061 (2019).
- Sawchuk, M. G., Head, P., Donner, T. J., Scarpella, E. Time-lapse imaging of Arabidopsis leaf development shows dynamic patterns of procambium formation. New Phytologist. 176 (3), 560-571 (2007).
- Linh, N. M., Scarpella, E. Confocal imaging of developing leaves. Current Protocols. 2 (1), e349 (2022).
- Poethig, R. S., Szymkowiak, E. J. Clonal analysis of leaf development in maize. Maydica. 40, 67-76 (1995).
- Sprangers, K., Thys, S., van Dusschoten, D., Beemster, G. T. S. Gibberellin enhances the anisotropy of cell expansion in the growth zone of the maize leaf. Frontiers in Plant Science. 11, 1163 (2020).
- Tsuda, K., et al. KNOTTED1 cofactors, BLH12 and BLH14, regulate internode patterning and vein anastomosis in maize. The Plant Cell. 29 (5), 1105-1118 (2017).
- Schindelin, J., et al. FIJI: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Plant Care Protocols – Maize. The Donald Danforth Plant Science Center’s Plant Growth Facility Available from: https://www.danforthcenter.org/our-work/core-facilities/plant-growth/ (2019)
- Mir, R., et al. A DII domain-based auxin reporter uncovers low auxin signaling during telophase and early G1. Plant Physiology. 173 (1), 863-871 (2017).
- DeBlasio, S. L., Sylvester, A. W., Jackson, D. Illuminating plant biology: Using fluorescent proteins for high-throughput analysis of protein localization and function in plants. Briefings in Functional Genomics. 9 (2), 129-138 (2010).
- Wu, Q., Luo, A., Zadrozny, T., Sylvester, A., Jackson, D. Fluorescent protein marker lines in maize: Generation and applications. The International Journal of Developmental Biology. 57 (6-8), 535-543 (2013).
- Mohanty, A., et al. Advancing cell biology and functional genomics in maize using fluorescent protein-tagged lines. Plant Physiology. 149 (2), 601-605 (2009).
- Baker, R. F., et al. Sucrose transporter ZmSut1 expression and localization uncover new insights into sucrose phloem loading. Plant Physiology. 172 (3), 1876-1898 (2016).
- Gallavotti, A., Yang, Y., Schmidt, R. J., Jackson, D. The relationship between auxin transport and maize branching. Plant Physiology. 147 (4), 1913-1923 (2008).
- Krishnakumar, V., et al. A maize database resource that captures tissue-specific and subcellular-localized gene expression, via fluorescent tags and confocal imaging (Maize Cell Genomics Database). Plant and Cell Physiology. 56 (1), 12 (2015).
- Snapp, E. L. Fluorescent proteins: A cell biologist’s user guide. Trends in Cell Biology. 19 (11), 649-655 (2009).
- Geng, Y., Zhou, Y. Confocal live imaging of shoot apical meristems from different plant species. Journal of Visualized Experiments. (145), e59369 (2019).
- Stanislas, T., Hamant, O., Traas, J. In-vivo analysis of morphogenesis in plants. Methods in Cell Biology. 139, 203-223 (2017).
- Fodor, E., Ayaydin, F. Fluorescent probes and live imaging of plant cells. Advances in Plant Ecophysiology Techniques. , 241-251 (2018).
- Grandjean, O., et al. In vivo analysis of cell division, cell growth, and differentiation at the shoot apical meristem in Arabidopsis. The Plant Cell. 16 (1), 74-87 (2004).
- Conklin, P. A., Johnston, R., Conlon, B. R., Shimizu, R., Scanlon, M. J. Plant homeodomain proteins provide a mechanism for how leaves grow wide. Development. 147 (20), (2020).
- Shaw, S. L. Imaging the live plant cell. The Plant Journal. 45 (4), 573-598 (2006).
- Klaus, A. V., Schawaroch, V., Frischmann, K. J. Confocal imaging and three-dimensional visualization of thick autofluorescent specimens. Methods in Molecular Biology. 1075, 213-225 (2014).
- Forster, B., Van De Ville, D., Berent, J., Sage, D., Unser, M. Extended depth-of-focus for multi-channel microscopy images: a complex wavelet approach. 2004 2nd IEEE International Symposium on Biomedical Imaging: Nano to Macro (IEEE Cat No. 04EX821). IEEE. , 660-663 (2004).
- Preibisch, S., Saalfeld, S., Tomancak, P. Globally optimal stitching of tiled 3D microscopic image acquisitions. Bioinformatics. 25 (11), 1463-1465 (2009).
- Phillips, K. A., et al. vanishing tassel2 encodes a grass-specific tryptophan aminotransferase required for vegetative and reproductive development in maize. The Plant Cell. 23 (2), 550-566 (2011).
- Robil, J. M., et al. GrasVIQ: An image analysis framework for automatically quantifying vein number and morphology in grass leaves. The Plant Journal. 107 (2), 629-648 (2021).
- Helliwell, C. A., Chandler, P. M., Poole, A., Dennis, E. S., Peacock, W. J. The CYP88A cytochrome P450, ent-kaurenoic acid oxidase, catalyzes three steps of the gibberellin biosynthesis pathway. Proceedings of the National Academy of Sciences. 98 (4), 2065-2070 (2001).
- Gutierrez, R., Quiroz-Figueroa, F., Vazquez-Ramos, J. M. Maize cyclin D2 expression, associated kinase activity and effect of phytohormones during germination. Plant and Cell Physiology. 46 (1), 166-173 (2005).
- Atkinson, J. A., Wells, D. M. An updated protocol for high throughput plant tissue sectioning. Frontiers in Plant Science. 8, 1721 (2017).
- Lux, A., Morita, S., Abe, J., Ito, K. An improved method for clearing and staining free-hand sections and whole-mount samples. Annals of Botany. 96 (6), 989-996 (2005).
- Heriche, M., Arnould, C., Wipf, D., Courty, P. E. Imaging plant tissues: Advances and promising clearing practices. Trends in Plant Science. 27 (6), 601-615 (2022).
- Kurihara, D., Mizuta, Y., Sato, Y., Higashiyama, T. ClearSee: A rapid optical clearing reagent for whole-plant fluorescence imaging. Development. 142 (23), 4168-4179 (2015).
- Chuck, G., Muszynski, M., Kellogg, E., Hake, S., Schmidt, R. J. The control of spikelet meristem identity by the branched silkless1 gene in maize. Science. 298 (5596), 1238-1241 (2002).
- Tran, T. M., et al. An optimized whole-mount immunofluorescence method for shoot apices. Current Protocols. 1 (4), e101 (2021).
- O’Connor, D. L. PINs Lost and PINs Gained: Auxin-Transport Mediated Patterning in the Grasses. University of California, Berkeley. , (2012).
- Sharman, B. C., Hitch, P. A. Initiation of procambial strands in leaf primordia of bread wheat, Triticum aestivum L. Annals of Botany. 31 (2), 229-243 (1967).
- Serra, L., Tan, S., Robinson, S., Langdale, J. A. Flip-flap: A simple dual-view imaging method for 3D reconstruction of thick plant samples. Plants. 11 (4), 506 (2022).
- Colin, L., et al. Imaging the living plant cell: From probes to quantification. The Plant Cell. 34 (1), 247-272 (2022).

