Forbedrede metoder til forberedelse af tværsnit og valsede hele monteringer af majsbladprimordia til fluorescens og konfokal billeddannelse
Summary
Majsbladprimordia er dybt beklædt og rullet, hvilket gør dem vanskelige at studere. Her præsenterer vi metoder til forberedelse af tværsnit og udrullede hele monteringer af majsbladprimordier til fluorescens og konfokal billeddannelse.
Abstract
I majs (Zea mays) og andre græsser (Poaceae) er bladprimordierne dybt beklædt og rullet i bladhvirvlen, hvilket gør det vanskeligt at studere tidlig bladudvikling. Her beskriver vi metoder til forberedelse af tværsnit og udrullede hele monteringer af majsbladprimordia til fluorescens og konfokal billeddannelse. Den første metode bruger en trådfjerner til at fjerne de øverste dele af ældre blade, udsætte spidsen af bladprimordium og tillade dens måling for mere nøjagtig tværsnitsprøveudtagning. Den anden metode bruger klar, dobbeltsidet nanotape til at rulle ud og montere helbladet primordia til billeddannelse. Vi viser nytten af de to metoder til at visualisere og analysere fluorescerende proteinreportere i majs. Disse metoder giver en løsning på udfordringerne ved den karakteristiske morfologi af majsbladprimordia og vil være nyttige til at visualisere og kvantificere bladanatomiske og udviklingsmæssige træk i majs og andre græsarter.
Introduction
Græsafgrøder er en vigtig kilde til mad og biobrændstof til den globale befolkning1, og forbedring af bladanatomi har potentialet til at øge deres produktivitet 2,3. Vores nuværende forståelse af, hvordan bladanatomi reguleres i græsser, er imidlertid begrænset4 og kræver analyse af bladprimordia, da mange anatomiske og fysiologiske træk ved bladet er forudbestemt tidligt i udviklingen 5,6,7. Cellulære billeddannelsesteknikker, såsom fluorescens og konfokal billeddannelse, er uundværlige for at studere græsbladanatomi og cellulære træk, men disse teknikker er vanskelige at anvende på græsbladprimordia, fordi de er dybt beklædt og rullet i bladhvirvlen. Vi løste dette problem ved at udvikle metoder til forberedelse af tværsnit og udrullede helbladsmonteringer til fluorescens og konfokal analyse af majsbladprimordia, et modelsystem til undersøgelse af græsbladanatomi og udvikling 2,8.
Majsbladet består som alle græsblade af et remlignende blad med en kappe, der vikles rundt om stilken og udvikler skud 9,10,11,12,13. Bladene udvikler sig fra skuddet apikale meristem (SAM) i et distichous mønster, hvor hvert nyt blad starter i den modsatte position af det foregående blad, hvilket resulterer i to rækker blade langs den lodrette akse (figur 1A)14 . Udviklingsstadiet for hvert bladprimordium identificeres ved dets position i forhold til SAM, med det nærmeste primordium betegnet som plastochron1 (P1) og de følgende primordier betegnet som P2, P3 osv. (figur 1B, C)2. Under udviklingen (figur 1D) fremstår bladprimordiet først som en halvmåneformet støttepille omkring bunden af SAM (P1) og vokser derefter til et hætteformet primordium, der strækker sig over meristemet (P2)9,10,11. Emhættens basale margener udvider sig derefter sideværts og overlapper hinanden, når spidsen vokser opad og danner et kegleformet primordium (P3-P5)10. Primordiet vokser derefter hurtigt i længden, og kappe-bladgrænsen ved bunden bliver mere fremtrædende med dannelsen af ligule, den frynselignende fremspring på bladets adaxiale side (P6/P7). Endelig ruller bladet ud, når det kommer ud af hvirvlen under steady-state vækst, hvor de delende celler er begrænset inden for bladets lille basale område og danner en gradient med ekspanderende og differentierende celler langs den proksimale-distale akse (P7 / P8)15. Skudspidsen af en majsplante indeholder flere primordia på forskellige udviklingsstadier, hvilket gør den til en fremragende model til at studere bladudvikling8.
Nøjagtig analyse af tidlig bladudvikling kræver iscenesættelse eller brug af standardiserede kriterier til at definere forskellige stadier af primordiumudvikling i forhold til andre vækst- eller morfologiske parametre. Fordi bladprimordierne er skjult i græsskuddet, bruger efterforskere typisk parametre som plantens alder eller størrelsen af de nye blade som forudsigere for stadierne og størrelserne af bladet primordia 9,16. I majs bestemmes plantens kronologiske alder enten af antallet af dage efter plantning eller spiring (DAP/DAG)17,18. Det vegetative stadium (V-trin) bestemmes af det øverste blad med en synlig krave, en lys linje på den abaxiale side mellem bladet og kappen, der svarer til positionen af ligule og aurikler, et par kileformede regioner ved bunden af bladet (figur 1A, B) 17,19 . Mellem 20 og 25 DAG overgår SAM til et blomsterstandmeristem og ophører med at producere nye blade20. Vækstraterne for majsbladprimordia kan variere afhængigt af miljøet og plantens genotype. Af denne grund kan plantens alder og størrelsen af de nye blade ikke nøjagtigt forudsige størrelsen af bladprimordia; Brug af disse parametre kan dog hjælpe med at forudsige rækkevidden af Primordia-stadier og -størrelser til eksperimentelle formål.
Tværsnitsanalyse er en populær metode til undersøgelse af bladanatomi og udvikling i majs og andre græsser, fordi det giver mulighed for prøveudtagning af flere plastokroner i en enkelt sektion på tværs af skuddet21,22,23. Denne metode er også praktisk til cellulær billeddannelse af friske prøver, da de omgivende blade fungerer som et stillads, der holder bladets primordia på plads under sektionering og montering24. En ulempe ved denne metode er imidlertid, at det kan være udfordrende præcist at lokalisere målplastochronen og regionen inden for primordium, når man sektionerer fra et intakt skud. Da bladvæksten varierer på tværs af plastokroner og langs den proksimale-distale akse2,5, kan upræcis prøveudtagning resultere i en forkert fortolkning af primordiumets udviklingsstadium og region i et givet afsnit. Derfor er udvikling af en metode til præcis tværsnitsprøvetagning afgørende for at sikre nøjagtigheden og reproducerbarheden af anatomiske og udviklingsmæssige analyser af græsbladprimordia.
Helbladsmonteringsanalyse muliggør omfattende og integrativ undersøgelse af vævs- og cellulære processer, der forekommer på helorganskala, såsom proliferativ vækst25 og venemønster26,27,28. Metoden giver et paradermalt overblik over bladet, hvilket gør det muligt at opdage forskellige processer og mønstre, der ellers ville være vanskelige at opdage ved hjælp af tværsnitsanalyse24,27. I modsætning til i Arabidopsis, hvor der allerede findes etablerede metoder til billeddannelse af helbladsmonteringer29,30, findes der i øjeblikket ingen standardmetode til billeddannelse af rullet helbladsmontering i græsser. En tidligere protokol for udrullning af isolerede majsblade primordia involverede usædvanlige materialer og var ikke egnet til cellulær billeddannelse31. Avancerede billeddannelsesteknikker, såsom computertomografi (CT) og magnetisk resonansbilleddannelse (MR), kan erhverve 3D anatomisk information uden at isolere og udrulle primordia 11,32,33, men de er dyre og kræver specialudstyr. Udvikling af en teknik til at overvinde de begrænsninger, der er pålagt af den valsede og koniske morfologi af bladprimordia i majs og andre græsser, ville fremme undersøgelser af deres anatomiske og udviklingsmæssige træk.
Her præsenterer vi metoder til forberedelse af tværsnit og udrullede hele monteringer af majsbladprimordier til fluorescens og konfokal billeddannelse. Vi brugte disse metoder til at kvantificere veneantal og kortlægge den rumlige-temporale hormonfordeling i majsbladprimordia med fluorescerende proteiner (FP’er)24. Den første metode går ud på at fjerne den øverste del af ældre blade fra majsplanter med en trådfjerner (figur 1E). Ved at eksponere spidsen af primordium (P5-P7) bliver det muligt at bestemme dens længde uden helt at skulle fjerne de ældre omgivende blade, hvilket muliggør nem og præcis sektionering. Den anden metode involverer udrulning og montering af helbladet primordia (P3-P7) med klar, dobbeltsidet nanotape (figur 1F). Disse metoder er egnede til visualisering af forskellige FP’er24, men har brug for optimering til brug af fluorescerende farvestoffer og rydningsreagenser. Derudover skitserer vi nogle procedurer for samkopiering af z-stakke, syning af billeder og sammenlægning af kanaler i ImageJ/FIJI34, som gælder for de billeder, der produceres ved hjælp af de to metoder. Disse metoder er nyttige til rutinemæssig fluorescens eller konfokal billeddannelse af majsblade, men de kan også tilpasses til andre modelgræsarter, såsom ris, Setaria og Brachypodium.
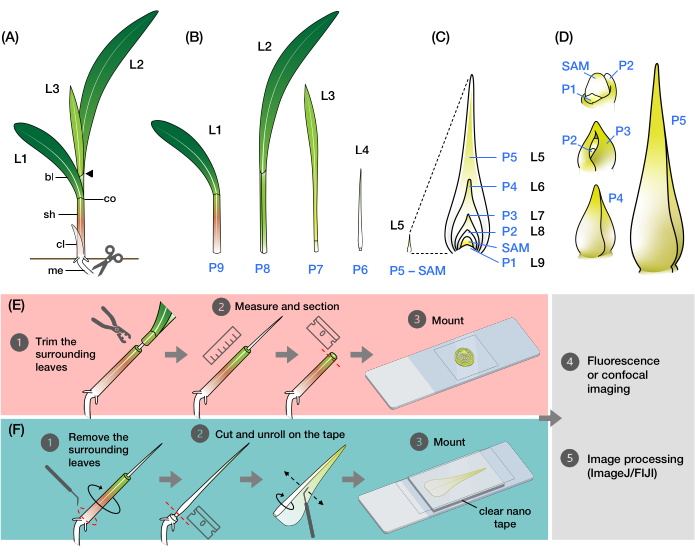
Figur 1: Organisation og morfologi af majsbladprimordia og oversigt over metoderne. A) Skematisk gengivelse af en majsplante. Majs har en distichous phyllotaxy, hvor det nye blad starter i den modsatte position af det forrige blad. Bladnummeret angiver den kronologiske rækkefølge, hvori bladene opstod ved spiring (dvs. første blad, L1; andet blad, L2; tredje blad, L3 osv.). Hvert blad har et distalt blad og en basalkappe afgrænset af en krave, der svarer til ligule og auricle. Det øverste blad med kraven synlig angiver det vegetative stadium. Frøplanten i dette eksempel er på V2-stadiet, med L2-kraven (pilespids) synlig. Saksikonet angiver placeringen ved mesocotyl (mig), hvor frøplanten skal skæres for at blive indsamlet. (B) Skematisk gengivelse af det dissekerede skud, der viser isoleret L1 til L4, med bladet primordia L5 til L9 vist som et forstørret billede i (C). Plastochrontallet angiver primordiumets position i forhold til SAM, med det yngste bladprimordium (P1) tættest på SAM og det ældre bladprimordia (P2, P3, P4 osv.) successivt længere væk2. D) Skematisk gengivelse af morfologien af majsbladprimordia fra P1 til P5. E) Skematisk oversigt over metoden til tværsnitsanalyse af majsbladets primordia. (1) Trim de ældre blade med en trådfjerner. (2) Mål primordium og snit skuddet. (3) Monter sektionen på et dias til billeddannelse og behandling (4, 5). F) Skematisk oversigt over metoden til helmonteringsanalyse af majsbladets primordia. (1) Fjern de omgivende blade for at ekstrahere primordium. (2) Klip og rul primordium fladt ud på nanobåndet. (3) Monter prøven til billeddannelse og behandling (4, 5). Forkortelser: L = blad; bl = blad; sh = kappe; co = krave; mig = mesocotyl; V = vegetativ; P = plastochron; SAM = skyd apikal meristem. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Vi præsenterer to metoder til fremstilling af majsbladprimordia til cellulær billeddannelse. Den første metode (protokolafsnit 2) tillader måling af primordium til tværsnitsanalyse, mens den anden metode (protokolafsnit 3) muliggør udrullning og udfladning af primordium til helmonteret analyse. Disse metoder letter cellulær billeddannelse af FP’er i majsbladprimordia24 (som vist i figur 4 og figur 5) og giver enkle løsninger på udfordringerne ved billeddannelse af majsblade. Protokolafsnit 2 reducerer dissektionstiden og forbedrer prøveudtagningsnøjagtigheden ved at måle primordierne før sektionering i stedet for udelukkende at stole på iscenesættelsesparametre 9,16. Med kommercielt tilgængelig nanotape løser protokolafsnit 3 det mangeårige problem med billeddannelse af helbladet primordia i majs. Denne protokol forbedrer den tidligere metode, der brugte dialyserør 31, og er et meget billigere alternativ til CT og MR11,32,33. Men når det kommer til at visualisere bladanatomiske træk og producere optimale resultater, har begge protokoller nogle begrænsninger, som er skitseret i tabel 2 og diskuteres mere detaljeret nedenfor.
I protokolafsnit 2 stødte vi på vanskeligheder med at visualisere cellekonturer i tykke tværsnit af bladprimordia, og modfarvning med cellevægs- eller plasmamembranbindende fluorescerende farvestoffer gav ikke tilfredsstillende resultater. For eksempel gav FM 4-64 suboptimale resultater sammenlignet med plasmamembranens FP-markør, p Zm PIP2-1::ZmPIP2-1:CFP39 (PIP2-1-CFP; Figur 3A-D). For at overvinde denne begrænsning anbefaler vi at bruge et vibratomt til at producere tyndere vævssektioner (~ 0,1 mm)58, hvilket giver mulighed for en levende lysfeltbilleddannelse af cellekonturer eller optimering af modfarvningsprotokollen 47,59.
I protokolafsnit 3 er hovedbegrænsningen vanskeligheden ved at montere bladet uden at rive, beskadige eller luftbobler, som beskrevet i protokoltrin 3.2.5-3.2.6 (figur 3E-K). Da majsbladet er bilateralt symmetrisk, kan et halvbladsbeslag snarere end et helbladsbeslag være tilstrækkeligt til visualisering9. For at gøre dette kan primordium skæres med et barberblad langs længdeaksen efter udrullning op til midrib, så kun halvdelen af bladet kan monteres. En anden begrænsning i protokolafsnit 3 er, at bladets tykkelse kan begrænse fluoroforsignalets optiske opløsning under dyb billeddannelse. For at løse dette problem er det muligt at anvende en vævsrensningsteknik60. Vi fandt imidlertid, at ClearSee61, et almindeligt anvendt clearingreagens til billeddannelse af plantevæv, ikke er kompatibelt med protokollen, fordi det får prøven og dækslet til at løsne sig fra nanobåndet. En mulig løsning på dette problem kunne være at påføre en semipermeabel membran31 over bladprøven, så den kan behandles med clearingopløsningen, mens den holdes på plads af nanobåndet. En sådan metode, der gør det muligt at anvende flydende opløsninger på det uvalsede blad, kunne også anvendes til helmonteret RNA in situ-hybridisering og immunlokaliseringsteknikker, som tidligere er optimeret til udvikling af majsblomsterstande, men ikke til helbladet primordia62,63.
Vi beskrev protokoller for majs, som har store blade primordia selv på frøplantestadiet. Andre græsarter med meget mindre blade primordia, såsom ris, byg, hvede, Setaria og Brachypodium 16,23,64,65,66, kan kræve brug af yderligere præcisionsværktøjer for effektivt at anvende disse protokoller. Desuden var disse protokoller ikke beregnet til levende cellebilleddannelse, som fanger dynamiske processer i realtid med vævsdannelse og cellulære reaktioner. Men efterhånden som fluorescerende sonder, billeddannelsesteknologier og computerkapacitet fortsætter med at udvikle sig inden for levende cellebilleddannelse til planter67, kan fremtidig forskning bygge videre på disse protokoller for at udvikle levende cellebilleddannelsesstrategier, der er skræddersyet til de unikke egenskaber ved græsbladprimordia.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne vil gerne takke Maize Genetics Cooperation, Maize Cell Genomics Project, Dave Jackson (Cold Spring Harbor Laboratory, NY), Anne W. Sylvester (Marine Biological Laboratory, University of Chicago, IL), Andrea Gallavotti (Rutgers University, NJ) og Carolyn G. Rasmussen (University of California, Riverside) for at levere de mutante og transgene bestande samt Robert F. Baker og Alexander Jurkevich fra Advanced Light Microscopy Core ved University of Missouri-Columbia for deres hjælp med konfokal mikroskopi. JMR blev støttet af J. William Fulbright Fellowship, Diane P. og Robert E. Sharp Fund og National Science Foundation’s Plant Genome Research Program (IOS-1546873) til PM. CDTC, CMRV, EDCDP og RJRR støttes af Ateneo College Scholarship Program. CDTC, EDCDP og RJRR understøttes af DOST-SEI S&T Undergraduate Scholarship. DODL støttes af Fr. Thomas Steinbugler SJ Academic Scholarship. RJRR understøttes af Aiducation International – Pathways to Higher Education Scholarship. Dette arbejde blev støttet af School of Science and Engineering og Rizal Library, Ateneo de Manila University.
Materials
| Acrylic Gel Clear Double Sided Nano Tape 16.5 ft x 1.2 in, 2 mm thick | EZlifego Store (Amazon) | B07YB1ZXG6 | 1 roll |
| Bellucci Pick Curved micro probe 16.8 cm, 6.6 in | Bausch & Lomb | N1692 9 | 1 pc |
| Clayman guide microprobe Sinskey hook angled shaft, 11.6 cm, 4.6 in | Storz Opthalmic Instruments | E0542 | 1 pc |
| Dental Probe, Bent Needle, 14 cm (5.5 in) | Ted Pella | 13553 | 1 pc |
| DOWELL 10-22 AWG Wire Stripper | Dowell Store (Amazon) | 10-22 AWG | 1 pc |
| Feather Double Edge Carbon Steel Blades | Ted Pella | 121-9 | pkg/10; for fine sectioning |
| Frosted End Glass Microscope Slides, 75 mm x 25 mm x 1-1.2 mm | Ted Pella | 260442 | pkg/144 |
| GEM Single Edge, Stainless Steel Uncoated Blades | Ted Pella | 121-1 | box/200; for general cutting/sectioning |
| Glycerol | Thermo Scientific | PI17904 | 1 liter |
| ImageJ/FIJI with EDF plugin (version 17.05.2021) and Grid/Collection Stitching plugin | National Institutes of Health (NIH) USA | version 2.9.0/1.54s | The EDF plugin was developed by Alex Prudencio, Jesse Berent, and Daniel Sage for the Biomedical Imaging Group, École Polytechnique Fédérale de Lausanne (EPFL; http://bigwww.epfl.ch/demo/edf/). The grid/collection stitching software was developed by Stephan Preibisch for the Max Planck Institute of Molecular Cell Biology and Genetics (MPI-CBG). |
| Kimwipes Ex-L Small 111.76 mm x 213.36 mm | Kimtech Science | 34155 | box/280 ply |
| Micro Cover Glasses, 22 mm x 22 mm x 0.13 – 0.16 mm thick | Ted Pella | 260140 | 1 ounce |
| PU Gel Clear Double Sided Nano Tape 29.5 ft x 1.18 in, 1 mm thick | Yecaye Store (Amazon) | L354 W1.18 | 2 rolls |
| Superslip Cover Glasses, 24 mm x 50 mm x 0.13 – 0.16 mm thick | Ted Pella | 260166 | 1 ounce |
| Superslip Cover Glasses, 24 mm x 60 mm x 0.13 – 0.16 mm thick | Ted Pella | 260168 | 1 ounce |
| Tempered Glass Cutting Board | Hacaroa (Amazon) | B09XMXBT5S | 4 pc |
References
- McSteen, P., Kellogg, E. A. Molecular, cellular, and developmental foundations of grass diversity. Science. 377 (6606), 599-602 (2022).
- Wang, P., Vlad, D., Langdale, J. A. Finding the genes to build C4 rice. Current Opinion in Plant Biology. 31, 44-50 (2016).
- Wang, P., et al. Candidate regulators of early leaf development in maize perturb hormone signalling and secondary cell wall formation when constitutively expressed in rice. Scientific Reports. 7 (1), 4535 (2017).
- Perico, C., Tan, S., Langdale, J. A. Developmental regulation of leaf venation patterns: Monocot versus eudicots and the role of auxin. New Phytologist. 234 (3), 783-803 (2022).
- Wang, P., Kelly, S., Fouracre, J. P., Langdale, J. A. Genome-wide transcript analysis of early maize leaf development reveals gene cohorts associated with the differentiation of C4 Kranz anatomy. The Plant Journal. 75 (4), 656-670 (2013).
- Liu, W. Y., et al. Regulators of early maize leaf development inferred from transcriptomes of laser capture microdissection (LCM)-isolated embryonic leaf cells. Proceedings of the National Academy of Sciences. 119 (35), e2208795119 (2022).
- Liu, W. Y., et al. Anatomical and transcriptional dynamics of maize embryonic leaves during seed germination. Proceedings of the National Academy of Sciences. 110 (10), 3979-3984 (2013).
- Strable, J., Nelissen, H. The dynamics of maize leaf development: Patterned to grow while growing a pattern. Current Opinion in Plant Biology. 63, 102038 (2021).
- Reynolds, J. O., Eisses, J. F., Sylvester, A. W. Balancing division and expansion during maize leaf morphogenesis: Analysis of the mutant, warty-1. Development. 125 (2), 259-268 (1998).
- Richardson, A. E., et al. Evolution of the grass leaf by primordium extension and petiole-lamina remodeling. Science. 374 (6573), 1377-1381 (2021).
- Johnston, R., Leiboff, S., Scanlon, M. J. Ontogeny of the sheathing leaf base in maize (Zea mays). New Phytologist. 205 (1), 306-315 (2015).
- Sharman, B. C. Developmental anatomy of the shoot of Zea mays L. Annals of Botany. 6 (22), 245-282 (1942).
- Johnston, R., et al. Transcriptomic analyses indicate that maize ligule development recapitulates gene expression patterns that occur during lateral organ initiation. The Plant Cell. 26 (12), 4718-4732 (2014).
- Sharman, B. C. Leaf and bud initiation in the Gramineae. Botanical Gazette. 106 (3), 269-289 (1945).
- Nelissen, H., et al. A local maximum in gibberellin levels regulates maize leaf growth by spatial control of cell division. Current Biology. 22 (13), 1183-1187 (2012).
- Itoh, J., et al. Rice plant development: From zygote to spikelet. Plant and Cell Physiology. 46 (1), 23-47 (2005).
- Ritchie, S. W., Hanway, J. J., Benson, G. O. How a corn plant develops. Iowa State University of Science and Technology. , (1986).
- Freeling, M., Walbot, V. . The Maize Handbook. , (2013).
- Freeling, M., Hake, S. Developmental genetics of mutants that specify knotted leaves in maize. Genetics. 111 (3), 617-634 (1985).
- Durbak, A. R., et al. Transport of boron by the tassel-less1 aquaporin is critical for vegetative and reproductive development in maize. The Plant Cell. 26 (7), 2978-2995 (2014).
- Langdale, J. A., Lane, B., Freeling, M., Nelson, T. Cell lineage analysis of maize bundle sheath and mesophyll cells. Developmental Biology. 133 (1), 128-139 (1989).
- Bosabalidis, A. M., Evert, R. F., Russin, W. A. Ontogeny of the vascular bundles and contiguous tissues in the maize leaf blade. American Journal of Botany. 81 (6), 745-752 (1994).
- Junqueira, N. E. G., et al. Anatomy and ultrastructure of embryonic leaves of the C4 species Setaria viridis. Annals of Botany. 121 (6), 1163-1172 (2018).
- Robil, J. M., McSteen, P. Hormonal control of medial-lateral growth and vein formation in the maize leaf. New Phytologist. 238 (1), 125-141 (2023).
- Donnelly, P. M., Bonetta, D., Tsukaya, H., Dengler, R. E., Dengler, N. G. Cell cycling and cell enlargement in developing leaves of Arabidopsis. Developmental Biology. 215 (2), 407-419 (1999).
- Govindaraju, P., Verna, C., Zhu, T., Scarpella, E. Vein patterning by tissue-specific auxin transport. Development. 147 (13), (2020).
- Linh, N. M., Scarpella, E. Leaf vein patterning is regulated by the aperture of plasmodesmata intercellular channels. PLoS Biology. 20 (9), e3001781 (2022).
- Verna, C., Ravichandran, S. J., Sawchuk, M. G., Linh, N. M., Scarpella, E. Coordination of tissue cell polarity by auxin transport and signaling. eLife. 8, e51061 (2019).
- Sawchuk, M. G., Head, P., Donner, T. J., Scarpella, E. Time-lapse imaging of Arabidopsis leaf development shows dynamic patterns of procambium formation. New Phytologist. 176 (3), 560-571 (2007).
- Linh, N. M., Scarpella, E. Confocal imaging of developing leaves. Current Protocols. 2 (1), e349 (2022).
- Poethig, R. S., Szymkowiak, E. J. Clonal analysis of leaf development in maize. Maydica. 40, 67-76 (1995).
- Sprangers, K., Thys, S., van Dusschoten, D., Beemster, G. T. S. Gibberellin enhances the anisotropy of cell expansion in the growth zone of the maize leaf. Frontiers in Plant Science. 11, 1163 (2020).
- Tsuda, K., et al. KNOTTED1 cofactors, BLH12 and BLH14, regulate internode patterning and vein anastomosis in maize. The Plant Cell. 29 (5), 1105-1118 (2017).
- Schindelin, J., et al. FIJI: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Plant Care Protocols – Maize. The Donald Danforth Plant Science Center’s Plant Growth Facility Available from: https://www.danforthcenter.org/our-work/core-facilities/plant-growth/ (2019)
- Mir, R., et al. A DII domain-based auxin reporter uncovers low auxin signaling during telophase and early G1. Plant Physiology. 173 (1), 863-871 (2017).
- DeBlasio, S. L., Sylvester, A. W., Jackson, D. Illuminating plant biology: Using fluorescent proteins for high-throughput analysis of protein localization and function in plants. Briefings in Functional Genomics. 9 (2), 129-138 (2010).
- Wu, Q., Luo, A., Zadrozny, T., Sylvester, A., Jackson, D. Fluorescent protein marker lines in maize: Generation and applications. The International Journal of Developmental Biology. 57 (6-8), 535-543 (2013).
- Mohanty, A., et al. Advancing cell biology and functional genomics in maize using fluorescent protein-tagged lines. Plant Physiology. 149 (2), 601-605 (2009).
- Baker, R. F., et al. Sucrose transporter ZmSut1 expression and localization uncover new insights into sucrose phloem loading. Plant Physiology. 172 (3), 1876-1898 (2016).
- Gallavotti, A., Yang, Y., Schmidt, R. J., Jackson, D. The relationship between auxin transport and maize branching. Plant Physiology. 147 (4), 1913-1923 (2008).
- Krishnakumar, V., et al. A maize database resource that captures tissue-specific and subcellular-localized gene expression, via fluorescent tags and confocal imaging (Maize Cell Genomics Database). Plant and Cell Physiology. 56 (1), 12 (2015).
- Snapp, E. L. Fluorescent proteins: A cell biologist’s user guide. Trends in Cell Biology. 19 (11), 649-655 (2009).
- Geng, Y., Zhou, Y. Confocal live imaging of shoot apical meristems from different plant species. Journal of Visualized Experiments. (145), e59369 (2019).
- Stanislas, T., Hamant, O., Traas, J. In-vivo analysis of morphogenesis in plants. Methods in Cell Biology. 139, 203-223 (2017).
- Fodor, E., Ayaydin, F. Fluorescent probes and live imaging of plant cells. Advances in Plant Ecophysiology Techniques. , 241-251 (2018).
- Grandjean, O., et al. In vivo analysis of cell division, cell growth, and differentiation at the shoot apical meristem in Arabidopsis. The Plant Cell. 16 (1), 74-87 (2004).
- Conklin, P. A., Johnston, R., Conlon, B. R., Shimizu, R., Scanlon, M. J. Plant homeodomain proteins provide a mechanism for how leaves grow wide. Development. 147 (20), (2020).
- Shaw, S. L. Imaging the live plant cell. The Plant Journal. 45 (4), 573-598 (2006).
- Klaus, A. V., Schawaroch, V., Frischmann, K. J. Confocal imaging and three-dimensional visualization of thick autofluorescent specimens. Methods in Molecular Biology. 1075, 213-225 (2014).
- Forster, B., Van De Ville, D., Berent, J., Sage, D., Unser, M. Extended depth-of-focus for multi-channel microscopy images: a complex wavelet approach. 2004 2nd IEEE International Symposium on Biomedical Imaging: Nano to Macro (IEEE Cat No. 04EX821). IEEE. , 660-663 (2004).
- Preibisch, S., Saalfeld, S., Tomancak, P. Globally optimal stitching of tiled 3D microscopic image acquisitions. Bioinformatics. 25 (11), 1463-1465 (2009).
- Phillips, K. A., et al. vanishing tassel2 encodes a grass-specific tryptophan aminotransferase required for vegetative and reproductive development in maize. The Plant Cell. 23 (2), 550-566 (2011).
- Robil, J. M., et al. GrasVIQ: An image analysis framework for automatically quantifying vein number and morphology in grass leaves. The Plant Journal. 107 (2), 629-648 (2021).
- Helliwell, C. A., Chandler, P. M., Poole, A., Dennis, E. S., Peacock, W. J. The CYP88A cytochrome P450, ent-kaurenoic acid oxidase, catalyzes three steps of the gibberellin biosynthesis pathway. Proceedings of the National Academy of Sciences. 98 (4), 2065-2070 (2001).
- Gutierrez, R., Quiroz-Figueroa, F., Vazquez-Ramos, J. M. Maize cyclin D2 expression, associated kinase activity and effect of phytohormones during germination. Plant and Cell Physiology. 46 (1), 166-173 (2005).
- Atkinson, J. A., Wells, D. M. An updated protocol for high throughput plant tissue sectioning. Frontiers in Plant Science. 8, 1721 (2017).
- Lux, A., Morita, S., Abe, J., Ito, K. An improved method for clearing and staining free-hand sections and whole-mount samples. Annals of Botany. 96 (6), 989-996 (2005).
- Heriche, M., Arnould, C., Wipf, D., Courty, P. E. Imaging plant tissues: Advances and promising clearing practices. Trends in Plant Science. 27 (6), 601-615 (2022).
- Kurihara, D., Mizuta, Y., Sato, Y., Higashiyama, T. ClearSee: A rapid optical clearing reagent for whole-plant fluorescence imaging. Development. 142 (23), 4168-4179 (2015).
- Chuck, G., Muszynski, M., Kellogg, E., Hake, S., Schmidt, R. J. The control of spikelet meristem identity by the branched silkless1 gene in maize. Science. 298 (5596), 1238-1241 (2002).
- Tran, T. M., et al. An optimized whole-mount immunofluorescence method for shoot apices. Current Protocols. 1 (4), e101 (2021).
- O’Connor, D. L. PINs Lost and PINs Gained: Auxin-Transport Mediated Patterning in the Grasses. University of California, Berkeley. , (2012).
- Sharman, B. C., Hitch, P. A. Initiation of procambial strands in leaf primordia of bread wheat, Triticum aestivum L. Annals of Botany. 31 (2), 229-243 (1967).
- Serra, L., Tan, S., Robinson, S., Langdale, J. A. Flip-flap: A simple dual-view imaging method for 3D reconstruction of thick plant samples. Plants. 11 (4), 506 (2022).
- Colin, L., et al. Imaging the living plant cell: From probes to quantification. The Plant Cell. 34 (1), 247-272 (2022).

