Forbedrede metoder for fremstilling av tverrsnitt og utrullede hele fester av maisbladprimordia for fluorescens og konfokal avbildning
Summary
Maisbladprimordia er dypt innhyllet og rullet, noe som gjør dem vanskelige å studere. Her presenterer vi metoder for å forberede tverrsnitt og utrullede hele fester av maisbladprimordia for fluorescens og konfokal avbildning.
Abstract
I mais (Zea mays) og andre gress (Poaceae) er bladprimordiene dypt innhyllet og rullet i bladhvirvelen, noe som gjør det vanskelig å studere tidlig bladutvikling. Her beskriver vi metoder for fremstilling av tverrsnitt og utrullede hele fester av maisbladprimordia for fluorescens og konfokal avbildning. Den første metoden bruker en trådstripper for å fjerne de øvre delene av eldre blader, utsette spissen av bladprimordium og tillate måling for mer nøyaktig tverrsnittprøvetaking. Den andre metoden bruker klar, dobbeltsidig nanotape for å rulle ut og montere helbladprimordia for avbildning. Vi viser nytten av de to metodene for å visualisere og analysere fluorescerende proteinreportere i mais. Disse metodene gir en løsning på utfordringene som den særegne morfologien til maisbladprimordia gir, og vil være nyttige for å visualisere og kvantifisere bladets anatomiske og utviklingsmessige egenskaper hos mais og andre gressarter.
Introduction
Gressavlinger er en viktig kilde til mat og biodrivstoff for den globale befolkningen1, og forbedring av bladanatomi har potensial til å øke produktiviteten 2,3. Vår nåværende forståelse av hvordan bladanatomi reguleres i gress er imidlertid begrenset4 og krever analyse av bladprimordia, da mange anatomiske og fysiologiske egenskaper ved bladet er forhåndsbestemt tidlig i utviklingen 5,6,7. Cellulære bildebehandlingsteknikker, som fluorescens og konfokal avbildning, er uunnværlige for å studere gressbladanatomi og cellulære egenskaper, men disse teknikkene er vanskelige å bruke på gressbladprimordia fordi de er dypt omsluttet og rullet i bladhvirvelen. Vi løste dette problemet ved å utvikle metoder for å forberede tverrsnitt og utrullede helbladfester for fluorescens og konfokal analyse av maisbladprimordia, et modellsystem for å studere gressbladanatomi og utvikling 2,8.
Maisbladet, som alle gressblader, består av et stroppelignende blad med en kappe som vikler seg rundt stilken og utvikler skudd 9,10,11,12,13. Bladene utvikler seg fra skuddet apikale meristem (SAM) i et distichous mønster, hvor hvert nytt blad starter i motsatt posisjon av det forrige bladet, noe som resulterer i to rekker av blader langs den vertikale aksen (figur 1A) 14 . Utviklingsstadiet til hvert bladprimordium identifiseres ved dets posisjon i forhold til SAM, med nærmeste primordium betegnet som plastochron1 (P1) og følgende primordia betegnet som P2, P3 og så videre (figur 1B, C) 2. Under utviklingen (figur 1D) vises bladprimordiet først som en halvmåneformet støtte rundt bunnen av SAM (P1), og vokser deretter til et hetteformet primordium som strekker seg over meristem (P2)9,10,11. De basale kantene av hetten ekspanderer deretter sideveis og overlapper hverandre når spissen vokser oppover og danner et kjegleformet primordium (P3-P5)10. Primordium vokser da raskt i lengde, og slirebladgrensen ved basen blir mer fremtredende med dannelsen av ligulen, den frynselignende projeksjonen på bladets adaksiale side (P6/P7). Til slutt ruller bladet ut når det kommer ut av hvirvelen under steady-state vekst, hvor de delende cellene er begrenset innenfor den lille basale regionen av bladet, og danner en gradient med ekspanderende og differensierende celler langs den proksimal-distale aksen (P7 / P8) 15. Skuddspissen til en maisplante inneholder flere primordier på forskjellige utviklingsstadier, noe som gjør den til en utmerket modell for å studere bladutvikling8.
Nøyaktig analyse av tidlig bladutvikling krever staging eller bruk av standardiserte kriterier for å definere forskjellige stadier av primordiumutvikling i forhold til andre vekst- eller morfologiske parametere. Fordi bladprimordiene er skjult i gressskuddet, bruker forskere vanligvis parametere som plantens alder eller størrelsen på de fremvoksende bladene som prediktorer for stadiene og størrelsene på bladprimordia 9,16. I mais bestemmes plantens kronologiske alder enten av antall dager etter planting eller spiring (DAP/DAG)17,18. Det vegetative stadiet (V-trinnet) bestemmes av det øverste bladet med en synlig krage, en blek linje på den abaksiale siden mellom bladet og skjeden som tilsvarer posisjonen til ligule og auriklene, et par kileformede områder ved bunnen av bladet (figur 1A,B)17,19 . Mellom 20 og 25 DAG går SAM over i en blomsterstandsmeristem og slutter å produsere nye blader20. Vekstratene for maisbladprimordia kan variere avhengig av miljøet og genotypen til planten. Av denne grunn kan plantealder og størrelsen på de fremvoksende bladene ikke nøyaktig forutsi størrelsene på bladprimordia; Imidlertid kan bruk av disse parametrene bidra til å forutsi rekkevidden av Primordia-stadier og størrelser for eksperimentelle formål.
Tverrsnittsanalyse er en populær metode for å undersøke bladanatomi og utvikling i mais og andre gress fordi det muliggjør prøvetaking av flere plastokroner i en enkelt seksjon over skuddet21,22,23. Denne metoden er også praktisk for cellulær avbildning av ferske prøver, da de omkringliggende bladene fungerer som et stillas som holder bladprimordia på plass under seksjonering og montering24. En ulempe med denne metoden er imidlertid at det kan være utfordrende å nøyaktig lokalisere målplastokronen og regionen innenfor primordiet ved snitting fra et intakt skudd. Videre, fordi bladveksten varierer mellom plastokroner og langs den proksimal-distale aksen2,5, kan upresis prøvetaking resultere i en feil tolkning av utviklingsstadiet og regionen av primordium i et gitt avsnitt. Derfor er utvikling av en metode for presis tverrsnittsprøvetaking avgjørende for å sikre nøyaktigheten og reproduserbarheten av anatomiske og utviklingsmessige analyser av gressbladprimordia.
Helbladmonteringsanalyse muliggjør omfattende og integrativ undersøkelse av vev og cellulære prosesser som forekommer på hele organskalaen, for eksempel proliferativ vekst25 og venemønster26,27,28. Metoden gir en paradermal oversikt over bladet, slik at det oppdages forskjellige prosesser og mønstre som ellers ville være vanskelig å oppdage ved hjelp av tverrsnittanalyse24,27. I motsetning til i Arabidopsis, hvor det allerede er etablerte metoder for avbildning av helbladfester29,30, er det for tiden ingen standardmetode for avbildning av utrullede helbladfester i gress. En tidligere protokoll for utrulling av isolert maisbladprimordia involverte uvanlige materialer og var ikke egnet for cellulær avbildning31. Avanserte bildebehandlingsteknikker, som computertomografi (CT) og magnetisk resonansavbildning (MRI), kan skaffe 3D-anatomisk informasjon uten å isolere og rulle ut primordia 11,32,33, men de er dyre og krever spesialutstyr. Å utvikle en teknikk for å overvinne begrensningene pålagt av den rullede og koniske morfologien til bladprimordia i mais og andre gress, ville fremme undersøkelser av deres anatomiske og utviklingsmessige egenskaper.
Her presenterer vi metoder for å forberede tverrsnitt og utrullede hele fester av maisbladprimordia for fluorescens og konfokal avbildning. Vi brukte disse metodene til å kvantifisere veneantall og kartlegge den romlige-temporale hormonfordelingen i maisbladprimordia med fluorescerende proteiner (FPs)24. Den første metoden innebærer å fjerne den øvre delen av eldre blader fra maisplanter med en trådstripper (figur 1E). Ved å eksponere spissen av primordium (P5-P7), blir det mulig å bestemme lengden uten å måtte fjerne de eldre omkringliggende bladene helt, og dermed muliggjøre enkel og nøyaktig seksjonering. Den andre metoden innebærer å rulle ut og montere helbladprimordia (P3-P7) med klar, dobbeltsidig nanotape (figur 1F). Disse metodene er egnet for å visualisere forskjellige FPs24, men trenger optimalisering for bruk av fluorescerende fargestoffer og rydding av reagenser. I tillegg skisserer vi noen prosedyrer for sammenslåing av z-stabler, sammenslåing av bilder og sammenslåing av kanaler i ImageJ/FIJI34, som gjelder for bildene produsert av de to metodene. Disse metodene er nyttige for rutinemessig fluorescens eller konfokal avbildning av maisblader, men de kan også tilpasses for andre modellgressarter, som ris, Setaria og Brachypodium.
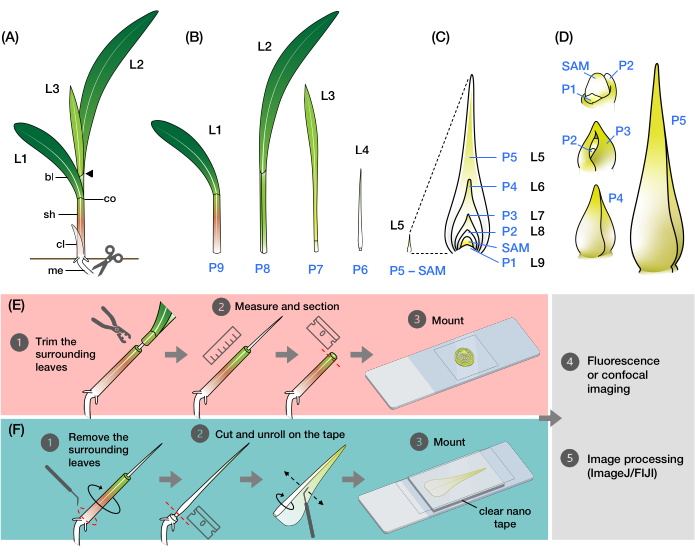
Figur 1: Organisering og morfologi av maisbladprimordier og oversikt over metodene . (A) Skjematisk fremstilling av en maisplante. Mais har en distichous phyllotaxy, med det nye bladet initiere på motsatt posisjon av forrige blad. Bladnummeret angir den kronologiske rekkefølgen som bladene kom fra spiring (dvs. første blad, L1; andre blad, L2; tredje blad, L3; etc.). Hvert blad har et distalt blad og en basal kappe avgrenset av en krage som tilsvarer ligule og auricle. Det øverste bladet med kragen synlig angir vegetativt stadium. Frøplanten i dette eksemplet er på V2-trinnet, med L2-kragen (pilspissen) synlig. Saksikonet indikerer stedet ved mesocotyl (me) der frøplanten må kuttes for å bli samlet. (B) Skjematisk fremstilling av dissekert opptak som viser isolert L1 til L4, med bladet primordia L5 til L9 vist som et forstørret bilde i (C). Gitokrontallet indikerer primordiums posisjon i forhold til SAM, med det yngste bladprimordium (P1) nærmest SAM og det eldre bladprimordiet (P2, P3, P4 og så videre) suksessivt lenger unna2. (D) Skjematisk fremstilling av morfologien til maisbladprimordia fra P1 til P5. (E) Skjematisk oversikt over metoden for tverrsnittsanalyse av maisbladet primordia. (1) Trim de eldre bladene med en trådstripper. (2) Mål primordium og seksjon skytingen. (3) Monter seksjonen på et lysbilde for avbildning og behandling (4, 5). (F) Skjematisk oversikt over metoden for helmontert analyse av maisbladet primordia. (1) Fjern de omkringliggende bladene for å trekke ut primordium. (2) Klipp ut og rull ut primordiumflaten på nanobåndet. (3) Monter prøven for avbildning og behandling (4, 5). Forkortelser: L = blad; bl = blad; sh = skjede; co = krage; meg = mesocotyl; V = vegetativ; P = plastokron; SAM = skyte apikal meristem. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Vi presenterer to metoder for å forberede maisbladprimordia for cellulær avbildning. Den første metoden (protokolldel 2) tillater måling av primordium for tverrsnittanalyse, mens den andre metoden (protokolldel 3) muliggjør utrulling og utflating av primordium for helmonteringsanalyse. Disse metodene letter cellulær avbildning av FPs i maisbladprimordia 24 (som vist i figur 4 og figur 5) og gir enkle løsninger på utfordringene med å avbilde utvikling av maisblader. Protokollseksjon 2 reduserer disseksjonstiden og forbedrer prøvetakingsnøyaktigheten ved å måle primordiene før seksjonering i stedet for å stole utelukkende på stagingparametere 9,16. Med kommersielt tilgjengelig nanotape løser protokollseksjon 3 det langvarige problemet med avbildning av helbladprimordia i mais. Denne protokollen forbedrer den forrige metoden, som brukte dialyserør 31, og er et mye billigere alternativ til CT og MR11,32,33. Men når det gjelder å visualisere bladanatomiske egenskaper og produsere optimale resultater, har begge protokollene noen begrensninger, som er skissert i tabell 2 og diskuteres mer detaljert nedenfor.
I protokolldel 2 opplevde vi problemer med å visualisere cellekonturer i tykke tverrsnitt av bladprimordiene, og motfarging med cellevegg- eller plasmamembranbindende fluorescerende fargestoffer ga ikke tilfredsstillende resultat. For eksempel ga FM 4-64 suboptimale resultater sammenlignet med plasmamembranen FP-markøren, pZmPIP2-1::ZmPIP2-1:CFP39 (PIP2-1-CFP; Figur 3A-D). For å overvinne denne begrensningen anbefaler vi å bruke en vibratome for å produsere tynnere vevsseksjoner (~0,1 mm)58 som vil muliggjøre en levende lysfeltavbildning av cellekonturer eller optimalisere motfargingsprotokollen47,59.
I protokollseksjon 3 er hovedbegrensningen vanskeligheten med å montere bladet uten å rive, skade eller luftbobler, som beskrevet i protokolltrinn 3.2.5-3.2.6 (figur 3E-K). Fordi maisbladet er bilateralt symmetrisk, kan et halvbladfeste i stedet for et helbladfeste være tilstrekkelig for visualisering9. For å gjøre dette kan primordiumet kuttes med et barberblad langs lengdeaksen etter å ha rullet det opp til midribben, slik at bare halvparten av bladet kan monteres. En annen begrensning ved protokollseksjon 3 er at tykkelsen på bladet kan begrense den optiske oppløsningen av fluoroforsignalet under dyp avbildning. For å løse dette problemet er det mulig å bruke en vevsryddingsteknikk60. Vi fant imidlertid ut at ClearSee61, et vanlig brukt clearingreagens for avbildning av plantevev, ikke er kompatibelt med protokollen fordi det får prøven og dekselet til å løsne fra nanobåndet. En potensiell løsning på dette problemet kan være å påføre en semipermeabel membran31 over bladprøven, slik at den kan behandles med ryddeløsningen mens den holdes på plass av nanobåndet. En slik metode som gjør det mulig å bruke flytende løsninger på det utrullede bladet, kan også brukes til helmontert RNA in situ-hybridisering og immunlokaliseringsteknikker, som tidligere har blitt optimalisert for å utvikle maisblomstrer, men ikke for helbladet primordia62,63.
Vi beskrev protokoller for mais, som har store bladprimordier selv på plantestadiet. Andre gressarter med mye mindre bladprimordia, som ris, bygg, hvete, Setaria og Brachypodium 16,23,64,65,66, kan kreve bruk av ekstra presisjonsverktøy for effektivt å anvende disse protokollene. Videre var disse protokollene ikke ment for levende celleavbildning, som fanger sanntids dynamiske prosesser for vevsdannelse og cellulære responser. Men som fluorescerende prober, bildebehandlingsteknologier og databehandlingsevner fortsetter å utvikle seg i levende celleavbildning for planter67, kan fremtidig forskning bygge på disse protokollene for å utvikle levende celleavbildningsstrategier skreddersydd for de unike egenskapene til gressbladprimordia.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne vil gjerne takke Maize Genetics Cooperation, Maize Cell Genomics Project, Dave Jackson (Cold Spring Harbor Laboratory, NY), Anne W. Sylvester (Marine Biological Laboratory, University of Chicago, IL), Andrea Gallavotti (Rutgers University, NJ), og Carolyn G. Rasmussen (University of California, Riverside) for å gi mutante og transgene aksjer, samt Robert F. Baker og Alexander Jurkevich fra Advanced Light Microscopy Core ved University of Missouri-Columbia for deres hjelp med konfokal mikroskopi. JMR ble støttet av J. William Fulbright Fellowship, The Diane P. og Robert E. Sharp Fund, og National Science Foundation’s Plant Genome Research Program (IOS-1546873) til PM. CDTC, CMRV, EDCDP og RJRR støttes av Ateneo College Scholarship Program. CDTC, EDCDP og RJRR støttes av DOST-SEI S&T Undergraduate Scholarship. DODL støttes av Fr. Thomas Steinbugler SJ Academic Scholarship. RJRR støttes av Aiducation International-Pathways to Higher Education Scholarship. Dette arbeidet ble støttet av School of Science and Engineering og Rizal Library, Ateneo de Manila University.
Materials
| Acrylic Gel Clear Double Sided Nano Tape 16.5 ft x 1.2 in, 2 mm thick | EZlifego Store (Amazon) | B07YB1ZXG6 | 1 roll |
| Bellucci Pick Curved micro probe 16.8 cm, 6.6 in | Bausch & Lomb | N1692 9 | 1 pc |
| Clayman guide microprobe Sinskey hook angled shaft, 11.6 cm, 4.6 in | Storz Opthalmic Instruments | E0542 | 1 pc |
| Dental Probe, Bent Needle, 14 cm (5.5 in) | Ted Pella | 13553 | 1 pc |
| DOWELL 10-22 AWG Wire Stripper | Dowell Store (Amazon) | 10-22 AWG | 1 pc |
| Feather Double Edge Carbon Steel Blades | Ted Pella | 121-9 | pkg/10; for fine sectioning |
| Frosted End Glass Microscope Slides, 75 mm x 25 mm x 1-1.2 mm | Ted Pella | 260442 | pkg/144 |
| GEM Single Edge, Stainless Steel Uncoated Blades | Ted Pella | 121-1 | box/200; for general cutting/sectioning |
| Glycerol | Thermo Scientific | PI17904 | 1 liter |
| ImageJ/FIJI with EDF plugin (version 17.05.2021) and Grid/Collection Stitching plugin | National Institutes of Health (NIH) USA | version 2.9.0/1.54s | The EDF plugin was developed by Alex Prudencio, Jesse Berent, and Daniel Sage for the Biomedical Imaging Group, École Polytechnique Fédérale de Lausanne (EPFL; http://bigwww.epfl.ch/demo/edf/). The grid/collection stitching software was developed by Stephan Preibisch for the Max Planck Institute of Molecular Cell Biology and Genetics (MPI-CBG). |
| Kimwipes Ex-L Small 111.76 mm x 213.36 mm | Kimtech Science | 34155 | box/280 ply |
| Micro Cover Glasses, 22 mm x 22 mm x 0.13 – 0.16 mm thick | Ted Pella | 260140 | 1 ounce |
| PU Gel Clear Double Sided Nano Tape 29.5 ft x 1.18 in, 1 mm thick | Yecaye Store (Amazon) | L354 W1.18 | 2 rolls |
| Superslip Cover Glasses, 24 mm x 50 mm x 0.13 – 0.16 mm thick | Ted Pella | 260166 | 1 ounce |
| Superslip Cover Glasses, 24 mm x 60 mm x 0.13 – 0.16 mm thick | Ted Pella | 260168 | 1 ounce |
| Tempered Glass Cutting Board | Hacaroa (Amazon) | B09XMXBT5S | 4 pc |
References
- McSteen, P., Kellogg, E. A. Molecular, cellular, and developmental foundations of grass diversity. Science. 377 (6606), 599-602 (2022).
- Wang, P., Vlad, D., Langdale, J. A. Finding the genes to build C4 rice. Current Opinion in Plant Biology. 31, 44-50 (2016).
- Wang, P., et al. Candidate regulators of early leaf development in maize perturb hormone signalling and secondary cell wall formation when constitutively expressed in rice. Scientific Reports. 7 (1), 4535 (2017).
- Perico, C., Tan, S., Langdale, J. A. Developmental regulation of leaf venation patterns: Monocot versus eudicots and the role of auxin. New Phytologist. 234 (3), 783-803 (2022).
- Wang, P., Kelly, S., Fouracre, J. P., Langdale, J. A. Genome-wide transcript analysis of early maize leaf development reveals gene cohorts associated with the differentiation of C4 Kranz anatomy. The Plant Journal. 75 (4), 656-670 (2013).
- Liu, W. Y., et al. Regulators of early maize leaf development inferred from transcriptomes of laser capture microdissection (LCM)-isolated embryonic leaf cells. Proceedings of the National Academy of Sciences. 119 (35), e2208795119 (2022).
- Liu, W. Y., et al. Anatomical and transcriptional dynamics of maize embryonic leaves during seed germination. Proceedings of the National Academy of Sciences. 110 (10), 3979-3984 (2013).
- Strable, J., Nelissen, H. The dynamics of maize leaf development: Patterned to grow while growing a pattern. Current Opinion in Plant Biology. 63, 102038 (2021).
- Reynolds, J. O., Eisses, J. F., Sylvester, A. W. Balancing division and expansion during maize leaf morphogenesis: Analysis of the mutant, warty-1. Development. 125 (2), 259-268 (1998).
- Richardson, A. E., et al. Evolution of the grass leaf by primordium extension and petiole-lamina remodeling. Science. 374 (6573), 1377-1381 (2021).
- Johnston, R., Leiboff, S., Scanlon, M. J. Ontogeny of the sheathing leaf base in maize (Zea mays). New Phytologist. 205 (1), 306-315 (2015).
- Sharman, B. C. Developmental anatomy of the shoot of Zea mays L. Annals of Botany. 6 (22), 245-282 (1942).
- Johnston, R., et al. Transcriptomic analyses indicate that maize ligule development recapitulates gene expression patterns that occur during lateral organ initiation. The Plant Cell. 26 (12), 4718-4732 (2014).
- Sharman, B. C. Leaf and bud initiation in the Gramineae. Botanical Gazette. 106 (3), 269-289 (1945).
- Nelissen, H., et al. A local maximum in gibberellin levels regulates maize leaf growth by spatial control of cell division. Current Biology. 22 (13), 1183-1187 (2012).
- Itoh, J., et al. Rice plant development: From zygote to spikelet. Plant and Cell Physiology. 46 (1), 23-47 (2005).
- Ritchie, S. W., Hanway, J. J., Benson, G. O. How a corn plant develops. Iowa State University of Science and Technology. , (1986).
- Freeling, M., Walbot, V. . The Maize Handbook. , (2013).
- Freeling, M., Hake, S. Developmental genetics of mutants that specify knotted leaves in maize. Genetics. 111 (3), 617-634 (1985).
- Durbak, A. R., et al. Transport of boron by the tassel-less1 aquaporin is critical for vegetative and reproductive development in maize. The Plant Cell. 26 (7), 2978-2995 (2014).
- Langdale, J. A., Lane, B., Freeling, M., Nelson, T. Cell lineage analysis of maize bundle sheath and mesophyll cells. Developmental Biology. 133 (1), 128-139 (1989).
- Bosabalidis, A. M., Evert, R. F., Russin, W. A. Ontogeny of the vascular bundles and contiguous tissues in the maize leaf blade. American Journal of Botany. 81 (6), 745-752 (1994).
- Junqueira, N. E. G., et al. Anatomy and ultrastructure of embryonic leaves of the C4 species Setaria viridis. Annals of Botany. 121 (6), 1163-1172 (2018).
- Robil, J. M., McSteen, P. Hormonal control of medial-lateral growth and vein formation in the maize leaf. New Phytologist. 238 (1), 125-141 (2023).
- Donnelly, P. M., Bonetta, D., Tsukaya, H., Dengler, R. E., Dengler, N. G. Cell cycling and cell enlargement in developing leaves of Arabidopsis. Developmental Biology. 215 (2), 407-419 (1999).
- Govindaraju, P., Verna, C., Zhu, T., Scarpella, E. Vein patterning by tissue-specific auxin transport. Development. 147 (13), (2020).
- Linh, N. M., Scarpella, E. Leaf vein patterning is regulated by the aperture of plasmodesmata intercellular channels. PLoS Biology. 20 (9), e3001781 (2022).
- Verna, C., Ravichandran, S. J., Sawchuk, M. G., Linh, N. M., Scarpella, E. Coordination of tissue cell polarity by auxin transport and signaling. eLife. 8, e51061 (2019).
- Sawchuk, M. G., Head, P., Donner, T. J., Scarpella, E. Time-lapse imaging of Arabidopsis leaf development shows dynamic patterns of procambium formation. New Phytologist. 176 (3), 560-571 (2007).
- Linh, N. M., Scarpella, E. Confocal imaging of developing leaves. Current Protocols. 2 (1), e349 (2022).
- Poethig, R. S., Szymkowiak, E. J. Clonal analysis of leaf development in maize. Maydica. 40, 67-76 (1995).
- Sprangers, K., Thys, S., van Dusschoten, D., Beemster, G. T. S. Gibberellin enhances the anisotropy of cell expansion in the growth zone of the maize leaf. Frontiers in Plant Science. 11, 1163 (2020).
- Tsuda, K., et al. KNOTTED1 cofactors, BLH12 and BLH14, regulate internode patterning and vein anastomosis in maize. The Plant Cell. 29 (5), 1105-1118 (2017).
- Schindelin, J., et al. FIJI: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Plant Care Protocols – Maize. The Donald Danforth Plant Science Center’s Plant Growth Facility Available from: https://www.danforthcenter.org/our-work/core-facilities/plant-growth/ (2019)
- Mir, R., et al. A DII domain-based auxin reporter uncovers low auxin signaling during telophase and early G1. Plant Physiology. 173 (1), 863-871 (2017).
- DeBlasio, S. L., Sylvester, A. W., Jackson, D. Illuminating plant biology: Using fluorescent proteins for high-throughput analysis of protein localization and function in plants. Briefings in Functional Genomics. 9 (2), 129-138 (2010).
- Wu, Q., Luo, A., Zadrozny, T., Sylvester, A., Jackson, D. Fluorescent protein marker lines in maize: Generation and applications. The International Journal of Developmental Biology. 57 (6-8), 535-543 (2013).
- Mohanty, A., et al. Advancing cell biology and functional genomics in maize using fluorescent protein-tagged lines. Plant Physiology. 149 (2), 601-605 (2009).
- Baker, R. F., et al. Sucrose transporter ZmSut1 expression and localization uncover new insights into sucrose phloem loading. Plant Physiology. 172 (3), 1876-1898 (2016).
- Gallavotti, A., Yang, Y., Schmidt, R. J., Jackson, D. The relationship between auxin transport and maize branching. Plant Physiology. 147 (4), 1913-1923 (2008).
- Krishnakumar, V., et al. A maize database resource that captures tissue-specific and subcellular-localized gene expression, via fluorescent tags and confocal imaging (Maize Cell Genomics Database). Plant and Cell Physiology. 56 (1), 12 (2015).
- Snapp, E. L. Fluorescent proteins: A cell biologist’s user guide. Trends in Cell Biology. 19 (11), 649-655 (2009).
- Geng, Y., Zhou, Y. Confocal live imaging of shoot apical meristems from different plant species. Journal of Visualized Experiments. (145), e59369 (2019).
- Stanislas, T., Hamant, O., Traas, J. In-vivo analysis of morphogenesis in plants. Methods in Cell Biology. 139, 203-223 (2017).
- Fodor, E., Ayaydin, F. Fluorescent probes and live imaging of plant cells. Advances in Plant Ecophysiology Techniques. , 241-251 (2018).
- Grandjean, O., et al. In vivo analysis of cell division, cell growth, and differentiation at the shoot apical meristem in Arabidopsis. The Plant Cell. 16 (1), 74-87 (2004).
- Conklin, P. A., Johnston, R., Conlon, B. R., Shimizu, R., Scanlon, M. J. Plant homeodomain proteins provide a mechanism for how leaves grow wide. Development. 147 (20), (2020).
- Shaw, S. L. Imaging the live plant cell. The Plant Journal. 45 (4), 573-598 (2006).
- Klaus, A. V., Schawaroch, V., Frischmann, K. J. Confocal imaging and three-dimensional visualization of thick autofluorescent specimens. Methods in Molecular Biology. 1075, 213-225 (2014).
- Forster, B., Van De Ville, D., Berent, J., Sage, D., Unser, M. Extended depth-of-focus for multi-channel microscopy images: a complex wavelet approach. 2004 2nd IEEE International Symposium on Biomedical Imaging: Nano to Macro (IEEE Cat No. 04EX821). IEEE. , 660-663 (2004).
- Preibisch, S., Saalfeld, S., Tomancak, P. Globally optimal stitching of tiled 3D microscopic image acquisitions. Bioinformatics. 25 (11), 1463-1465 (2009).
- Phillips, K. A., et al. vanishing tassel2 encodes a grass-specific tryptophan aminotransferase required for vegetative and reproductive development in maize. The Plant Cell. 23 (2), 550-566 (2011).
- Robil, J. M., et al. GrasVIQ: An image analysis framework for automatically quantifying vein number and morphology in grass leaves. The Plant Journal. 107 (2), 629-648 (2021).
- Helliwell, C. A., Chandler, P. M., Poole, A., Dennis, E. S., Peacock, W. J. The CYP88A cytochrome P450, ent-kaurenoic acid oxidase, catalyzes three steps of the gibberellin biosynthesis pathway. Proceedings of the National Academy of Sciences. 98 (4), 2065-2070 (2001).
- Gutierrez, R., Quiroz-Figueroa, F., Vazquez-Ramos, J. M. Maize cyclin D2 expression, associated kinase activity and effect of phytohormones during germination. Plant and Cell Physiology. 46 (1), 166-173 (2005).
- Atkinson, J. A., Wells, D. M. An updated protocol for high throughput plant tissue sectioning. Frontiers in Plant Science. 8, 1721 (2017).
- Lux, A., Morita, S., Abe, J., Ito, K. An improved method for clearing and staining free-hand sections and whole-mount samples. Annals of Botany. 96 (6), 989-996 (2005).
- Heriche, M., Arnould, C., Wipf, D., Courty, P. E. Imaging plant tissues: Advances and promising clearing practices. Trends in Plant Science. 27 (6), 601-615 (2022).
- Kurihara, D., Mizuta, Y., Sato, Y., Higashiyama, T. ClearSee: A rapid optical clearing reagent for whole-plant fluorescence imaging. Development. 142 (23), 4168-4179 (2015).
- Chuck, G., Muszynski, M., Kellogg, E., Hake, S., Schmidt, R. J. The control of spikelet meristem identity by the branched silkless1 gene in maize. Science. 298 (5596), 1238-1241 (2002).
- Tran, T. M., et al. An optimized whole-mount immunofluorescence method for shoot apices. Current Protocols. 1 (4), e101 (2021).
- O’Connor, D. L. PINs Lost and PINs Gained: Auxin-Transport Mediated Patterning in the Grasses. University of California, Berkeley. , (2012).
- Sharman, B. C., Hitch, P. A. Initiation of procambial strands in leaf primordia of bread wheat, Triticum aestivum L. Annals of Botany. 31 (2), 229-243 (1967).
- Serra, L., Tan, S., Robinson, S., Langdale, J. A. Flip-flap: A simple dual-view imaging method for 3D reconstruction of thick plant samples. Plants. 11 (4), 506 (2022).
- Colin, L., et al. Imaging the living plant cell: From probes to quantification. The Plant Cell. 34 (1), 247-272 (2022).

