De kliniek thuis brengen: een multimodaal ecosysteem voor gegevensverzameling thuis ter ondersteuning van adaptieve diepe hersenstimulatie
Summary
Het protocol toont een prototype van het multimodale gegevensverzamelingsplatform voor thuis dat onderzoek ondersteunt bij het optimaliseren van adaptieve diepe hersenstimulatie (aDBS) voor mensen met neurologische bewegingsstoornissen. We presenteren ook de belangrijkste bevindingen van het meer dan een jaar inzetten van het platform in het huis van een persoon met de ziekte van Parkinson.
Abstract
Adaptieve diepe hersenstimulatie (aDBS) is veelbelovend voor het verbeteren van de behandeling van neurologische aandoeningen zoals de ziekte van Parkinson (PD). aDBS maakt gebruik van symptoomgerelateerde biomarkers om stimulatieparameters in realtime aan te passen om de symptomen nauwkeuriger aan te pakken. Om deze dynamische aanpassingen mogelijk te maken, moeten voor elke individuele patiënt parameters voor een aDBS-algoritme worden bepaald. Dit vereist tijdrovende handmatige afstemming door klinische onderzoekers, waardoor het moeilijk is om een optimale configuratie te vinden voor een enkele patiënt of om op te schalen naar veel patiënten. Bovendien blijft de effectiviteit op lange termijn van aDBS-algoritmen die in de kliniek worden geconfigureerd terwijl de patiënt thuis is, een open vraag. Om deze therapie op grote schaal te implementeren, is een methodologie nodig om automatisch aDBS-algoritmeparameters te configureren en tegelijkertijd de therapieresultaten op afstand te monitoren. In dit artikel delen we een ontwerp voor een platform voor gegevensverzameling thuis om het veld te helpen beide problemen aan te pakken. Het platform bestaat uit een geïntegreerd hardware- en software-ecosysteem dat open-source is en het mogelijk maakt om thuis neurale, traagheids- en multicamera-videogegevens te verzamelen. Om de privacy van patiëntidentificeerbare gegevens te waarborgen, versleutelt en draagt het platform gegevens over via een virtueel particulier netwerk. De methoden omvatten het op elkaar afstemmen van datastromen in de tijd en het extraheren van pose-schattingen uit video-opnamen. Om het gebruik van dit systeem te demonstreren, hebben we dit platform ingezet bij een persoon met PD thuis en gegevens verzameld tijdens zelfgeleide klinische taken en perioden van vrij gedrag in de loop van 1,5 jaar. Gegevens werden geregistreerd bij subtherapeutische, therapeutische en supratherapeutische stimulatieamplitudes om de ernst van motorische symptomen onder verschillende therapeutische omstandigheden te evalueren. Deze op de tijd afgestemde gegevens tonen aan dat het platform in staat is om thuis multimodale gegevensverzameling te synchroniseren voor therapeutische evaluatie. Deze systeemarchitectuur kan worden gebruikt om geautomatiseerd aDBS-onderzoek te ondersteunen, om nieuwe datasets te verzamelen en om de langetermijneffecten van DBS-therapie buiten de kliniek te bestuderen voor mensen die lijden aan neurologische aandoeningen.
Introduction
Diepe hersenstimulatie (DBS) behandelt neurologische aandoeningen zoals de ziekte van Parkinson (PD) door elektrische stroom rechtstreeks aan specifieke delen van de hersenen te leveren. Er zijn wereldwijd naar schatting 8,5 miljoen gevallen van PD en DBS is een cruciale therapie gebleken wanneer medicatie onvoldoende is om de symptomen onder controle te houden 1,2. De effectiviteit van DBS kan echter worden beperkt door bijwerkingen die soms optreden bij stimulatie die conventioneel wordt toegediend met een vaste amplitude, frequentie enpulsbreedte3. Deze open-loop implementatie reageert niet op fluctuaties in de symptoomtoestand, wat resulteert in stimulatie-instellingen die niet goed zijn afgestemd op de veranderende behoeften van de patiënt. DBS wordt verder gehinderd door het tijdrovende proces van het afstemmen van stimulatieparameters, dat momenteel handmatig wordt uitgevoerd door clinici voor elke individuele patiënt.
Adaptieve DBS (aDBS) is een closed-loop benadering waarvan is aangetoond dat het een effectieve volgende iteratie van DBS is door stimulatieparameters in realtime aan te passen wanneer symptoomgerelateerde biomarkers worden gedetecteerd 3,4,5. Studies hebben aangetoond dat bèta-oscillaties (10-30 Hz) in de subthalamische kern (STN) consistent optreden tijdens bradykinesie, een vertraging van de beweging die kenmerkend is voor PD 6,7. Evenzo is bekend dat oscillaties met een hoog gamma (50-120 Hz) in de cortex optreden tijdens perioden van dyskinesie, een overmatige en onwillekeurige beweging die ook vaak wordt gezien bij PD8. Recent werk heeft met succes aDBS gedurende langere perioden buiten de kliniek toegediend5, maar de effectiviteit op lange termijn van aDBS-algoritmen die in de kliniek zijn geconfigureerd terwijl een patiënt thuis is, is niet vastgesteld.
Systemen op afstand zijn nodig om de in de tijd variërende effectiviteit van deze dynamische algoritmen vast te leggen bij het onderdrukken van symptomen die zich voordoen tijdens het dagelijks leven. Hoewel de dynamische stimulatiebenadering van aDBS mogelijk een nauwkeurigere behandeling mogelijk maakt met minder bijwerkingen3,9, lijdt aDBS nog steeds onder een hoge last voor clinici om handmatig stimulatieparameters voor elke patiënt te identificeren. Naast de toch al grote set parameters die tijdens conventionele DBS moeten worden geprogrammeerd, introduceren aDBS-algoritmen veel nieuwe parameters die ook zorgvuldig moeten worden aangepast. Deze combinatie van stimulatie- en algoritmeparameters levert een enorme parameterruimte op met een onbeheersbaar aantal mogelijke combinaties, waardoor aDBS niet kan worden opgeschaald naar veel patiënten10. Zelfs in onderzoeksomgevingen maakt de extra tijd die nodig is om aDBS-systemen te configureren en te beoordelen het moeilijk om algoritmen alleen in de kliniek adequaat te optimaliseren, en is het nodig om parameters op afstand bij te werken. Om van aDBS een behandeling te maken die schaalbaar is, moeten stimulatie en het afstemmen van algoritmeparameters worden geautomatiseerd. Bovendien moeten de resultaten van de therapie worden geanalyseerd in herhaalde onderzoeken om aDBS vast te stellen als een levensvatbare langetermijnbehandeling buiten de kliniek. Er is behoefte aan een platform dat gegevens kan verzamelen voor evaluatie op afstand van de effectiviteit van therapie, en om op afstand updates van aDBS-algoritmeparameters te implementeren.
Het doel van dit protocol is om een herbruikbaar ontwerp te bieden voor een multimodaal platform voor gegevensverzameling thuis om de effectiviteit van aDBS buiten de kliniek te verbeteren en om deze behandeling op te schalen naar een groter aantal individuen. Voor zover wij weten, is dit het eerste ontwerp van een platform voor gegevensverzameling dat op afstand therapeutische resultaten evalueert met behulp van videocamera’s voor thuis, draagbare sensoren, chronische neurale signaalopname en patiëntgestuurde feedback om aDBS-systemen te evalueren tijdens gecontroleerde taken en naturalistisch gedrag.
Het platform is een ecosysteem van hardware- en softwarecomponenten die zijn gebouwd op eerder ontwikkelde systemen5. Het is volledig te onderhouden via toegang op afstand na een eerste installatie van minimale hardware om multimodale gegevensverzameling van een persoon in het comfort van zijn huis mogelijk te maken. Een belangrijk onderdeel is het implanteerbare neurostimulatiesysteem (INS)11 dat neurale activiteit detecteert en stimulatie levert aan de STN, en de versnelling van borstimplantaten registreert. Voor het implantaat dat bij de eerste inzet wordt gebruikt, wordt neurale activiteit geregistreerd van bilaterale afleidingen die in de STN zijn geïmplanteerd en van elektrocorticografie-elektroden die over de motorische cortex zijn geïmplanteerd. Een video-opnamesysteem helpt clinici de ernst van de symptomen en de effectiviteit van de therapie te controleren, inclusief een grafische gebruikersinterface (GUI) om lopende opnames eenvoudig te kunnen annuleren om de privacy van de patiënt te beschermen. Video’s worden verwerkt om kinematische positietrajecten in tweedimensionaal (2D) of driedimensionaal (3D) te extraheren, en slimme horloges worden om beide polsen gedragen om hoeksnelheids- en versnellingsinformatie vast te leggen. Belangrijk is dat alle gegevens worden versleuteld voordat ze worden overgebracht naar langdurige cloudopslag, en dat de computer met patiëntidentificeerbare video’s alleen toegankelijk is via een virtueel particulier netwerk (VPN). Het systeem omvat twee benaderingen voor post-hoc tijdafstemming van alle gegevensstromen, en gegevens worden gebruikt om de bewegingskwaliteit van de patiënt op afstand te bewaken en om symptoomgerelateerde biomarkers te identificeren voor het verfijnen van aDBS-algoritmen. Het videogedeelte van dit werk toont het gegevensverzamelingsproces en animaties van kinematische trajecten die zijn geëxtraheerd uit verzamelde video’s.
Bij de ontwikkeling van het protocol zijn een aantal ontwerpoverwegingen leidend geweest:
Zorgen voor gegevensbeveiliging en privacy van patiënten: Het verzamelen van identificeerbare patiëntgegevens vereist uiterste zorgvuldigheid bij verzending en opslag om de Health Insurance Portability and Accountability Act (HIPAA) te zijn12,13 de privacy van de patiënt in zijn eigen huis te respecteren. In dit project werd dit bereikt door het opzetten van een aangepaste VPN om de privacy van al het gevoelige verkeer tussen systeemcomputers te waarborgen.
Veiligheidsgrenzen van de stimulatieparameter: Het is van cruciaal belang om ervoor te zorgen dat de patiënt veilig blijft tijdens het uitproberen van aDBS-algoritmen die onbedoelde effecten kunnen hebben. De INS van de patiënt moet door een arts worden geconfigureerd om veilige grenzen te hebben voor stimulatieparameters die geen onveilige effecten van overstimulatie of onderstimulatie mogelijk maken. Met het INS-systeem11 Deze functie wordt in dit onderzoek gebruikt en wordt mogelijk gemaakt door een programmeur van een arts.
Zorgen voor het veto van de patiënt: Zelfs binnen veilige parameterlimieten kan de dagelijkse variabiliteit van symptomen en stimulatiereacties leiden tot onaangename situaties voor de patiënt waarbij ze een hekel hebben aan een algoritme dat wordt getest en willen terugkeren naar normale klinische open-loop DBS. Het geselecteerde INS-systeem bevat een patiënttelemetriemodule (PTM) waarmee de patiënt zijn stimulatiegroep en stimulatieamplitude in mA handmatig kan wijzigen. Er is ook een INS-gekoppelde onderzoeksapplicatie die wordt gebruikt voor configuratie op afstand van de INS voorafgaand aan gegevensverzameling14, wat de patiënt ook in staat stelt om aDBS-onderzoeken af te breken en zijn therapie onder controle te houden.
Complex en natuurlijk gedrag vastleggen: Videogegevens werden in het platform opgenomen om clinici in staat te stellen de effectiviteit van de therapie op afstand te bewaken en kinematische trajecten uit pose-schattingen te extraheren voor gebruik in onderzoeksanalyses15. Hoewel draagbare sensoren minder opdringerig zijn, is het moeilijk om het volledige dynamische bewegingsbereik van een heel lichaam vast te leggen met alleen draagbare systemen. Video’s maken het mogelijk om tegelijkertijd het volledige bewegingsbereik van de patiënt en zijn symptomen in de loop van de tijd vast te leggen.
Bruikbaarheid van het systeem voor patiënten: Voor het verzamelen van multimodale gegevens thuis moeten meerdere apparaten worden geïnstalleerd en gebruikt in het huis van een patiënt, wat voor patiënten lastig kan worden om te navigeren. Om het systeem gebruiksvriendelijk te maken en tegelijkertijd de controle over de patiënt te garanderen, moeten alleen de apparaten die zijn geïmplanteerd of fysiek aan de patiënt zijn bevestigd (in dit geval inclusief het INS-systeem en slimme horloges) handmatig worden ingeschakeld voordat een opname wordt gestart. Voor apparaten die los staan van de patiënt (in dit geval gaat het om gegevens die zijn opgenomen met videocamera’s), worden de opnames automatisch gestart en beëindigd zonder dat er interactie van de patiënt nodig is. Bij het ontwerp van de GUI is ervoor gezorgd dat het aantal knoppen tot een minimum is beperkt en dat diepe menubomen zijn vermeden, zodat interacties eenvoudig zijn. Nadat alle apparaten zijn geïnstalleerd, liet een onderzoekscoördinator de patiënt zien hoe hij met alle apparaten kon communiceren via patiëntgerichte GUI’s die deel uitmaken van elk apparaat, zoals hoe opnames op elk apparaat kunnen worden beëindigd en hoe ze hun medicatiegeschiedenis en symptoomrapporten kunnen invoeren.
Transparantie van gegevensverzameling: Het is absoluut noodzakelijk om duidelijk aan te geven wanneer camera’s zijn ingeschakeld, zodat mensen weten wanneer ze worden opgenomen en de opname kunnen onderbreken als ze een moment van privacy nodig hebben. Om dit te bereiken, wordt een camerasysteemtoepassing gebruikt om video-opnames te besturen met een patiëntgerichte GUI. De GUI wordt automatisch geopend wanneer de applicatie wordt gestart en geeft de tijd en datum van de volgende geplande opname weer. Wanneer een opname aan de gang is, wordt in een bericht aangegeven wanneer de opname volgens de planning moet worden beëindigd. In het midden van de GUI wordt een grote afbeelding van een rood licht weergegeven. Het beeld laat zien dat het licht fel verlicht is wanneer er een opname aan de gang is, en verandert in een niet-verlicht beeld wanneer de opnamen zijn uitgeschakeld.
Het protocol beschrijft methoden voor het ontwerpen, bouwen en implementeren van een platform voor gegevensverzameling thuis, voor het controleren van de kwaliteit van de verzamelde gegevens op volledigheid en robuustheid, en voor het nabewerken van gegevens voor gebruik in toekomstig onderzoek.
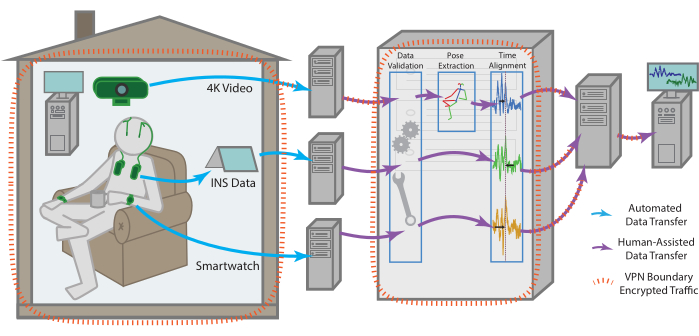
Figuur 1: Gegevensstroom. Gegevens voor elke modaliteit worden onafhankelijk van de woonplaats van de patiënt verzameld voordat ze worden verwerkt en samengevoegd tot één eindpunt voor externe opslag. De gegevens voor elke modaliteit worden automatisch verzonden naar een eindpunt voor externe opslag. Met de hulp van een van de teamleden kan het vervolgens worden opgehaald, gecontroleerd op geldigheid, tijd afgestemd op verschillende modaliteiten en worden onderworpen aan meer modaliteitsspecifieke voorbewerking. De gecompileerde dataset wordt vervolgens geüpload naar een extern opslageindpunt dat veilig toegankelijk is voor alle teamleden voor voortdurende analyse. Alle machines met gegevenstoegang, vooral voor gevoelige gegevens zoals onbewerkte video, zijn ingesloten in een VPN die ervoor zorgt dat alle gegevens veilig worden overgedragen en opgeslagen gegevens altijd worden versleuteld. Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
We delen het ontwerp voor een thuisprototype van een multimodaal gegevensverzamelingsplatform ter ondersteuning van toekomstig onderzoek naar neuromodulatieonderzoek. Het ontwerp is open-source en modulair, zodat elk stuk hardware kan worden vervangen en elk softwareonderdeel kan worden bijgewerkt of gewijzigd zonder dat het algehele platform instort. Hoewel de methoden voor het verzamelen en de-identificeren van neurale gegevens specifiek zijn voor de geselecteerde INS, zijn de overige methoden en de algemene benadering…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dit materiaal is gebaseerd op werk dat wordt ondersteund door het National Science Foundation Graduate Research Fellowship Program (DGE-2140004), de Weill Neurohub en het National Institute of Health (UH3NS100544). Alle meningen, bevindingen en conclusies of aanbevelingen in dit materiaal zijn die van de auteur(s) en weerspiegelen niet noodzakelijkerwijs de mening van de National Science Foundation, de Weill Neurohub of het National Institute of Health. We danken Tianjiao Zhang voor zijn deskundig advies over platformontwerp en de integratie van videogegevens. We danken in het bijzonder de patiënt voor hun deelname aan dit onderzoek en voor de feedback en het advies over netwerkbeveiliging en platformontwerp.
Materials
| Analysis RCS Data Processing | OpenMind | https://github.com/openmind-consortium/Analysis-rcs-data, open-source | |
| Apple Watches | Apple, Inc | Use 2 watches for each patient, one on each wrist | |
| BRIO ULTRA HD PRO BUSINESS WEBCAM | Logitech | 960-001105 | Used 3 in our platform design |
| DaVinci Resolve video editing software | DaVinci Resolve | used to support camera calibration | |
| Dell XPS PC | Dell | 2T hard disk drive, 500GB SSD | |
| Dropbox | Dropbox | ||
| ffmpeg | N/A | open-source, install to run the Video Recording App | |
| Gooseneck mounts for webcams | N/A | ||
| GPU | Nvidia | A minimum of 8GB GPU memory is recommended to run OpenPose, 12GB is ideal | |
| Java 11 | Oracle | Install to run the Video Recording App | |
| Microsoft Surface tablet | Microsoft | ||
| NoMachine | NoMachine | Ideal when using a Linux OS, open-source | |
| OpenPose | N/A | open-source | |
| Rclone file transfer program | Rclone | Encrypts data and copies or moves data to offsite storage, open-source | |
| StrivePD app | RuneLabs | We installed the app on the Apple Watches to start recordings and upload data to an online portal. | |
| Summit RC+S neuromodulation system | Medtronic | For investigational use only | |
| touchscreen-compatible monitor | N/A | ||
| Video for Linux 2 API | The Linux Kernel | Install if using a Linux OS for video recording | |
| Wasabi | Wasabi | Longterm cloud data storage | |
| WireGuard VPN Protocol | WireGuard | open-source |
References
- World Health Organization. . Parkinson disease. , (2022).
- Herrington, T. M., Cheng, J. J., Eskandar, E. N. Mechanisms of deep brain stimulation. Journal of Neurophysiology. 115 (1), 19-38 (2016).
- Little, S., et al. Adaptive deep brain stimulation for Parkinson’s disease demonstrates reduced speech side effects compared to conventional stimulation in the acute setting. Journal of Neurology, Neurosurgery & Psychiatry. 87 (12), 1388-1389 (2016).
- Mohammed, A., Bayford, R., Demosthenous, A. Toward adaptive deep brain stimulation in Parkinson’s disease: a review. Neurodegenerative Disease Management. 8 (2), 115-136 (2018).
- Gilron, R., et al. Long-term wireless streaming of neural recordings for circuit discovery and adaptive stimulation in individuals with Parkinson’s disease. Nature Biotechnology. 39 (9), 1078-1085 (2021).
- Ray, N. J., et al. Local field potential beta activity in the subthalamic nucleus of patients with Parkinson’s disease is associated with improvements in bradykinesia after dopamine and deep brain stimulation. Experimental Neurology. 213 (1), 108-113 (2008).
- Neumann, W. J., et al. Subthalamic synchronized oscillatory activity correlates with motor impairment in patients with Parkinson’s disease. Movement Disorders: Official Journal of the Movement Disorder Society. 31 (11), 1748-1751 (2016).
- Swann, N. C., et al. Adaptive deep brain stimulation for Parkinson’s disease using motor cortex sensing. J. Neural Eng. 11, (2018).
- Little, S., et al. Adaptive deep brain stimulation in advanced Parkinson disease. Annals of Neurology. 74 (3), 449-457 (2013).
- Connolly, M. J., et al. Multi-objective data-driven optimization for improving deep brain stimulation in Parkinson’s disease. Journal of Neural Engineering. 18 (4), 046046 (2021).
- Stanslaski, S., et al. Creating neural "co-processors" to explore treatments for neurological disorders. 2018 IEEE International Solid – State Circuits Conference – (ISSCC). , 460-462 (2018).
- . Rights (OCR), O. for C. The HIPAA Privacy Rule. HHS.gov. , (2008).
- . Rights (OCR), O. for C. The Security Rule. HHS.gov. , (2009).
- Perrone, R., Gilron, R. . SCBS Patient Facing App (Summit Continuous Bilateral Streaming). , (2021).
- Strandquist, G., et al. . In-Home Video and IMU Kinematics of Self Guided Tasks Correlate with Clinical Bradykinesia Scores. , (2023).
- Donenfeld, J. A. WireGuard: Next Generation Kernel Network Tunnel. Proceedings 2017 Network and Distributed System Security Symposium. , (2017).
- etzion. . Ubuntu 20.04 and TPM2 encrypted system disk – Running Systems. , (2021).
- Craig-Wood, N. . Rclone. , (2023).
- Chen, W., et al. The Role of Large-Scale Data Infrastructure in Developing Next-Generation Deep Brain Stimulation Therapies. Frontiers in Human Neuroscience. 15, 717401 (2021).
- Hidalgo, G. i. n. &. #. 2. 3. 3. ;. s., et al. . CMU-Perceptual-Computing-Lab/openpose. , (2023).
- Cao, Z., Hidalgo, G., Simon, T., Wei, S. E., Sheikh, Y. OpenPose: Realtime Multi-Person 2D Pose Estimation Using Part Affinity Fields. IEEE Transactions on Pattern Analysis and Machine Intelligence. 43 (1), 172-186 (2021).
- Cao, Z. . openpose/calibration_module.md at master · CMU-Perceptual-Computing-Lab/openpose. , (2023).
- Sellers, K. K., et al. Analysis-rcs-data: Open-Source Toolbox for the Ingestion, Time-Alignment, and Visualization of Sense and Stimulation Data From the Medtronic Summit RC+S System. Frontiers in Human Neuroscience. 15, 398 (2021).
- Ranti, C. . Rune Labs Stream API. , (2023).
- . ffmpeg development community. FFmpeg Formats Documentation. , (2023).
- Goetz, C. G., et al. Movement Disorder Society-sponsored revision of the Unified Parkinson’s Disease Rating Scale (MDS-UPDRS): Scale presentation and clinimetric testing results: MDS-UPDRS: Clinimetric Assessment. Movement Disorders. 23 (15), 2129-2170 (2008).

