Generering av patient-härledda podocyter från hudbiopsier
Summary
Detta manuskript beskriver ett tvåstegsprotokoll för att generera patientspecifika podocyter från dermala fibroblaster via episomal omprogrammering till humaninducerade pluripotenta stamceller (hiPSCs) och efterföljande differentiering till podocyter.
Abstract
Podocyter är epitelceller som sitter på urinplatsen i den glomerulära filtreringsbarriären som bidrar till glomerulus selektiva filterfunktion. Mutationer i podocytspecifika gener kan orsaka fokal segmentell glomeruloskleros (FSGS), och podocyter påverkas också i många andra primära och sekundära nefropatier. På grund av deras differentierade natur är primära cellodlingsmodeller begränsade för podocyter. Därför används vanligen villkorligt odödliga celler. Dessa villkorligt odödliga podocyter (ciPodocyter) har emellertid flera begränsningar: cellerna kan dedifferentiera i odling, särskilt när de når sammanflöde, och flera podocytspecifika markörer uttrycks antingen bara lite eller inte alls. Detta ifrågasätter användningen av ciPodocyter och deras tillämplighet för fysiologisk, patofysiologisk och klinisk räckvidd. Här beskriver vi ett protokoll för generering av humana podocyter – inklusive patientspecifika podocyter – från en hudstansbiopsi genom episomal omprogrammering av dermala fibroblaster till hiPSC och efterföljande differentiering till podocyter. Dessa podocyter liknar in vivo-podocyter mycket bättre när det gäller morfologiska egenskaper, som utvecklingen av fotprocesser och uttrycket av den podocytspecifika markören. Slutligen, men ändå viktigare, upprätthåller dessa celler patienternas mutationer, vilket resulterar i en förbättrad ex vivo-modell för att studera podocytsjukdomar och potentiella terapeutiska substanser i ett individualiserat tillvägagångssätt.
Introduction
Podocyter är specialiserade, postmitotiska njurepitelceller som bildar njurens glomerulära filtreringsbarriär tillsammans med det glomerulära basalmembranet (GBM), glomerulära endotelceller och glykokalyx. Fenotypiskt består podocyter av en cellkropp och primära, mikrotubulidrivna membranförlängningar, liksom sekundära förlängningar som kallas fotprocesser 1,2. Den glomerulära filtreringsbarriären som filtrerar urin från blodet är byggd av fenestrerat endotel, GBM och en specialiserad typ av intercellulär korsning som förbinder närliggande podocytfotprocesser, kallad slitsmembranet av podoctyes3. Under friska förhållanden behålls proteiner större än albumin från filtreringsbarriären på grund av deras storlek och laddning4.
Mutationer i cytoskeletala eller podocytspecifika gener, såväl som cirkulerande faktorer som påverkar podocytsignalvägar, är kända för att inducera podocytefacement, avlossning eller apoptos, vilket resulterar i proteinuri och glomerulär skleros. I synnerhet är cytoskeletal omläggning, förändringar i podocytpolaritet eller skada på fotprocesser med tillhörande förlust av slitskorsningar avgörande5. På grund av deras terminalt differentierade status kan podocyter knappast ersättas efter avlägsnande av GBM. Men om podocyter är fästa vid GBM kan de fortfarande återhämta sig från utplåning och reformera interdigiterande fotprocesser 6,7,8. Ytterligare förståelse av de händelser som leder till podocytskador vid olika glomerulära sjukdomar kan ge nya terapeutiska mål som kommer att hjälpa till att utveckla behandlingar för dessa sjukdomar. Podocytskador är ett kännetecken för olika glomerulära sjukdomar, inklusive fokal segmentell glomeruloskleros (FSGS), diabetesnefropati, minimal förändringssjukdom och membranös glomerulonefropati, vilket kräver tillförlitliga podocyte ex vivo-modeller för att studera de patologiska mekanismerna och potentiella behandlingsmetoder för dessa sjukdomar 9,10. Podocyter kan studeras ex vivo genom klassisk primär cellodling baserat på isolering av glomeruli genom differentialsiktning11. På grund av det terminalt differentierade tillståndet med begränsad spridningskapacitet använder de flesta forskare mus- eller humana ciPodocytcellinjer som uttrycker temperaturkänsliga varianter av SV40 large T-antigenet. Alternativt isoleras ciPodocyter från transgena möss som har SV40 Tag immortalizing gen 1,12.
CiPodocyter förökar sig vid 33 °C, men går in i tillväxtstopp och börjar differentiera vid 37 °C13,14. Man måste komma ihåg att experimentella data som erhållits med dessa celler bör tolkas med viss försiktighet, eftersom cellerna genereras med hjälp av en onaturlig geninsättning15. Eftersom dessa celler har en odödlig gen förändras den cellulära fysiologin på grund av pågående proliferation12. Podocytcellinjer genererade av detta tillvägagångssätt har nyligen ifrågasatts, eftersom mus-, human- och rått-ciPodocyter uttrycker mindre än 5% av synaptopodin och nefrin på proteinnivå, liksom NPHS1 och NPHS2 på mRNA-nivå jämfört med glomerulärt uttryck16. Dessutom uttrycker de flesta podocytcellinjer inte nefrin17,18. Chittiprol et al. beskrev också en signifikant skillnad i cellmotilitet och svar på puromycin och doxorubicin i ciPodocyter16. Podocyter finns i urinen efter avlägsnande från GBM i olika glomerulära sjukdomar 19,20,21,22. Livskraftiga urinpodocyter kan odlas ex vivo i upp till 2-3 veckor, men de flesta celler genomgår apoptos23,24. Intressant är att podocyter inte bara finns i urinen hos patienter med glomerulär sjukdom utan också i urinen hos friska försökspersoner, troligen när de är senescent-igen med en begränsad potential för replikation i kultur24. Dessutom är det urin-härledda podocytantalet begränsat, och cellerna dedifferentierar i odling, visar mindre fotprocesser, förändrar morfologi och viktigast av allt har begränsad spridningskapacitet. Uttrycket av podocytspecifika gener saknas, försvinner inom några veckor eller varierar mellan dessa cellkloner. Vissa celler som är positiva för den podocytspecifika markören uttryckte markören för tubulära epitelceller eller myofibroblaster och mesangiala celler, vilket tyder på dedifferentiering och/eller transdifferentiering av de odlade urinpodocyterna24,25.
Nyligen har genereringen av ciPodocytcellinjer härrörande från urinen hos patienter och friska frivilliga genom transduktion med ett värmekänsligt SV40 stort T-antigen och hTERT beskrivits26. mRNA-uttryck för synaptopodin, nestin och CD2-associerat protein detekterades, men podocin mRNA saknades i alla kloner. Förutom problemen med urinpodocyter innehåller dessa celler också den införda odödliga genen, vilket resulterar i de nackdelar som diskuterats ovan.
Däremot har humant inducerade pluripotenta stamceller (hiPSC) en enorm kapacitet att självförnya och differentiera till flera celltyper under lämpliga förhållanden. Det har tidigare visats att hiPSC kan fungera som en nästan obegränsad källa till podocyter27,28.
Här beskrivs ett tvåstegsprotokoll för att generera patientspecifika podocyter från dermala fibroblaster av hudstansbiopsier med efterföljande episomal omprogrammering till hiPSC och en slutlig differentiering till hiPSC-härledda podocyter (figur 1).
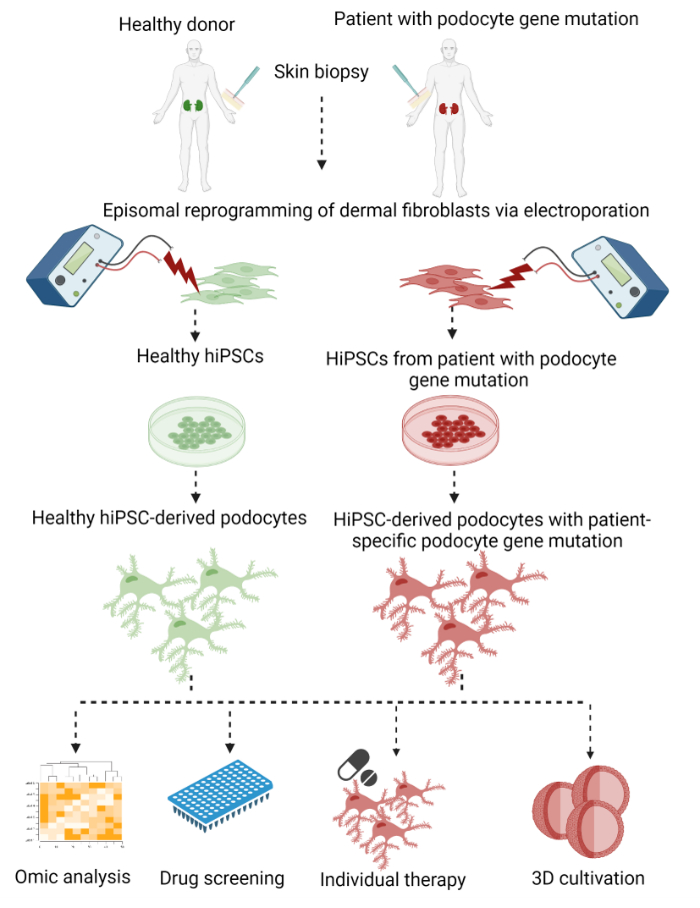
Figur 1: Protokoll för att generera patientspecifika hiPSC-härledda podocyter. Grafisk översikt över protokollet för att generera patientspecifika podocyter från dermala fibroblaster av en hudbiopsi genom omprogrammering till hiPSC och differentiering till podocyter. Klicka här för att se en större version av denna figur.
Som ett första steg växte somatiska dermala fibroblaster ut från en hudstansbiopsi och omprogrammerades till hiPSC med hjälp av en integrationsfri metod genom elektroporering med plasmider som uttrycker transkriptionsfaktorerna OCT3/4, KLF4, SOX2 och c-MYC 29,30,31. Uppkomna hiPSC-kolonier valdes därefter ut och utvidgades. Differentiering började med induktionen av den mesodermala linjen genom aktivering av WNT-signalvägen, följt av generering av nefronprogenitorceller som fortfarande kunde föröka sig. Slutligen differentierades cellerna i podocyter. I denna procedur modifierade och kombinerade vi tidigare publicerade protokoll för episomal omprogrammering för generering av hiPSC av Bang et al.32 och Okita et al.33, samt ett protokoll för differentiering av hiPSC till podocyter av Musah et al.28,34,35.
Faktum är att podocyter genererade av vårt protokoll hade en fenotyp närmare podocyter in vivo, avseende utvecklingen av ett distinkt nätverk av primära och sekundära fotprocesser och uttrycket av podocytspecifika markörer, som synaptopodin, podocin och nefrin. Med användning av hiPSC-härledda podocyter bibehålls patientens genetiska bakgrund under omprogrammering och differentiering. Detta möjliggör patientspecifik podocytsjukdomsmodellering och upptäckt av potentiella terapeutiska substanser ex vivo i ett nästan obegränsat cellantal. Dessutom är detta protokoll minimalt invasivt, kostnadseffektivt, etiskt acceptabelt och kan underlätta nya vägar för läkemedelsutveckling.
Protocol
Representative Results
Discussion
Detta cellodlingsbaserade protokoll kombinerar episomal omprogrammering av humana dermala fibroblaster till patientspecifika hiPSC och efterföljande differentiering till hiPSC-härledda podocyter. Detta gör det möjligt för oss att studera mutationsrelaterade förändringar av podocyter från patienter med genetisk glomerulär sjukdom avseende podocytskada. Protokollet för att omprogrammera dermala fibroblaster med en integrationsfri metod genom elektroporering är anpassat från det publicerade arbetet av Bang et al.32 och Okita et al.33. Protokollet för att skilja podocyter från hiPSC är anpassat från det publicerade protokollet från Musah et al.28,34,35. Det finns redan publikationer tillgängliga som beskriver genereringen av podocyter från hiPSCs 27,34,35. Protokollet som tillhandahålls här är dock optimerat och billigare när det gäller differentiering av hiPSC till podocyter. Jämfört med det publicerade protokollet från Musah et al. testade vi detta protokoll på olika beläggningsreagens, som vitronektin, lamininsilke-511 och solubiliserad basalmembranmatris. Koncentrationerna av vitronektin och lamininsilke-511 kan minskas till 2,5 μg/ml istället för 5 μg/ml 28,34,35. Dessutom var det möjligt att minska koncentrationerna av BMP7 och aktivin A-två mycket dyra tillväxtfaktorer – med 50%, från 100 ng / ml till 50 ng / ml.
Detta möjliggör billigare differentiering. Nefronprogenitorceller från dag 7 förökade sig fortfarande, och möjligheten till frysning visades tidigare. Vi expanderade dessa celler efter upptining och före slutlig differentiering i basmedium innehållande Dulbeccos modifierade Eagle-medium (DMEM) och B27 i flera dagar, vilket minskade kostnaderna ytterligare. Förutom differentieringsstegen beskriver detta protokoll utväxten av fibroblaster från hudbiopsier med efterföljande generation av patientspecifika hiPSC via episomal omprogrammering. Kombinationen av dessa två metoder möjliggör generering av patientspecifika podocyter. Därför tillhandahålls här ett komplett steg-för-steg-protokoll för att generera patientspecifika hiPSC-härledda podocyter som inte beskrivits tidigare så detaljerat.
Eftersom det övergripande protokollet innehåller flera olika celltyper är det viktigt att karakterisera de genererade celltyperna i olika steg. Celler är i odling under en längre tid, så kvalitetskontroll bör utföras vid olika passager. Vid arbete med hiPSC är daglig utfodring samt cellbeteende och morfologiövervakning nödvändig. Differentieringsmediets sterilitet måste säkerställas genom sterilisering av filter genom ett 0,2 μm filter. Hela protokollet, från hudbiopsi till hiPSC-härledda podocyter, tar flera månader, men det är möjligt att frysa cellerna i olika stadier av processen. Fibroblaster, utvalda hiPSC-kloner och proliferativa nefronprogenitorceller efter 7 dagar i nefronprogenitordifferentieringsmedium kan frysas och en fungerande cellbank kan genereras.
Även om hiPSC-härledda friska podocyter utvecklar ett distinkt nätverk av primära och sekundära fotprocesser (figur 5A, B) och uttrycker typisk podocytspecifik markör (figur 6A-C), är karakteristiska slitsmembran, som ses in vivo, svåra att efterlikna i klassiska tvådimensionella cellodlingsmodeller. Dessutom är intercellkommunikation med andra glomerulära celltyper inte möjlig i denna monokulturinställning.
På grund av deras terminaldifferentierade tillstånd och brist på spridningskapacitet är det svårt att studera podocyter ex vivo. Med hjälp av villkorligt odödliggörande primära podocyter är det möjligt att övervinna denna begränsning genom införandet av en värmekänslig omkopplare, vilket resulterar i en cellodlingsmodell där celler prolifererar vid 33 ° C och differentierar vid 37 ° C13,14. Även om dessa ciPodocyter har hög potential för podocytforskning, finns det begränsningar, som bristen på marköruttryck, dedifferentierad morfologi och misslyckande med att bilda fotprocesser15,16.
Differentieringen av podocyter från patienthärledda somatiska celler möjliggör generering och jämförelse av sjuka podocyter med friska kontrollceller ex vivo. Detta gör det möjligt för oss att studera podocytskador på grund av mutationer i podocytspecifika gener. Dessutom har arbetet med hiPSC potential att skapa tredimensionella cellodlingssjukdomsmodeller, eller snarare organoider43,44. Samodling av hiPSC-härledda podocyter med andra glomerulära celler, som glomerulära endotelceller eller mesangiala celler, kan leda till nya insikter om intercellkommunikation vid hälsa och glomerulär sjukdom.
Dessutom kan karakterisering och behandling av de patientspecifika podocyterna utföras ex vivo i high-throughput-analys. Det individualiserade tillvägagångssättet öppnar möjligheten att undersöka nya terapeutiska mål för specifika mutationer och att utföra individualiserad medicin i framtiden.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Detta arbete finansierades av Interdisciplinary Center for Clinical Research (IZKF) vid Friedrich-Alexander University Erlangen-Nürnberg med bidragsnummer M4-IZKF-F009 som gavs till Janina Müller-Deile, och av Bundesministerium für Bildung und Forschung (BMBF) under projektnamnet STOP-FSGS-Speed Translation-Oriented Progress to Treat FSGS, bidragsnummer 01GM2202D som gavs till Janina Müller-Deile. Vi tackar Annalena Kraus för stödet med att ta SEM-bilder.
Materials
| 0.2 µm sterile filter | Rotilab | P668.1 | for sterilization of differentiation medium |
| all-trans retinoic acid | Stem Cell Technologies | 72262 | supplement for differentiation |
| B27 supplement (50 x), serum free | Gibco | 17504044 | supplement for serum-free differentiation medium |
| BG iMatrix-511 Silk | biogems | RL511S | additional option of extracellular matrix reagent used in coating solution to coat cell culture plastics suitable for hiPSC culture |
| Bovine serum albumin (BSA) | Roth | 8076.4 | |
| CELLSTAR Filter Cap Cell Culture Flasks, T75, 250 mL | Greiner bio-one | 82050-856 | cell culture plastics suitable for fibroblast culture |
| CHIR99021 (5 mg) | Sigma-Aldrich | 252917-06-9 | supplement for differentiation |
| Corning Matrigel hESC qualified matrix | Corning | 354277 | additional option of extracellular matrix reagent used in coating solution to coat cell culture plastics suitable for hiPSC culture (solubilized basement membrane matrix) |
| countess Cell Counting Chamber Slides | Invitrogen | C10283 | to count cells |
| countess II FL Automated Cell Counter | Invitrogen | to count cells | |
| cryoPure tubes, 2 ml, QuickSeal screw cap, white | Sarstedt | 72380 | cryovials for freezing of cells |
| dimethyl sulfoxide (DMSO) | Roth | A994.1 | for fibroblast freezing medium |
| DMEM/F12 (1:1) (1 x) | Gibco | 11320074 | basic medium for differentiation |
| DMEM/F12 + Glutamax | Gibco | 10565018 | basic medium for fibroblast medium |
| EVOS M5000 Imaging System | Thermo Fisher Scientific | AMF5000 | phase contrast microscope |
| fetal bovine serum premium, inactivated (FCS) | PAN Biotech | P301902 | serum for fibroblast medium, fibroblast freezing medium and podocyte maintenance medium |
| fisherbrand Electroporation Cuvettes Plus, 4 mm gap, 800 µL capacity, sterile | Fisherbrand | FB104 | cuvette used for electroporation/episomal reprogramming of fibroblasts (4mm gap) |
| fluoromount-G Mounting Medium, with DAPI | Invitrogen | 00-4959-52 | mounting medium containing dapi |
| gauge needle (0.6 x 30 mm) | BD Microlance3 | 300700 | for separation of hiPSC colonies into small pieces |
| human Recombinant Activin A Protein | 78001.1 | Stem cell technologies | supplement for differentiation |
| human recombinant bone morphogenetic protein 7 (BMP7) | Peprotech | 120-03P | supplement for differentiation |
| human VEGF-165 Recombinant Protein | Thermo Scientific | PHC9394 | supplement for differentiation |
| insulin-transferrin-selenium (ITS -G) (100 x) | Gibco | 41400045 | supplement for podocyte maintenance medium |
| LB medium | Roth | X964.1 | for sterility test of hiPSC culture |
| lookOut Mycoplasma PCR Detection Kit | Sigma Aldrich | MP0035-1KT | commercial mycoplasma detection kit |
| microscope slides | Diagonal GmbH & Co.KG | 21,102 | |
| microtube 1.5 mL | Sarstedt | 72706400 | |
| mTeSR1 Complete Kit | Stem Cell Technologies | 85850 | basic medium for serum-free hiPSC culture medium |
| nalgene freezing container Mr.Frosty | Roth | AC96.1 | to ensure optimal freezing conditions |
| normal goat serum | abcam | ab 7481 | for preincubation solution and antibody diluent |
| nunc 24 well plates | Thermo Scientific | 142485 | cell culture plastics suitable for hiPSC culture |
| nunc 48 well plates | Thermo Scientific | 152640 | cell culture plastics suitable for hiPSC culture |
| nunc 6 well plates | Thermo Scientific | 140685 | cell culture plastics suitable for hiPSC culture |
| nunc EasYDish Dishes 100 mm | Thermo Scientific | 150466 | cell culture plastics suitable for hiPSC culture |
| nunc MicroWell 96-Well, Nunclon Delta-Treated, Flat-Bottom Microplate | Thermo Scientific | 167008 | cell culture plastics suitable for hiPSC culture |
| nutriFreez D10 Cryopreservation Medium | Sartorius | 05-713-1E | serum-free cryopreservation medium for cryopreservation of hiPSC and nephron progenitor cells |
| Opti-MEM | Gibco | 11058021 | electroporation medium |
| pCXLE-hMLN | Addgene | #27079 | plasmid for episomal reprogramming |
| pCXLE-hOCT3/4 plasmid | Addgene | #27077 | plasmid for episomal reprogramming |
| pCXLE-hSK plasmid | Addgene | #27078 | plasmid for episomal reprogramming |
| penicillin-streptomycin | Sigma-Aldrich | P4333-100ML | to avoid bacterial contamination |
| plastic coverslips | Sarstedt | 83.1840.002 | for immunofluorescent stainings of hiPSCs and hiPSC-derived podocytes |
| ROTI Histofix | Roth | P087.3 | commercial paraformaldehyde (4 %) for fixation of cells |
| RPMI 1640 + L-Glutamine | Gibco | 21875034 | basic medium for podocyte maintenance medium |
| staining chamber StainTray Black lid | Roth | HA51.1 | |
| stemPro Accutase Cell Dissociation Reagent | Gibco | A1110501 | enzymatic cell detachment solution used for dissociation of hiPSCs |
| sterile phosphate buffered saline (PBS) (1 x) | Gibco | 14190094 | used for washing and coating |
| sterile water | Roth | T1432 | |
| syringe without needle 20 mL | BD Plastipak | 300629 | to filter sterilize differentiation medium |
| TC dish 100 mm | Sarstedt | 8,33,902 | sterile cell culture plastics used for cutting the skin biopsy and fibroblast culture |
| TC dish 35 mm | Sarstedt | 8,33,900 | sterile cell culture plastics used for outgrowing fibroblasts from skin biopsy |
| triton X 100 | Roth | 3051.3 | for preincubation solution |
| trypan Blue Stain (0.4 %) for use with the Countess Automated Cell Counter | Invitrogen | T10282 | to count cells |
| trypsin-EDTA (10 x) | Biowest | X0930-100 | dissociation reagent used for fibroblasts and nephron progenitor cells |
| tube 15 mL | Greiner bio-one | 188271-N | |
| tube 50 mL | Greiner bio-one | 227261 | |
| vitronectin ACF | Sartorius | 05-754-0002 | extracellular matrix reagent used in coating solution to coat cell culture plastics suitable for hiPSC culture |
| Y-27632 dihydrochloride (10 mg) | Tocris | 1254 | to avoid apoptosis of hiPSCs during splitting |
| Primary antibodies | |||
| OCT4 | Stem Cell Technologies | 60093.1 | pluripotency marker, dilution 1:200 |
| SSEA-4 | Stem Cell Technologies | 60062FI.1 | pluripotency marker, dilution 1:100 |
| Ki67 | Abcam | ab15580 | proliferation marker, dilution 1:300 |
| synaptopodin | Proteintech | 21064-1-AP | podocyte-specific marker, dilution 1:200 |
| nephrin | Progen | GP-N2 | podocyte-specific marker, dilution 1:25 |
| podocin | proteintech | 20384-1-AP | podocyte-specific marker, dilution 1:100 |
| Secondary antibodies | |||
| goat anti-Guinea Pig IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor 555 | Invitrogen | A21435 | secondary anditbody, dilution 1:1000 |
| alexa Fluor 647 Goat Anti-Rabbit SFX Kit, highly cross-adsorbed | Invitrogen | A31634 | secondary anditbody, dilution 1:1000 |
| donkey anti-Rabbit IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor 488 | Invitrogen | A21206 | secondary anditbody, dilution 1:1000 |
| goat anti-Mouse IgG (H+L) Cross-Adsorbed Secondary Antibody, Alexa Fluor 555 | Invitrogen | A21422 | secondary anditbody, dilution 1:1000 |
| goat anti-Mouse IgG (H+L) Cross-Adsorbed Secondary Antibody, Alexa Fluor 488 | Invitrogen | A11001 | secondary anditbody, dilution 1:1000 |
References
- Mundel, P., et al. Rearrangements of the cytoskeleton and cell contacts induce process formation during differentiation of conditionally immortalized mouse podocyte cell lines. Experimental Cell Research. 236 (1), 248-258 (1997).
- Grgic, I., et al. Imaging of podocyte foot processes by fluorescence microscopy. Journal of the American Society of Nephrology. 23 (5), 785-791 (2012).
- Grahammer, F., Schell, C., Huber, T. B. The podocyte slit diaphragm-from a thin grey line to a complex signalling hub. Nature Reviews Nephrology. 9 (10), 587-598 (2013).
- Deen, W. M., Lazzara, M. J., Myers, B. D. Structural determinants of glomerular permeability. American Journal of Physiology. Renal Physiology. 281 (4), F579-F596 (2001).
- Schell, C., Huber, T. B. The evolving complexity of the podocyte cytoskeleton. Journal of the American Society of Nephrology. 28 (11), 3166-3174 (2017).
- Muller-Deile, J., Schiffer, M. Podocyte directed therapy of nephrotic syndrome-can we bring the inside out. Pediatric Nephrology. 31 (3), 393-405 (2016).
- Boehlke, C., et al. Hantavirus infection with severe proteinuria and podocyte foot-process effacement. American Journal of Kidney Diseases. 64 (3), 452-456 (2014).
- Schiffer, M., et al. Pharmacological targeting of actin-dependent dynamin oligomerization ameliorates chronic kidney disease in diverse animal models. Nature Medicine. 21 (6), 601-609 (2015).
- Kopp, J. B., et al. Podocytopathies. Nature Reviews. Disease Primers. 6 (1), 68 (2020).
- Wiggins, R. C. The spectrum of podocytopathies: a unifying view of glomerular diseases. Kidney International. 71 (12), 1205-1214 (2007).
- Mundel, P., Reiser, J., Kriz, W. Induction of differentiation in cultured rat and human podocytes. Journal of the American Society of Nephrology. 8 (5), 697-705 (1997).
- Jat, P. S., et al. Direct derivation of conditionally immortal cell lines from an H-2Kb-tsA58 transgenic mouse. Proceedings of the National Academy of Sciences. 88 (12), 5096-5100 (1991).
- Saleem, M. A., et al. A conditionally immortalized human podocyte cell line demonstrating nephrin and podocin expression. Journal of the American Society of Nephrology. 13 (3), 630-638 (2002).
- Eto, N., et al. Podocyte protection by darbepoetin: preservation of the cytoskeleton and nephrin expression. Kidney International. 72 (4), 455-463 (2007).
- Krtil, J., Platenik, J., Kazderova, M., Tesar, V., Zima, T. Culture methods of glomerular podocytes. Kidney & Blood Pressure Research. 30 (3), 162-174 (2007).
- Chittiprol, S., Chen, P., Petrovic-Djergovic, D., Eichler, T., Ransom, R. F. Marker expression, behaviors, and responses vary in different lines of conditionally immortalized cultured podocytes. American Journal of Physiology. Renal Physiology. 301 (3), F660-F671 (2011).
- Shih, N. Y., et al. CD2AP localizes to the slit diaphragm and binds to nephrin via a novel C-terminal domain. The American Journal of Pathology. 159 (6), 2303-2308 (2001).
- Yan, K., Khoshnoodi, J., Ruotsalainen, V., Tryggvason, K. N-linked glycosylation is critical for the plasma membrane localization of nephrin. Journal of the American Society of Nephrology. 13 (5), 1385-1389 (2002).
- Sir Elkhatim, R., Li, J. Y., Yong, T. Y., Gleadle, J. M. Dipping your feet in the water: podocytes in urine. Expert Review of Molecular Diagnostics. 14 (4), 423-437 (2014).
- Camici, M. Urinary detection of podocyte injury. Biomedicine & Pharmacotherapy. 61 (5), 245-249 (2007).
- Muller-Deile, J., et al. Overexpression of preeclampsia induced microRNA-26a-5p leads to proteinuria in zebrafish. Scientific Reports. 8 (1), 3621 (2018).
- Schenk, H., et al. Removal of focal segmental glomerulosclerosis (FSGS) factor suPAR using CytoSorb. Journal of Clinical Apheresis. 32 (6), 444-452 (2017).
- Petermann, A., Floege, J. Podocyte damage resulting in podocyturia: a potential diagnostic marker to assess glomerular disease activity. Nephron. Clinical Practice. 106 (2), c61-c66 (2007).
- Vogelmann, S. U., Nelson, W. J., Myers, B. D., Lemley, K. V. Urinary excretion of viable podocytes in health and renal disease. American Journal of Physiology. Renal Physiology. 285 (1), F40-F48 (2003).
- Petermann, A. T., et al. Podocytes that detach in experimental membranous nephropathy are viable. Kidney International. 64 (4), 1222-1231 (2003).
- Sakairi, T., et al. Conditionally immortalized human podocyte cell lines established from urine. American Journal of Physiology. Renal Physiology. 298 (3), F557-F567 (2010).
- Rauch, C., et al. Differentiation of human iPSCs into functional podocytes. PLoS One. 13 (9), e0203869 (2018).
- Musah, S., et al. Mature induced-pluripotent-stem-cell-derived human podocytes reconstitute kidney glomerular-capillary-wall function on a chip. Nature Biomedical Engineering. 1, 0069 (2017).
- Takahashi, K., Okita, K., Nakagawa, M., Yamanaka, S. Induction of pluripotent stem cells from fibroblast cultures. Nature Protocols. 2 (12), 3081-3089 (2007).
- Takahashi, K., Yamanaka, S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell. 126 (4), 663-676 (2006).
- Teshigawara, R., Cho, J., Kameda, M., Tada, T. Mechanism of human somatic reprogramming to iPS cell. Laboratory Investigation. 97 (10), 1152-1157 (2017).
- Bang, J. S., et al. Optimization of episomal reprogramming for generation of human induced pluripotent stem cells from fibroblasts. Animal Cells and Systems. 22 (2), 132-139 (2018).
- Okita, K., et al. A more efficient method to generate integration-free human iPS cells. Nature Methods. 8 (5), 409-412 (2011).
- Musah, S., Dimitrakakis, N., Camacho, D. M., Church, G. M., Ingber, D. E. Directed differentiation of human induced pluripotent stem cells into mature kidney podocytes and establishment of a Glomerulus Chip. Nature Protocols. 13 (7), 1662-1685 (2018).
- Burt, M., Bhattachaya, R., Okafor, A. E., Musah, S. Guided differentiation of mature kidney podocytes from human induced pluripotent stem cells under chemically defined conditions. Journal of Visualized Experiments. (161), e61299 (2020).
- Vangipuram, M., Ting, D., Kim, S., Diaz, R., Schule, B. Skin punch biopsy explant culture for derivation of primary human fibroblasts. Journal of Visualized Experiments. (77), e3779 (2013).
- Hoffding, M. K., Hyttel, P. Ultrastructural visualization of the Mesenchymal-to-Epithelial Transition during reprogramming of human fibroblasts to induced pluripotent stem cells. Stem Cell Research. 14 (1), 39-53 (2015).
- Bharathan, S. P., et al. Systematic evaluation of markers used for the identification of human induced pluripotent stem cells. Biology Open. 6 (1), 100-108 (2017).
- Scholzen, T., Gerdes, J. The Ki-67 protein: from the known and the unknown. Journal of Cellular Physiology. 182 (3), 311-322 (2000).
- Sun, X., Kaufman, P. D. Ki-67: more than a proliferation marker. Chromosoma. 127 (2), 175-186 (2018).
- Vaz, I. M., et al. Chromosomal aberrations after induced pluripotent stem cells reprogramming. Genetics and Molecular Biology. 44 (3), 20200147 (2021).
- Reiser, J., Altintas, M. M. Podocytes. F1000Research. 5, 114 (2016).
- Ohmori, T., et al. Impaired NEPHRIN localization in kidney organoids derived from nephrotic patient iPS cells. Scientific Reports. 11 (1), 3982 (2021).
- Morizane, R., Bonventre, J. V. Generation of nephron progenitor cells and kidney organoids from human pluripotent stem cells. Nature Protocols. 12 (1), 195-207 (2017).

