Transgenekspression i dyrkede celler ved anvendelse af urensede rekombinante adenoassocierede virale vektorer
Summary
Rekombinant adeno-associeret virus (rAAV) anvendes i vid udstrækning til klinisk og præklinisk genlevering. En undervurderet anvendelse til rAAV’er er den robuste transduktion af dyrkede celler uden behov for oprensning. For forskere, der er nye inden for rAAV, leverer vi en protokol til transgen-kassettekloning, råvektorproduktion og transduktion af cellekultur.
Abstract
Rekombinante adeno-associerede virale vektorer (rAAV) kan opnå potent og holdbar transgenekspression uden integration i en bred vifte af vævstyper, hvilket gør dem til et populært valg til genlevering i dyremodeller og i kliniske omgivelser. Ud over terapeutiske anvendelser er rAAV’er et nyttigt laboratorieværktøj til levering af transgener, der er skræddersyet til forskerens eksperimentelle behov og videnskabelige mål i dyrkede celler. Nogle eksempler inkluderer eksogene reportergener, overekspressionskassetter, RNA-interferens og CRISPR-baserede værktøjer, herunder dem til genom-wide screens. rAAV-transduktioner er mindre skadelige for celler end elektroporation eller kemisk transfektion og kræver ikke noget specielt udstyr eller dyre reagenser at producere. Rå lysater eller konditionerede medier indeholdende rAAV’er kan tilsættes direkte til dyrkede celler uden yderligere oprensning for at transducere mange celletyper – et undervurderet træk ved rAAV’er. Her leverer vi protokoller til grundlæggende transgen-kassettekloning og demonstrerer, hvordan man producerer og anvender rå rAAV-præparater på dyrkede celler. Som bevis for princippet demonstrerer vi transduktion af tre celletyper, der endnu ikke er rapporteret i rAAV-applikationer: placentaceller, myoblaster og tyndtarmorganoider. Vi diskuterer passende anvendelser til rå rAAV-præparater, begrænsningerne af rAAV’er til genlevering og overvejelser om valg af capsid. Denne protokol skitserer en enkel, billig og effektiv metode for forskere til at opnå produktiv DNA-levering i cellekultur ved hjælp af rAAV uden behov for besværlige titrerings- og oprensningstrin.
Introduction
Belysning af de molekylære baser af cellulære funktioner kræver ofte ekspression af transgent DNA i cellekultur. For at blive udtrykt skal transgener trænge gennem en celles selektive membran og nå kernen 1,2. Derfor er evnen til effektivt at omgå cellens fysiske barrierer og manipulere dens centrale processer en nødvendighed for at anvende transgenese til at afdække nye biologiske fænomener. En tilgang udnytter virussens iboende evne til at levere og udtrykke fremmed DNA 3,4.
Adeno-associeret virus (AAV) er en af de mindste pattedyrvirus: dens 4,7 kilobase (kb), enkeltstrengede DNA-genom indeholder to gener, rep (for replikation) og cap (for capsid), pakket inde i et 60-mer icosahedral capsid, der måler 25 nm. Rep / cap-generne har flere promotorer, læserammer og splejsningsprodukter, der koder for mindst ni unikke proteiner, der kræves til viral replikation, produktion og emballering 5,6. Derudover indeholder begge ender af genomet sekundære strukturer kaldet inverterede terminale gentagelser (ITR’er), der er nødvendige for DNA-replikation, genompakning og nedstrømsbehandling under transduktion 7,8,9,10. ITR’erne er de eneste DNA-elementer, der kræves til emballering af genomet i kapsiden, og derfor kan AAV klones til transgenleveringsformål ved at erstatte de virale rep / cap-gener med en forskers valg af regulatoriske elementer og / eller gener af interesse6. Den resulterende rekombinante AAV (rAAV), med et konstrueret vektorgenom (VG), anvendes i vid udstrækning i klinikken for human genterapi og har samlet succeser11. En undervurderet brug af vektoren er i laboratoriet; rAAV’er kan effektivt opnå transgenekspression i dyrkede celler for at opfylde en forskers eksperimentelle behov12.
Den mest almindelige metode til fremstilling af rAAV er ved triple-plasmidtransfektion til HEK293- eller 293T-celler (figur 1). Det første plasmid, almindeligvis kaldet cis-plasmidet, indeholder det ønskede transgen flankeret af ITR’er (pAAV). Afhængigt af applikationen kan cisplasmider med fælles elementer, såsom stærke promotorer eller CRISPR-baserede værktøjer, købes. Den anden er pRep / Cap-plasmidet, der indeholder vildtype AAV-rep– og cap-gener, der leveres i trans – dvs. på et separat, ikke-ITR-indeholdende plasmid, der udtrykker regulatoriske og strukturelle elementer, der derefter interagerer med cis-plasmidet – og kaldes således transplasmidet. Ud over fysisk at omslutte VG påvirker kapsiden cellulær tropisme12,13. Ved at levere det serotype-specifikke cap-gen in-trans er forskere let i stand til at maksimere transduktionseffektiviteten ved at vælge en optimeret capsid-serotype til deres givne målcelle. Endelig kræver AAV som et Dependoparvovirus en hjælpervirus for at aktivere rep / cap-ekspression fra sine virale promotorer, opnået ved adenovirale hjælpergener, tilvejebragt på et tredje plasmid såsom pAdΔF614,15. Efter 72 timers triple-plasmidtransfektion kan vektoren frigives fra producentceller til kulturmediet ved gentagne fryse-/optøningscyklusser. Hele pladens indhold opsamles derefter, og store cellulære affald fjernes ved centrifugering; den resulterende mediesupernatant er et råt rAAV-præparat, der er klar til downstream-transduktioner.
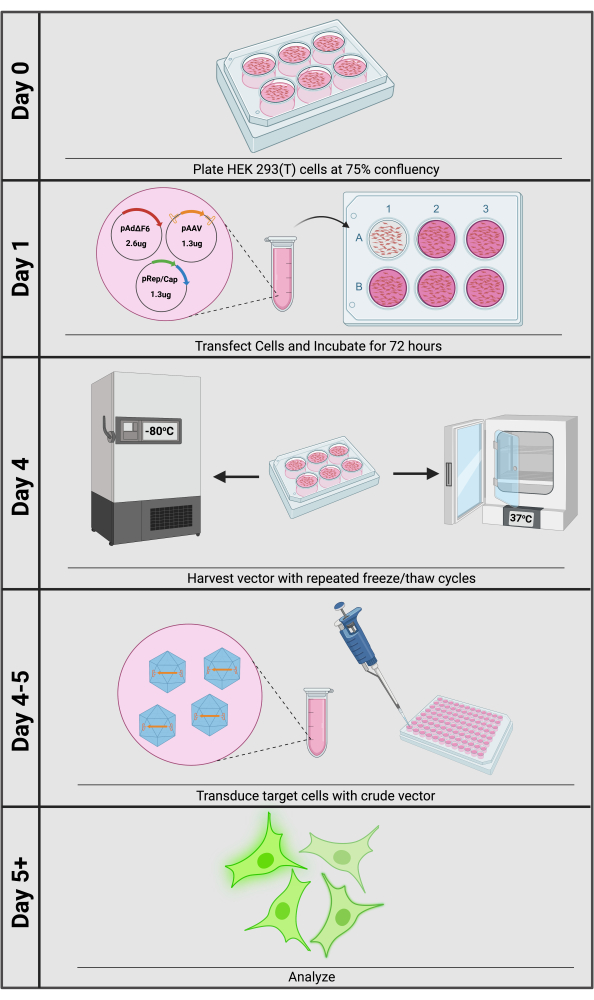
Figur 1: Oversigt over produktion af rå rAAV-vektorer. Rå rAAV produktion og transduktion kan udføres inden for 5 dage. Klik her for at se en større version af denne figur.
rAAV kan være mere gunstig for transgenlevering sammenlignet med andre transfektionsmetoder, som almindeligvis er forbundet med cellulær toksicitet, lav effektivitet og dyre reagenser og udstyr, såsom til elektroporation eller kemisk / lipidbaseret transfektion16,17. rAAV omgår disse forhindringer og giver ofte potent transgenekspression med minimal toksicitet og minimal praktisk tid. Det er vigtigt, at produktion af rAAV og anvendelse af det i cellekultur er enkel og sjældent kræver rensning af vektoren fra kulturmediet (figur 1). Derudover integrerer rAAV ikke sin VG i værtsgenomet, i modsætning til lentiviral transgenlevering, og sænker dermed risikoen for insertionel mutagenese18. På trods af de potentielle fordele ved at bruge rAAV til transgenlevering skal begrænsninger overvejes. Det er vigtigt, at transgenets størrelse, herunder ITR’erne, ikke overstiger 4,9 kb på grund af kapsidets fysiske begrænsninger, hvilket begrænser en forskers evne til effektivt at levere store regulatoriske elementer og transgener. Da rAAV desuden er en ikke-integrerende virus, resulterer transduktion i forbigående transgenekspression i delende celler og er muligvis ikke praktisk til stabil ekspression. Imidlertid kan metoder, der bruger dobbelt rAAV-leveret Cas9 og homologi-rettet reparation (HDR) skabeloner, bruges til stabilt at indsætte sekvenser på specifikke genomiske loci, hvis en forsker ønsker19.
Protocol
Representative Results
Discussion
Kloning
Kloningsprotokollen er ikke begrænset til plasmidet pAAV.CMV.Luc.IRES.EGFP.SV40, der anvendes ovenfor, og kan let ændres baseret på en forskers eksperimentelle behov. Mange ITR-holdige plasmider er let tilgængelige online til køb. For eksempel er plasmider indeholdende både Cas9 og et sgRNA-kloningssted tilgængelige, men kræver få yderligere trin såsom oligonukleotidglødning og PNK-behandling30. Derudover kan plasmider, der indeholder et multipelt kloningssted (MCS) med kun ITR’er og ingen indre reguleringselementer, findes31. Hvis forskellige plasmider skal anvendes, er restriktionsenzymerne (RE), der anvendes til fordøjelsen, typisk de eneste elementer, der muligvis skal ændres i denne protokol. En begrænsning af rAAV er dog dens begrænsede lastkapacitet. På grund af kapsidet fysiske begrænsninger bør vektorgenomet ikke overstige 4,9 kb, inklusive ITR’erne.
Ved isolering af plasmid fra bakterier er det afgørende at anvende et endotoksin-lavt eller -frit midiprep- eller maxiprep-kit til at afbøde skade på celler under triple-plasmidtransfektion eller transduktion. Plasmid fra miniprep-sæt indeholder ofte højere urenheder, reducerede koncentrationer og færre supercoiled DNA, som alle kan påvirke downstream-produktionen af rAAV og anbefales derfor ikke.
Det er afgørende at forstå ITR’s struktur og egenskaber under kloning. For det første er det ekstremt vanskeligt at bruge PCR gennem ITR. Kloningsdesign, der kræver PCR-forstærkning gennem ITR’er, bør undgås og desuden begrænse brugen af Gibson-samlingskloningsteknikken. Som sådan er restriktionsenzymkloning den foretrukne metode til kloning i ITR-holdige plasmider. Desuden er visse primere til Sanger-sekventering muligvis ikke kompatible, hvis det sekventerede område indeholder ITR. I stedet anbefales det at bruge primere, der sekvenserer væk fra ITR’erne og ind i vektorgenomlegemet for at få mere præcise sekventeringsresultater. For det andet er ITR’er tilbøjelige til deletioner, omlejringer og mutationer, når de omdannes til bakterier til plasmidamplifikation32,33. For at afbøde disse hændelser anbefales det at anvende kompetente bakteriestammer, såsom Stbl3, med rekombinationsmangel og inkubere dem ved 30 °C for at bremse celledelinger. Endelig er det blevet observeret, at mindre kolonier kan korrespondere med kloner uden omlejringer eller sletninger, da de uden ITR kan give en vækstfordel og være større. Derfor anbefales det at vælge kolonier, der er små.
Vektor produktion
Den vellykkede produktion af rAAV-vektor kan påvirkes af flere elementer. En kritisk faktor er sundheden for HEK293- eller 293T-celler, der anvendes til transfektion. Generelt er lave passagetal ideelle, da stærkt passerede celler kan udvise genotypiske og fænotypiske varianser, der kan reducere rAAV-titere. Derudover bør tætheden af de frøede celler være 75% -90% sammenløb for effektiv produktion. Sparsomme celler genererer lave vektorudbytter, fordi der er færre celler til rådighed til at producere vektorer, mens tilgroede celler ikke vil blive effektivt transfekteret.
Variationer mellem reagenspartier, cellebestande og generel lab-to-lab-variabilitet bidrager til forskelle i transfektionseffektivitet og produktionstiter. En optimerelig faktor, der kan føre til titerforbedringer, er plasmid: PEI-forholdet i transfektionsreaktioner. Det er vigtigt at bruge frisk (<1 måned gammel) PEI MAX. Det anbefales, at et plasmid:PEI-forhold på 1:1 anvendes som udgangspunkt, og hvis transfektions- eller transduktionseffektiviteten synes dårlig, skal du teste flere forskellige forhold. Titeroptimering er nemmest, hvis du bruger et transgen med en visuel aflæsning, såsom CMV.Luc.IRES.EGFP reporter trangen, der anvendes heri som udgangsmateriale til kloning. For at udføre optimeringen skal du følge protokoltrin 3 ved hjælp af en 12-brøndplade og nedskalere plasmidmasserne og reagensvolumenerne med to (den endelige plasmidmasse er 2,6 μg). Juster PEI-volumenet i overensstemmelse hermed, så det svarer til forhold fra 1: 0.75 til 1: 3, med stigende trin på 0.25 (figur 6). Hver reaktion fortyndes med 950 μL SF-medier efter 15 min. For nemheds skyld kan en masterblanding indeholdende de tredobbelte plasmider fremstilles og pipetteres individuelt i 1,5 ml rør, inden PEI tilsættes – se supplerende fil 2. Høst vektoren, transducerceller af interesse og billede. Brønden med den højeste transduktionseffektivitet (andel af GFP + celler) svarer til den højeste titer og mest optimale ratio af PEI:DNA.
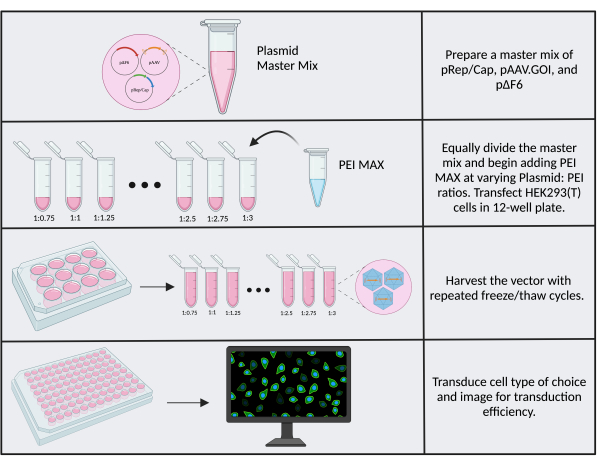
Figur 6: Arbejdsproces for optimering af PEI. Skematisk over de trin, der kræves til PEI-optimering. Flere forhold mellem plasmid: PEI testes for at bestemme det optimale forhold. Klik her for at se en større version af denne figur.
Overvejelser om høst og titer
Fryse-/optøningsteknikken, der anvendes til at høste rAAV-vektor, lyserer effektivt HEK293-celler på en måde, der er forenelig med den direkte anvendelse af det klarede lysat til transduce dyrkede celler. Visse rAAV-serotyper, såsom AAV1, AAV8 og AAV9, frigives fra celler under vektorproduktion og kan høstes fra det dyrkede cellemedium uden fryse-/optøningscyklusser34. Den her beskrevne metode giver typisk titere i størrelsesordenen 1 x 10 10 VG/ml ved brug af AAV2-kapsider og 1 x10 11 VG/ml for AAV8. Mens højere titere kan opnås ved vaskemiddel eller anden kemisk baseret lysis, er disse skadelige for celler i downstream-brug og kræver, at rAAV’er renses yderligere fra lysatet. Lavere titer er en afvejning, som en forsker bør overveje, når han bestemmer, om rå præparater er egnede til deres forskningsbehov, men de marginalt lavere titere produceret ved de metoder, der er beskrevet her, kan transducere mange celletyper meget godt (se repræsentative resultater). Ud over transfektionseffektivitet og cellesundhed varierer vektortitere afhængigt af kapsiden, der anvendes under rAAV-produktion og størrelsen og sekvensen af transgenet inden for VG35.
Ved høst af rå vektorpræparater kan plasmid-DNA, der blev anvendt under triple-plasmidtransfektion, være til stede, og selvom det er sjældent, resultere i nedstrøms transfektion under transduktion. Desuden kan uemballerede VG’er binde sig til ydersiden af kapsider og påberåbe sig et medfødt immunrespons på nøgen og fremmed enkeltstrenget DNA36,37. Derfor kan følsomme celletyper kræve, at vektorpræparater fordøjes og renses for at fjerne uemballerede VG’er og plasmid.
Hvis man ønsker at beregne titeren for et råpræparat, kan qPCR udføres for at kvantificere antallet af emballerede VG inde i DNase-resistente partikler (DRP). Kort fortalt fordøjes en lille mængde råpræparat DNase-fordøjet for at fjerne plasmid-DNA, forurenende nukleinsyrer eller delvist pakket VG. Prøven udsættes derefter for qPCR, og den beskyttede VG inde i DRP’er kvantificeres, hvilket resulterer i en titer med enheder af vektorgenom pr. ml råpræparat38. Det anbefales ikke at udføre vektortitrering ved hjælp af ELISA-baserede assays, der kvantificerer capsidtitere. Sammenlignet med vildtype AAV-virus lider rAAV af en andel tomme og delvist emballerede kapsider39. ELISA vil kvantificere alle kapsider uanset deres genomindhold og vil overvurdere de transducible enheder, der er til stede i et præparat, hvilket kræver en pakket VG.
Overvejelser om transduktion
Mange faktorer påvirker rAAV-transduktioner, og der bør tages passende hensyn til ethvert nyt eksperiment. Afhængigt af promotoren, der driver transgenekspression, kan ekspressionsdebut forekomme så tidligt som 4 timer efter transduktion (hpt), og topekspression opnås typisk med 48 hkt. Det er vigtigt at huske varigheden af tiden fra den indledende såning af celler til det eksperimentelle endepunkt. Dette er for at estimere cellernes startsammenløb og sikre, at de ikke vokser over ved afslutningen af eksperimentet. Hvis celler bliver oversammenflydende, kan cellulær adfærd ændres på grund af et stressrespons og kan forvirre eksperimentelle resultater. Nogle celletyper, som U2-OS, kan tolerere overvækst / kontakthæmning ganske godt. Derudover kan de modstå lange perioder (48 timer +) i serumfrit konditioneret medium – produktet af denne produktionsprotokol. Imidlertid kan følsomme celletyper kræve serumtilsætning eller fortynding af det rå præparat med specielt vækstmedium for at opretholde helbredet under transduktion. En let reduceret transduktionseffektivitet ved brug af serumholdige medier er en potentiel afvejning for cellesundhed og bør overvejes af forskeren.
For hurtigt delende celler er en startsammenløb på omkring 50% typisk optimal til applikationer, der afsluttes 48 hpt. Imidlertid kan sammenløbet justeres i overensstemmelse hermed baseret på eksperimentets behov. Det anbefales ikke at transducere udødeliggjorte cellelinjer af monolagstypen over 75% sammenløb på grund af nedsat transduktionseffektivitet. De fleste dyrkede celletyper transduceres med succes og sunde efter inkubation natten over med rå rAAV-præparater, efterfulgt af en ændring til friske serumholdige medier om morgenen.
Capsidserotype er en vigtig faktor at overveje, når der produceres rAAV til transducering af en målcelle, da kapsiden er den primære determinant for cellulær tropisme og efterfølgende transgenekspression13. AAV2 er en meget anvendt serotype på grund af dens evne til effektivt at transducere mange typer dyrkede celler12. Denne egenskab ved AAV2 kan tilskrives heparinsulfatproteoglycaner (HSPG’er), der tjener som den primære bindingsfaktor for AAV2 og de høje niveauer af HSPG’er på dyrkede celler fra tilpasningen til dyrkning i en skål40. Andre kapsider, såsom AAV9, er mindre effektive til at transducere brede celletyper og kan forklares ved deres afhængighedstilknytningsfaktorer, der ikke udtrykkes i denne indstilling41. Derfor anbefaler vi AAV2 som førstevalgskapsid i dyrkede celler, hvis en ønsket målcelle ikke tidligere er testet med rAAV i litteraturen.
Bemærk, at en væsentlig begrænsning ved rå vektorpræparater er, at de er uegnede til transducering af dyremodeller. In vivo-undersøgelser kræver, at præparaterne renses og underkastes en kvalitetsvurdering.
Transgenekspression og overvejelser om potentiel integration
rAAV’er resulterer ikke pålideligt i permanent ekspression af transgenet. Over tid kan VG’er blive tavse, og transgene udtryk kan lukkes ned efter flere passager42. Derudover forbliver størstedelen af VG’er episomale og rAAV’er indeholder ikke de virale Rep-proteiner, der ville formidle hyppig integration i værtsgenomet som i en vildtype viral lysogen infektion eller fremme replikation af VG’er43. Som et resultat vil episomer i transducerede celler til sidst blive fortyndet ud blandt datterceller gennem divisioner.
Integration på basalniveau er en mulighed for alt leveret transgent DNA-materiale. Imidlertid er ITR-holdige VG’er tilbøjelige til integration med en højere frekvens44. Derfor kan permanent ekspression af et transgen observeres i en lille delmængde af celler. Brugere bør overveje denne mulighed, især når de bruger rAAV til at levere DNA-skærende enzymer, såsom Cas9, da dobbeltstrengede brud kan resultere i en endnu større hyppighed af integration og permanent ekspression45. Selvom dette gør rAAV til en god kandidat til at levere homologirettede reparationsskabeloner til endogen mærkning eller gentilføjelse, bør muligheden for Cas9-indsættelse overvejes 19,46.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker Robert Tjian og Xavier Darzacq for deres støtte og brug af laboratorieudstyr. Vi takker Mark Kay for hans gave af KP1 og LK03 rep / cap plasmider, og Luk Vandenberghe for AAV4 rep / cap plasmid. Finansieringen blev ydet af Howard Hughes Medical Institute (34430, RT) og California Institute for Regenerative Medicine Training Program EDUC4-12790. N.W. anerkender finansiering fra Berkeley Stem Cell Center via et Siebel postdoc-stipendium og fra German Research Foundation (DFG) via et Walter Benjamin-stipendium.
Materials
| Snapgene DNA viewing sofrware | Snapgene | ||
| pAAV.CMV.Luc.IRES.EGFP.SV40 | AddGene | 105533 | |
| pAAV2/2 (Rep/Cap) | AddGene | 104963 | |
| pAdΔF6 | AddGene | 112867 | |
| LB Agar Carbenicillin | Sigma-Aldrich | L0418 | |
| Boekel Scientific Economy Digital Incubator | Boekel Scientific | 133000 | |
| LB medium, powder | MP Biomedicals | 113002042 | |
| Carbencillin (Disodium) | GoldBio | C-103-5 | |
| New Brunswick I26 Shaker | Eppendorf | M1324-0000 | |
| 50 mL Centrifuge Tubes | Corning | 430828 | |
| Centrifuge 5810 R | Eppendorf | 22627040 | |
| QIAGEN Plasmid Plus Midi Kit | Qiagen | 12945 | |
| PCR PULL-APART 8-TUBE STRIPS | USA Scientific | 1402-3900 | |
| Mastercycler nexus | Eppendorf | 6333000022 | |
| dNTP | Thermo Fisher Scientific | 18427013 | |
| 5x Phusion Buffer | NEB | B0518S | Provided with purchase of Phusion Polymerase |
| Phusion High-Fidelity DNA Polymerase | NEB | M0530S | |
| Gel Loading Dye, Orange (6X) | NEB | B7022S | |
| DNA Clean & Concentrator-100 | Zymo | D4029 | |
| Zymoclean Gel DNA Recovery Kit | Zymo | D4001 | |
| NotI-HF | NEB | R3189S | |
| EcoRI-HF | NEB | R3101S | |
| CutSmart Buffer (10x) | NEB | B6004S | Provided with purchase of restriction enzyme |
| UltraPure Agarose | Thermo Fisher Scientific | 16500100 | |
| Ethidium Bromide | Sigma-Aldrich | E1510 | |
| T4 DNA Ligase | NEB | M0202S | |
| T4 DNA Ligase Reaction Buffer | NEB | B0202S | Provided with purchase of T4 Ligase |
| Eppendorf Safe-Lock Tubes (1.5mL) | Eppendorf | 22363204 | |
| Precision Microprocessor Water Bath | Thermo Scientific | 51221046 | |
| Sterile Plastic Culture Tubes | Fisher Scientific | 149566B | |
| 2.0 mL Microcentrifuge Tube | Thomas Scientific | 1149Y01 | |
| ZR Plasmid Miniprep – Classic | Zymo | D4015 | |
| Xma1 | NEB | R0180S | |
| Sma1 | NEB | R0141S | |
| HEK 293T cells | ATCC | CRL-3216 | |
| Falcon 6-well | Corning | 353046 | |
| Gibco DMEM, high glucose, pyruvate | Thermo-Fisher | 11995065 | |
| Sanyo MCO-18AIC(UV) CO2 Incubator | Marshall Scientific | MCO-18AIC | |
| PEI MAX (Polyethylenimine Hydrochloride) | Polysciences | 24765-100 | |
| Mixer Vortex Genie 2 | Electron Microscopy Sciences | 102091-234 | |
| Sanyo Ultra Low Freezer | Sanyo | 14656-15267-16219 | |
| INCU-Line IL 10 with transparent window | VWR | 390-0384 | |
| Eppendorf Microcentrifuges | Eppendorf | 05-400-005 | |
| Falcon 96-well | Corning | 353072 | |
| C57BL/6J mice | JAX | strain #000664 | |
| organoid growth medium | STEMCELL Technologies | 6005 | |
| L Wnt-3A cells | ATCC | CRL-2647 | |
| nicotinamide | Sigma | N0636-100G | |
| ROCK inhibitor | STEMCELL Technologies | 72302 | |
| CHIR99021 | STEMCELL Technologies | 72052 | |
| Corning Matrigel Growth Factor Reduced (GFR) Basement Membrane | Fisher | 356231 | |
| 24-well plate | Fisher | 08-772-1 | |
| D-PBS | Thermo Fisher Scientific | 14-190-250 | |
| TrypLE Express | Fisher | 12604013 | |
| DMEM/F-12 with 15 mM HEPES | STEMCELL Technologies | 36254 | |
| polybrene | Millipore Sigma | TR-1003-G | |
| 48-well plates | Fisher | 08-772-3D | |
| Thermo Scientific Nunc Lab-Tek Chambered Coverglass | Fisher | 12-565-470 | |
| BeWo cells | ATCC | CCL-98 | |
| F-12K Medium | ATCC | 30-2004 | |
| Hepa1-6 | ATCC | CRL-1830 | |
| Huh7 | UC Berkeley BSD Cell Culture Facility | HUH-7 | |
| C2C12 | ATCC | CRL-1772 | |
| HSkMC | ATCC | PCS-950-010 | |
| Skeletal Muscle Cell Growth Medium | Sigma | C-23060 | |
| Skeletal Muscle Differentiation Medium | Sigma | C-23061 | |
| Invitrogen EVOS Digital Color Fluorescence Microscope | Fisher Scientific | 12-563-340 | |
| Perkin Elmer Opera Phenix | Perkin Elmer | HH14001000 | |
| PhenoPlate 96-well | Perkin Elmer | 6055302 | |
| DMEM, high glucose, no glutamine, no phenol red | Thermo-Fisher | 31053028 | |
| GlutaMAX Supplement | Thermo-Fisher | 35050079 | |
| Sodium Pyruvate | Thermo-Fisher | 11360070 | |
| pAAV2/5 (Rep/Cap) | Addgene | 104964 | |
| pAAV2/8 (Rep/Cap) | Addgene | 112864 | |
| pAAV-DJ-N589X (Rep/Cap) | Addgene | 130878 | |
| pAAV2/9n (Rep/Cap) | Addgene | 112865 | |
| pAnc80L65AAP | Addgene | 92307 | |
| KP1 (rep/cap) | gifted by Professor Mark Kay (Stanford University) | ||
| LK03 (rep/cap) | gifted by Professor Mark Kay (Stanford University) | ||
| pAAV4 (rep/cap) | gifted by Professor Luk Vandenberghe (Harvard Medical School) | ||
| pAAV.Cas9.sgRNA | Addgene | 61591 | |
| pAAV.MCS | Addgene | 46954 | |
| gBlock (synthetic DNA fragement) | IDT |
References
- Pillay, S., et al. Corrigendum: An essential receptor for adeno-associated virus infection. Nature. 539 (7629), 456 (2016).
- Nicolson, S. C., Samulski, R. J. Recombinant adeno-associated virus utilizes host cell nuclear import machinery to enter the nucleus. Journal of Virology. 88 (8), 4132-4144 (2014).
- Lundstrom, K. Viral Vectors in Gene Therapy. Diseases. 6 (2), 42 (2018).
- Daya, S., Berns, K. I. Gene therapy using adeno-associated virus vectors. Clinical Microbiology Reviews. 21 (4), 583-593 (2008).
- Ling, C., et al. The Adeno-Associated Virus Genome Packaging Puzzle. Journal of Molecular and Genetic Medicine. 9 (3), 175 (2015).
- Maurer, A. C., Weitzman, M. D. Adeno-Associated Virus Genome Interactions Important for Vector Production and Transduction. Human Gene Therapy. 31 (9-10), 499-511 (2020).
- Srivastava, A. Replication of the adeno-associated virus DNA termini in vitro. Intervirology. 27 (3), 138-147 (1987).
- Wang, X. S., Ponnazhagan, S., Srivastava, A. Rescue and replication of adeno-associated virus type 2 as well as vector DNA sequences from recombinant plasmids containing deletions in the viral inverted terminal repeats: selective encapsidation of viral genomes in progeny virions. Journal of Virology. 70 (3), 1668-1677 (1996).
- Earley, L. F., et al. Adeno-Associated Virus Serotype-Specific Inverted Terminal Repeat Sequence Role in Vector Transgene Expression. Human Gene Therapy. 31 (3-4), 151-162 (2020).
- Yang, J., et al. Concatamerization of adeno-associated virus circular genomes occurs through intermolecular recombination. Journal of Virology. 73 (11), 9468-9477 (1999).
- Au, H. K. E., Isalan, M., Mielcarek, M. Gene Therapy Advances: A Meta-Analysis of AAV Usage in Clinical Settings. Frontiers in Medicine. 8, 809118 (2021).
- Ellis, B. L., et al. A survey of ex vivo/in vitro transduction efficiency of mammalian primary cells and cell lines with Nine natural adeno-associated virus (AAV1-9) and one engineered adeno-associated virus serotype. Virology Journal. 10, 74 (2013).
- Zincarelli, C., Soltys, S., Rengo, G., Rabinowitz, J. E. Analysis of AAV serotypes 1-9 mediated gene expression and tropism in mice after systemic injection. Molecular Therapy. 16 (6), 1073-1080 (2008).
- Atchison, R. W., Casto, B. C., Hammon, W. M. Adenovirus-Associated Defective Virus Particles. Science. 149 (3685), 754-756 (1965).
- Meier, A. F., Fraefel, C., Seyffert, M. The Interplay between Adeno-Associated Virus and its Helper Viruses. Viruses. 12 (6), 662 (2020).
- Djurovic, S., Iversen, N., Jeansson, S., Hoover, F., Christensen, G. Comparison of nonviral transfection and adeno-associated viral transduction on cardiomyocytes. Molecular Biotechnology. 28 (1), 21-32 (2004).
- Batista Napotnik, T., Polajzer, T., Miklavcic, D. Cell death due to electroporation – A review. Bioelectrochemistry. 141, 107871 (2021).
- McCarty, D. M., Young, S. M., Samulski, R. J. Integration of adeno-associated virus (AAV) and recombinant AAV vectors. Annual Review of Genetics. 38, 819-845 (2004).
- Yang, Y., et al. A dual AAV system enables the Cas9-mediated correction of a metabolic liver disease in newborn mice. Nature Biotechnology. 34 (3), 334-338 (2016).
- Stacey, G. N. Cell culture contamination. Methods in Molecular Biology. 731, 79-91 (2011).
- Parks, W. P., Melnick, J. L., Rongey, R., Mayor, H. D. Physical assay and growth cycle studies of a defective adeno-satellite virus. Journal of Virology. 1 (1), 171-180 (1967).
- Bantel-Schaal, U., zur Hausen, H. Characterization of the DNA of a defective human parvovirus isolated from a genital site. Virology. 134 (1), 52-63 (1984).
- Gao, G. P., et al. Novel adeno-associated viruses from rhesus monkeys as vectors for human gene therapy. Proceedings of the National Academy of Science United States of America. 99 (18), 11854-11859 (2002).
- Gao, G., et al. Clades of Adeno-associated viruses are widely disseminated in human tissues. Journal of Virology. 78 (12), 6381-6388 (2004).
- Zinn, E., et al. In Silico Reconstruction of the Viral Evolutionary Lineage Yields a Potent Gene Therapy Vector. Cell Reports. 12 (6), 1056-1068 (2015).
- Grimm, D., et al. In vitro and in vivo gene therapy vector evolution via multispecies interbreeding and retargeting of adeno-associated viruses. Journal of Virology. 82 (12), 5887-5911 (2008).
- Lisowski, L., et al. Selection and evaluation of clinically relevant AAV variants in a xenograft liver model. Nature. 506 (7488), 382-386 (2014).
- Pekrun, K., et al. Using a barcoded AAV capsid library to select for clinically relevant gene therapy vectors. JCI Insight. 4 (22), e131610 (2019).
- Colon-Thillet, R., Jerome, K. R., Stone, D. Optimization of AAV vectors to target persistent viral reservoirs. Virology Journal. 18 (1), 85 (2021).
- Ran, F. A., et al. In vivo genome editing using Staphylococcus aureus Cas9. Nature. 520 (7546), 186-191 (2015).
- Britton, S., Coates, J., Jackson, S. P. A new method for high-resolution imaging of Ku foci to decipher mechanisms of DNA double-strand break repair. The Journal of Cell Biology. 202 (3), 579-595 (2013).
- Bi, X., Liu, L. F. DNA rearrangement mediated by inverted repeats. Proceedings of the National Academy of Science United States of America. 93 (2), 819-823 (1996).
- Samulski, R. J., Berns, K. I., Tan, M., Muzyczka, N. Cloning of adeno-associated virus into pBR322: rescue of intact virus from the recombinant plasmid in human cells. Proceedings of the National Academy of Science United States of America. 79 (6), 2077-2081 (1982).
- Vandenberghe, L. H., et al. Efficient serotype-dependent release of functional vector into the culture medium during adeno-associated virus manufacturing. Human Gene Therapy. 21 (10), 1251-1257 (2010).
- Sommer, J. M., et al. Quantification of adeno-associated virus particles and empty capsids by optical density measurement. Molecular Therapy. 7 (1), 122-128 (2003).
- Zhu, J., Huang, X., Yang, Y. The TLR9-MyD88 pathway is critical for adaptive immune responses to adeno-associated virus gene therapy vectors in mice. The Journal of Clinical Investigation. 119 (8), 2388-2398 (2009).
- Wagner, H., Bauer, S. All is not Toll: new pathways in DNA recognition. The Journal of Experimental Medicine. 203 (2), 265-268 (2006).
- Sanmiguel, J., Gao, G., Vandenberghe, L. H. Quantitative and Digital Droplet-Based AAV Genome Titration. Methods in Molecular Biology. 1950, 51-83 (2019).
- Grimm, D., et al. Titration of AAV-2 particles via a novel capsid ELISA: packaging of genomes can limit production of recombinant AAV-2. Gene Therapy. 6 (7), 1322-1330 (1999).
- Summerford, C., Samulski, R. J. Membrane-associated heparan sulfate proteoglycan is a receptor for adeno-associated virus type 2 virions. Journal of Virology. 72 (2), 1438-1445 (1998).
- Bell, C. L., et al. The AAV9 receptor and its modification to improve in vivo lung gene transfer in mice. The Journal of Clinical Investigation. 121 (6), 2427-2435 (2011).
- McCown, T. J., Xiao, X., Li, J., Breese, G. R., Samulski, R. J. Differential and persistent expression patterns of CNS gene transfer by an adeno-associated virus (AAV) vector. Brain Research. 713 (1-2), 99-107 (1996).
- Weitzman, M. D., Kyostio, S. R., Kotin, R. M., Owens, R. A. Adeno-associated virus (AAV) Rep proteins mediate complex formation between AAV DNA and its integration site in human DNA. Proceedings of the National Academy of Science United States of America. 91 (13), 5808-5812 (1994).
- Miller, D. G., Petek, L. M., Russell, D. W. Adeno-associated virus vectors integrate at chromosome breakage sites. Nature Genetics. 36 (7), 767-773 (2004).
- Hanlon, K. S., et al. High levels of AAV vector integration into CRISPR-induced DNA breaks. Nature Communications. 10 (1), 4439 (2019).
- Porteus, M. H., Cathomen, T., Weitzman, M. D., Baltimore, D. Efficient gene targeting mediated by adeno-associated virus and DNA double-strand breaks. Molecular and Cellular Biology. 23 (10), 3558-3565 (2003).

