Transgenuttryck i odlade celler med hjälp av orenade rekombinanta adenoassocierade virusvektorer
Summary
Rekombinant adenoassocierat virus (rAAV) används i stor utsträckning för klinisk och preklinisk genleverans. En underskattad användning för rAAV är den robusta transduktionen av odlade celler utan behov av rening. För forskare som är nya inom rAAV tillhandahåller vi ett protokoll för kloning av transgenkassetter, råvektorproduktion och cellodlingstransduktion.
Abstract
Rekombinanta adenoassocierade virala vektorer (rAAV) kan uppnå potent och hållbart transgenuttryck utan integration i ett brett spektrum av vävnadstyper, vilket gör dem till ett populärt val för genleverans i djurmodeller och i kliniska miljöer. Förutom terapeutiska tillämpningar är rAAVs ett användbart laboratorieverktyg för att leverera transgener skräddarsydda för forskarens experimentella behov och vetenskapliga mål i odlade celler. Några exempel är exogena reportergener, överuttryckskassetter, RNA-interferens och CRISPR-baserade verktyg, inklusive de för genomomfattande skärmar. rAAV-transduktioner är mindre skadliga för cellerna än elektroporering eller kemisk transfektion och kräver ingen speciell utrustning eller dyra reagenser för att produceras. Rålysat eller konditionerade medier som innehåller rAAVs kan tillsättas direkt till odlade celler utan ytterligare rening för att transducera många celltyper – en underskattad egenskap hos rAAVs. Här tillhandahåller vi protokoll för grundläggande transgen kassettkloning och demonstrerar hur man producerar och applicerar råa rAAV-preparat på odlade celler. Som bevis på principen visar vi transduktion av tre celltyper som ännu inte har rapporterats i rAAV-applikationer: placentaceller, myoblaster och tunntarmsorganoider. Vi diskuterar lämpliga användningsområden för råa rAAV-preparat, begränsningarna för rAAVs för genleverans och överväganden för kapsidval. Detta protokoll beskriver en enkel, billig och effektiv metod för forskare att uppnå produktiv DNA-leverans i cellkultur med hjälp av rAAV utan behov av mödosam titrering och reningssteg.
Introduction
Att klarlägga de molekylära grunderna för cellulära funktioner kräver ofta uttryck av transgent DNA i cellodling. För att kunna uttryckas måste transgener tränga igenom cellens selektiva membran och nå kärnan 1,2. Därför är förmågan att effektivt kringgå cellens fysiska barriärer och manipulera dess centrala processer en nödvändighet för att tillämpa transgenes för att avslöja nya biologiska fenomen. Ett tillvägagångssätt drar nytta av virusens inneboende förmåga att leverera och uttrycka främmande DNA 3,4.
Adeno-associerat virus (AAV) är ett av de minsta däggdjursvirusen: dess 4,7 kilobas (kb), enkelsträngade DNA-genom innehåller två gener, rep (för replikat) och lock (för kapsid), förpackade inuti en 60-mer ikosaedrisk kapsid som mäter 25 nm. Rep/cap-generna har flera promotorer, läsramar och skarvprodukter som kodar för minst nio unika proteiner som krävs för viral replikation, produktion och förpackning 5,6. Dessutom innehåller båda ändarna av genomet sekundära strukturer som kallas inverterade terminalupprepningar (ITR) som är nödvändiga för DNA-replikation, genompaketering och nedströmsbearbetning under transduktion 7,8,9,10. ITR:erna är de enda DNA-element som krävs för att paketera genomet i kapsiden, och därför kan AAV klonas för transgenleveransändamål genom att ersätta de virala rep/cap-generna med en forskares val av regulatoriska element och/eller gener av intresse6. Den resulterande rekombinanta AAV (rAAV), med ett konstruerat vektorgenom (VG), används i stor utsträckning i kliniken för human genterapi och har samlat på sig framgångar11. En underskattad användning av vektorn är i laboratoriet; rAAVs kan effektivt uppnå transgenuttryck i odlade celler för att uppfylla en forskares experimentella behov12.
Den vanligaste metoden för att producera rAAV är genom trippelplasmidtransfektion till HEK293- eller 293T-celler (figur 1). Den första plasmiden, vanligen kallad cis-plasmiden, innehåller den önskade transgenen flankerad av ITR (pAAV). Beroende på applikation finns cis-plasmider med gemensamma element, såsom starka promotorer eller CRISPR-baserade verktyg, att köpa. Den andra är pRep/Cap-plasmiden som innehåller vildtyps-AAV-rep- och cap-generna som tillhandahålls in-trans – dvs på en separat, icke-ITR-innehållande plasmid som uttrycker regulatoriska och strukturella element som sedan interagerar med cis-plasmiden – och kallas därför transplasmiden. Förutom att fysiskt omsluta VG påverkar kapsiden cellulär tropism12,13. Genom att tillhandahålla den serotypspecifika cap-genen in-trans kan forskare enkelt maximera transduktionseffektiviteten genom att välja en optimerad kapsidserotyp för sin givna målcell. Slutligen, som ett Dependoparvovirus, kräver AAV ett hjälparvirus för att aktivera rep/cap-uttryck från sina virala promotorer, vilket uppnås av adenovirala hjälpargener, som tillhandahålls på en tredje plasmid såsom pAdΔF614,15. Efter 72 timmars trippelplasmidtransfektion kan vektorn frisättas från producentceller till odlingsmediet genom upprepade frys-/upptiningscykler. Hela plattans innehåll samlas sedan upp och stora cellulära rester avlägsnas genom centrifugering; den resulterande mediasupernatanten är ett grovt rAAV-preparat som är redo för nedströms transduktioner.
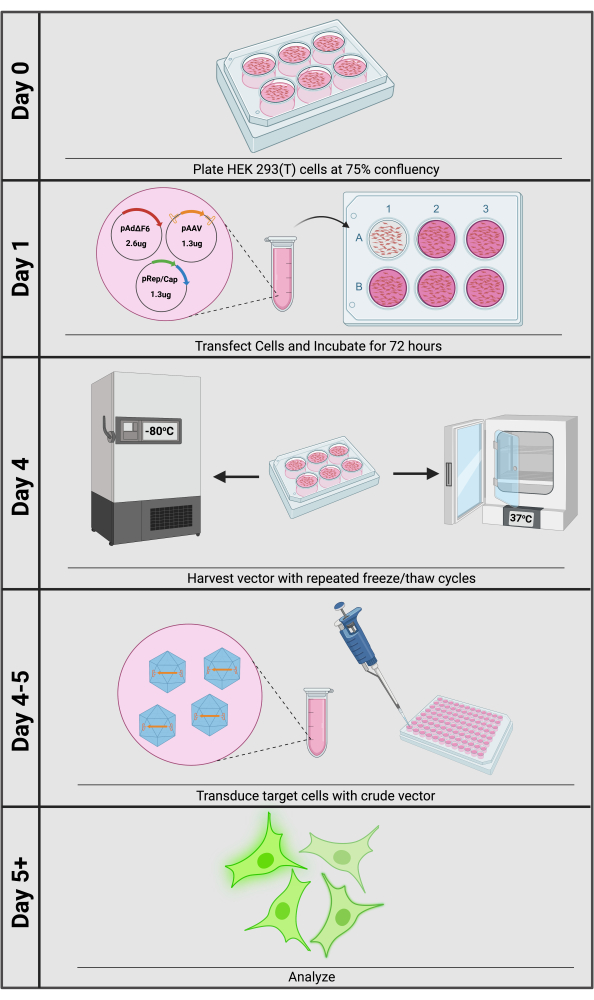
Figur 1: Översikt över produktionen av rAAV-vektorer i råolja. Rå rAAV-produktion och transduktion kan åstadkommas inom 5 dagar. Klicka här för att se en större version av denna figur.
rAAV kan vara mer gynnsamt för transgenleverans jämfört med andra transfektionsmetoder, som vanligtvis är förknippade med cellulär toxicitet, låg effektivitet och dyra reagenser och utrustning, såsom för elektroporering eller kemisk/lipidbaserad transfektion16,17. rAAV kringgår dessa hinder och ger ofta ett potent transgenuttryck med minimal toxicitet och minimal praktisk tid. Det är viktigt att det är enkelt att producera rAAV och tillämpa det i cellodling och att det sällan kräver rening av vektorn från odlingsmediet (figur 1). Dessutom integrerar rAAV inte sin VG i värdgenomet, till skillnad från lentiviral transgenleverans, och minskar därmed risken för insertionsmutagenes18. Trots de potentiella fördelarna med att använda rAAV för transgenleverans måste begränsningar beaktas. Det är viktigt att notera att storleken på transgenen, inklusive ITR, inte bör överstiga 4,9 kb på grund av kapsidens fysiska begränsningar, vilket begränsar en forskares förmåga att effektivt leverera stora regulatoriska element och transgener. Dessutom, eftersom rAAV är ett icke-integrerande virus, resulterar transduktion i transient transgenuttryck i delande celler och kanske inte är praktiskt för stabilt uttryck. Metoder som använder dubbla rAAV-levererade Cas9- och homologiriktade reparationsmallar (HDR) kan dock användas för att stabilt infoga sekvenser på specifika genomiska loci om enforskare så önskar.
Protocol
Representative Results
Discussion
Kloning
Kloningsprotokollet är inte begränsat till plasmiden pAAV.CMV.Luc.IRES.EGFP.SV40 som används ovan och kan enkelt ändras baserat på en forskares experimentella behov. Många ITR-innehållande plasmider finns lätt tillgängliga online för köp. Till exempel finns plasmider som innehåller både Cas9 och ett sgRNA-kloningsställe tillgängliga, men kräver få ytterligare steg såsom oligonukleotidglödgning och PNK-behandling30. Dessutom kan plasmider som innehåller ett multipelt kloningsställe (MCS) med endast ITR och utan inre regulatoriska element hittas31. Om olika plasmider ska användas är restriktionsenzymerna (RE) som används för matsmältning vanligtvis de enda elementen som kan behöva ändras i detta protokoll. En begränsning med rAAV är dock dess begränsade lastkapacitet. På grund av kapsidens fysiska begränsningar bör vektorgenomet inte överstiga 4,9 kb, inklusive ITR.
Vid isolering av plasmid från bakterier är det viktigt att använda ett endotoxin-lågt eller -fritt midiprep- eller maxiprep-kit för att mildra skador på celler under trippelplasmidtransfektion eller transduktion. Plasmider från miniprep-kit innehåller ofta högre föroreningar, minskade koncentrationer och färre superlindade DNA, som alla kan påverka nedströmsproduktionen av rAAV och rekommenderas därför inte.
Det är viktigt att förstå ITR:s struktur och egenskaper under kloning. För det första är det extremt svårt att använda PCR genom ITR. Kloningskonstruktioner som kräver PCR-amplifiering genom ITR bör undvikas och dessutom begränsa användningen av Gibson-kloningstekniken. Kloning med restriktionsenzymer är därför den föredragna metoden för kloning till ITR-innehållande plasmider. Dessutom kan det hända att vissa primers för Sanger-sekvensering inte är kompatibla om den sekvenserade regionen innehåller ITR. Istället rekommenderas det att använda primers som sekvenserar bort från ITR:erna och in i vektorgenomkroppen för att få mer exakta sekvenseringsresultat. För det andra är ITR benägna att raderas, omarrangeras och mutationer när de omvandlas till bakterier för plasmidamplifiering32,33. För att mildra dessa händelser rekommenderas att man använder kompetenta bakteriestammar med rekombinationsbrist, såsom Stbl3, och att inkubera dem vid 30 °C för att bromsa celldelningen. Slutligen har det observerats att mindre kolonier kan motsvara kloner utan omlagringar eller deletioner, eftersom de som saknar ITR kan ge en tillväxtfördel och vara större. Därför rekommenderas det att välja kolonier som är små.
Produktion av vektorer
En framgångsrik produktion av rAAV-vektor kan påverkas av flera faktorer. En kritisk faktor är hälsan hos HEK293- eller 293T-celler som används för transfektion. I allmänhet är låga passagetal idealiska, eftersom celler med hög passage kan uppvisa genotypiska och fenotypiska varianser som kan minska rAAV-titrar. Dessutom bör densiteten hos de sådda cellerna vara 75%-90% sammanflöde för effektiv produktion. Glesa celler genererar låga vektorutbyten eftersom det finns färre celler tillgängliga för att producera vektorer, medan övervuxna celler inte kommer att transfekteras effektivt.
Variationer mellan reagenspartier, celllager och allmän lab-till-lab-variabilitet bidrar till skillnader i transfektionseffektivitet och produktionstiter. En optimerbar faktor som kan leda till titerförbättringar är plasmid:PEI-förhållandet i transfektionsreaktioner. Det är viktigt att använda färsk (<1 månad gammal) PEI MAX. Det rekommenderas att ett plasmid:PEI-förhållande på 1:1 används som utgångspunkt, och om transfektionen eller transduktionseffektiviteten verkar dålig, testa flera olika förhållanden. Titeroptimering är enklast om man använder en transgen med visuell avläsning, såsom CMV.Luc.IRES.EGFP reporter trangene som används här som utgångsmaterial för kloning. För att utföra optimeringen, följ protokollsteg 3 med en 12-hålars platta och skala ner plasmidmassorna och reagensvolymerna med två (den slutliga plasmidmassan är 2,6 μg). Justera PEI-volymen i enlighet med detta för att motsvara förhållanden från 1:0.75 till 1:3, med ökande steg om 0.25 (figur 6). Späd varje reaktion med 950 μl SF-media efter 15 minuter. För enkelhetens skull kan en masterblandning som innehåller trippelplasmiderna tillverkas och pipetteras individuellt i 1,5 ml rör innan PEI tillsätts, se tilläggsfil 2. Skörda vektorn, transducera celler av intresse och bild. Brunnen med den högsta transduktionseffektiviteten (andelen GFP+-celler) motsvarar den högsta titern och det mest optimala förhållandet mellan PEI:DNA.
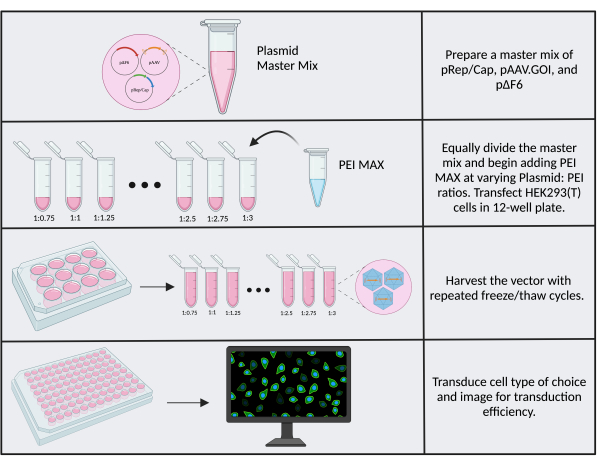
Bild 6: Arbetsflöde för PEI-optimering. Schematisk bild av de steg som krävs för PEI-optimering. Multipla plasmidförhållanden: PEI testas för att bestämma det optimala förhållandet. Klicka här för att se en större version av denna figur.
Att tänka på vid skörd och titer
Frys-/upptiningstekniken som används för att skörda rAAV-vektorn lyserar effektivt HEK293-celler på ett sätt som är förenligt med direkt användning av det klarade lysatet för att transducera odlade celler. Vissa rAAV-serotyper, såsom AAV1, AAV8 och AAV9, frisätts från celler under vektorproduktion och kan skördas från det odlade cellmediet utan frys-/upptiningscykler34. Metoden som beskrivs här ger vanligtvis titrar i storleksordningen 1 x 10 10 VG/ml vid användning av AAV2-kapsider och 1 x10 11 VG/ml för AAV8. Även om högre titrar kan uppnås genom tvättmedel eller annan kemikaliebaserad lys, är dessa skadliga för celler i nedströms användning och kräver att rAAVs renas ytterligare från lysatet. Lägre titer är en avvägning som en forskare bör överväga när de avgör om råa preparat är lämpliga för deras forskningsbehov, men de marginellt lägre titrarna som produceras med de metoder som beskrivs här kan transducera många celltyper mycket bra (se representativa resultat). Förutom transfektionseffektivitet och cellhälsa varierar vektortitrarna beroende på kapsiden som används under rAAV-produktionen och storleken och sekvensen av transgenen inom VG35.
Vid skörd av råa vektorpreparat kan plasmid-DNA som användes under trippelplasmidtransfektion förekomma och, även om det är sällsynt, resultera i nedströmstransfektion under transduktion. Dessutom kan oförpackade VG binda till utsidan av kapsider och åberopa ett medfött immunsvar mot naket och främmande enkelsträngat DNA36,37. Därför kan känsliga celltyper kräva att vektorpreparat DNas smälts och renas för att avlägsna oförpackade VG och plasmider.
Om man vill beräkna titern för ett råpreparat kan qPCR utföras för att kvantifiera antalet förpackade VG inuti DNasresistenta partiklar (DRP). Kortfattat kan man säga att en liten mängd råpreparat DNas-smälts för att avlägsna plasmid-DNA, kontaminerande nukleinsyror eller delvis förpackad VG. Provet utsätts sedan för qPCR och den skyddade VG inuti DRP kvantifieras, vilket resulterar i en titer med enheter av vektorgenom per ml råpreparat38. Det rekommenderas inte att utföra vektortitrering med ELISA-baserade analyser som kvantifierar kapsidtitrater. Jämfört med AAV-virus av vildtyp lider rAAV av en andel tomma och delvis förpackade kapsider39. ELISA kommer att kvantifiera alla kapsider oavsett deras genominnehåll och kommer att överskatta de transducibla enheter som finns i ett preparat, vilket kräver en förpackad VG.
Att tänka på vid transduktion
Många faktorer påverkar rAAV-transduktioner och lämpliga överväganden bör göras för alla nya experiment. Beroende på promotorn som driver transgenuttrycket, kan uttrycksdebuten ske så tidigt som 4 timmar efter transduktion (hpt), och topputtryck uppnås vanligtvis vid 48 hpt. Det är viktigt att komma ihåg hur lång tid det tar från den första sådden av celler till det experimentella effektmåttet. Detta för att uppskatta cellernas startsammanflöde och se till att de inte växer för mycket i slutet av experimentet. Om cellerna blir överkonfluenta kan cellulärt beteende förändras på grund av en stressrespons och kan förvirra experimentella resultat. Vissa celltyper, som U2-OS, tål överväxt/kontakthämning ganska bra. Dessutom tål de långa perioder (48 h+) i serumfritt konditionerat medium – produkten av detta produktionsprotokoll. Känsliga celltyper kan dock kräva serumtillsats eller utspädning av det råa preparatet med ett speciellt odlingsmedium för att bibehålla hälsan under transduktionen. En något minskad transduktionseffektivitet från användning av seruminnehållande media är en potentiell kompromiss för cellhälsan och bör övervägas av forskaren.
Vanligtvis, för celler som delar sig snabbt, är ett startsammanflöde på cirka 50 % optimalt för applikationer som kommer att avslutas 48 hpt. Sammanflödet kan dock justeras i enlighet med detta baserat på experimentets behov. Det rekommenderas inte att transducera odödliga cellinjer av monolagertyp över 75 % sammanflöde på grund av minskad transduktionseffektivitet. De flesta odlade celltyper är framgångsrikt transducerade och friska efter inkubation över natten med råa rAAV-preparat, följt av ett byte till färska seruminnehållande medier på morgonen.
Kapsidserotyp är en viktig faktor att ta hänsyn till när man producerar rAAV för att transducera en målcell, eftersom kapsiden är den primära determinanten för cellulär tropism och efterföljande transgenuttryck13. AAV2 är en allmänt använd serotyp på grund av dess förmåga att effektivt överföra många typer av odlade celler12. Denna egenskap hos AAV2 kan tillskrivas heparinsulfatproteoglykaner (HSPG) som fungerar som den primära bindningsfaktorn för AAV2 och de höga nivåerna av HSPG på odlade celler från anpassning till odling i en maträtt40. Andra kapsider, såsom AAV9, är mindre effektiva när det gäller att transducera breda celltyper och kan förklaras av deras beroendebindningsfaktorer som inte uttrycks i denna inställning41. Därför rekommenderar vi AAV2 som förstahandsval av kapsid i odlade celler om en önskad målcell inte tidigare har testats med rAAV i litteraturen.
Observera att en stor begränsning med råa vektorpreparat är att de är olämpliga för transducering av djurmodeller. In vivo-studier kräver att preparaten renas och genomgår en kvalitetsbedömning.
Transgenuttryck och potentiella integrationsöverväganden
rAAV leder inte på ett tillförlitligt sätt till permanent uttryck av transgenen. Med tiden kan VG tystas och transgena uttryck kan stängas av efter flera passager42. Dessutom förblir majoriteten av VG episomala och rAAVs innehåller inte de virala Rep-proteiner som skulle förmedla frekvent integration i värdgenomet som i en vildtypsviral lysogen infektion eller främja replikation av VG43. Som ett resultat kommer episomer i transducerade celler så småningom att spädas ut bland dottercellerna genom delningar.
Integrering på basalnivå är en möjlighet för allt levererat transgent DNA-material. ITR-innehållande VG:er är dock benägna att integreras med en högre frekvens44. Därför kan permanent uttryck av en transgen observeras i en liten undergrupp av celler. Användare bör överväga denna möjlighet, särskilt när de använder rAAV för att leverera DNA-skärande enzymer, såsom Cas9, eftersom dubbelsträngade brott kan resultera i en ännu högre frekvens av integration och permanent uttryck45. Även om detta gör rAAV till en bra kandidat för att leverera homologiriktade reparationsmallar för endogen märkning eller genaddition, bör möjligheten till Cas9-insättning övervägas19,46.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi tackar Robert Tjian och Xavier Darzacq för deras stöd och användning av laboratorieutrustning. Vi tackar Mark Kay för hans gåva av KP1 och LK03 rep/cap plasmiderna, och Luk Vandenberghe för AAV4 rep/cap plasmid. Finansieringen tillhandahölls av Howard Hughes Medical Institute (34430, R. T.) och California Institute for Regenerative Medicine Training Program EDUC4-12790. N.W. bekräftar finansiering från Berkeley Stem Cell Center via ett postdoktoralt stipendium från Siebel och från German Research Foundation (DFG) via ett Walter Benjamin-stipendium.
Materials
| Snapgene DNA viewing sofrware | Snapgene | ||
| pAAV.CMV.Luc.IRES.EGFP.SV40 | AddGene | 105533 | |
| pAAV2/2 (Rep/Cap) | AddGene | 104963 | |
| pAdΔF6 | AddGene | 112867 | |
| LB Agar Carbenicillin | Sigma-Aldrich | L0418 | |
| Boekel Scientific Economy Digital Incubator | Boekel Scientific | 133000 | |
| LB medium, powder | MP Biomedicals | 113002042 | |
| Carbencillin (Disodium) | GoldBio | C-103-5 | |
| New Brunswick I26 Shaker | Eppendorf | M1324-0000 | |
| 50 mL Centrifuge Tubes | Corning | 430828 | |
| Centrifuge 5810 R | Eppendorf | 22627040 | |
| QIAGEN Plasmid Plus Midi Kit | Qiagen | 12945 | |
| PCR PULL-APART 8-TUBE STRIPS | USA Scientific | 1402-3900 | |
| Mastercycler nexus | Eppendorf | 6333000022 | |
| dNTP | Thermo Fisher Scientific | 18427013 | |
| 5x Phusion Buffer | NEB | B0518S | Provided with purchase of Phusion Polymerase |
| Phusion High-Fidelity DNA Polymerase | NEB | M0530S | |
| Gel Loading Dye, Orange (6X) | NEB | B7022S | |
| DNA Clean & Concentrator-100 | Zymo | D4029 | |
| Zymoclean Gel DNA Recovery Kit | Zymo | D4001 | |
| NotI-HF | NEB | R3189S | |
| EcoRI-HF | NEB | R3101S | |
| CutSmart Buffer (10x) | NEB | B6004S | Provided with purchase of restriction enzyme |
| UltraPure Agarose | Thermo Fisher Scientific | 16500100 | |
| Ethidium Bromide | Sigma-Aldrich | E1510 | |
| T4 DNA Ligase | NEB | M0202S | |
| T4 DNA Ligase Reaction Buffer | NEB | B0202S | Provided with purchase of T4 Ligase |
| Eppendorf Safe-Lock Tubes (1.5mL) | Eppendorf | 22363204 | |
| Precision Microprocessor Water Bath | Thermo Scientific | 51221046 | |
| Sterile Plastic Culture Tubes | Fisher Scientific | 149566B | |
| 2.0 mL Microcentrifuge Tube | Thomas Scientific | 1149Y01 | |
| ZR Plasmid Miniprep – Classic | Zymo | D4015 | |
| Xma1 | NEB | R0180S | |
| Sma1 | NEB | R0141S | |
| HEK 293T cells | ATCC | CRL-3216 | |
| Falcon 6-well | Corning | 353046 | |
| Gibco DMEM, high glucose, pyruvate | Thermo-Fisher | 11995065 | |
| Sanyo MCO-18AIC(UV) CO2 Incubator | Marshall Scientific | MCO-18AIC | |
| PEI MAX (Polyethylenimine Hydrochloride) | Polysciences | 24765-100 | |
| Mixer Vortex Genie 2 | Electron Microscopy Sciences | 102091-234 | |
| Sanyo Ultra Low Freezer | Sanyo | 14656-15267-16219 | |
| INCU-Line IL 10 with transparent window | VWR | 390-0384 | |
| Eppendorf Microcentrifuges | Eppendorf | 05-400-005 | |
| Falcon 96-well | Corning | 353072 | |
| C57BL/6J mice | JAX | strain #000664 | |
| organoid growth medium | STEMCELL Technologies | 6005 | |
| L Wnt-3A cells | ATCC | CRL-2647 | |
| nicotinamide | Sigma | N0636-100G | |
| ROCK inhibitor | STEMCELL Technologies | 72302 | |
| CHIR99021 | STEMCELL Technologies | 72052 | |
| Corning Matrigel Growth Factor Reduced (GFR) Basement Membrane | Fisher | 356231 | |
| 24-well plate | Fisher | 08-772-1 | |
| D-PBS | Thermo Fisher Scientific | 14-190-250 | |
| TrypLE Express | Fisher | 12604013 | |
| DMEM/F-12 with 15 mM HEPES | STEMCELL Technologies | 36254 | |
| polybrene | Millipore Sigma | TR-1003-G | |
| 48-well plates | Fisher | 08-772-3D | |
| Thermo Scientific Nunc Lab-Tek Chambered Coverglass | Fisher | 12-565-470 | |
| BeWo cells | ATCC | CCL-98 | |
| F-12K Medium | ATCC | 30-2004 | |
| Hepa1-6 | ATCC | CRL-1830 | |
| Huh7 | UC Berkeley BSD Cell Culture Facility | HUH-7 | |
| C2C12 | ATCC | CRL-1772 | |
| HSkMC | ATCC | PCS-950-010 | |
| Skeletal Muscle Cell Growth Medium | Sigma | C-23060 | |
| Skeletal Muscle Differentiation Medium | Sigma | C-23061 | |
| Invitrogen EVOS Digital Color Fluorescence Microscope | Fisher Scientific | 12-563-340 | |
| Perkin Elmer Opera Phenix | Perkin Elmer | HH14001000 | |
| PhenoPlate 96-well | Perkin Elmer | 6055302 | |
| DMEM, high glucose, no glutamine, no phenol red | Thermo-Fisher | 31053028 | |
| GlutaMAX Supplement | Thermo-Fisher | 35050079 | |
| Sodium Pyruvate | Thermo-Fisher | 11360070 | |
| pAAV2/5 (Rep/Cap) | Addgene | 104964 | |
| pAAV2/8 (Rep/Cap) | Addgene | 112864 | |
| pAAV-DJ-N589X (Rep/Cap) | Addgene | 130878 | |
| pAAV2/9n (Rep/Cap) | Addgene | 112865 | |
| pAnc80L65AAP | Addgene | 92307 | |
| KP1 (rep/cap) | gifted by Professor Mark Kay (Stanford University) | ||
| LK03 (rep/cap) | gifted by Professor Mark Kay (Stanford University) | ||
| pAAV4 (rep/cap) | gifted by Professor Luk Vandenberghe (Harvard Medical School) | ||
| pAAV.Cas9.sgRNA | Addgene | 61591 | |
| pAAV.MCS | Addgene | 46954 | |
| gBlock (synthetic DNA fragement) | IDT |
References
- Pillay, S., et al. Corrigendum: An essential receptor for adeno-associated virus infection. Nature. 539 (7629), 456 (2016).
- Nicolson, S. C., Samulski, R. J. Recombinant adeno-associated virus utilizes host cell nuclear import machinery to enter the nucleus. Journal of Virology. 88 (8), 4132-4144 (2014).
- Lundstrom, K. Viral Vectors in Gene Therapy. Diseases. 6 (2), 42 (2018).
- Daya, S., Berns, K. I. Gene therapy using adeno-associated virus vectors. Clinical Microbiology Reviews. 21 (4), 583-593 (2008).
- Ling, C., et al. The Adeno-Associated Virus Genome Packaging Puzzle. Journal of Molecular and Genetic Medicine. 9 (3), 175 (2015).
- Maurer, A. C., Weitzman, M. D. Adeno-Associated Virus Genome Interactions Important for Vector Production and Transduction. Human Gene Therapy. 31 (9-10), 499-511 (2020).
- Srivastava, A. Replication of the adeno-associated virus DNA termini in vitro. Intervirology. 27 (3), 138-147 (1987).
- Wang, X. S., Ponnazhagan, S., Srivastava, A. Rescue and replication of adeno-associated virus type 2 as well as vector DNA sequences from recombinant plasmids containing deletions in the viral inverted terminal repeats: selective encapsidation of viral genomes in progeny virions. Journal of Virology. 70 (3), 1668-1677 (1996).
- Earley, L. F., et al. Adeno-Associated Virus Serotype-Specific Inverted Terminal Repeat Sequence Role in Vector Transgene Expression. Human Gene Therapy. 31 (3-4), 151-162 (2020).
- Yang, J., et al. Concatamerization of adeno-associated virus circular genomes occurs through intermolecular recombination. Journal of Virology. 73 (11), 9468-9477 (1999).
- Au, H. K. E., Isalan, M., Mielcarek, M. Gene Therapy Advances: A Meta-Analysis of AAV Usage in Clinical Settings. Frontiers in Medicine. 8, 809118 (2021).
- Ellis, B. L., et al. A survey of ex vivo/in vitro transduction efficiency of mammalian primary cells and cell lines with Nine natural adeno-associated virus (AAV1-9) and one engineered adeno-associated virus serotype. Virology Journal. 10, 74 (2013).
- Zincarelli, C., Soltys, S., Rengo, G., Rabinowitz, J. E. Analysis of AAV serotypes 1-9 mediated gene expression and tropism in mice after systemic injection. Molecular Therapy. 16 (6), 1073-1080 (2008).
- Atchison, R. W., Casto, B. C., Hammon, W. M. Adenovirus-Associated Defective Virus Particles. Science. 149 (3685), 754-756 (1965).
- Meier, A. F., Fraefel, C., Seyffert, M. The Interplay between Adeno-Associated Virus and its Helper Viruses. Viruses. 12 (6), 662 (2020).
- Djurovic, S., Iversen, N., Jeansson, S., Hoover, F., Christensen, G. Comparison of nonviral transfection and adeno-associated viral transduction on cardiomyocytes. Molecular Biotechnology. 28 (1), 21-32 (2004).
- Batista Napotnik, T., Polajzer, T., Miklavcic, D. Cell death due to electroporation – A review. Bioelectrochemistry. 141, 107871 (2021).
- McCarty, D. M., Young, S. M., Samulski, R. J. Integration of adeno-associated virus (AAV) and recombinant AAV vectors. Annual Review of Genetics. 38, 819-845 (2004).
- Yang, Y., et al. A dual AAV system enables the Cas9-mediated correction of a metabolic liver disease in newborn mice. Nature Biotechnology. 34 (3), 334-338 (2016).
- Stacey, G. N. Cell culture contamination. Methods in Molecular Biology. 731, 79-91 (2011).
- Parks, W. P., Melnick, J. L., Rongey, R., Mayor, H. D. Physical assay and growth cycle studies of a defective adeno-satellite virus. Journal of Virology. 1 (1), 171-180 (1967).
- Bantel-Schaal, U., zur Hausen, H. Characterization of the DNA of a defective human parvovirus isolated from a genital site. Virology. 134 (1), 52-63 (1984).
- Gao, G. P., et al. Novel adeno-associated viruses from rhesus monkeys as vectors for human gene therapy. Proceedings of the National Academy of Science United States of America. 99 (18), 11854-11859 (2002).
- Gao, G., et al. Clades of Adeno-associated viruses are widely disseminated in human tissues. Journal of Virology. 78 (12), 6381-6388 (2004).
- Zinn, E., et al. In Silico Reconstruction of the Viral Evolutionary Lineage Yields a Potent Gene Therapy Vector. Cell Reports. 12 (6), 1056-1068 (2015).
- Grimm, D., et al. In vitro and in vivo gene therapy vector evolution via multispecies interbreeding and retargeting of adeno-associated viruses. Journal of Virology. 82 (12), 5887-5911 (2008).
- Lisowski, L., et al. Selection and evaluation of clinically relevant AAV variants in a xenograft liver model. Nature. 506 (7488), 382-386 (2014).
- Pekrun, K., et al. Using a barcoded AAV capsid library to select for clinically relevant gene therapy vectors. JCI Insight. 4 (22), e131610 (2019).
- Colon-Thillet, R., Jerome, K. R., Stone, D. Optimization of AAV vectors to target persistent viral reservoirs. Virology Journal. 18 (1), 85 (2021).
- Ran, F. A., et al. In vivo genome editing using Staphylococcus aureus Cas9. Nature. 520 (7546), 186-191 (2015).
- Britton, S., Coates, J., Jackson, S. P. A new method for high-resolution imaging of Ku foci to decipher mechanisms of DNA double-strand break repair. The Journal of Cell Biology. 202 (3), 579-595 (2013).
- Bi, X., Liu, L. F. DNA rearrangement mediated by inverted repeats. Proceedings of the National Academy of Science United States of America. 93 (2), 819-823 (1996).
- Samulski, R. J., Berns, K. I., Tan, M., Muzyczka, N. Cloning of adeno-associated virus into pBR322: rescue of intact virus from the recombinant plasmid in human cells. Proceedings of the National Academy of Science United States of America. 79 (6), 2077-2081 (1982).
- Vandenberghe, L. H., et al. Efficient serotype-dependent release of functional vector into the culture medium during adeno-associated virus manufacturing. Human Gene Therapy. 21 (10), 1251-1257 (2010).
- Sommer, J. M., et al. Quantification of adeno-associated virus particles and empty capsids by optical density measurement. Molecular Therapy. 7 (1), 122-128 (2003).
- Zhu, J., Huang, X., Yang, Y. The TLR9-MyD88 pathway is critical for adaptive immune responses to adeno-associated virus gene therapy vectors in mice. The Journal of Clinical Investigation. 119 (8), 2388-2398 (2009).
- Wagner, H., Bauer, S. All is not Toll: new pathways in DNA recognition. The Journal of Experimental Medicine. 203 (2), 265-268 (2006).
- Sanmiguel, J., Gao, G., Vandenberghe, L. H. Quantitative and Digital Droplet-Based AAV Genome Titration. Methods in Molecular Biology. 1950, 51-83 (2019).
- Grimm, D., et al. Titration of AAV-2 particles via a novel capsid ELISA: packaging of genomes can limit production of recombinant AAV-2. Gene Therapy. 6 (7), 1322-1330 (1999).
- Summerford, C., Samulski, R. J. Membrane-associated heparan sulfate proteoglycan is a receptor for adeno-associated virus type 2 virions. Journal of Virology. 72 (2), 1438-1445 (1998).
- Bell, C. L., et al. The AAV9 receptor and its modification to improve in vivo lung gene transfer in mice. The Journal of Clinical Investigation. 121 (6), 2427-2435 (2011).
- McCown, T. J., Xiao, X., Li, J., Breese, G. R., Samulski, R. J. Differential and persistent expression patterns of CNS gene transfer by an adeno-associated virus (AAV) vector. Brain Research. 713 (1-2), 99-107 (1996).
- Weitzman, M. D., Kyostio, S. R., Kotin, R. M., Owens, R. A. Adeno-associated virus (AAV) Rep proteins mediate complex formation between AAV DNA and its integration site in human DNA. Proceedings of the National Academy of Science United States of America. 91 (13), 5808-5812 (1994).
- Miller, D. G., Petek, L. M., Russell, D. W. Adeno-associated virus vectors integrate at chromosome breakage sites. Nature Genetics. 36 (7), 767-773 (2004).
- Hanlon, K. S., et al. High levels of AAV vector integration into CRISPR-induced DNA breaks. Nature Communications. 10 (1), 4439 (2019).
- Porteus, M. H., Cathomen, T., Weitzman, M. D., Baltimore, D. Efficient gene targeting mediated by adeno-associated virus and DNA double-strand breaks. Molecular and Cellular Biology. 23 (10), 3558-3565 (2003).

