Tredimensionel bioprint af humane iPSC-afledte neuron-astrocyt-kokulturer til screeningsapplikationer
Summary
Her præsenterer vi en protokol til fremstilling af 3D-bioprintede cokulturer af iPSC-afledte neuroner og astrocytter. Denne samkulturmodel, der genereres inden for et hydrogelstillads i 96- eller 384-brøndformater, demonstrerer høj levedygtighed efter udskrivning og neuritvækst inden for 7 dage og viser ekspressionen af modenhedsmarkører for begge celletyper.
Abstract
For at en cellemodel skal være levedygtig til lægemiddelscreening, skal systemet opfylde krav til gennemstrømning og homogenitet sammen med at have en effektiv udviklingstid. Mange offentliggjorte 3D-modeller opfylder dog ikke disse kriterier. Dette begrænser derfor deres anvendelighed i tidlige lægemiddelopdagelsesapplikationer. Tredimensionel (3D) bioprint er en ny teknologi, der kan anvendes til udvikling af 3D-modeller for at fremskynde udviklingstiden, øge standardiseringen og øge gennemstrømningen. Her præsenterer vi en protokol til udvikling af 3D bioprintede cokulturmodeller af humane inducerede pluripotente stamceller (iPSC)-afledte glutamaterge neuroner og astrocytter. Disse cokulturer er indlejret i en hydrogelmatrix af bioaktive peptider, ekstracellulære matrixproteiner (ECM) i fuld længde og med en fysiologisk stivhed på 1,1 kPa. Modellen kan hurtigt etableres i 96-brønds og 384-brønds formater og giver en gennemsnitlig levedygtighed efter tryk på 72%. Astrocyt-til-neuron-forholdet i denne model er vist at være 1:1,5, hvilket er inden for det fysiologiske område for den menneskelige hjerne. Disse 3D bioprintede cellepopulationer viser også udtryk for modne neurale celletype markører og vækst af neurit og astrocyt fremskrivninger inden for 7 dage efter kultur. Som et resultat er denne model velegnet til analyse ved hjælp af cellefarvestoffer og immunfarvningsteknikker sammen med neuritudvækstassays. Evnen til at producere disse fysiologisk repræsentative modeller i stor skala gør dem ideelle til brug i screeningsassays med medium til høj gennemstrømning til neurovidenskabelige mål.
Introduction
Forskning i sygdomme i centralnervesystemet (CNS) i lægemiddelforskningsindustrien udvides1. Imidlertid har mange udbredte CNS-sygdomme som epilepsi, skizofreni og Alzheimers sygdom stadig ingen helbredende behandlinger 2,3,4. Manglen på effektive behandlinger på tværs af CNS-sygdomme kan, i det mindste delvist, tilskrives manglen på nøjagtige in vitro-modeller af hjernen5. Dette har resulteret i en translationel kløft mellem nuværende in vitro-modeller og in vivo-data og en efterfølgende flaskehals i forskningsindsatsen.
Drevet af dette translationelle hul har der været en betydelig stigning i udviklingen af nye 3D-cellemodeller inden for de seneste år, herunder neurale organoider, neurosfæroider og stilladsbaserede modeller6. 3D-strukturen af disse modeller hjælper med at rekapitulere det neurale mikromiljø, herunder biomekaniske belastninger, celle-cellekontakter og hjernens ekstracellulære matrix (ECM)7. Hjernens ECM er et dynamisk element i neurofysiologi, der optager rummet mellem neurale celletyper, herunder neuroner, astrocytter, oligodendrocytter og den neurovaskulære enhed7. Rekapitulation af hjernens ECM har vist sig at påvirke neuronal morfologi og neuronal fyring, og mange komplekse 3D-modeller af hjernen har vist aflejring af ECM-proteiner ved neurale celletyper 8,9,10,11. Stilladsbaserede modeller består af modne neurale cokulturer suspenderet i en porøs, syntetisk eller biologisk hydrogelmatrix, som repræsenterer hjernens ECM12. I modsætning til organoid- og sfæroidsystemer tillader stilladsbaserede 3D-modeller tilpasning af tilstedeværende ECM-proteiner og har den ekstra fordel ved tunbarhed af hydrogelstivhed for at efterligne biomekaniske belastninger13,14.
Selvom et overvældende flertal af neurale 3D-modeller viser en øget rekapitulation af hjernens mikromiljø, er ikke alle modeller velegnede til implementering af lægemiddelopdagelsesapplikationer15. For at en 3D-model kan implementeres i industrielle processer, skal systemet opfylde gennemløbskrav til screeningsansøgninger og have en relativt kort udviklingstid16. 3D Bioprinting er en ny teknologi, der giver mulighed for at skabe 3D-stilladsbaserede neurale modeller med hurtig udviklingstid, øget gennemstrømning og højere niveauer af præcisionskontrol sammen med fjernelse af variabilitet forårsaget af menneskelige fejl17. Denne protokol præsenterer en 3D-samkulturmodel af humane iPSC-afledte glutamaterge neuroner og astrocytter i et hydrogelstillads. Dette hydrogelstillads indeholder fysiologisk repræsentative bioaktive peptider (RGD, IKVAV, YIGSR) og ECM-proteiner inden for en mimetisk biomekanisk stivhed. Disse ECM-proteiner i fuld længde omfatter laminin-211 i fuld længde og hyaluronsyre, der er rigelig i den menneskelige cortex, med en stivhed på 1,1 kPa i overensstemmelse med in vivo-målinger 18. Denne model er designet med praktisk anvendelighed til lægemiddelopdagelse og er oprettet ved hjælp af en 3D-bioprinter i et 96-brønds eller 384-brønds pladeformat, der er egnet til screeningsanalyse ved hjælp af billeddannelsesteknikker med cellefarvestoffer og antistoffer sammen med neuritudvækstassays. Celler viser ekspression af neurale celletypemarkører og vækst af neurit og astrocytiske fremskrivninger inden for 7 dage efter kultur. Således vil denne protokol præsentere metoden til at udvikle en højkapacitets 3D neural cokulturmodel til brug i lægemiddelopdagelsesapplikationer.
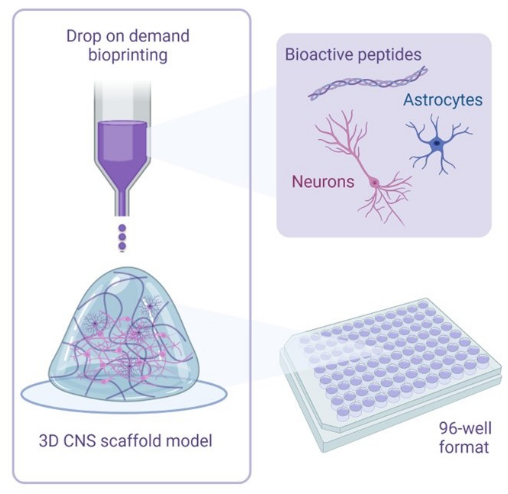
Figur 1: Illustrativ oversigt over metoder anvendt til 3D-bioprint-samkulturer. Humane iPSC-afledte neuroner og astrocytter kombineres med aktivator- og bioblækopløsninger, der indeholder bioaktive peptider, og bioprintes til hydrogelstilladser i 96-brønds- eller 384-brøndformater ved hjælp af drop-on-demand bioprintteknologi. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Behovet for nøjagtige modeller af CNS har aldrig været højere, og begrænsninger af todimensionelle (2D) traditionelle cellekulturmodeller har drevet en generation af komplekse CNS-modeller i de senere år19. Imidlertid har mange komplekse 3D-modeller, der repræsenterer interaktioner mellem neurale celletyper og ECM, begrænsninger, der forhindrer anvendelsen af disse modeller i industrielle processer 6,20,21. I denne protokol udvikler vi en 3D-samkulturmodel af humane iPSC-afledte neuroner og astrocytter, som sigter mod at løse nogle af disse begrænsninger ved hjælp af 3D-bioprintteknologi til at skabe et bioaktivt hydrogelstillads i 96-brønd og 384-brøndformater.
Metoden til udvikling af disse modeller er blevet forenklet gennem pladekortdesignsoftwaren, automatisk genererede udskrivningsprotokoller og guidet udskrivningsproces fra bioprinteren. På grund af den følsomme karakter af de følsomme iPSC-afledte celletyper, der anvendes i denne protokol, skal der dog udvises forsigtighed med følgende kritiske trin i optøning og dyrkning. For det første har inkluderingen af ROCK-hæmmer (ROCKi) flere fordele gennem hele bioprintprocessen og under tidlig kultur. Celleoptøning er et kritisk punkt, hvor neuronerne kan opleve et stressrespons, og ukorrekte optøningsprotokoller kan mindske chancerne for overlevelse22. Det anbefales typisk at optø celler, tilføje medier og hæve celler til inkubatortemperatur så effektivt som muligt23. Under bioprintprocessen beskrevet i denne protokol er det imidlertid nødvendigt, at neuroner og astrocytter resuspenderes i en aktivatoropløsning snarere end medier, og celler hæves ikke over stuetemperatur før slutningen af udskriftskørslen (op til 30 minutter efter optøning). Tilsætningen af ROCKi til mediet umiddelbart efter optøning og inkludering heraf under de to centrifugeringstrin (trin 2.1–2.7 og 1.3.15-1.3.20) er således bydende nødvendig for at hæmme cellestressveje, hvilket ville resultere i lavere levedygtighedsniveauer24. Desuden har ROCKi vist sig at fremme neuritudvækst og forbedre neuronal modning25. Således fortsættes ROCKi-tilskud i 48 timer efter bioprint. Men, Det er bydende nødvendigt at fjerne ROCKi tilskud efter 48 timer for at sikre fuldstændig afvaskning under de efterfølgende medieændringer, før celler anvendes til analyse.
Et yderligere trin, der kræver kritisk opmærksomhed, er under tilføjelse af medier efter udskrivning og medieændringer (trin 2.8-2.13). Det bioprintede hydrogelstillads har en tilsvarende biomekanisk stivhed på kun 1,1 kPa, svarende til gråt stof. Som beskrevet i trin 2.10 er det afgørende at pipette forsigtigt ind i siden af brønden under tilsætning af medier og aspiration for at forhindre forstyrrelser. Dette er især relevant for 384-brøndplader, hvor gelniveauet optager en højere andel af det samlede brøndvolumen. Denne metode bør også anvendes i 2D-kontrolbrønde for at forhindre kantløft af celler og klipning af neuritudvækst. Forfatterne vil også gerne fremhæve betydningen af steril teknik i bioprinteren, som bør behandles med samme forsigtighed som et biosikkerhedsskab, der anvendes til iPSC-afledte cellekulturer. Dette omfatter steril filtrering af 70 % EtOH og dH2O, der anvendes i grønlysnings- og udskrivningsprocedurerne, opbevaring af låg på patroner og plader, mens hænderne flyttes ind og ud af bioprinteren, og dekontaminering af overflader inde i bioprinteren med 70 % ethanolservietter før og efter udskrivning.
Det bioprintede hydrogelstillads, der er dannet af bioblæk- og aktivatorløsninger, der er udvalgt til at udvikle denne model, er udvalgt blandt en række bioblæk- og aktivatorløsninger udviklet af Inventia Life Science til brug i RASTRUM-bioprinteren. Laminin og hyaluronsyre blev identificeret som molekyler af relevans for iPSC-afledt neuronal modning på grund af deres rolle i aksonal vejledning, synapsedannelse og dannelse af det perineuronale net26,27. Desuden blev en biomekanisk stivhed på 1,1 kPa valgt, da hydrogeler med lavere densitet har vist sig at muliggøre bedre neuritudvækst fra neuroner12. Hvis der foretages ændringer i protokollen ved hjælp af neuroner og astrocytter, der er blevet differentieret internt eller fra en anden kommerciel leverandør, anbefales det at foretage en matrixudvælgelsestest for at bestemme det mest støttende hydrogelstillads15. Desuden kan det også være nødvendigt at optimere celletætheden, hvis der foretages ændringer i cellekilder for at sikre optimal levedygtighed og forhindre overfyldning af hydrogel. For alle ændringer og fejlfinding relateret til bioprinterfunktionen anbefaler forfatterne at kontakte producenter og henvise til producentprotokoller.
CNS indeholder en bred vifte af neuronale undertyper og gliaceller, som alle findes i forskellige hjernenicher og har specifikke roller, der bidrager til neurale funktioner28. Inden for rammerne af dette brede anvendelsesområde repræsenterer denne model kun de to mest rigelige celletyper (astrocytter og excitatoriske glutamaterge neuroner). Vigtige celletyper såsom mikroglia, oligodendrocytter og blod-hjerne-barrieredannende endotelceller udelades fra dette system. Inkluderingen af microglia kan være relevant i fokus på neuroimmune interaktioner, og oligodendrocytter kan være af interesse for sygdomme, der påvirker central myelinisering. Ud over deres rolle i patologi udskiller celler såsom blod-hjerne-barrieredannende endotelceller lægemiddelmetaboliserende enzymer, hvilket kan påvirke brugen af denne model til farmakokinetiske assays29. En yderligere begrænsning af modellen kan være forholdet mellem astrocytter og neuroner; Forholdet mellem astrocytter og neuroner varierer meget mellem hjerneområder med foreslåede værdier på mellem 1:1 og 1:330,31. Denne model har et omtrentligt forhold på 1: 1,5 astrocytter til neuroner; Således er denne model muligvis ikke relevant for modelhjerneområder, hvor astrocytter er mere rigelige, såsom i hvide substansområder30.
Andre protokoller til udvikling af 3D bioprintede samkulturmodeller er blevet offentliggjort i de senere år. En publikation af Sullivan et al., 2021, præsenterede en 3D bioprintet neural model ved hjælp af iPSC-afledte neurale stamceller, som demonstrerer høj levedygtighed efter udskrivning og forbedring af neuronal funktion sammenlignet med 2D-kulturer32. I denne protokol blev neurale stamceller imidlertid anvendt som cellekilde og blev opretholdt i kultur i 4 uger. I denne protokol blev kommercielt tilgængelige iPSC-afledte glutamaterge neuroner og astrocytter anvendt. Dette gør det muligt at etablere et 3D-netværk af samdyrkede celler på så lidt som 7 dage; Som det fremgår af neuritvækstanalysen, begynder neuritudvæksten inden for 24 timer og fortsætter lineært i hele 156 timer-perioden, for hvilken cellevækst blev overvåget. Den hurtige etablering af disse netværk kan delvis tilskrives brugen af glutamaterge neuroner, der bruger optimeret doxycyclin-inducerbar genekspression af NGN2, som viser ekspression af modne neuronale subtypemarkører inden for 7 dage, selv i 2D-kultur33. Forkortelsen af denne vækstperiode ved hjælp af denne teknik er vigtig for implementering af modeller inden for den biofarmaceutiske industri, da analyseudvikling kræver hurtig vending og udvikling af cellemodeller15.
Afslutningsvis viser denne model potentiale for en 3D-model af neuroner og astrocytter, som etableres hurtigt og bekvemt til screeningsformål. Fremtidige applikationer til denne modeltype kunne være til lægemiddelopdagelsesindsats på tværs af forskellige CNS-sygdomme med mulighed for at udvide til forskellige sygdomme ved hjælp af patient- eller genredigerede sygdoms-iPSC-linjer. Desuden tillader brugen af doxycyclin-inducerbare NGN2-ekspression iPSC-afledte glutamaterge neuroner celler at nå modenhed på kortere tid, hvilket kan bruges til at udvikle modeller af den aldrende hjerne til neurodegenerationsforskning. Dette system kan også udvides ved brug af yderligere celletyper i samkultur, herunder mikroglia og oligodendrocytter.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne vil gerne takke Alex Volkerling, Martin Engel og Rachel Bleach for deres hjælp med at udvikle protokollen og feedback på manuskriptet.
Materials
| 2-mercaptoethanol | Thermofisher | 31350010 | |
| 384-well plate | PerkinElmer | 6057300 | |
| 96-well plate | PerkinElmer | 6055300 | |
| Activator fluid F299 | Inventia Life Science | N/A | |
| Activator fluid F3 | Inventia Life Science | N/A | |
| B27 (50x) minus Vit A | Thermofisher | 12587010 | |
| Bioink fluid F261 | Inventia Life Science | N/A | |
| Bioink fluid F32 | Inventia Life Science | N/A | |
| Doxycycline hyclate | Sigma Aldrich | D5207 | |
| GlutaMAX (100x) | Thermofisher | 35050061 | |
| Goat anti-mouse IgG H&L Alexa Fluor 647 | Abcam | ab150115 | |
| Goat anti-rabbit IgG H&L Alexa Fluor 488 | Abcam | ab150077 | |
| Hoechst | Abcam | ab228551 | |
| Human BDNF Recombinant Protein | Thermofisher | PHC7074 | |
| Human NT3 Recombinant Protein | Thermofisher | PHC7036 | |
| iCell Astrocytes | Fujifilm CDI | 1434 | |
| INCell Analyser 6500HS | Molecular Devices | N/A | high content imaging system |
| Incucyte S3 | Sartorius | N/A | |
| ioGlutamatergic Neurons (Large vial) | Bit.bio | e001 | |
| Laminin (1 mg/mL) | Sigma Aldrich | L2020 | |
| Live/dead kit (Calcein-AM, Ethidium homo-dimer-1) | Invitrogen | L3224 | |
| Mouse anti-BIII tubulin NL637 conjugated | R&D systems | SC024 | |
| Neurobasal media | Thermofisher | 21103049 | |
| Normal Donkey Serum | Abcam | ab7475 | |
| NucBlue Live (Hoechst 33342) | Thermofisher | R37605 | |
| Opti-MEM | Thermofisher | 11058021 | |
| Paraformaldehyde | Sigma Aldrich | P6148 | |
| PEI 50% in H2O | Sigma Aldrich | 181978 | |
| Pierce Borate Buffer 20x | Thermofisher | 28341 | |
| Prism | GraphPad | Data analysis software | |
| Rabbit anti-ionotropic glutamatre receptor 2 (GluR2) | Abcam | ab206293 | |
| RASTRUM(TM) Bioprinter | Inventia Life Science | N/A | Bioprinter |
| RASTRUM(TM) Bioprinter Cartridges | Inventia Life Science | N/A | Bioprinter Cartridges |
| RASTRUM(TM) Targeting plate | Inventia Life Science | N/A | Targeting plate |
| Rho kinase (ROCK) inhibitor | Abcam | ab120129 | |
| Sheep anti-GFAP NL493 conjugated | R&D systems | SC024 | |
| Signals Image Artist | PerkinElmer | N/A | Image analysis platform |
| Triton X-100 | Thermofisher | HFH10 | |
| Zeiss Axio Observer | Zeiss | N/A | Inverted microscope platform |
References
- Jung, Y. L., Hwang, J., Yoo, H. S. Disease burden metrics the innovations of leading pharmaceutical companies: a global and regional comparative study. Globalization and Health. 16 (1), 80-80 (2020).
- Potkin, S. G., et al. The neurobiology of treatment-resistant schizophrenia: paths to antipsychotic resistance and a roadmap for future research. npj Schizophrenia. 6, 1 (2020).
- Zahra, W., et al., Keswani, C., et al. The Global Economic Impact of Neurodegenerative Diseases: Opportunities and Challenges. Bioeconomy for Sustainable Development. , (2019).
- Perucca, E. The pharmacological treatment of epilepsy: recent advances and future perspectives. Acta Epileptologica. 3 (1), 22 (2021).
- Nikolakopoulou, P., et al. Recent progress in translational engineered in vitro models of the central nervous system. Brain. 143 (11), 3181-3213 (2020).
- Whitehouse, C., Corbett, N., Brownlees, J. 3D models of neurodegeneration: implementation in drug discovery. Trends in Pharmacological Sciences. 44 (4), 208-221 (2023).
- Rauti, R., Renous, N., Maoz, B. M. Mimicking the brain extracellular matrix in vitro: A review of current methodologies and challenges. Israel Journal of Chemistry. 60 (12), 1141-1151 (2020).
- Fawcett, J. W., Oohashi, T., Pizzorusso, T. The roles of perineuronal nets and the perinodal extracellular matrix in neuronal function. Nature Reviews Neuroscience. 20 (8), 451-465 (2019).
- Lam, D., et al. Tissue-specific extracellular matrix accelerates the formation of neural networks and communities in a neuron-glia co-culture on a multi-electrode array. Scientific Reports. 9, 4159 (2019).
- Roll, L., Lessmann, K., Brüstle, O., Faissner, A. Cerebral organoids maintain the expression of neural stem cell-associated glycoepitopes and extracellular matrix. Cells. 11 (5), 760 (2022).
- Yan, Y., Bejoy, J., Marzano, M., Li, Y. The use of pluripotent stem cell-derived organoids to study extracellular matrix development during neural degeneration. Cells. 8 (3), 242 (2019).
- Ma, L., et al. 3D bioprinted hyaluronic acid-based cell-laden scaffold for brain microenvironment simulation. Bio-Design and Manufacturing. 3 (3), 164-174 (2020).
- Liaw, C. -. Y., Ji, S., Guvendiren, M. Engineering 3D hydrogels for personalized in vitro human tissue models. Advanced Healthcare Materials. 7 (4), 1701165 (2018).
- Ma, J., Huang, C. Composition and mechanism of three-dimensional hydrogel system in regulating stem cell fate. Tissue Engineering Part B: Reviews. 26 (6), 498-518 (2020).
- Belfiore, L., et al. Generation and analysis of 3D cell culture models for drug discovery. European Journal of Pharmaceutical Sciences. 163, 105876 (2021).
- Langhans, S. A. Three-dimensional in vitro cell culture models in drug discovery and drug repositioning. Frontiers in Pharmacology. 9, 6 (2018).
- Engel, M., Belfiore, L., Aghaei, B., Sutija, M. Enabling high throughput drug discovery in 3D cell cultures through a novel bioprinting workflow. SLAS Technology. 27 (1), 32-38 (2022).
- Takamura, T., et al. Influence of age on global and regional brain stiffness in young and middle-aged adults. Journal of Magnetic Resonance Imaging. 51 (3), 727-733 (2020).
- Slanzi, A., Iannoto, G., Rossi, B., Zenaro, E., Constantin, G. In vitro models of neurodegenerative diseases. Frontiers in Cell and Developmental Biology. 8, 328 (2020).
- de Souza, N. Organoid variability examined. Nature Methods. 14 (7), 655-655 (2017).
- Hernández, D., et al. Culture variabilities of human iPSC-derived cerebral organoids are a major issue for the modelling of phenotypes observed in Alzheimer’s disease. Stem Cell Review and Reports. 18 (2), 718-731 (2022).
- Li, R., et al. Differentiation of human iPS cells into sensory neurons exhibits developmental stage-specific cryopreservation challenges. Frontiers in Cell and Developmental Biology. 9, 796960 (2021).
- Nishiyama, Y., et al. Safe and efficient method for cryopreservation of human induced pluripotent stem cell-derived neural stem and progenitor cells by a programmed freezer with a magnetic field. Neuroscience Research. 107, 20-29 (2016).
- Uhrig, M., Ezquer, F., Ezquer, M. Improving cell recovery: Freezing and thawing optimization of induced pluripotent stem cells. Cells. 11 (5), 799 (2022).
- Harbom, L. J., et al. The effect of rho kinase inhibition on morphological and electrophysiological maturity in iPSC-derived neurons. Cell and Tissue Research. 375 (3), 641-654 (2019).
- Koh, H. S., Yong, T., Chan, C. K., Ramakrishna, S. Enhancement of neurite outgrowth using nano-structured scaffolds coupled with laminin. Biomaterials. 29 (26), 3574-3582 (2008).
- Tarus, D., et al. Design of hyaluronic acid hydrogels to promote neurite outgrowth in three dimensions. ACS Applied Materials & Interfaces. 8 (38), 25051-25059 (2016).
- Brain Initiative Cell Census Network (BICCN). Initiative Cell Census Network (BICCN). A multimodal cell census and atlas of the mammalian primary motor cortex. Nature. 598 (7879), 86-102 (2021).
- Dauchy, S., et al. Expression and transcriptional regulation of ABC transporters and cytochromes P450 in hCMEC/D3 human cerebral microvascular endothelial cells. Biochemical Pharmacology. 77 (5), 897-909 (2009).
- Herculano-Houzel, S. The glia/neuron ratio: How it varies uniformly across brain structures and species and what that means for brain physiology and evolution. Glia. 62 (9), 1377-1391 (2014).
- von Bartheld, C. S., Bahney, J., Herculano-Houzel, S. The search for true numbers of neurons and glial cells in the human brain: A review of 150 years of cell counting. The Journal of Comparative Neurology. 524 (18), 3865-3895 (2016).
- Sullivan, M. A., et al. 3D bioprinting of stem cell-derived central nervous system cells enables astrocyte growth, vasculogenesis and enhances neural differentiation/function. bioRxiv. , (2022).
- Pawlowski, M., et al. Inducible and deterministic forward programming of human pluripotent stem cells into neurons, skeletal myocytes, and oligodendrocytes. Stem Cell Reports. 8 (4), 803-812 (2017).

