Een experiment met behulp van functionele nabij-infraroodspectroscopie en robotgeassisteerde multi-joint richtbewegingen van de onderste ledematen
Summary
Geschat wordt dat 1 op de 6 mensen wereldwijd tijdens zijn leven een beroerte zal krijgen, met langdurige invaliditeit tot gevolg, waarvan de revalidatiemechanismen nog steeds slecht worden begrepen. Deze studie stelt een protocol voor om hersenactivatie te evalueren door middel van functionele nabij-infraroodspectroscopie (fNIRS) tijdens een robottherapiesessie voor de onderste ledematen.
Abstract
Beroerte treft elk jaar wereldwijd ongeveer 17 miljoen mensen en is een belangrijke oorzaak van langdurige invaliditeit. Robottherapie is veelbelovend gebleken bij het helpen van patiënten met een beroerte om verloren motorische functies terug te krijgen. Een mogelijke manier om het begrip van hoe motorisch herstel plaatsvindt te vergroten, is het bestuderen van hersenactiviteit tijdens de bewegingen die het doelwit zijn van therapie bij gezonde personen. Functionele nabij-infraroodspectroscopie (fNIRS) is naar voren gekomen als een veelbelovende neuroimaging-techniek voor het onderzoeken van neurale onderbouwing van motorische functies. Deze studie had tot doel fNIRS neurale correlaten van complexe bewegingen van de onderste ledematen bij gezonde proefpersonen te onderzoeken. Deelnemers werd gevraagd om gedurende 6 minuten rust- en bewegingscycli uit te voeren met behulp van een robotapparaat voor motorische revalidatie. De taak vereiste gecoördineerde knie- en enkelgewrichtsbewegingen om doelen aan te wijzen die op een computerscherm werden weergegeven. Er werden twee experimentele omstandigheden onderzocht met verschillende niveaus van bewegingsondersteuning die door de robot worden geboden. De resultaten toonden aan dat het fNIRS-protocol effectief hersengebieden detecteerde die verband houden met motorische controle tijdens de taak. Opmerkelijk is dat alle proefpersonen een grotere activering vertoonden in het contralaterale premotorische gebied tijdens de toestand zonder assistentie in vergelijking met de geassisteerde toestand. Concluderend lijkt fNIRS een waardevolle benadering te zijn voor het detecteren van veranderingen in de oxyhemoglobineconcentratie geassocieerd met multi-gewrichtsgerichte bewegingen van de onderste ledematen. Dit onderzoek kan bijdragen aan het begrip van motorische herstelmechanismen voor beroertes en kan de weg vrijmaken voor verbeterde revalidatiebehandelingen voor patiënten met een beroerte. Er is echter verder onderzoek nodig om het potentieel van fNIRS bij het bestuderen van motorische functies en de toepassingen ervan in klinische omgevingen volledig op te helderen.
Introduction
Epidemiologische gegevens geven aan dat er wereldwijd elk jaar ~17 miljoen nieuwe gevallen van beroerte zijn, met een toename van de incidentie in lage- en middeninkomenslanden. Het aantal nieuwe gevallen zal naar schatting toenemen tot 77 miljoen in 20302. Motorische stoornissen als gevolg van een beroerte beïnvloeden vaak de mobiliteit van de patiënt en de deelname aan dagelijkse activiteiten, wat bijdraagt aan een lage kwaliteit van leven. Traditionele motorische revalidatie omvat manuele therapie, maar in de afgelopen decennia zijn robotsystemen voor revalidatie ontwikkeld. Deze systemen kunnen therapie leveren met hoge intensiteit, dosis, kwantificeerbaarheid, betrouwbaarheid, herhaalbaarheid en flexibiliteit3 en hebben potentieel getoond als effectieve revalidatiebehandelingen voor zowel acute als chronische patiënten met een beroerte 4,5,6. Naast het leveren van therapie kunnen robotsystemen voor revalidatie worden gebruikt als evaluatie-instrumenten, omdat ze kunnen worden uitgerust met sensoren die kinematische/kinetische gegevens van de beweging van de patiënt kunnen meten 7,8. Voor motorische revalidatie van de bovenste ledematen is niet alleen bewezen dat dergelijke gegevens nuttig zijn voor het beoordelen van het niveau van motorisch herstel van de patiënt dat wordt uitgelokt door robottherapie en dienden ze als een aanvullend hulpmiddel bij traditionele klinische beoordelingen 9,10, maar hebben ze ook bijgedragen aan het bevorderen van het begrip van het proces van motorisch herstel na een beroerte11, 12 evenals neurale controle van beweging en motorisch leren bij gezonde proefpersonen 3,13,14. Als gevolg hiervan hebben deze bevindingen een basis gelegd voor het verbeteren van revalidatiebehandelingen15.
In de afgelopen twee decennia zijn er veel robotapparaten voor neurorevalidatie van de onderste ledematen voorgesteld, variërend van exoskeletten die het lichaamsgewicht van de patiënt ondersteunen tijdens het lopen (bijv. over een loopband, zoals Lokomat16) tot stationaire robotsystemen waarmee de patiënt de enkel, knie of voet kan trainen zonder te lopen (zoals de Rutgers Ankle17, de High-Performance Ankle Rehabilitation Robot18 en de enkel-/voetrevalidatierobot van het Gwangju Institute of Science and Technology (GIST)19) of actieve voetorthesen die worden aangedreven exoskeletten die door de patiënt worden gedragen om over de grond of over een loopband te lopen (zoals de Powered Gait Orthosis20 en de MIT Anklebot21). Zie 22,23,4 voor een recensie over robots voor revalidatie van de onderste ledematen.
De resultaten van klinische onderzoeken naar robotapparaten voor revalidatie van de onderste ledematen bij patiënten met een beroerte zijn bemoedigend en hebben aangetoond dat deze systemen het bewegingsbereik (ROM), de spierkracht of het looppatroon van de gewrichten kunnen verbeteren, afhankelijk van het specifieke apparaat en het klinische protocol (zie 24,25 voor een overzicht van de werkzaamheid van robots van de onderste ledematen voor revalidatie). Hoewel is gepostuleerd dat robotondersteunde therapie neuroplastische veranderingen bevordert, die uiteindelijk resulteren in verbeterde motorische vaardigheden26, blijft het grotendeels onduidelijk hoe het proces van motorisch herstel van een beroerte precies plaatsvindt en welke robottrainingsprotocollen het proces van herstel van de motorische vaardigheden van de onderste ledematen optimaliseren. In feite is er een significante, groeiende ongelijkheid tussen de toenemende ontwikkeling van revalidatierobots (door academische onderzoekers of commerciële entiteiten) en het beperkte begrip van de neurofysiologische mechanismen die ten grondslag liggen aan motorisch herstel4. Metingen van bewegingskinematica of gewrichtskoppels die met ingebouwde sensoren zijn uitgevoerd, hebben bijgedragen aan het kwantitatief beschrijven van motorische gedragsveranderingen die optreden wanneer patiënten de motorische vaardigheden van de onderste ledematen herstellen 27,28,29, waardoor deze leemte gedeeltelijk wordt opgevuld. De neurale correlaten die aan dergelijke veranderingen ten grondslag liggen, zijn echter minder onderzocht. Dit heeft verschillende redenen.
Functionele beeldvorming van de hersenen is tijdrovend en soms moeilijk te voltooien in de context van klinische onderzoeken, waarbij de belasting van de patiënt vaak minimaal moet worden gehouden om de kans te maximaliseren dat de patiënt zich aan het onderzoek houdt. Dit geldt met name voor personen die een beroerte hebben gehad, gezien het feit dat vermoeidheid en spierzwakte na een beroerte vaak worden waargenomen30. Ook beeldvormingsmodaliteiten die gebaseerd zijn op magnetische velden, zoals functionele Magnetic Resonance Imaging (fMRI), vereisen dat zowel patiënt- als robothardware magneetveilig is.
Van de niet-invasieve beeldvormingsmodaliteiten is functionele nabij-infraroodspectroscopie (fNIRS) een beeldvormingstechniek die bijzonder geschikt is voor het beoordelen van hersenactiviteitsgebieden bij proefpersonen die robottherapie ondergaan. Net als fMRI meet fNIRS de zuurstoftoevoer/deoxygenatie in het bloed in de hersenen. In tegenstelling tot fMRI is fNIRS echter volledig compatibel met robothardware en is het vaak draagbaar en zelfs bruikbaar aan het bed. fNIRS heeft ook lage kosten en minder gevoeligheid voor bewegingsartefacten 31,32,33.
Ondanks de duidelijke voordelen en het wijdverbreide gebruik in veel klinische omgevingen sinds de eerste introductie in de late jaren 7034, hebben slechts enkele onderzoeken fNIRS gebruikt om hersenactiviteit te kwantificeren die verband houdt met bewegingen van de onderste ledematen en motorisch herstel van een beroerte. FNIRS-studies gericht op het ophelderen van mechanismen van neurale controle van beweging en/of mechanismen of evaluatie van motorisch herstel na een beroerte hebben meestal bewegingen van één gewricht onderzocht (bijv. dorsaalflexie, plantairflexie of knie-extensiebewegingen35,36,37), lopen 38,39,40,41,42,43 of fietsen 44. Zie45 voor een recensie. Evenzo hebben fNIRS-onderzoeken naar robotondersteunde therapie voor de onderste ledematen zich vooral gericht op robotondersteunde looprevalidatie; Zie46 voor een recensie. Een paar studies hebben zich gericht op het gebruik van fNIRS als onderdeel van een Brain-Computer Interface (BCI)-systeem om besturingssignalen voor robotapparaten af te leiden47,48; hoewel dit onderzoeksgebied ook afhankelijk is van de verwerking van fNIRS-signalen, is het doel anders en voornamelijk gericht op het decoderen van de intenties van patiënten (bijv. patiënten met ernstige motorische handicaps).
De hierin gepresenteerde pilotstudie maakt deel uit van een eerste poging om de effecten van een robotsysteem voor revalidatie van de onderste ledematen te onderzoeken. De robot kan doelgerichte revalidatie van de onderste ledematen leveren, waarbij wordt getraind in dagelijkse bewegingen met meerdere gewrichten, en therapie geven aan afzonderlijke gewrichten (bijv. knie of enkel) van de onderste ledematen (d.w.z. een bottom-up revalidatieprogramma implementeren).
De studie had tot doel de haalbaarheid te onderzoeken van een experimenteel protocol dat de verwerving van fNIRS-gegevens vereiste tijdens het uitvoeren van gerichte bewegingen van de onderste ledematen, met meerdere gewrichten. De duur van de data-acquisitieperiode in deze studie, die beperkt was tot 6 minuten, is korter dan bij typische fNIRS-protocollen. Dit was een bewuste keuze met als doel de bruikbaarheid en klinische toepasbaarheid van dit onderzoek te vergroten, met name bij patiënten met beperkte mobiliteit of kracht. Het identificeren van fNIRS-correlaten van dergelijke complexe bewegingen met meerdere gewrichten en het verkrijgen van inzicht in hoe hersenactiviteit werd gemoduleerd door robotassistentie waren ook aandachtspunten. Hiervoor werden twee experimenteersessies uitgevoerd met dezelfde deelnemers: één zonder robotassistentie en één met robotassistentie. Ten slotte is het belangrijk op te merken dat deze studie zich richtte op gezonde proefpersonen om een basis te leggen voor toekomstig onderzoek in termen van de haalbaarheid van het registratieprotocol en de evaluatie van hersenactiviteit tijdens bewegingen die het doelwit zijn van robottherapie.
Apparaat
Een draagbare robot die is ontworpen om revalidatie van de onderste ledematen te leveren (zie figuur 1) werd gebruikt om onze experimenten uit te voeren. De robot heeft een 3D-bereikbare werkruimte en is compact en licht, met een gewicht van ongeveer 35 lb., waardoor hij gemakkelijk te vervoeren en te installeren is.
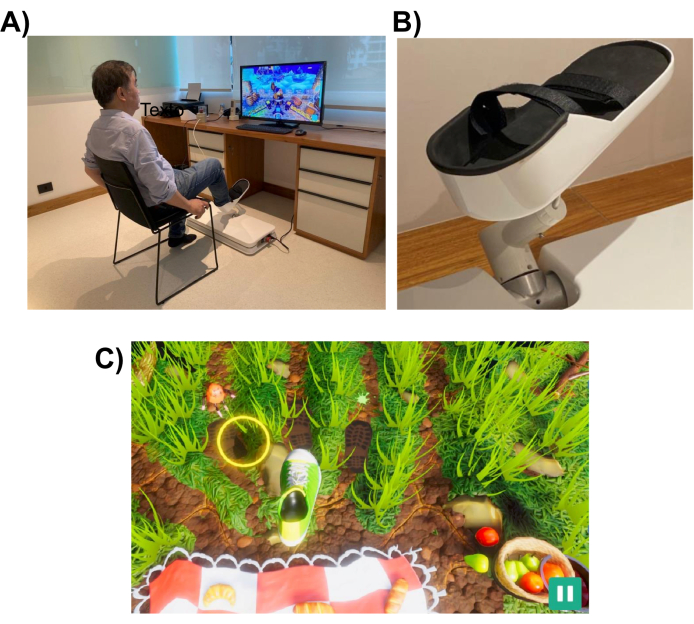
Figuur 1: Experimentele opstelling. (A) Het robotsysteem (geïnstalleerd op de vloer) ontworpen voor de onderste ledematen. Een vrijwilliger wordt getoond die de interface met zijn rechtervoet gebruikt. (B) Ondersteuningsstructuur voor de voet van de proefpersoon die bevestiging aan het robotsysteem mogelijk maakt. (C) Een screenshot van het Picnic-spel. Het doel van het spel is om de voet (groene en witte schoen) naar het doel (gele cirkel) te verplaatsen. Klik hier om een grotere versie van deze figuur te bekijken.
Het robotsysteem is ontworpen om een patiënt te helpen bij het uitvoeren van bewegingen van de onderste ledematen die vergelijkbaar zijn met die van alledaagse taken, zoals wijzen of schoppen. Het maakt gebruik van interactieve virtual reality-games, die worden weergegeven op een computermonitor of een televisiescherm dat voor het robotapparaat is geplaatst (zie figuur 1). De effector aan het uiteinde van de robot wordt bevestigd aan de onderste ledematen van de patiënt (bijv. enkel) en de positie ervan wordt toegewezen aan de positie van een cursor op het scherm. Een typisch spel toont de bewegingsdoelen van de patiënt (bijv. het object waarnaar moet worden gewezen of waar de bal moet worden geschopt).
Om de bewegingstaak te voltooien, kan de robot de patiënt helpen met een niveau van ondersteuning dat kan variëren van volledige hulp tot geen. Het niveau van robotondersteuning wordt aan het begin van elke revalidatiesessie gekozen op basis van de mate van motorische beperking van de patiënt. De bewegingen die door de proefpersoon worden uitgevoerd, worden door het spel gebruikt om de prestaties van de patiënt te scoren en hen feedback te geven over hun prestaties (bijv. ROM, aantal bewegingen en niveau van robotassistentie). De spellen zijn ontworpen om interactief en vermakelijk te zijn om de interesse en aandacht van de patiënt vast te houden. In dit onderzoek speelden de deelnemers het “Picnic-spel”, waarbij de speler moest voorkomen dat de insecten de handdoek bereikten en het voedsel stalen (zie figuur 1, onderste paneel, voor een screenshot).
Data-acquisitie werd uitgevoerd met een draagbaar fNIRS-acquisitiesysteem met twee verschillende optodes met continue golven (760 nm en 850 nm), 8 dual-tip LED-bronnen en 8 dual-tip actieve detectoren. De signalen werden verkregen met behulp van een bemonsteringsfrequentie van 10,17 Hz. Een laptop werd gebruikt voor de kalibratie-optimalisatie en signaalregistratie met behulp van een Wi-Fi-netwerk dat door het fNIRS-systeem werd gecreëerd.
Een dop werd gebruikt om de optodes op de vooraf bepaalde locaties vast te houden. De bronnen en detectoren werden volgens het 10-10 internationale EEG-systeem in een raster ruimtelijke verdeling geplaatst. Elk fNIRS-kanaal werd gedefinieerd door een bron-detectorpaar met interoptode-afstanden van ongeveer 30 mm. De optodes werden geplaatst over de aanvullende motor-, premotor- en motorgebieden op de locaties die worden weergegeven in figuur 2. Het totale aantal kanalen was 28, waarvan 8 korteafstandskanalen die aan elke bron waren gekoppeld met behulp van een glasvezeladapter aan een enkele detector. Gezien de multiplexing-opstelling van de hardware, is het mogelijk om informatie over korte afstanden uit alle bronnen te verkrijgen met slechts één detector.
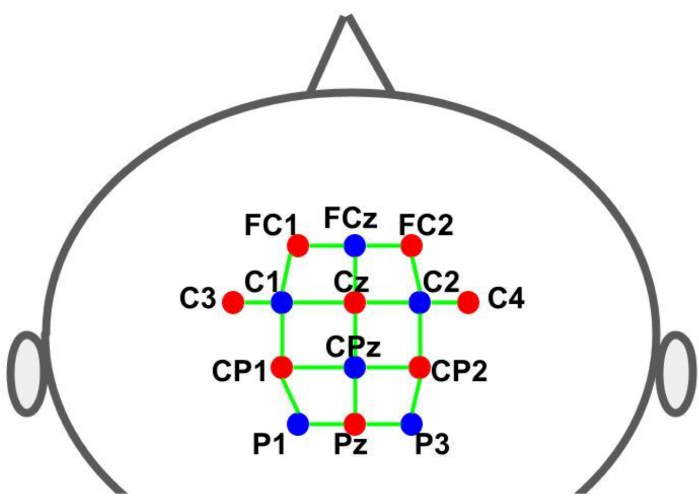
Figuur 2: Montagelay-out met behulp van het 10-10 EEG-systeem. De letters en cijfers geven de locaties van de bron/detector aan. De rode en blauwe stippen vertegenwoordigen respectievelijk de bron- en detectoroptodes. De groene lijnen vertegenwoordigen de fNIRS-kanalen die bestaan uit bron- en detectorparen. Klik hier om een grotere versie van deze figuur te bekijken.
Experimenteel ontwerp
Het experiment werd uitgevoerd onder twee verschillende experimentele omstandigheden, die verschilden in het niveau van assistentie dat door de robot werd geboden voor de bewegingen van de proefpersoon. In de eerste toestand was de robot geprogrammeerd om geen hulp te bieden aan de bewegingen van de proefpersoon, terwijl in de tweede toestand de robot de voet- en beenbewegingen van de proefpersoon bestuurde (robotondersteunde beweging).
Elk experiment volgde een blokontwerpparadigma met afwisselende cycli van een motorische taak (het spelen van het spel – 30 s) en rusten (30 s), zoals geïllustreerd in figuur 3. Het begin en einde van elke fase (spel/spel of rust) werden via het computerscherm visueel aan de proefpersoon gesignaleerd. Tijdens de rustfase werd een bericht weergegeven dat een pauze aangaf. Elke cyclus (spelen/spel + rust) duurde 60 s en werd zes keer herhaald, wat resulteerde in een totale looptijd van 360 s (6 min).
De deelnemers speelden het “Picknickspel”, waarbij het doel was om te voorkomen dat insecten bij de handdoek zouden komen en voedsel zouden stelen. Dit spel omvatte een opeenvolging van bewegingen van de onderste ledematen, beginnend bij een aangewezen thuisdoel (beginpositie) en zich uitstrekkend naar een van de drie buitenste doelen voordat ze terugkeerden naar het thuisdoel. Op het scherm werden de buitenste doelen visueel weergegeven als geanimeerde bewegende insecten, die de deelnemers moesten bereiken en erop moesten stappen. Er waren drie naar buiten reikende doelen, elk willekeurig een gelijk aantal keren gepresenteerd, naast een gemeenschappelijk thuisdoel voor elke beweging. De afstand die de voet nodig had om van het thuisdoel naar de positie van de buitenste doelen te reizen, vormde een boog van ongeveer 26 cm. De motorische taak vereiste de uitvoering van bewegingen met meerdere gewrichten, waarbij coördinatie tussen knieflexie/-extensie, plantairflexie en dorsaalflexiebewegingen vereist was.
De fNIRS-gegevensregistraties werden gesynchroniseerd met de visuele stimuli die door het spel aan de proefpersoon werden gepresenteerd via een transistor-transistor-logic (TTL)-puls die door de robot werd gegenereerd. Pulsen werden gegenereerd aan het begin van elke fase (spel/spel en rust). Zo werd alle timingcontrole uitgevoerd door het spel, dat visuele aanwijzingen (doelen) aan de deelnemer gaf om elke beweging te starten, TTL-signalen naar het fNIRS-systeem stuurde om de opnames van de hersenactiviteit te markeren en, indien nodig voor het experiment, signalen naar het robotbesturingssysteem stuurde om bewegingsondersteuning te starten.
Protocol
Representative Results
Discussion
In deze proof-of-concept-studie werd de haalbaarheid onderzocht van het maken van conclusies over het in kaart brengen van hersenactiviteit met behulp van fNIRS-gegevens van gezonde proefpersonen terwijl ze oefenden met verschillende soorten bewegingen met behulp van een robot voor revalidatie van de onderste ledematen. Typische fNIRS-opnamesessies bij volwassenen duren langer dan 6 min54. Om opnames echter haalbaar te maken in de context van een revalidatiesetting, moet de totale duur van het exp…
Disclosures
The authors have nothing to disclose.
Acknowledgements
De meningen, hypothesen, conclusies en aanbevelingen van deze studie zijn die van de auteurs en vertegenwoordigen niet noodzakelijkerwijs de mening van de financieringsinstantie. JRS is de Sao Paulo Research Foundation (FAPESP, subsidienummers 2021/05332-8, 2018/04654-9, 2018/21934-5 en 2023/02538-0) en Jackson Cionek dankbaar voor technologische ondersteuning. AMM en Vivax Ltda zijn FAPESP (São Paulo Research Foundation) en FINEP (Braziliaans Innovatiebureau) dankbaar. Dit project werd gefinancierd met subsidies van FAPESP (subsidienummer 2018/09559-4) en FINEP (subsidienummer 2019/09933-6).
Materials
| 32 inch Smart TV | Samsung | N/A | TV connected to robot via HDMI cable |
| 8-detector silicon photodiode (SiPD) optodes for optical detection with dual tip | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| 8-source optodes bundle for optical illumination with dual tip | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| Aurora acquisition software | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| Laptop Precision XPS 13 | Dell Technologies (Round Rock, TX, USA) | ||
| nirsLAB fNIRS Analysis software | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| NIRSports2 fNIRS acquisition system | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | It has two different continuous wave optics (760 and 850 nm), 8 dual-ended LED sources and 8 dual-ended active detectors. |
| R | R-project.org (open source software) | https://www.r-project.org/ | |
| Standard cut cap, black color for up to 128 holders. | Easycap GmbH (Wörthsee, Germany) | https://www.easycap.de/ | |
| Vivax Assistive Rehabilitation Machine (ARM) | Vivax Ltda (São Paulo, Brazil) | https://vivaxbr.com/home/ | It is a portable robot designed to deliver lower limb rehabilitation. It has a 3D reachable workspace and is compact and light, weighing about 35 lb., which makes it easy to transport and to install. |
References
- GBD 2016 Stroke Collaborators. Global, regional, and national burden of stroke, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. The Lancet. Neurology. 18 (5), 439-458 (2019).
- GBD 2019 Stroke Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. The Lancet. Neurology. 20 (10), 795-820 (2021).
- Huang, V. S., Krakauer, J. W. Robotic neurorehabilitation: a computational motor learning perspective. Journal of NeuroEngineering and Rehabilitation. 6, 5 (2009).
- Hobbs, B., Artemiadis, P. A Review of Robot-Assisted Lower-Limb Stroke Therapy: Unexplored Paths and Future Directions in Gait Rehabilitation. Frontiers in neurorobotics. 14, 19 (2020).
- Bertani, R., Melegari, C., De Cola, M. C., Bramanti, A., Bramanti, P., Calabrò, R. S. Effects of robot-assisted upper limb rehabilitation in stroke patients: a systematic review with meta-analysis. Neurological Sciences. 38 (9), 1561-1569 (2017).
- Warutkar, V., Dadgal, R., Mangulkar, U. R. Use of robotics in gait rehabilitation following stroke: A review. Cureus. 14 (11), e31075 (2022).
- Dipietro, L., et al. Changing motor synergies in chronic stroke. Journal of Neurophysiology. 98 (2), 757-768 (2007).
- Dipietro, L., et al. Learning, not adaptation, characterizes stroke motor recovery: evidence from kinematic changes induced by robot-assisted therapy in trained and untrained task in the same workspace. IEEE Trans Neural Syst Rehabil Eng. 20 (1), 48-57 (2012).
- Bosecker, C., Dipietro, L., Volpe, B., Krebs, H. I. Kinematic robot-based evaluation scales and clinical counterparts to measure upper limb motor performance in patients with chronic stroke. Neurorehabilitation and Neural Repair. 24 (1), 62-69 (2010).
- Krebs, H. I., et al. Robotic measurement of arm movements after stroke establishes biomarkers of motor recovery. Stroke. 45 (1), 200-204 (2014).
- Volpe, B. T., et al. Robotic devices as therapeutic and diagnostic tools for stroke recovery. Archives of Neurology. 66 (9), 1086-1090 (2009).
- Hogan, N., et al. Motions or muscles? Some behavioral factors underlying robotic assistance of motor recovery. Journal of Rehabilitation Research and Development. 43 (5), 605-618 (2006).
- Shadmehr, R., Wise, S. P. . The Computational Neurobiology of Reaching and Pointing: A Foundation for Motor Learning. , (2005).
- Dipietro, L., Poizner, H., Krebs, H. I. Spatiotemporal dynamics of online motor correction processing revealed by high-density electroencephalography. J Cogn Neurosci. 26 (9), 1966-1980 (2014).
- Krebs, H., et al. Rehabilitation robotics: Performance-based progressive robot-assisted therapy. Autonomous Robots. 15, 7-20 (2003).
- Colombo, G., Joerg, M., Schreier, R., Dietz, V. Treadmill training of paraplegic patients using a robotic orthosis. Journal of Rehabilitation Research and Development. 37 (6), 693-700 (2000).
- Girone, M., et al. A Stewart platform-based system for ankle telerehabilitation. Autonomous Robots. 10, 203-212 (2001).
- Saglia, J. A., Tsagarakis, N. G., Dai, J. S., Caldwell, D. G. A high-performance redundantly actuated parallel mechanism for ankle rehabilitation. The International Journal of Robotics Research. 28 (9), 1216-1227 (2009).
- Yoon, J., Ryu, J. A novel reconfigurable ankle/foot rehabilitation robot. , 2290-2295 (2005).
- Ruthenberg, B. J., Wasylewski, N. A., Beard, J. E. An experimental device for investigating the force and power requirements of a powered gait orthosis. Journal of Rehabilitation Research and Development. 34 (2), 203-213 (1997).
- Forrester, L. W., et al. Clinical application of a modular ankle robot for stroke rehabilitation. NeuroRehabilitation. 33 (1), 85-97 (2013).
- Díaz, I., Gil, J. J., Sánchez, E. Lower-limb robotic rehabilitation: Literature review and challenges. Journal of Robotics. 2011, 759764 (2011).
- Zhang, X., Yue, Z., Wang, J. Robotics in lower-limb rehabilitation after stroke. Behavioural Neurology. 2017, 3731802 (2017).
- Zhang, M., Davies, T. C., Xie, S. Effectiveness of robot-assisted therapy on ankle rehabilitation – a systematic review. Journal of NeuroEngineering and Rehabilitation. 10, 30 (2013).
- Lo, K., Stephenson, M., Lockwood, C. Effectiveness of robotic assisted rehabilitation for mobility and functional ability in adult stroke patients: a systematic review protocol. JBI Database of Systematic Reviews and Implementation Reports. 15 (1), 39-48 (2017).
- Belda-Lois, J. M., et al. Rehabilitation of gait after stroke: a review towards a top-down approach. Journal of NeuroEngineering and Rehabilitation. 8, 66 (2011).
- Bortole, M., et al. The H2 robotic exoskeleton for gait rehabilitation after stroke: early findings from a clinical study. Journal of NeuroEngineering and Rehabilitation. 12, 54 (2015).
- Banala, S. K., Kim, S. H., Agrawal, S. K., Scholz, J. P. Robot assisted gait training with active leg exoskeleton (ALEX). IEEE Transactions on Neural Systems and Rehabilitation Engineering. 17 (1), 2-8 (2009).
- Bartenbach, V., Wyss, D., Seuret, D., Riener, R. A lower limb exoskeleton research platform to investigate human-robot interaction. 2015 IEEE International Conference on Rehabilitation Robotics (ICORR). 2015, 600-605 (2015).
- Hinkle, J. L., et al. Poststroke fatigue: Emerging evidence and approaches to management: A scientific statement for healthcare professionals from the American heart association. Stroke. 48 (7), e159-e170 (2017).
- Balardin, J. B., Zimeo Morais, G. A., Furucho, R. A., Trambaiolli, L. R., Sato, J. R. Impact of communicative head movements on the quality of functional near-infrared spectroscopy signals: negligible effects for affirmative and negative gestures and consistent artifacts related to raising eyebrows. Journal of Biomedical Optics. 22 (4), 4601 (2017).
- Nazeer, H., Naseer, N., Mehboob, A., Khan, M. J., Khan, R. A., Khan, U. S., Ayaz, Y. Enhancing classification performance of fNIRS-BCI by identifying cortically active channels using the z-score method. Sensors. 20 (23), 6995 (2020).
- Ayaz, H., et al. Optical imaging and spectroscopy for the study of the human brain: status report. Neurophotonics. 9, S24001 (2022).
- Chen, W. L., et al. Functional near-infrared spectroscopy and its clinical application in the field of neuroscience: Advances and future directions. Frontiers in Neuroscience. 14, 724 (2020).
- Yamamoto, K., Miyata, T., Onozuka, A., Koyama, H., Ohtsu, H., Nagawa, H. Plantar flexion as an alternative to treadmill exercise for evaluating patients with intermittent claudication. European Journal of Vascular and Endovascular Surgery. 33 (3), 325-329 (2007).
- Formenti, D., et al. Effects of knee extension with different speeds of movement on muscle and cerebral oxygenation. PeerJ. 6, 5704 (2018).
- Miyai, I., et al. Cortical mapping of gait in humans: a near-infrared spectroscopic topography study. NeuroImage. 14 (5), 1186-1192 (2001).
- Miyai, I., et al. Premotor cortex is involved in restoration of gait in stroke. Annals of Neurology. 52 (2), 188-194 (2002).
- Mihara, M., et al. Sustained prefrontal activation during ataxic gait: a compensatory mechanism for ataxic stroke?. NeuroImage. 37 (4), 1338-1345 (2007).
- Rea, M., et al. Lower limb movement preparation in chronic stroke: A pilot study toward an fNIRS-BCI for gait rehabilitation. Neurorehabilitation and Neural Repair. 28 (6), 564-575 (2014).
- Holtzer, R., Verghese, J., Allali, G., Izzetoglu, M., Wang, C., Mahoney, J. R. Neurological gait abnormalities moderate the functional brain signature of the posture first hypothesis. Brain Topography. 29 (2), 334-343 (2016).
- Kim, H. Y., Yang, S. P., Park, G. L., Kim, E. J., You, J. S. Best facilitated cortical activation during different stepping, treadmill, and robot-assisted walking training paradigms and speeds: A functional near-infrared spectroscopy neuroimaging study. NeuroRehabilitation. 38 (2), 171-178 (2016).
- Khan, H., Nazeer, H., Engell, H., Naseer, N., Korostynska, O., Mirtaheri, P. Prefrontal cortex activation measured during different footwear and ground conditions using fNIRS-A case study. 2021 IEEE International Conference on Artificial Intelligence and Mechatronics Systems (AIMS). , 1-6 (2021).
- Lin, P. Y., Chen, J. J., Lin, S. I. The cortical control of cycling exercise in stroke patients: an fNIRS study). Human Brain Mapping. 34 (10), 2381-2390 (2013).
- Yang, M., Yang, Z., Yuan, T., Feng, W., Wang, P. A systemic review of functional near-infrared spectroscopy for stroke: Current application and future directions. Frontiers in Neurology. 10, 58 (2019).
- Berger, A., Horst, F., Müller, S., Steinberg, F., Doppelmayr, M. Current state and future prospects of EEG and fNIRS in robot-assisted gait rehabilitation: A brief review. Frontiers in Human Neuroscience. 13, 172 (2019).
- Khan, R. A., Naseer, N., Qureshi, N. K., et al. fNIRS-based Neurorobotic Interface for gait rehabilitation. J NeuroEngineering Rehabil. 15 (1), 7 (2018).
- Khan, H., Naseer, N., Yazidi, A., Eide, P. K., Hassan, H. W., Mirtaheri, P. Analysis of Human Gait Using Hybrid EEG-fNIRS-Based BCI System: A Review. Front. Hum. Neurosci. 14, (2020).
- Delpy, D. T., Cope, M. Quantification in tissue near-infrared spectroscopy. Philosophical Transactions of the Royal Society B: Biological Sciences. 352 (1354), 649-659 (1997).
- Huppert, T. J. Commentary on the statistical properties of noise and its implication on general linear models in functional near-infrared spectroscopy. Neurophotonics. 3, 010401 (2016).
- Alexandre, F., Heraud, N., Oliver, N., Varray, A. Cortical implication in lower voluntary muscle force production in non-hypoxemic COPD patients. PLoS One. 9 (6), 100961 (2014).
- Yoon, T., Vanden Noven, M. L., Nielson, K. A., Hunter, S. K. Brain areas associated with force steadiness and intensity during isometric ankle dorsiflexion in men and women. Experimental Brain Research. 232 (10), 3133-3145 (2014).
- Ciccarelli, O., et al. Identifying brain regions for integrative sensorimotor processing with ankle movements. Experimental Brain Research. 166 (1), 31-42 (2005).
- Udina, C., et al. Functional near-infrared spectroscopy to study cerebral hemodynamics in older adults during cognitive and motor tasks: A review. Frontiers in Aging Neuroscience. 11, 367 (2020).
- Thickbroom, G. W., Phillips, B. A., Morris, I., Byrnes, M. L., Mastaglia, F. L. Isometric force-related activity in sensorimotor cortex measured with functional MRI. Experimental Brain Research. 121 (1), 59-64 (1998).
- Derosière, G., Alexandre, F., Bourdillon, N., Mandrick, K., Ward, T. E., Perrey, S. Similar scaling of contralateral and ipsilateral cortical responses during graded unimanual force generation. NeuroImage. 85 (1), 471-477 (2014).
- Shi, P., Li, A., Yu, H. Response of the cerebral cortex to resistance and non-resistance exercise under different trajectories: A functional near-infrared spectroscopy study. Frontiers in Neuroscience. 15, 685920 (2021).
- Dettmers, C., et al. Relation between cerebral activity and force in the motor areas of the human brain. Journal of Neurophysiology. 74 (2), 802-815 (1995).
- Keisker, B., Hepp-Reymond, M. C., Blickenstorfer, A., Kollias, S. S. Differential representation of dynamic and static power grip force in the sensorimotor network. The European Journal of Neuroscience. 31 (8), 1483-1491 (2010).
- Harada, T., Miyai, I., Suzuki, M., Kubota, K. Gait capacity affects cortical activation patterns related to speed control in the elderly. Experimental Brain Research. 193 (3), 445-454 (2009).
- Saleh, S., et al. The role of premotor areas in dual tasking in healthy controls and persons with multiple sclerosis: An fNIRS imaging study. Frontiers in Behavioral Neuroscience. 12, 296 (2018).
- Bonnal, J., et al. Relation between cortical activation and effort during robot-mediated walking in healthy people: A functional near-infrared spectroscopy neuroimaging study (fNIRS). Sensors. 22 (15), 5542 (2022).
- Shibuya, K., Sadamoto, T., Sato, K., Moriyama, M., Iwadate, M. Quantification of delayed oxygenation in ipsilateral primary motor cortex compared with contralateral side during a unimanual dominant-hand motor task using near-infrared spectroscopy. Brain Research. 1210, 142-147 (2008).
- Dai, T. H., Liu, J. Z., Sahgal, V., Brown, R. W., Yue, G. W. Relationship between muscle output and functional MRI-measured brain activation. Experimental brain research. 140 (3), 290-300 (2001).
- Cabibel, V., Hordacre, B., Perrey, S. Implication of the ipsilateral motor network in unilateral voluntary muscle contraction: the cross-activation phenomenon. Journal of Neurophysiology. 123 (5), 2090-2098 (2020).
- Akselrod, M., Martuzzi, R., Serino, A., vander Zwaag, W., Gassert, R., Blanke, O. Anatomical and functional properties of the foot and leg representation in areas 3b, 1 and 2 of primary somatosensory cortex in humans: A 7T fMRI study. NeuroImage. 159, 473-487 (2017).
- Brigadoi, S., Cooper, R. J. How short is short? Optimum source-detector distance for short-separation channels in functional near-infrared spectroscopy. Neurophotonics. 2 (2), 025005 (2015).
- Funahashi, S. Prefrontal contribution to decision-making under free-choice conditions. Frontiers in Neuroscience. 11, 431 (2017).
- Simon, S. R., Meunier, M., Piettre, L., Berardi, A. M., Segebarth, C. M., Boussaoud, D. Spatial attention and memory versus motor preparation: premotor cortex involvement as revealed by fMRI. Journal of Neurophysiology. 88 (4), 2047-2057 (2002).
- Desmurget, M., Sirigu, A. A parietal-premotor network for movement intention and motor awareness. Trends in Cognitive Sciences. 13 (10), 411-419 (2009).
- Nachev, P., Kennard, C., Husain, M. Functional role of the supplementary and pre-supplementary motor areas. Nature reviews. Neuroscience. 9 (11), 856-869 (2008).
- Thoenissen, D., Zilles, K., Toni, I. Differential involvement of parietal and precentral regions in movement preparation and motor intention. The Journal of neuroscience: the official journal of the Society for Neuroscience. 22 (20), 9024-9034 (2002).
- Al-Quraishi, M. S., Elamvazuthi, I., Tang, T. B., Al-Qurishi, M., Adil, S. H., Ebrahim, M. Bimodal data fusion of simultaneous measurements of EEG and fNIRS during lower limb movements. Brain Sciences. 11 (6), 713 (2021).
- Bishnoi, A., Holtzer, R., Hernandez, M. E. Brain Activation Changes While Walking in Adults with and without Neurological Disease: Systematic Review and Meta-Analysis of Functional Near-Infrared Spectroscopy Studies. Brain sciences. 11 (3), 291 (2021).
- Oh, S., Song, M., Kim, J. Validating attentive locomotion training using interactive treadmill: an fNIRS study. Journal of NeuroEngineering and Rehabilitation. 15 (1), 122 (2018).

