Моделирование и моделирование обонятельной доставки лекарств с пассивным и активным контроля интраназально ингаляционных Pharmaceutical Аэрозоли
Summary
This manuscript reviews the modeling and simulations of different protocols to deliver medications to the olfactory region in image-based nasal airway models. Multiple software modules are used to develop the anatomically accurate nose model, generate computational mesh, simulate nasal airflows, and predict particle deposition at the olfactory region.
Abstract
Есть много преимуществ прямой нос к мозгу доставки лекарственных средств в лечении неврологических расстройств. Тем не менее, его применение ограничено крайне низкой эффективностью доставки (<1%) к обонятельной выстилки, которая непосредственно соединяет мозг. Крайне важно разработать методики новых более эффективно доставлять лекарства к неврологическим обонятельной области. Целью данного исследования является разработка численного платформу для моделирования и улучшения интраназально обонятельный доставки лекарств. Спаренная метод изображения CFD был представлен, что синтезировали развитие на основе образа модели, качество Meshing, моделирование жидкости и отслеживание магнитной частицы. С помощью этого метода, выступления трех интраназальных протоколов доставки численно оценивались и сравнивались. Были также изучены численно Влияния дыхательных маневров, магнит макета, напряженность магнитного поля, положения высвобождения лекарственного средства и размера частиц на обонятельный дозировке.
Из хimulations, мы обнаружили, что клинически значимым обонятельная дозировка (до 45%) было осуществлено с использованием комбинации расположения магнита и селективного высвобождения лекарственного средства. 64-кратная выше поставка дозы было предсказано в случае с магнитофоретического руководством по сравнению со случаем без него. Тем не менее, точное наведение интраназально вдыхаемых аэрозолей в обонятельной области остается сложной из-за нестабильного характера магнитофореза, а также высокой чувствительности обонятельного дозировке пациенто, Device- и факторов частиц, связанных с.
Introduction
Лекарственные средства , поставляемые в обонятельную область может обойти гематоэнцефалический барьер и непосредственно проникают в мозг, что приводит к эффективному поглощению и быстрое начало действия препаратов 1,2. Однако обычные носовые устройства , такие как назальные спреи насосов и обеспечивают чрезвычайно низкие дозы в обонятельной области (<1%) через носовые пути 3,4. Это в первую очередь связано со сложной структурой человеческого носа , который состоит из узких, запутанных проходов (рисунок 1). Обонятельная область размещает над верхним проходом, где лишь очень небольшая часть вдыхаемого воздуха может достигать 5,6. Кроме того, обычные устройства для ингаляции зависит от аэродинамических сил для транспортировки терапевтических агентов для целевой области 7. Там нет никакого дальнейшего контроля над движениями частиц после их освобождения. Таким образом, переноса и осаждения этих частиц преимущественно зависят от их начальных скоростей и положений выпуска. В связина свернутой носовой ход, а также отсутствие контроля частиц, большинство частиц лекарственного средства оказались в ловушке в переднем отделе носа и не может достичь обонятельной области 8.
Хотя есть много вариантов носовых устройств, те , которые предназначены специально для целевой доставки обонятельной редко сообщалось 7,9. Одним из исключений является Hoekman и Ho 10 , который разработал обонятельный преференциальный устройства доставки и продемонстрировали более высокие уровни лекарственного средства Кора-на-крови у крыс в противоположность использованию капли носа. Тем не менее, масштабирование результатов осаждения у крыс для человека не является простым делом, принимая во внимание огромные анатомо-физиологические различия между этими двумя видами 11. Многие существуют ограничения при использовании адаптированных версий стандартных назальных устройств для обонятельных поставок. Одним из основных регресс является то, что только очень небольшая часть препаратов, могут быть доставлены в обонятельную слизистую оболочку, через которую лекарственные средства могут войти вголовной мозг. Численное моделирование предсказывает , что менее 0,5% от интраназально наночастиц может внести в обонятельной области 3,5. Скорость осаждения еще ниже (0,007%) для частиц микронных 12. Для того, чтобы сделать доставку нос к мозгу клинически осуществимым, обонятельная скорость осаждения должна быть значительно улучшена.
Там существует несколько возможных подходов к улучшению обонятельный доставки. Один из возможных подходов является смарт – идея ингалятор , предложенный Kleinstreuer и др. 13 , в качестве частицы выпавшие в одном регионе, в основном , от одной конкретной области на входе, то можно доставить частицы в сайт – мишень, выпуская их только из определенных областей на входе , Смарт – метод доставки , как было показано , чтобы создать гораздо более эффективную доставку легких , чем традиционные методы. 13,14 Предполагается , что эта идея смарт – доставки также может быть применен в интраназальной доставки лекарственных средств к Improve дозировок к обонятельной выстилки. Выпуская частицы в различные положения при открытии ноздрей и из разных глубин в полости носа, улучшение обонятельные эффективности доставки и сокращение отходов лекарственного средства в переднем отделе носа возможны.
Другой возможный способ активно управлять движением частиц в носовую полость с помощью различных полевых сил, таких как электрический или магнитной силы. Электрический контроль заряженных частиц было предложено для адресной доставки лекарств для человеческого носа и легких 15-17. Си и др. 18 численно протестировали производительность электрического руководством заряженных частиц и предсказанную значительно улучшились обонятельные дозы. Точно так же, наведение ферромагнитных частиц лекарственного средства с соответствующим магнитным полем также имеет потенциал для частиц мишени в обонятельную слизистую оболочку. Поведения ингаляционных агентов, если ферромагнитное, может быть изменена путем введения соответствующих магнитных сил <suр> 19. ДАМ и др. 20 показали , что это практично целевой ферромагнитных частиц в конкретных областях в легких мышей. По упаковки терапевтических агентов с наночастицами суперпарамагнитных оксида железа, осаждение в одном легком мыши под воздействием сильного магнитного поля была значительно увеличена по сравнению с другими 20 легких.
Частицы считались сферическими и варьировались от 150 нм до 30 мкм в диаметре. Основное уравнение 21:
(1) 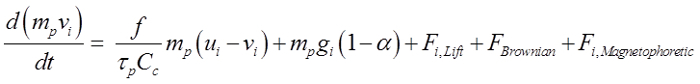
Выше уравнение описывает движение частицы , регулируемой силы сопротивления, силы тяжести, Саффмана подъемной силы 22, броуновского силы для наночастиц и магнитофоретического силы , если их поместить в магнитное поле. Здесь v я скорость частицы, U I является скорость потока, τ рвремя отклика частиц, С С поправочный коэффициент Cunningham, и α представляет собой отношение плотности воздуха / частиц. Для того, чтобы эффективно руководить интраназально наркотики в обонятельной области, необходимо для приложенные магнитофоретического силы, чтобы преодолеть как инерцию частицы и силы тяготения. В этом исследовании, композит 20% маггемиту (γ-Fe 2 O 3, 4,9 г / см 3) и 80% активного агента предполагалось, что дает плотность приблизительного 1,78 г / см 3 и относительную магнитную проницаемость 50. выбор гамма-Fe 2 O 3 было обусловлено его низкой цитотоксических. Железо (3+) , ионы широко распространены в человеческом организме , и немного выше , концентрация ионов не вызывает значительных побочных эффектов 23.
Protocol
Representative Results
Discussion
Спаренная метод изображения CFD был представлен в данном исследовании, который включал разработку изображения на основе модели, качество сцепление, моделирование воздушных потоков и отслеживание магнитного частиц. Несколько программных модулей были реализованы в достижение этой цел?…
Divulgations
The authors have nothing to disclose.
Acknowledgements
Это исследование было профинансировано Центрального Мичиганского университета инновационных исследований Grant P421071 и начале карьеры Грант P622911.
Materials
| MIMICS 13 | Materialise Inc, Ann Arbor, MI | MR image segmentation | |
| Gambit | ANSYS Inc, Canonsburg, PA | Model development | |
| ANSYS ICEMCFD | ANSYS Inc, Canonsburg, PA | Meshing | |
| ANSYS Fluent | ANSYS Inc, Canonsburg, PA | Fluid and particle simulation | |
| COMSOL Multiphsics | COMSOL Inc, Burlington, MA | Magnetic particle tracing |
References
- Mistry, A., Stolnik, S., Illum, L. Nanoparticles for direct nose-to-brain delivery of drugs. Int. J. Pharm. 379 (1), 146-157 (2009).
- Alam, S., et al. Development and evaluation of thymoquinone-encapsulated chitosan nanoparticles for nose-to-brain targeting: a pharmacoscintigraphic study. Int. J. Nanomedicine. 7 (11), 5705-5718 (2012).
- Shi, H., Kleinstreuer, C., Zhang, Z. Laminar airflow and nanoparticle or vapor deposition in a human nasal cavity model. J. Biomech. Eng. 128 (5), 697-706 (2006).
- Si, X., Xi, J., Kim, J., Zhou, Y., Zhong, H. Modeling of release position and ventilation effects on olfactory aerosol drug delivery. Respir. Physiol. Neurobiol. 186 (1), 22-32 (2013).
- Si, X., Xi, J., Kim, J. Effect of laryngopharyngeal anatomy on expiratory airflow and submicrometer particle deposition in human extrathoracic airways. Open J. Fluid D. 3 (4), 286-301 (2013).
- Xi, J., Longest, P. W. Numerical predictions of submicrometer aerosol deposition in the nasal cavity using a novel drift flux approach. Int. J. Heat Mass Transfer. 51 (23), 5562-5577 (2008).
- Illum, L. Nasal drug delivery: new developments and strategies. Drug Discov. Today. 7 (23), 1184-1189 (2002).
- El Taoum, K. K., Xi, J., Kim, J. W., Berlinski, A. In vitro evaluation of aerosols delivered via the nasal route. Respir. Care. 60 (7), 1015-1025 (2015).
- Misra, A., Kher, G. Drug delivery systems from nose to brain. Curr. Pharm. Biotechnol. 13 (12), 2355-2379 (2012).
- Hoekman, J. D., Ho, R. J. Y. Effects of Localized Hydrophilic Mannitol and Hydrophobic Nelfinavir Administration Targeted to Olfactory Epithelium on Brain Distribution. Aaps Pharmscitech. 12 (2), 534-543 (2011).
- Corley, R. A., et al. Comparative Computational Modeling of Airflows and Vapor Dosimetry in the Respiratory Tracts of Rat, Monkey, and Human. Toxicol. Sci. 128 (2), 500-516 (2012).
- Shi, H., Kleinstreuer, C., Zhang, Z. Modeling of inertial particle transport and deposition in human nasal cavities with wall roughness. J. Aerosol Sci. 38 (4), 398-419 (2007).
- Kleinstreuer, C., Zhang, Z., Donohue, J. F. Targeted drug-aerosol delivery in human respiratory system. Annu. Rev. Biomed. Eng. 10 (4), 195-220 (2008).
- Kleinstreuer, C., Zhang, Z., Li, Z., Roberts, W. L., Rojas, C. A new methodology for targeting drug-aerosols in the human respiratory system. Int. J. Heat Mass Transfer. 51 (23), 5578-5589 (2008).
- Wilson, I. B. The deposition of charged particles in tubes, with reference to the retention of therapeutic aerosols in the human lung. J. Colloid Sci. 2 (2), 271-276 (1947).
- Wong, J., Chan, H. -. K., Kwok, P. C. L. Electrostatics in pharmaceutical aerosols for inhalation. Ther Deliv. 4 (8), 981-1002 (2013).
- Bailey, A. G. The inhalation and deposition of charged particles within the human lung. Journal of Electrostatics. 42 (1), 25-32 (1997).
- Xi, J., Si, X. A., Gaide, R. Electrophoretic particle guidance significantly enhances olfactory drug delivery: a feasibility study. PLoS ONE. 9 (1), e86593 (2014).
- Martin, A., Finlay, W. Alignment of magnetite-loaded high aspect ratio aerosol drug particles with magnetic fields. Aerosol Sci. Technol. 42 (4), 295-298 (2008).
- Dames, P., et al. Targeted delivery of magnetic aerosol droplets to the lung. Nature Nanotechnology. 2 (8), 495-499 (2007).
- Xi, J., Longest, P. W. Transport and deposition of micro-aerosols in realistic and simplified models of the oral airway. Ann. Biomed. Eng. 35 (4), 560-581 (2007).
- Longest, P. W., Xi, J. Effectiveness of direct Lagrangian tracking models for simulating nanoparticle deposition in the upper airways. Aerosol Sci. Technol. 41 (4), 380-397 (2007).
- Xi, J., Zhang, Z., Si, X. A., Yang, J., Deng, W. Optimization of magnetophoretic-guided drug delivery to the olfactory region in a human nose model. Biomech. Model. Mechanobiol. In. , (2015).
- Longest, P. W., Hindle, M., Das Choudhuri, S., Xi, J. X. Comparison of ambient and spray aerosol deposition in a standard induction port and more realistic mouth-throat geometry. J. Aerosol Sci. 39 (7), 572-591 (2008).
- Xi, J., et al. Design and Testing of Electric-Guided Delivery of Charged Particles to the Olfactory Region: Experimental and Numerical Studies. Curr. Drug Deliv. 13 (9), 1-15 (2015).
- Zhou, Y., Guo, M., Xi, J., Irshad, H., Cheng, Y. -. S. Nasal deposition in infants and children. Journal of aerosol medicine and pulmonary drug delivery. 27 (2), 110-116 (2014).
- Xi, J., Yuan, J. E., Si, X. A., Hasbany, J. Numerical optimization of targeted delivery of charged nanoparticles to the ostiomeatal complex for treatment of rhinosinusitis. Int. J. Nanomedicine. 10 (7), 4847-4861 (2015).

