En guide til Strukturert Illumination TIRF Mikros i høy hastighet med flere farger
Summary
This article provides an in depth guide for the assembly and operation of a structured illumination microscope operating with total internal reflection fluorescence illumination (TIRF-SIM) to image dynamic biological processes with optical super-resolution in multiple colors.
Abstract
Optisk super-oppløsning avbildning med strukturert belysning mikroskopi (SIM) er en viktig teknologi for visualisering av prosesser på molekylært nivå i den kjemiske og biomedisinsk vitenskap. Selv om kommersielle SIM-systemer er tilgjengelige, systemer som er tilpasset designet i laboratoriet kan utkonkurrere kommersielle systemer, sistnevnte vanligvis designet for enkel bruk og generelle applikasjoner, både når det gjelder bildegjengivelse og hastighet. Denne artikkelen presenterer en grundig guide til å bygge et SIM system som bruker total intern refleksjon (TIR) belysning og er i stand til bildebehandling på opptil 10 Hz i tre farger med en oppløsning på 100 nm. På grunn av kombinasjonen av SIM og TIRF, gir systemet bedre bildekontrast enn konkurrerende teknologier. For å oppnå disse spesifikasjonene er flere optiske elementer som brukes til å aktivere automatisk kontroll over polarisasjonstilstand og romlig struktur av belysningslys for alle tilgjengelige eksitasjon WAVelengths. Full informasjon om maskinvare gjennomføring og kontroll er gitt for å oppnå synkronisering mellom eksitasjon lys mønster generasjon, bølgelengde, polarisering stat og kamerastyring med vekt på å oppnå maksimal oppkjøpet frame rate. En trinn-for-trinn-protokoll for systemet justering og kalibrering er presentert og den oppnåelige oppløsningen forbedringen er godkjent for ideelle testprøver. Muligheten for video-rate super-oppløsning avbildning er demonstrert med levende celler.
Introduction
I løpet av det siste halvt tiår, har super-oppløsning mikros modnet og flyttet fra spesialist optikk laboratorier i hendene på biologen. Kommersielle mikroskop løsninger finnes for de tre hovedvarianter for å oppnå optisk super-oppløsning: enkelt molekyl lokalisering mikroskopi (SMLM), stimulert emisjon utarming mikroskopi (STED), og strukturert belysning mikroskopi (SIM) 1,2. SMLM som photoactivated lokalisering mikroskopi (PALM) og stokastisk optisk gjenoppbygging mikroskopi (STORM) har vært de mest populære teknikker, hovedsakelig på grunn av enkelheten i den optiske setup og løfte om høy romlig oppløsning, lett ned til 20 nm. Imidlertid super-oppløsning mikros via enkelt molekyl lokalisering har en iboende trade-off: romlig oppløsning oppnåe er avhengig av akkumulere et tilstrekkelig antall individuelle fluoroforen lokaliseringene, og dermed begrenser tidsmessig oppløsning. Imaging dynamisk prosesses i levende celler blir derfor problematisk som man må tilstrekkelig smake bevegelsen av strukturen av interesse å hindre bevegelsesartefakter og samtidig skaffe nok lokaliserings hendelser i den tiden til å rekonstruere et bilde. For å møte disse kravene, har levende celle SMLM demonstrasjoner fått den nødvendige økningen i fluorophore photoswitching priser ved i stor grad øke eksitasjon makt, og dette fører igjen til fototoksisitet og oksidativt stress, og dermed begrense utvalget overlevelsestider og biologisk relevans tre.
En klar fordel med STED både over og SIM SMLM er at det kan bildet med super-oppløsning i tykke prøver, for eksempel lateral oppløsning på omkring 60 nm ble oppnådd i organotypiske hjernesnitt ved dybder opp til 120 pm 4. Imaging på slike dybder med ett mål implementasjoner av SMLM eller SIM er ugjørlig, men blir mulig med enten single-molekyl lys ark eller gitter lys ark microscopy 5. Video-rate STED har også blitt demonstrert og brukt til å kartlegge synaptic vesicle mobilitet, men så langt har dette vært begrenset til bildebehandling små synsfelt 6.
For anvendelser i cellebiologi og molekylære egen montering reaksjoner 7 – 12 som krever avbildning med høy tidsoppløsning over mange tidspunkter, strukturert belysning mikroskopi (SIM) kan være godt egnet, da den ikke er avhengig av photophysical egenskapene til en spesiell fluorescerende sonde. Til tross for dette iboende fordel av SIM, inntil nå bruken har i hovedsak vært begrenset til bildebehandling faste celler eller saktegående prosesser. Dette er på grunn av begrensninger i kommersielt tilgjengelige SIM-systemer: oppkjøpet bildefrekvens på disse instrumentene ble begrenset av rotasjonshastighet rister brukes til å generere de nødvendige sinusbelysningsmønstre samt polariseringen opprettholde optikk. Den nyeste generasjonen av kommersielle SIMinstrumenter er i stand til rask bildebehandling, men de er veldig dyrt for alle, men sentrale bildetjenester.
Denne protokollen presenterer en guide til byggingen av et fleksibelt SIM system for avbildning raske prosesser i tynne prøver og nær basal overflaten av levende celler. Den benytter total indre refleksjon fluorescens (TIRF) for å generere et belysningsmønster som trenger dypere enn omtrent 150 nm inn i prøve 13 som vesentlig reduserer ute av fokus bakgrunnssignal. Ideen om å kombinere SIM med TIRF er nesten like gammel som SIM seg 14, men ble ikke realisert eksperimentelt før 2006 15. Den første in vivo bildene oppnådd med TIRF-SIM ble rapportert i 2009 16 oppnå bildefrekvens på 11 Hz å visualisere tubulin og kinesin dynamikk, og to farge TIRF-SIM-systemer har blitt presentert 17,18. Nå nylig, en guide for bygging og bruk av en enkelt farge to-bjelke SIM system ble presentert med ramme-hastighet på opptil 18 Hz 19,20.
Oppsettet presenteres her er i stand til SIM super oppløsning bildebehandling ved 20 Hz i tre farger, hvorav to kan betjenes i TIRF-SIM. Hele systemet er bygget opp rundt et invertert mikroskop ramme og bruker en motorisert xy oversettelsestrinnet med en piezo-aktivert z stadium. For å generere sinus eksitasjon mønstre som kreves for TIRF-SIM, bruker systemet presentert en ferroelektrisk romlig lys modulator (SLM). Binære grating mønstre vises på SLM og de resulterende ± 1 diffraksjon bestillinger blir filtrert, videresendt og fokusert inn i TIR ringen på objektivet. De nødvendige faseforskyvninger og rotasjonene til gitterne blir påført ved å endre det fremviste bildet SLM. Denne protokollen beskriver hvordan å bygge og justere slik eksitasjon bane, detaljer justeringen av utslipps banen, og presenterer testprøver for å sikre optimal justering. Det er også de skriftlærde problemstillinger og utfordringer spesielt for høy hastighet TIRF-SIM vedrørende polarisering kontroll og synkronisering av komponenter.
Design Betraktninger og begrensninger
Før du monterer TIRF-SIM-systemet som presenteres i denne protokollen, er det flere design begrensninger for å vurdere som bestemmer valg av optiske komponenter. Alle forkortelser av optiske komponenter se figur 1.
Spatial Lys Modulator (SLM)
En binær ferroelektrisk SLM er brukt i dette oppsettet som det er i stand til å undermillisekund mønster svitsjing. Gråtone nematiske SLMs kan brukes, men disse gir sterkt redusert koblingstider. Hver av eller på bildeelement i en binær fase SLM vil gi enten et π eller 0-faseforskyvning til den innfallende plan bølgefront, og derfor om en periodisk gittermønster blir vist på SLM den vil fungere som en fase diffraksjonsgitter.
ent "> Total Internal Reflection (TIR) For å oppnå TIR og produsere et flyktig felt, må den innfallende vinkel på eksitasjon bjelkene på glassprøven grensesnitt være større enn den kritiske vinkel 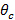 . Dette angir den minste innfallsvinkelen som kreves, og følgelig også den maksimale avstand, eller periode, av den flyktige belysningsmønster. Den maksimale innfallsvinkelen
. Dette angir den minste innfallsvinkelen som kreves, og følgelig også den maksimale avstand, eller periode, av den flyktige belysningsmønster. Den maksimale innfallsvinkelen 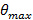 (Den åpningsvinkel) er begrenset av den numeriske apertur (NA) for objektivlinsen som kan beregnes ut fra definisjonen
(Den åpningsvinkel) er begrenset av den numeriske apertur (NA) for objektivlinsen som kan beregnes ut fra definisjonen 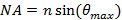 . Dette bestemmer den minste avstanden mønster kan oppnås i henhold til formel Abbe
. Dette bestemmer den minste avstanden mønster kan oppnås i henhold til formel Abbe 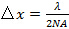 som knytter NA og bølgelengde
som knytter NA og bølgelengde 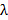 til et minimum mønsteravstanden <imgalt = "Equation" src = "/ files / ftp_upload / 53988 / 53988eq6.jpg" />. I praksis får man et 1,49 NA oljeneddyppingsobjektivet TIRF objektiv en maksimal innfallsvinkel på rundt 79 ° og et minimum mønster periode på prøven på 164 nm ved bruk av en eksitasjonsbølgelengde på 488 nm. Disse to vinklene definerer en ring på baksiden åpning av målet over hvilken instrumentet oppnår TIR belysning (dvs.. TIR-ring), og hvor de to brennpunkter eksitasjon må plasseres nøyaktig og presist roteres for å generere hver belysningsmønster.
til et minimum mønsteravstanden <imgalt = "Equation" src = "/ files / ftp_upload / 53988 / 53988eq6.jpg" />. I praksis får man et 1,49 NA oljeneddyppingsobjektivet TIRF objektiv en maksimal innfallsvinkel på rundt 79 ° og et minimum mønster periode på prøven på 164 nm ved bruk av en eksitasjonsbølgelengde på 488 nm. Disse to vinklene definerer en ring på baksiden åpning av målet over hvilken instrumentet oppnår TIR belysning (dvs.. TIR-ring), og hvor de to brennpunkter eksitasjon må plasseres nøyaktig og presist roteres for å generere hver belysningsmønster.
Rekonstruksjon av TIRF-SIM-bilder krever kjøp av minimum tre fase skift per mønster rotasjon derfor SLM mønster perioden må være delelig med 3 (se figur 1). For eksempel vil en periode på 9 piksler for 488 nm lys og 12 piksler for 640 nm lys. For en omfattende diskusjon av SLM mønster design, inkludert underpiksel optimalisering av mønster avstand ved hjelp skåret gitter, Se tidligere arbeid av Kner et al. 16 og Lu-Walther et al. 20 Posisjonen av de to eksitasjon brennpunktene må være inne i TIR ring for alle bølgelengder, men diffraksjonsvinkelen av de ± en ordre fra SLM er bølgelengden avhengig. For standard SIM, kan flerfarget bildebehandling oppnås ved å optimalisere gitteret periode for lengst bølgelengde, og tolerer et tap i ytelse for de kortere kanaler. For TIRF-SIM imidlertid å optimalisere for en bølgelengde vil si at den andre bølgelengde brennpunktene ikke lenger er innenfor TIR ringen. For eksempel, ved bruk av et gitter periode på 9 piksler er tilstrekkelig til å gi TIRF til 488 nm, som foci er ved 95% av diameteren av ryggen åpning og inne i TIR ringen, men for 640 nm denne perioden vil posisjonere foci utenfor blenderåpningen. Av denne grunn ulike pikselmønsteravstander må brukes for hver eksitasjon bølgelengde.
Justeringen av TIRF-SIM eksitasjon banener ekstremt følsomme for små endringer i stillingen av det dikroiske speilet (DM4 i figur 1) i mikroskop kroppen, mye mer enn i konvensjonell SIM. Bruk av en roterende filter kube turret anbefales ikke, i stedet bruke en enkelt, multi-band dichroic speil, som holdes i en fast posisjon og designet spesielt for eksitasjonsbølgelengdene brukt. Det er viktig at bare de høyeste kvalitet dikroiske speil er brukt. Disse krever tykke substrater på minst 3 mm, og er ofte betegnet som "bilde flat" av produsentene. Alle andre underlag føre til uutholdelig aberrasjon og bildekvaliteten i TIRF-SIM.
polarisering kontroll
For å oppnå TIRF-SIM det er nødvendig å rotere polarisasjonstilstanden av eksitasjonslyset i synkronitet med belysningsmønster slik at den forblir asimutalt polarisert i den objektive eleven planet i forhold til den optiske aksen (dvs.. s-polarisert). Justering av polarisasjonen kontroll optikk vil avhenge av den bestemte optiske elementet anvendes, for eksempel en Pockels-celle 21, eller en halv bølgeplate i en motorisert dreietrinn 22. I denne protokollen en tilpasset flytende krystall variabel retarder (LCVR) brukes, designet for å gi full-bølge (2π) retardance over bølgelengdeområdet 488-640 nm som det tillater rask (~ msek) veksling. Ved anvendelse av en flytende-krystall retarderer er det viktig å bruke en høy kvalitet komponent: standard komponenter er vanligvis ikke stabile nok til å gi en konstant retardance over lengden av kameraets eksponeringstid som fører til en tåkelegge ut av belysningsmønster og lav modulasjon kontrast . Flytende krystall retardere er også sterkt temperaturavhengig og krever bygget i temperaturkontroll.
synkronisering
Lasere må synkroniseres med SLM. Binære ferroelectric SLMs er internt balansert med switching mellom en på staten og av-tilstand. Pikslene bare fungere som en halv bølgeplater i enten deres på eller av staten, men ikke i løpet av inter bytte tid. Derfor lasere skal kun være slått på under på / av statene via LED Aktiver signal fra SLM å hindre en reduksjon i mønster kontrast på grunn av mellomliggende tilstand av pikslene. En akusto-optisk modulator (AOM) kan alternativt bli brukt som en hurtig lukker dersom lasere ikke kan digitalt modulert.
Valg av linser
Basert på disse begrensninger, i den nødvendige demagnification av SLM planet på prøven planet gir de ønskede belysningsmønster kan bestemmes. Dette gjør beregning av brennvidde på de to linsene L3 og L4 i bildet stafett teleskop og eksitasjon kondensatoren objektivet L5. I dette systemet en 100X / 1.49NA oljeneddyppingsobjektivet objektiv brukes med 488 nm og 640 nm eksitasjon, bruker dermed brennvidde på 300 og 140 mmfor L4 og L3, og 300 mm for L5, noe som gir en total demagnification av 357X, tilsvarende en SLM pikselstørrelse på 38 nm på prøven planet. Ved hjelp av denne kombinasjon av linser, SLM gitterperioder 9 for 488 nm lys og 12 piksler for 640 nm gi mønster avstander på 172 og 229 nm i prøven, tilsvarende anslagsvinkler på henholdsvis 70 ° og 67 °. For et glass-vann-grenseflaten, er den kritiske vinkel 61 °, og er uavhengig av bølgelengden, og derfor disse to mønster avstander tillate TIRF eksitasjon for begge bølgelengder. En objektivlinse er utstyrt med en korreksjon krage er anvendelig for korreksjon av sfæriske avvik som innføres ved variasjoner i dekktykkelse, eller hvis arbeider ved 37 ° C.
Bilde Reconstruction
Når rå SIM data har blitt kjøpt opp er det et spørsmål om beregnings innsats for å generere super-løst bilder i en to-trinns prosess. For det første må belysningsmønster som skal bestemmes forhvert bilde og for det andre, må komponentene i SIM-spekteret separeres og kombineres på riktig måte som for å doble den effektive OTF bæreren (se Figur 6, innfellinger).
Presis kunnskap om de projiserte belysningsmønstre er viktig, som super-løst frekvenskomponenter må være ublandet så nøyaktig som mulig for å hindre gjenstander forårsaket av de gjenværende delene av overlappende komponenter. Vi bestemmer den belysningsmønster parametere a posteriori fra den rå bildedata ved å følge prosedyren innføres ved Gustafsson et al. 23 Kort sagt, et sett av belysningsparametre som beskriver en normalisert todimensjonal sinusoid har til å bli funnet for hver av de 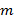 eksitasjon mønstre
eksitasjon mønstre 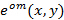 :
:
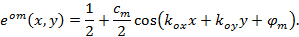
herved 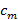 og
og 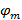 beskrive frynse kontrasten og mønsteret startfasen av hvert enkelt bilde m hhv. Komponentene i bølgevektor,
beskrive frynse kontrasten og mønsteret startfasen av hvert enkelt bilde m hhv. Komponentene i bølgevektor, 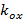 og
og 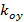 Bare endres med forskjellige orienteringer
Bare endres med forskjellige orienteringer 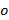 av mønsteret og kan antas å være konstant på annen måte. Til grovt bestemme komponentene i bølgevektor en krysskorrelasjon av rå bilde spektra er utført, som er raffinert ved å påføre underpiksel skifter til en av de kryss-korrelerte bilder som for å optimalisere overlapping. Dette gjøres via multiplikasjon av fast-plass fase gradienter
av mønsteret og kan antas å være konstant på annen måte. Til grovt bestemme komponentene i bølgevektor en krysskorrelasjon av rå bilde spektra er utført, som er raffinert ved å påføre underpiksel skifter til en av de kryss-korrelerte bilder som for å optimalisere overlapping. Dette gjøres via multiplikasjon av fast-plass fase gradienter 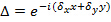 som induserer en underpiksel skifte i frekvens-plass. Legg merke til at det er nyttig å ha et godt estimat av bølge-vektorer før selve mønsteret estimering og dette kan bli funnet ved å avbilde et fluorescerende sjikt vulst.
som induserer en underpiksel skifte i frekvens-plass. Legg merke til at det er nyttig å ha et godt estimat av bølge-vektorer før selve mønsteret estimering og dette kan bli funnet ved å avbilde et fluorescerende sjikt vulst.
Som det fasetrinn mellom forskjøvet mønster er 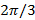 , Altså.
, Altså. 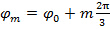 , Separasjon av frekvenskomponenter kan utføres av en Fourier-transformasjon langs de "faseaksen". Den globale fase
, Separasjon av frekvenskomponenter kan utføres av en Fourier-transformasjon langs de "faseaksen". Den globale fase 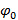 og pannelugg kontrast
og pannelugg kontrast 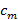 kan deretter bli bestemt ved anvendelse av lineær regresjon sammensatt av forskjellige komponenter. De enkelte separerte komponenter blir så kombinert ved hjelp av en generalisert Wiener filter. For en detaljert beskrivelse av både parameter utvinning og gjennomføring av generalisert Wiener filter øvrig henvises det til Gustafssonet al., 23 hvor den samme algoritmen blir brukt.
kan deretter bli bestemt ved anvendelse av lineær regresjon sammensatt av forskjellige komponenter. De enkelte separerte komponenter blir så kombinert ved hjelp av en generalisert Wiener filter. For en detaljert beskrivelse av både parameter utvinning og gjennomføring av generalisert Wiener filter øvrig henvises det til Gustafssonet al., 23 hvor den samme algoritmen blir brukt.
Protocol
Representative Results
Discussion
Spesialbygde TIRF-SIM-systemer som oppsettet beskrevet i denne protokollen er i stand til flerfarget super oppløsning bildebehandling i høy hastighet i forhold til kommersielt tilgjengelige mikroskoper. Den iboende fordel med SIM som en super-oppløsning teknikk er at den tidsoppløsningen ikke er begrenset av photophysics til fluoroforen, sammenlignet med andre metoder slik som enkelt molekyl lokalisering mikroskopi (SMLM) eller punkt skanning metoder slik som stimulert emisjon uttømming mikroskopi ( STED). I motsetning til disse andre teknikker, ikke SIM ikke krever photoswitchable eller depletable fluoroforer så flerfarget bildebehandling er grei. Ikke TIRF-SIM-systemer, for eksempel optisk seksjonering SIM og multifokal SIM kan vanligvis oppnå forbedringer av 1,7 ganger eller mindre oppløsning i praksis i motsetning til den faktor på to forbedring rapportert her, og kommersielle systemer er også ofte langsommere og mindre fleksibelt enn systemet presentert i denne protokollen.
"> De to viktigste vanskeligheter med å gjennomføre denne teknikken er for det første nødvendigheten for nøyaktig posisjonering av de seks SIM bjelkene innenfor TIR sone av den tilsiktede rygg åpning, som krever en møysommelig og tidskrevende optiske innretningsprosedyre. For det andre, for å produsere høy mønster kontrast på prøven, er polarisering rotasjon avgjørende. for lave NA 2D-SIM-systemer, kan polarisering rotasjon unngås ved forsiktig valg av den lineære polarisering orientering, men dette blir umulig for TIRF-SIM 25. for høy hastighet flerfarget bildebehandling, elektro- optisk polarisasjon kontroll er nødvendig, og dette øker kompleksiteten og kostnadene av systemet.Begrensninger av teknikken
TIRF-SIM, som konvensjonelt TIRF, er naturligvis begrenset til observasjon av biologiske strukturer og prosesser som ligger ved basalcellemembran som kan bli opplyst ved 150-200 nm penetrasjonsdybden av det svinnende felt. MensSIM-kortet er ofte sitert som mindre photodamaging til celler enn enten STED eller SMLM, betyr lateral oppløsning fordobling fortsatt øke det nødvendige antall fotoner med minst 4 ganger 5 sammenlignet med konvensjonelle TIRF mikroskopi. For bildebehandling ved høy bildefrekvens med korte eksponeringer ganger, nødvendiggjør dette foton økning bruk av økt belysning intensiteter. Mens noen fluorophore kan brukes for SIM avbildning av faste eller saktegående prøver, høy lysstyrke fluorescerende proteiner eller neste generasjons syntetiske fargestoffer med forbedret fotostabilitet er anbefalt for live celle bildebehandling.
Selv om denne implementeringen er i stand til å avbilde en enkelt farge på SIM bildefrekvens på over 20 Hz, er flerfarget bildebehandling i fremlagt system begrenset av koplingstiden av den motoriserte utslipp filter hjulet. På grunn av den store størrelsen på sCMOS kamera brikken, ville bruk av et multibånd-utslipp filtrer og bildesplitte optikk være mulig og tillate samtidig jegmaging med flere bølgelengder på farts straff. En annen mulighet vil være å veksle de forskjellige eksitasjon lasere og bruke en multiband hakkfilter for å avvise eksitasjonslyset. Bruken av en binær ferroelektrisk SLM i denne utførelse er heller ikke optimal. Diffraksjonseffektiviteten av en slik SLM er meget lav, slik at mesteparten av det innfallende lys er i den nullte ordens refleksjon, som filtreres ut av den romlige masken. For applikasjoner som krever svært høy bildefrekvens, er bildehastigheten derfor begrenset av utgangseffekten av laserdioder. SLM introduserer også noen ellipticity i polarisering for bølgelengder unna 550 nm utformingen bølgelengde der pikslene ikke opererer som ideelle halvbølgeplater. Selv om dette kan kompenseres for ved hjelp av en ekstra LCVR, kan den ideelle løsningen være bruk av en digital mikro-speil-enhet (DMD) som en mønstergenerator.
mulige endringer
Oppsettet presented her er fleksibel og lettere modifisert enn kommersielle virkemidler slik at andre bildediagnostikk som for eksempel 3D-SIM, rask 2D-SIM, multifokal SIM (MSIM) og ikke-lineær SIM (NL-SIM) kan implementeres 21,34,35.
2D-SIM kan være godt egnet for avbilding forholdsvis flat, raskt bevegelige strukturer, slik som omkrets endoplasmatiske retikulum. Den perifere ER ligger dypere inne i cellen enn det som kan bli opplyst ved bruk av en TIRF flyktig felt men på grunn av sin flate struktur kan avbildes ved hjelp av standard 2D-SIM med ubetydelig ut-av-fokus bakgrunn. I tillegg til bruken av forbedrede optiske snitterekonstruksjonsalgoritmer undertrykke ut-av-fokus lys utvide bruken av 2D-SIM til optisk tykke prøver, enskjønt der aksial oppløsning dobling er ikke nødvendig 21.
I MSIM blir prøven opplyst av en sparsom gitter av eksitasjon foci 36. Dette modalitet kan implementeres ved å fjerne den romlige maske (SM) Og erstatte det med et polarisasjonsfilter. SLM fungerer nå som en amplitude modulator. De binære SIM-gitter som vises på SLM kan erstattes av en 2D gitter av flekker, med størrelsen av flekkene valgt å være lik størrelsen av en diffraksjon begrenset fokus i bildeplanet. I figur 7A er et gitter på 4 x 4 bildeelement kvadrater vist på SLM (innfelt) som når demagnified på prøven genererer diffraksjon begrenset foci av 150 x 150 nm, gitt den fysiske SLM pikselstørrelse på 13,62 um. Eksitasjon foci kan så oversettes ved å forskyve den gittermønsteret på SLM og dette gjentas flere ganger for å belyse hele synsfeltet. Bildene er kjøpt for hvert oversatt mønster posisjon og stack er post-behandlet for å gi et rekonstruert bilde med forbedret oppløsning på opptil en faktor på 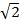 og redusert ut av fokus lys sammenlignet med tilsvarende vidfelt bilde30. Dette modalitet kan være nyttig for avbildning tykke, tette prøver som standard SIM er uegnet, for eksempel lav kontrast strukturer som farget røde blodceller (figur 7C), selv om oppkjøpet tid er økt på grunn av det store antallet av rå rammer kreves per synsfelt (i dette tilfellet N = 168).
og redusert ut av fokus lys sammenlignet med tilsvarende vidfelt bilde30. Dette modalitet kan være nyttig for avbildning tykke, tette prøver som standard SIM er uegnet, for eksempel lav kontrast strukturer som farget røde blodceller (figur 7C), selv om oppkjøpet tid er økt på grunn av det store antallet av rå rammer kreves per synsfelt (i dette tilfellet N = 168).
Endelig kan oppsettet endres for å muliggjøre enten høy NA lineær TIRF-SIM eller mønstret aktivering ikke-lineær SIM (PA NL-SIM), som presenterte nylig av Li et al., Ved bruk av en ultrahøy 1,7 NA objektiv eller tillegg av en 405 nm fotoaktivering laser og forsiktig optimalisering av SLM gittermønster 35.
fremtidige Applications
SIM er fortsatt en rask utvikling teknikk og mange applikasjoner i biovitenskap vil bli aktivert i fremtiden. Hastigheten, oppløsning og kontrast forbedringer av teknikk og evnen til å bruke standard fluoroforer mean for det Bioimaging blir SIM satt til å erstatte konvensjonelle mange mikroskop systemer, for eksempel konfokale og brede feltplattformer. Kommersielle SIM-systemer er allerede tilgjengelig i dag med fremragende tekniske spesifikasjoner, men de er utenfor den økonomiske rekkevidden av mange forskningslaboratorier, og, viktigst, de er fleksible til å bli endret og utviklet for å implementere den nyeste forskningen utviklingen på feltet. De mangler også viktig evne til å "være tilrettelagt for forsøket på hånden", ofte en kritisk flaskehals i cutting edge life science forskning. Systemet er beskrevet her vil være spesielt godt egnet til å studere dynamiske prosesser nær celleoverflaten, for in vitro studier av rekonstituert bilags systemer, for å studere overflatekjemi i materialer og naturvitenskap, f.eks. 2D materialer, og mange andre programmer.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet med tilskudd fra Leverhulme Trust, Engineering og Fysisk Sciences Research Council [EP / H018301 / 1, EP / G037221 / 1]; Alzheimer Research UK [Aruk-EG2012A-1]; Wellcome Trust [089703 / Z / 09 / Z] og Medical Research Council [MR / K015850 / 1, MR / K02292X / 1]. Vi takker E. Avezov og M. Lu for transfeksjon av LifeAct-GFP og cytosolic-GFP celler henholdsvis, og W. Chen for utarbeidelse av HEK293 kultur. Vi takker også K. O'Holleran for å få hjelp med utformingen av mikroskop, og L. Shao og R. Heintzmann for nyttige diskusjoner og forslag.
Materials
| 488 nm laser | Toptica | iBeam SMART | with digital modulation |
| 561 nm laser | Coherent | OBIS LS | with digital modulation |
| 640 nm laser | Cobolt | MLD | with digital modulation |
| Long-pass dichroic mirrors | Thorlabs | for combining excitation beams | |
| Quad band dichroic mirror | Chroma | ZT405/488/561/640rpc | 3 mm thick, TIRF imaging flat, mounted in Olympus BX filter cube |
| Quad band dichroic mirror | Chroma | ZT405/488/561/640rpc | From same batch as above, 25 x 25 mm |
| 1" square kinematic mount | Edmund Optics | 58-860 | |
| Glan-Taylor calcite polarizers | Thorlabs | GT5-A | For alignment of LCVR |
| Glan-Taylor mount | Thorlabs | SM05PM5 | |
| Achromatic half wave plate | Thorlabs | AHWP05M-600 | 400 – 800 nm |
| Rotation cage mount | Thorlabs | CRM1/M | For HWP |
| Liquid Crystal Variable Retarder | Meadowlark Optics | SWIFT | Custom built to provide full wave retardance over the range 488 to 640 nm. |
| LCVR controller | Meadowlark Optics | D3060HV | Two channel high voltage controller for liquid crystal retarders |
| Achromatic quarter wave plate | Meadowlark Optics | AQM-100-0545 | |
| Rotation cage mount | Thorlabs | CRM1P/M | For QWP |
| 10 mm achromatic doublet | Thorlabs | AC080-010-A-ML | For beam expander |
| 200 mm achromatic doublet | Thorlabs | AC254-200-A-ML | For beam expander |
| Cage XY Translators | Thorlabs | CXY1 | |
| Ferroelectric spatial light modulator | Forth Dimension Displays | M0787-00249 | SXGA-3DM (IFF) Microdisplay Type M249, 1280 x 1024 pixels, with driver board |
| SLM mounting frame | Forth Dimension Displays | M0787-10014 | Fixed to custom built aluminium mount |
| Ø50.8 mm Gimbal Mirror Mount | Thorlabs | GM200/M | For SLM mounting |
| Two-Axis Linear Translation Stage with Rotating Platform | Thorlabs | XYR1/M | For SLM mounting |
| Rail carrier | Newport | M-PRC-3 | For SLM mounting |
| Precision Optical Rail | Newport | PRL-6 | For SLM mounting |
| 300 mm achromatic doublet lens | Qioptiq | G322 273 322 | f = 300 mm, 31.5 mm diameter |
| 140 mm achromatic doublet lens | Qioptiq | G322 239 322 | f = 140 mm, 31.5 mm diameter |
| Precision XY Translation Mounts | Thorlabs | LM2XY | |
| Lens Mounting Adapters | Thorlabs | SM2AD32 | For mounting 31.5 mm lenses in 2" mounts |
| Translation stages | Comar | 12XT65 | Dovetail, side drive |
| XY Translator with Differential Drives | Thorlabs | ST1XY-D/M | for spatial filter |
| Rotation cage mount | Thorlabs | CRM1/M | for spatial filter |
| 300 mm achromatic doublet | Thorlabs | AC508-300-A-ML | Excitation tube lens |
| Automated XY stage with Z-piezo top plate | ASI | PZ-2150-XYFT-PZ-IX71 | with MS-2000 controller |
| Inverted microscope frame | Olympus | IX-71 | |
| Objective lens | Olympus | UAPON100XOTIRF | 100X/1.49NA |
| High speed filter wheel | Prior Scientific | HF110A | with Prior ProScan III controller |
| Bandpass emission filters | Semrock | FF01-525/30, FF01-676/29 | |
| sCMOS camera | Hamamatsu | ORCA Flash v4.0 | |
| Stage top incubator | OKO Lab | H301-K-FRAME | For live cell imaging, with Bold Line temperature and CO2 controllers |
| Stainless steel optical posts | Thorlabs | TR series | for mounting optical components |
| Post holders | Thorlabs | PH series | for mounting optical components |
| Kinematic mirror mounts | Thorlabs | KM100 | for mounting 1" mirrors |
| Shearing interferometer | Thorlabs | SI100 | |
| 100 nm fluorescent microspheres | Life Technologies | T-7279 | Tetraspeck |
| Rhodamine 6G | Sigma Aldrich | 83697-250MG | |
| 8 well glass bottom dishes | ibidi | 80827 | with #1.5 coverglass |
| Nunc Lab-Tek II Chambered Coverglass | Thermo Fisher Scientific | 155409 | with #1.5 coverglass |
| 0.01mm microscope reticle slide | EMS | 68039-22 | |
| CellLight Tubulin-GFP, BacMam 2.0 | Thermo Fisher Scientific | C10613 |
References
- Heintzmann, R., Cremer, C. G. Laterally modulated excitation microscopy: improvement of resolution by using a diffraction grating. BiOS Eur. 3568, 185-196 (1999).
- Gustafsson, M. G. L. Surpassing the lateral resolution limit by a factor of two using structured illumination microscopy. J. Microsc. 198 (2), 82-87 (2000).
- Shim, S. H., et al. Super-resolution fluorescence imaging of organelles in live cells with photoswitchable membrane probes. Proc. Natl. Acad. Sci. U. S. A. 109 (35), 13978-13983 (2012).
- Urban, N. T., Willig, K. I., Hell, S. W., Nägerl, U. V. STED Nanoscopy of Actin Dynamics in Synapses Deep Inside Living Brain Slices. Biophys. J. 101 (5), 1277-1284 (2011).
- Liu, Z., Lavis, L. D., Betzig, E. Imaging Live-Cell Dynamics and Structure at the Single-Molecule Level. Mol. Cell. 58 (4), 644-659 (2015).
- Westphal, V., et al. Video-Rate Far-Field Optical Nanoscopy Dissects Synaptic Vesicle Movement. Science. 320 (5873), 246-249 (2008).
- Davies, T., et al. CYK4 Promotes Antiparallel Microtubule Bundling by Optimizing MKLP1 Neck Conformation. PLOS Biol. 13 (4), e1002121 (2015).
- Laine, R. F., et al. Structural analysis of herpes simplex virus by optical super-resolution imaging. Nat. Commun. 6, 5980 (2015).
- Pinotsi, D., et al. Direct observation of heterogeneous amyloid fibril growth kinetics via two-color super-resolution microscopy. Nano Lett. 14 (1), 339-345 (2014).
- Esbjörner, E. K., et al. Direct observations of amyloid β Self-assembly in live cells provide insights into differences in the kinetics of Aβ(1-40) and Aβ(1-42) aggregation. Chem. Biol. 21 (6), 732-742 (2014).
- Michel, C. H., et al. Extracellular monomeric tau protein is sufficient to initiate the spread of tau protein pathology. J. Biol. Chem. 289 (2), 956-967 (2014).
- Pinotsi, D., Kaminski Schierle, G. S., Kaminski, C. F. Optical Super-Resolution Imaging of β-Amyloid Aggregation In Vitro and In Vivo: Method and Techniques. Syst. Biol. Alzheimer’s Dis. SE – 6. 1303, 125-141 (2016).
- Axelrod, D. Cell-substrate contacts illuminated by total internal reflection fluorescence. J. Cell Biol. 89 (1), 141-145 (1981).
- Cragg, G. E., So, P. T. Lateral resolution enhancement with standing evanescent waves. Opt. Lett. 25 (1), 46-48 (2000).
- Chung, E., Kim, D., So, P. T. Extended resolution wide-field optical imaging: objective-launched standing-wave total internal reflection fluorescence microscopy. Opt. Lett. 31 (7), 945 (2006).
- Kner, P., Chhun, B. B., Griffis, E. R., Winoto, L., Gustafsson, M. G. L. Super-resolution video microscopy of live cells by structured illumination. Nat. Methods. 6 (5), 339-342 (2009).
- Fiolka, R., Shao, L., Rego, E. H., Davidson, M. W., Gustafsson, M. G. L. Time-lapse two-color 3D imaging of live cells with doubled resolution using structured illumination. Proc. Natl. Acad. Sci. U. S. A. 109 (14), 5311-5315 (2012).
- Brunstein, M., Wicker, K., Hérault, K., Heintzmann, R., Oheim, M. Full-field dual-color 100-nm super-resolution imaging reveals organization and dynamics of mitochondrial and ER networks. Opt. Express. 21 (22), 26162-26173 (2013).
- Förster, R., et al. Simple structured illumination microscope setup with high acquisition speed by using a spatial light modulator. Opt. Express. 22 (17), 20663 (2014).
- Lu-Walther, H. W., et al. fastSIM: a practical implementation of fast structured illumination microscopy. Methods Appl. Fluoresc. 3, 014001 (2015).
- Shaw, M., Zajiczek, L., O’Holleran, K. High speed structured illumination microscopy in optically thick samples. Methods. , (2015).
- von Olshausen, P. . Total internal reflection microscopy: super-resolution imaging of bacterial dynamics and dark field imaging. , (2012).
- Gustafsson, M. G. L., et al. Three-dimensional resolution doubling in wide-field fluorescence microscopy by structured illumination. Biophys. J. 94 (12), 4957-4970 (2008).
- Meadowlark Optics Inc. . Basic Polarization Techniques and Devices. , (2005).
- O’Holleran, K., Shaw, M. Polarization effects on contrast in structured illumination microscopy. Opt. Lett. 37 (22), 4603 (2012).
- Brankner, S. Z., Hobson, M. . Synchronization and Triggering with the ORCA-Flash4.0 Scientific CMOS Camera. , (2013).
- Gustafsson, M. G. L., et al. Three-dimensional resolution doubling in wide-field fluorescence microscopy by structured illumination. Biophys. J. 94 (12), 4957-4970 (2008).
- Wicker, K. Non-iterative determination of pattern phase in structured illumination microscopy using auto-correlations in Fourier space. Opt. Express. 21 (21), 24692 (2013).
- Boulanger, J., Pustelnik, N., Condat, L. Non-smooth convex optimization for an efficient reconstruction in structured illumination microscopy. 2014 IEEE 11th Int. Symp. Biomed. Imaging. 3 (1), 995-998 (2014).
- Ströhl, F., Kaminski, C. F. A joint Richardson-Lucy deconvolution algorithm for the reconstruction of multifocal structured illumination microscopy data. Methods Appl. Fluoresc. 3 (1), 014002 (2015).
- Mudry, E., et al. Structured illumination microscopy using unknown speckle patterns. Nat. Photonics. 6 (5), 312-315 (2012).
- Ayuk, R., et al. Structured illumination fluorescence microscopy with distorted excitations using a filtered blind-SIM algorithm. Opt. Lett. 38 (22), 4723 (2013).
- Ball, G., et al. SIMcheck: a Toolbox for Successful Super-resolution Structured Illumination Microscopy. Sci. Rep. 5, 15915 (2015).
- York, A. G., et al. Resolution doubling in live, multicellular organisms via multifocal structured illumination microscopy. Nat. Methods. 9 (7), 749-754 (2012).
- Li, D., et al. Extended-resolution structured illumination imaging of endocytic and cytoskeletal dynamics. Science. 349 (6251), (2015).
- York, A. G., et al. Resolution doubling in live, multicellular organisms via multifocal structured illumination microscopy. Nat. Methods. 9 (7), 749-754 (2012).

