En guide till strukturerad belysning TIRF Mikroskopi Höghastighets med flera färger
Summary
This article provides an in depth guide for the assembly and operation of a structured illumination microscope operating with total internal reflection fluorescence illumination (TIRF-SIM) to image dynamic biological processes with optical super-resolution in multiple colors.
Abstract
Optisk superupplösning med strukturerad belysning mikroskopi (SIM) är en nyckelteknik för visualisering av processer på molekylär nivå i den kemiska och biomedicinska vetenskaperna. Även kommersiella SIM system finns tillgängliga, system som är specialanpassade utformade i laboratoriet kan överträffa kommersiella system, den senare typiskt utformad för enkel användning och allmänna tillämpningar, både när det gäller bildbehandling trohet och hastighet. I denna artikel presenteras en fördjupad guide till att bygga ett SIM-system som använder total inre reflektion (TIR) belysning och kan avbildning upp till 10 Hz i tre färger och en upplösning nå 100 nm. På grund av kombinationen av SIM-kortet och TIRF ger systemet bättre bildkontrast än konkurrerande tekniker. För att uppnå dessa specifikationer är flera optiska element används för att möjliggöra automatiserad kontroll över polarisationstillståndet och rumsliga struktur belysnings ljus för alla tillgängliga excitation wavelengths. Fullständig information om genomförande och kontroll hårdvara ges för att uppnå synkronisering mellan excitationsljus mönster generation, våglängd, polarisation tillstånd, och kamerakontroll med betoning på att uppnå maximal förvärv bildhastighet. Ett steg-för-steg-protokoll för systemjustering och kalibrering presenteras och den uppnåeliga upplösningen förbättringen valideras ideal testproverna. Möjligheten för video-rate superupplösning demonstreras med levande celler.
Introduction
Under det senaste ett halvt decennium har super-upplösning mikroskopi mognat och flyttade från specialiserade optik labb i händerna på biolog. Kommersiella mikroskop finns lösningar för de tre huvudsakliga varianter för att uppnå optisk superupplösning: enda molekyl lokalisering mikroskopi (SMLM), stimulerade utarmning emissions mikroskopi (STED), och strukturerad belysning mikroskopi (SIM) 1,2. SMLM såsom photoactivated lokalisering mikroskopi (PALM) och stokastiska optisk rekonstruktion mikroskopi (STORM) har varit de mest populära tekniker, till stor del på grund av enkelheten i optiska setup och löftet om hög rumslig upplösning, lätt ner till 20 nm. Emellertid super-resolution mikroskopi via enda molekyl lokalisering kommer med en inneboende kompromiss: den rumsliga upplösningen som kan uppnås är beroende av att ackumulera ett tillräckligt antal enskilda fluoroforenhetema lokaliseringar, därav begränsar den temporala upplösningen. Imaging dynamisk processes i levande celler blir därför problematiskt eftersom ett fullgott sätt prov rörelse strukturen av intresse för att förhindra rörelseartefakter samtidigt skaffa tillräckligt med lokaliserings händelser under den tiden för att rekonstruera en bild. För att möta dessa krav har levande cell SMLM demonstrationer erhållit erforderliga ökningen av fluoroforen photoswitching priser genom att kraftigt öka excitation makt, och detta leder i sin tur till fototoxicitet och oxidativ stress, vilket begränsar provöverlevnadstider och biologisk relevans 3.
En klar fördel med STED över både SIM och SMLM är att det kan bilden med superupplösning i tjocka prover, t ex lateral upplösning på cirka 60 nm uppnåddes i organotypiska hjärnan skivor på djup upp till 120 ^ m 4. Imaging vid sådana djup med enda mål implementeringar av SMLM eller SIM är ogenomförbar, men blir möjligt med antingen enda molekyl ljus ark eller galler ljus ark microscopy 5. Video-rate STED har också påvisats och används för att kartlägga synaptiska vesikler rörlighet, men hittills har begränsats till avbildning små synfält 6.
För tillämpningar inom cellbiologi och självmonterings reaktioner molekylär 7 – 12 som kräver avbildning med hög tidsupplösning under många tidpunkter, strukturerad belysning mikroskopi (SIM) kan vara väl lämpad eftersom det inte är beroende av fotofysikaliska egenskaperna hos en viss fluorescerande sond. Trots denna fördel för SIM, fram till nu dess användning har i huvudsak begränsad till avbildning fixerade celler eller långsamma processer. Detta är på grund av begränsningar i kommersiellt tillgängliga SIM-system: förvärv bildfrekvens på dessa instrument har begränsats av rotationshastigheten hos de gitter används för att generera de erforderliga sinusbelysningsmönster samt polarisationsbevarande optik. Den senaste generationen av kommersiell SIMinstrument klarar av snabb avbildning, men de är oöverkomligt dyrt att alla utom centrala avbildningsmöjligheter.
Detta protokoll presenteras en guide till konstruktionen av ett flexibelt SIM-system för avbildning av snabba processer i tunna prover och nära den basala ytan av levande celler. Den sysselsätter total inre reflektion fluorescens (TIRF) för att generera en belysningsmönster som tränger djupare än ca 150 nm i provet 13 som avsevärt minskar ofokuserad bakgrundssignal. Idén att kombinera SIM med TIRF är nästan lika gammal som SIM sig 14 men inte insett experimentellt före 2006 15. Den första in vivo bilder som erhållits med TIRF-SIM rapporterades under 2009 16 uppnå frame rates på 11 Hz att visualisera tubulin och kinesin dynamik, och två färg TIRF-SIM-system har presenterats 17,18. Senast, en guide för konstruktion och användning av en enda färg två-beam SIM sYSTEM presenterades med bildhastigheter på upp till 18 Hz 19,20.
Upplägget presenteras här är i stånd att SIM superupplösning på 20 Hz i tre färger, varav två kan drivas i TIRF-SIM. Hela systemet är uppbyggt runt ett inverterat mikroskop ram och använder sig av en motordriven xy translationssteg med en piezo-manövrerad z skede. Att generera sinusexciteringsmönster som krävs för TIRF-SIM, systemet presenterades använder en ferroelektrisk (Spatial Light Modulator SLM). Binära gittermönster visas på SLM och de resulterande ± 1 diffraktionsordningar filtreras, förmedlas och fokuseras i TIR ring objektiv. De nödvändiga fasförskjutningar och rotationer av gitter tillämpas genom att ändra den visade SLM bilden. Detta protokoll beskriver hur man bygger och rikta en sådan exciteringsbana, detaljer anpassningen av banan utsläpp, och presenterar testprov för att säkerställa optimal inriktning. Det från också beskrivs hur de frågor och utmaningar som är speciella för hög hastighet TIRF-SIM om polarisering kontroll och synkronisering av komponenter.
Design Överväganden och begränsningar
Innan du monterar TIRF-SIM-systemet som presenteras i detta protokoll, det finns flera konstruktionskrav att överväga som avgör valet av optiska komponenter. Alla förkortningar av optiska komponenter se figur 1.
Spatial Light Modulator (SLM)
En binär ferroelektrisk SLM används i denna installation eftersom den kan under millisekund mönster växling. Gråskala nematisk SLM kan användas, men dessa erbjuder kraftigt reducerad kopplingstider. Vardera på eller av bildpunkt i en binär fas SLM förlänar antingen en π eller 0 fasförskjutning till den infallande plan vågfront, därför om ett periodiskt gitter mönster visas på SLM den kommer att fungera som en fas diffraktionsgitter.
ent "> total intern reflektion (TIR) För att uppnå TIR och producera ett evanescent fält, måste infallsvinkeln av exciterings- strålarna vid glas-prov gränsyta att vara större än den kritiska vinkeln 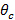 . Detta ställer den minsta infallsvinkeln som krävs, och därmed även den maximala avstånd, eller tid, av den flyktiga belysningsmönster. Den maximala infallsvinkel
. Detta ställer den minsta infallsvinkeln som krävs, och därmed även den maximala avstånd, eller tid, av den flyktiga belysningsmönster. Den maximala infallsvinkel 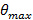 (Acceptansvinkeln) begränsas av den numeriska aperturen (NA) hos objektivlinsen som kan beräknas från definitionen
(Acceptansvinkeln) begränsas av den numeriska aperturen (NA) hos objektivlinsen som kan beräknas från definitionen 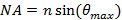 . Detta bestämmer minimi mönstret avstånd uppnås enligt Abbe formel
. Detta bestämmer minimi mönstret avstånd uppnås enligt Abbe formel 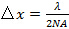 som förbinder NA och våglängd
som förbinder NA och våglängd 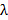 till ett minimum mönsteravståndet <imgalt = "Ekvation" src = "/ filer / ftp_upload / 53988 / 53988eq6.jpg" />. I praktiken ger en 1,49 NA oljeimmersion TIRF mål en maximal infallsvinkel på ca 79 ° och minst mönster period på provet av 164 nm med användning av en excitationsvåglängd av 488 nm. Dessa två vinklar definierar en ring på baksidan öppning mål under vilken instrumentet uppnår TIR belysning (dvs. TIR ring) och i vilken de två exciterings fokus måste placeras exakt och precist roteras för att generera varje belysningsmönster.
till ett minimum mönsteravståndet <imgalt = "Ekvation" src = "/ filer / ftp_upload / 53988 / 53988eq6.jpg" />. I praktiken ger en 1,49 NA oljeimmersion TIRF mål en maximal infallsvinkel på ca 79 ° och minst mönster period på provet av 164 nm med användning av en excitationsvåglängd av 488 nm. Dessa två vinklar definierar en ring på baksidan öppning mål under vilken instrumentet uppnår TIR belysning (dvs. TIR ring) och i vilken de två exciterings fokus måste placeras exakt och precist roteras för att generera varje belysningsmönster.
Rekonstruktion av TIRF-SIM bilder kräver förvärv av minst tre fas skift per mönster rotation därför SLM mönster perioden måste vara delbart med tre (se figur 1). Till exempel kan en period av 9 bildpunkter för 488 nm-belysning och 12 pixlar för 640 nm-belysning. För en omfattande diskussion om SLM mönsterdesign, inklusive delpixel optimering av mönsteravstånd använder klippta galler, Se tidigare arbete Kner et al. 16 och Lu-Walther et al. 20 Placeringen av de två exciterings fokus måste vara inne i TIR ring för alla våglängder, men diffraktionsvinkeln av ± 1 order från SLM är våglängden beroende. För standard SIM, kan flerfärgsbildalstring uppnås genom optimering av gitterperioden för den längsta våglängden, och tolerera en förlust i prestanda för de kortare kanaler. För TIRF-SIM dock optimera för en våglängd betyder att den andra våglängden fokus är inte längre inom TIR ringen. Exempelvis med användning av ett gitter period av 9 bildpunkter är tillräcklig för att ge TIRF för 488 nm, enligt de foci är vid 95% av diametern hos den bakre öppningen och inom TIR ringen, men för 640 nm denna period skulle positionera foci utanför öppningen. Av denna anledning olika pixelmönster mellanrum måste användas för varje exciteringsvåglängd.
Anpassningen av TIRF-SIM excitationsvägenär extremt känslig för små förändringar i positionen för den dikroiska spegeln (DM4 i figur 1) i mikroskopkroppen, mycket mer så än i konventionell SIM. rekommenderas inte användning av en roterande filter kub torn, istället använda en enda flerbands dikroisk spegel, som hålls i ett fast läge och utformats speciellt för exciteringsvåglängder som används. Det är viktigt att endast de högsta kvalitet dikroiska speglar används. Dessa kräver tjocka substrat av minst 3 mm, och ofta betecknas som "imaging platta" av tillverkarna. Alla andra substrat leder till oacceptabla avvikelser och bildförsämring i TIRF-SIM.
polarisationsstyrning
Att uppnå TIRF-SIM är det väsentligt att rotera polarisationstillståndet hos excitationsljuset i synchronicity med belysningsmönstret på sådant sätt att det förblir azimutalt polariserat i den objektiva pupillplanet med avseende på den optiska axeln (dvs.. s-polariserade). Inriktning av polariseringsstyr optik kommer att bero på den specifika optiska elementet användas, t ex en Pockels-cell 21, eller en halv våg plattan i en motordriven rotationssteget 22. I detta protokoll en anpassad flytande kristaller variabel retarder (LCVR) används, utformad för att ge full-wave (2π) hämmande över våglängdsområdet 488-640 nm, eftersom det möjliggör snabb (~ ms) växling. Om man använder en flytande kristall retarder är det väsentligt att använda en hög kvalitet komponent: standardkomponenter är vanligtvis inte tillräckligt stabila för att ge en konstant hämmande förmåga över längden av kamerans exponeringstid som leder till en suddig ut ur belysningsmönstret och låg moduleringskontrast . Flytande kristallretar är också starkt temperaturberoende och kräver inbyggd temperaturkontroll.
Synkronisering
Lasrarna måste synkroniseras med SLM. Binära ferroelektriska SLM internt viktad switching mellan ett på-tillstånd och fråntillstånd. Pixlarna bara fungera som en halv våg plattor i antingen deras på eller av staten, men inte under interomkopplingstiden. Därför bör stängas lasrarna endast under on / off stater via LED aktiveringssignalen från SLM för att förhindra en minskning av mönster kontrast till följd av mellanliggande tillstånd av pixlarna. En akusto-optisk modulator (AOM) skulle alternativt kunna användas som en snabb slutare om lasrarna inte kan digitalt modulerad.
Val av linser
Baserat på dessa begränsningar, till önskad förstoringsreduktion av SLM planet på preparatplanet ge de önskade belysningsmönster kan fastställas. Detta medger beräkning av de brännvidder på de två linserna L3 och L4 i bildrelä teleskopet och excitation kondensorlins L5. I detta system en 100X / 1.49NA oljeimmersionsobjektiv används med 488 nm och 640 nm excitation, använder därmed brännvidder på 300 och 140 mmför L4 och L3, och 300 mm för L5, vilket ger en total förstoringsreduktion av 357X, vilket motsvarar en SLM pixelstorlek på 38 nm vid preparatplanet. Med användning av denna kombination av linser, SLM gitterperioder 9 för 488 nm-belysning och 12 bildpunkter för 640 nm ger mönsteravstånd på 172 och 229 nm vid provet, motsvarande infallsvinklar av 70 ° och 67 ° respektive. För ett glas vatten gränssnitt, är den kritiska vinkeln 61 °, och är oberoende av våglängd, därför dessa två mönster avstånd tillåter TIRF excitation för båda våglängderna. En objektivlins utrustad med en korrekturring är användbar för korrigering av sfärisk aberration som införs genom variationer i täckglas tjocklek, eller om drift vid 37 ° C.
bildrekonstruktion
En gång har förvärvats rå SIM data är det en fråga om beräknings ansträngning för att generera superupplösta bilder i en två-stegsprocess. För det första har belysningsmönstret som skall fastställas förvarje bild och för det andra måste komponenterna i SIM-spektrum separeras och rekombineras på lämpligt sätt så att fördubbla den effektiva OTF stöd (se figur 6, infällningar).
Exakt kunskap om de planerade belysningsmönster är av största vikt, eftersom de superupplösta frekvenskomponenter måste vara oblandad så exakt som möjligt för att förhindra artefakter som orsakas av kvarvarande delar av överlappande komponenter. Vi bestämmer belysningsmönsterparametrar i efterhand från råbilddata enligt det förfarande som införts av et al. Gustafsson 23 Kort sagt, en uppsättning belysningsparametrar som beskriver en normaliserad tvådimensionell sinus har hittas för var och en av 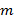 exciteringsmönster
exciteringsmönster 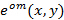 :
:
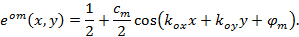
Härmed 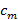 och
och 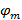 beskriver frans kontrast och mönstret inledningsfasen av varje enskild bild m respektive. Komponenterna hos vågvektorn,
beskriver frans kontrast och mönstret inledningsfasen av varje enskild bild m respektive. Komponenterna hos vågvektorn, 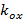 och
och 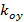 Endast förändras med olika inriktningar
Endast förändras med olika inriktningar 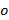 av mönstret och kan antas vara annars konstant. Att grovt bestämma komponenterna hos vågvektorn en korskorrelation av rå bildspektra utförs, som raffineras genom tillämpning av sub-pixel skift till en av de tvär korrelerade bilder för att optimera överlappningen. Detta sker via multiplikation av verkliga rymd fas gradienter
av mönstret och kan antas vara annars konstant. Att grovt bestämma komponenterna hos vågvektorn en korskorrelation av rå bildspektra utförs, som raffineras genom tillämpning av sub-pixel skift till en av de tvär korrelerade bilder för att optimera överlappningen. Detta sker via multiplikation av verkliga rymd fas gradienter 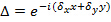 att inducera en subpixel förskjutning i frekvens-utrymme. Observera att det är bra att ha en god uppskattning av våg-vektorerna innan själva mönstret uppskattningen och detta kan hittas genom att avbilda en fluorescerande pärla skikt.
att inducera en subpixel förskjutning i frekvens-utrymme. Observera att det är bra att ha en god uppskattning av våg-vektorerna innan själva mönstret uppskattningen och detta kan hittas genom att avbilda en fluorescerande pärla skikt.
Eftersom fas steg mellan skiftade mönster är 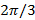 , Ie.
, Ie. 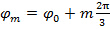 , Separation av frekvenskomponenter kan utföras av en Fourier-trans längs "fas axel". Den globala fas
, Separation av frekvenskomponenter kan utföras av en Fourier-trans längs "fas axel". Den globala fas 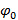 och frans kontrast
och frans kontrast 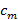 kan sedan bestämmas med användning av komplex linjär regression av olika komponenter. De individuella separerade komponenterna kombineras sedan med användning av en generaliserad Wiener-filter. För en detaljerad beskrivning av både parameter utvinning och genomförande av den generaliserade Wiener filter vi hänvisar läsaren till Gustafssonet al. 23 där samma algoritm används.
kan sedan bestämmas med användning av komplex linjär regression av olika komponenter. De individuella separerade komponenterna kombineras sedan med användning av en generaliserad Wiener-filter. För en detaljerad beskrivning av både parameter utvinning och genomförande av den generaliserade Wiener filter vi hänvisar läsaren till Gustafssonet al. 23 där samma algoritm används.
Protocol
Representative Results
Discussion
Skräddarsydda TIRF-SIM system såsom installationen beskrivs i detta protokoll är kapabla att flerfärgad superupplösning med hög hastighet jämfört med kommersiellt tillgängliga mikroskop. Den inneboende fördelen med SIM som en super-resolution tekniken är att den temporala upplösningen inte är begränsad av de fotofysik av fluoroforen, jämfört med andra metoder, såsom enda molekyl lokalisering mikroskopi (SMLM) eller punktscanningsmetoder såsom stimulerad utarmning utsläpps mikroskopi ( STED). Till skillnad från dessa andra tekniker, inte SIM inte kräva photoswitchable eller tömmas fluoroforer så flerfärgsbildalstring är okomplicerad. Icke TIRF-SIM-system, till exempel optisk sektione SIM och multifokal SIM kan oftast uppnå upplösning förbättringar av 1,7 gånger eller mindre i praktiken i motsats till faktor förbättring 2 redovisas här, och kommersiella system är också ofta långsammare och mindre flexibelt än systemet presenteras i detta protokoll.
"> De två största svårigheterna vid genomförandet av denna teknik är för det första att det är nödvändigt för exakt positionering av de sex SIM balkar inom TIR zonen av målet rygg öppning, vilket kräver en mödosam och tidskrävande optisk inriktning förfarandet. För det andra, för att producera hög mönster kontrast på provet, är polariseringsrotations viktigt. för låga NA 2D-SIM-system, kan polariseringsrotation undvikas genom noggrant val av linjär polarisation orientering, men det blir omöjligt för TIRF-SIM 25. för hög hastighet flerfärgsbildalstring, elektro- optisk polarisering kontroll är nödvändig och detta ökar komplexiteten och kostnaden för systemet.Begränsningar av tekniken
TIRF-SIM, som konventionell TIRF, är naturligtvis begränsad till observation av biologiska strukturer och processer som ligger på den basala cellmembranet som kan belysas av 150-200 nm penetration av försvinnande fält. MedanSIM citeras ofta som mindre photodamaging till celler än antingen STED eller SMLM, inte i sidled fördubbling upplösning fortfarande öka erforderligt antal fotoner med åtminstone fyra gånger fem jämfört med konventionell TIRF mikroskopi. För avbildning med hög bildfrekvens med korta exponeringar gånger, kräver detta foton ökning användning av ökade belysningsnivåer. Även om alla fluorofor kan användas för SIM avbildning av fasta eller långsamma prover, hög ljusstyrka fluorescerande proteiner eller nästa generations syntetiska färgämnen med förbättrad fotostabilitet rekommenderas för levande cell imaging.
Även om detta genomförande är i stånd att avbilda en enda färg på SIM-frame rates på över 20 Hz, är flerfärgsbildalstring i den presenterade systemet begränsas av omkopplingstiden för motordrivna emissionsfilterhjulet. På grund av den stora storleken på sCMOS kamerachip, skulle användningen av ett flerbandsemissionsfilter och bild skärare optik vara möjligt och medge samtidig jagmaging med multipla våglängder på någon hastighet straff. En annan möjlighet skulle vara att alternera de olika exciterings lasrar och använda en flerbands notchfilter för att avvisa exciteringsljuset. Användning av en binär ferroelektrisk SLM i denna implementering är inte heller optimal. Diffraktionsverkningsgraden av en sådan SLM är mycket låg, så de flesta av det infallande ljuset är i det nollte ordningens reflektion, som filtreras ut genom den rumsliga mask. För applikationer som kräver mycket hög bildhastighet, är utskriftshastighet begränsas därför av uteffekten av laserdioder. SLM introducerar också en del ellipticitet i polarisationen för våglängder bort från 550 nm designen våglängd där pixlarna inte fungerar som ideala halv våg plattor. Även om detta skulle kunna kompenseras med en extra LCVR kan den idealiska lösningen vara att använda en digital mikrospegelanordning (DMD) som en mönstergenerator.
möjliga ändringar
Inställnings presented här är flexibel och lättare modifieras än kommersiella instrument så att andra avbildningsmetoder såsom 3D-SIM, snabb 2D-SIM, multifokal SIM (MSIM) och icke-linjär SIM (NL-SIM) kan genomföras 21,34,35.
2D-SIM kan vara väl lämpad för avbildning relativt platt, snabbrörliga strukturer som den perifera endoplasmatiska nätverket. Den perifera ER ligger djupare i cellen än vad som kan belysas med hjälp av en TIRF försvinnande fält men på grund av sin platta struktur kan avbildas med standard 2D-SIM med försumbar out-of-fokus bakgrund. Dessutom, användningen av förbättrade optiska sektionerekonstruktionsalgoritmer trycka out-of-fokus ljus utöka användningen av 2D-SIM optiskt tjocka prover, även om där axiell upplösning fördubbling krävs inte 21.
I MSIM provet belyses av en gles galler av excitation härdar 36. Denna modalitet kan genomföras genom att helt enkelt ta bort den rumsliga mask (SM) Och ersätta den med en polarisator. SLM fungerar nu som en amplitud-modulator. De binära SIM gitter som visas på SLM kan ersättas av en 2D-gitter av fläckar, med storleken av fläckarna som valts för att vara lika med storleken på en diffraktionsbegränsad fokus i bildplanet. I figur 7A är ett galler av 4 x 4 pixel rutor visas på SLM (infälld) som när förminskade på provet genererar diffraktionsbegränsad härdar av 150 x 150 nm, med tanke på den fysiska SLM pixelstorlek på 13,62 pm. Excitation fokus kan sedan översättas genom att flytta gallermönster på SLM och detta upprepas flera gånger för att belysa hela synfältet. Bilder förvärvas för varje översatt mönsterpositionen och stapeln är efterbehandlade för att ge en rekonstruerad bild med förbättrad upplösning på upp till en faktor av 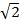 och minskad out-of-fokus ljus jämfört med motsvarande widefield bilden30. Denna modalitet kan vara användbara för avbildning av tjocka, täta prover för vilken standard SIM är olämpliga, till exempel låg kontrast strukturer såsom färgade röda blodkroppar (Figur 7C), även om förvärvstiden ökar på grund av det stora antalet rå ramar krävs per synfältet (i det här fallet N = 168).
och minskad out-of-fokus ljus jämfört med motsvarande widefield bilden30. Denna modalitet kan vara användbara för avbildning av tjocka, täta prover för vilken standard SIM är olämpliga, till exempel låg kontrast strukturer såsom färgade röda blodkroppar (Figur 7C), även om förvärvstiden ökar på grund av det stora antalet rå ramar krävs per synfältet (i det här fallet N = 168).
Slutligen kan installationen modifieras för att möjliggöra antingen hög-NA linjär TIRF-SIM eller mönstrade aktivering icke-linjär SIM (PA NL-SIM), som lades fram nyligen av Li et al., Genom användning av en ultra 1,7 NA mål eller tillägg av en 405 nm fotoaktivering laser och noggrann optimering av SLM gittermönster 35.
framtida tillämpningar
SIM är fortfarande en snabbt växande teknik och många tillämpningar inom livsvetenskaperna kommer att aktiveras i framtiden. Hastighet, upplösning och kontrast förbättringar av tekniken och förmåga att använda standard fluoroforer mean att för Bioimaging är SIM inställd på att ersätta konventionella många mikroskopsystem, såsom konfokala och breda fält plattformar. Kommersiella SIM-system finns redan idag med enastående tekniska specifikationer, men de är utanför den finansiella räckhåll för många forskningslaboratorier, och, framför allt, de är oflexibla att ändras och utvecklas för att genomföra de senaste forskningsutvecklingen inom området. De saknar också det väsentliga förmåga att "anpassas för försöket till hands", ofta en kritisk flaskhals i framkant biovetenskaplig forskning. Systemet som beskrivs här kommer att vara särskilt väl lämpad för att studera dynamiska processer nära cellytan, för in vitro-studier i ombildade tvåskiktsmembran system, för att studera ytkemin i materialen och fysik, t.ex.. av 2D material, och många andra tillämpningar.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Detta arbete har finansierats med bidrag från Leverhulme Trust, Engineering and Physical Sciences Research Council [EP / H018301 / 1, EP / G037221 / 1]; Alzheimers Research UK [Aruk-EG2012A-1]; Wellcome Trust [089.703 / Z / 09 / Z] och Medical Research Council [MR / K015850 / 1, MR / K02292X / 1]. Vi tackar E. Avezov och M. Lu för transfektion av LifeAct-GFP och cytosoliska-GFP celler respektive och W. Chen för beredning av HEK293 kultur. Vi tackar även K. O'Holleran för hjälp med utformningen av mikroskop, och L. Shao och R. Heintzmann för nyttiga diskussioner och förslag.
Materials
| 488 nm laser | Toptica | iBeam SMART | with digital modulation |
| 561 nm laser | Coherent | OBIS LS | with digital modulation |
| 640 nm laser | Cobolt | MLD | with digital modulation |
| Long-pass dichroic mirrors | Thorlabs | for combining excitation beams | |
| Quad band dichroic mirror | Chroma | ZT405/488/561/640rpc | 3 mm thick, TIRF imaging flat, mounted in Olympus BX filter cube |
| Quad band dichroic mirror | Chroma | ZT405/488/561/640rpc | From same batch as above, 25 x 25 mm |
| 1" square kinematic mount | Edmund Optics | 58-860 | |
| Glan-Taylor calcite polarizers | Thorlabs | GT5-A | For alignment of LCVR |
| Glan-Taylor mount | Thorlabs | SM05PM5 | |
| Achromatic half wave plate | Thorlabs | AHWP05M-600 | 400 – 800 nm |
| Rotation cage mount | Thorlabs | CRM1/M | For HWP |
| Liquid Crystal Variable Retarder | Meadowlark Optics | SWIFT | Custom built to provide full wave retardance over the range 488 to 640 nm. |
| LCVR controller | Meadowlark Optics | D3060HV | Two channel high voltage controller for liquid crystal retarders |
| Achromatic quarter wave plate | Meadowlark Optics | AQM-100-0545 | |
| Rotation cage mount | Thorlabs | CRM1P/M | For QWP |
| 10 mm achromatic doublet | Thorlabs | AC080-010-A-ML | For beam expander |
| 200 mm achromatic doublet | Thorlabs | AC254-200-A-ML | For beam expander |
| Cage XY Translators | Thorlabs | CXY1 | |
| Ferroelectric spatial light modulator | Forth Dimension Displays | M0787-00249 | SXGA-3DM (IFF) Microdisplay Type M249, 1280 x 1024 pixels, with driver board |
| SLM mounting frame | Forth Dimension Displays | M0787-10014 | Fixed to custom built aluminium mount |
| Ø50.8 mm Gimbal Mirror Mount | Thorlabs | GM200/M | For SLM mounting |
| Two-Axis Linear Translation Stage with Rotating Platform | Thorlabs | XYR1/M | For SLM mounting |
| Rail carrier | Newport | M-PRC-3 | For SLM mounting |
| Precision Optical Rail | Newport | PRL-6 | For SLM mounting |
| 300 mm achromatic doublet lens | Qioptiq | G322 273 322 | f = 300 mm, 31.5 mm diameter |
| 140 mm achromatic doublet lens | Qioptiq | G322 239 322 | f = 140 mm, 31.5 mm diameter |
| Precision XY Translation Mounts | Thorlabs | LM2XY | |
| Lens Mounting Adapters | Thorlabs | SM2AD32 | For mounting 31.5 mm lenses in 2" mounts |
| Translation stages | Comar | 12XT65 | Dovetail, side drive |
| XY Translator with Differential Drives | Thorlabs | ST1XY-D/M | for spatial filter |
| Rotation cage mount | Thorlabs | CRM1/M | for spatial filter |
| 300 mm achromatic doublet | Thorlabs | AC508-300-A-ML | Excitation tube lens |
| Automated XY stage with Z-piezo top plate | ASI | PZ-2150-XYFT-PZ-IX71 | with MS-2000 controller |
| Inverted microscope frame | Olympus | IX-71 | |
| Objective lens | Olympus | UAPON100XOTIRF | 100X/1.49NA |
| High speed filter wheel | Prior Scientific | HF110A | with Prior ProScan III controller |
| Bandpass emission filters | Semrock | FF01-525/30, FF01-676/29 | |
| sCMOS camera | Hamamatsu | ORCA Flash v4.0 | |
| Stage top incubator | OKO Lab | H301-K-FRAME | For live cell imaging, with Bold Line temperature and CO2 controllers |
| Stainless steel optical posts | Thorlabs | TR series | for mounting optical components |
| Post holders | Thorlabs | PH series | for mounting optical components |
| Kinematic mirror mounts | Thorlabs | KM100 | for mounting 1" mirrors |
| Shearing interferometer | Thorlabs | SI100 | |
| 100 nm fluorescent microspheres | Life Technologies | T-7279 | Tetraspeck |
| Rhodamine 6G | Sigma Aldrich | 83697-250MG | |
| 8 well glass bottom dishes | ibidi | 80827 | with #1.5 coverglass |
| Nunc Lab-Tek II Chambered Coverglass | Thermo Fisher Scientific | 155409 | with #1.5 coverglass |
| 0.01mm microscope reticle slide | EMS | 68039-22 | |
| CellLight Tubulin-GFP, BacMam 2.0 | Thermo Fisher Scientific | C10613 |
References
- Heintzmann, R., Cremer, C. G. Laterally modulated excitation microscopy: improvement of resolution by using a diffraction grating. BiOS Eur. 3568, 185-196 (1999).
- Gustafsson, M. G. L. Surpassing the lateral resolution limit by a factor of two using structured illumination microscopy. J. Microsc. 198 (2), 82-87 (2000).
- Shim, S. H., et al. Super-resolution fluorescence imaging of organelles in live cells with photoswitchable membrane probes. Proc. Natl. Acad. Sci. U. S. A. 109 (35), 13978-13983 (2012).
- Urban, N. T., Willig, K. I., Hell, S. W., Nägerl, U. V. STED Nanoscopy of Actin Dynamics in Synapses Deep Inside Living Brain Slices. Biophys. J. 101 (5), 1277-1284 (2011).
- Liu, Z., Lavis, L. D., Betzig, E. Imaging Live-Cell Dynamics and Structure at the Single-Molecule Level. Mol. Cell. 58 (4), 644-659 (2015).
- Westphal, V., et al. Video-Rate Far-Field Optical Nanoscopy Dissects Synaptic Vesicle Movement. Science. 320 (5873), 246-249 (2008).
- Davies, T., et al. CYK4 Promotes Antiparallel Microtubule Bundling by Optimizing MKLP1 Neck Conformation. PLOS Biol. 13 (4), e1002121 (2015).
- Laine, R. F., et al. Structural analysis of herpes simplex virus by optical super-resolution imaging. Nat. Commun. 6, 5980 (2015).
- Pinotsi, D., et al. Direct observation of heterogeneous amyloid fibril growth kinetics via two-color super-resolution microscopy. Nano Lett. 14 (1), 339-345 (2014).
- Esbjörner, E. K., et al. Direct observations of amyloid β Self-assembly in live cells provide insights into differences in the kinetics of Aβ(1-40) and Aβ(1-42) aggregation. Chem. Biol. 21 (6), 732-742 (2014).
- Michel, C. H., et al. Extracellular monomeric tau protein is sufficient to initiate the spread of tau protein pathology. J. Biol. Chem. 289 (2), 956-967 (2014).
- Pinotsi, D., Kaminski Schierle, G. S., Kaminski, C. F. Optical Super-Resolution Imaging of β-Amyloid Aggregation In Vitro and In Vivo: Method and Techniques. Syst. Biol. Alzheimer’s Dis. SE – 6. 1303, 125-141 (2016).
- Axelrod, D. Cell-substrate contacts illuminated by total internal reflection fluorescence. J. Cell Biol. 89 (1), 141-145 (1981).
- Cragg, G. E., So, P. T. Lateral resolution enhancement with standing evanescent waves. Opt. Lett. 25 (1), 46-48 (2000).
- Chung, E., Kim, D., So, P. T. Extended resolution wide-field optical imaging: objective-launched standing-wave total internal reflection fluorescence microscopy. Opt. Lett. 31 (7), 945 (2006).
- Kner, P., Chhun, B. B., Griffis, E. R., Winoto, L., Gustafsson, M. G. L. Super-resolution video microscopy of live cells by structured illumination. Nat. Methods. 6 (5), 339-342 (2009).
- Fiolka, R., Shao, L., Rego, E. H., Davidson, M. W., Gustafsson, M. G. L. Time-lapse two-color 3D imaging of live cells with doubled resolution using structured illumination. Proc. Natl. Acad. Sci. U. S. A. 109 (14), 5311-5315 (2012).
- Brunstein, M., Wicker, K., Hérault, K., Heintzmann, R., Oheim, M. Full-field dual-color 100-nm super-resolution imaging reveals organization and dynamics of mitochondrial and ER networks. Opt. Express. 21 (22), 26162-26173 (2013).
- Förster, R., et al. Simple structured illumination microscope setup with high acquisition speed by using a spatial light modulator. Opt. Express. 22 (17), 20663 (2014).
- Lu-Walther, H. W., et al. fastSIM: a practical implementation of fast structured illumination microscopy. Methods Appl. Fluoresc. 3, 014001 (2015).
- Shaw, M., Zajiczek, L., O’Holleran, K. High speed structured illumination microscopy in optically thick samples. Methods. , (2015).
- von Olshausen, P. . Total internal reflection microscopy: super-resolution imaging of bacterial dynamics and dark field imaging. , (2012).
- Gustafsson, M. G. L., et al. Three-dimensional resolution doubling in wide-field fluorescence microscopy by structured illumination. Biophys. J. 94 (12), 4957-4970 (2008).
- Meadowlark Optics Inc. . Basic Polarization Techniques and Devices. , (2005).
- O’Holleran, K., Shaw, M. Polarization effects on contrast in structured illumination microscopy. Opt. Lett. 37 (22), 4603 (2012).
- Brankner, S. Z., Hobson, M. . Synchronization and Triggering with the ORCA-Flash4.0 Scientific CMOS Camera. , (2013).
- Gustafsson, M. G. L., et al. Three-dimensional resolution doubling in wide-field fluorescence microscopy by structured illumination. Biophys. J. 94 (12), 4957-4970 (2008).
- Wicker, K. Non-iterative determination of pattern phase in structured illumination microscopy using auto-correlations in Fourier space. Opt. Express. 21 (21), 24692 (2013).
- Boulanger, J., Pustelnik, N., Condat, L. Non-smooth convex optimization for an efficient reconstruction in structured illumination microscopy. 2014 IEEE 11th Int. Symp. Biomed. Imaging. 3 (1), 995-998 (2014).
- Ströhl, F., Kaminski, C. F. A joint Richardson-Lucy deconvolution algorithm for the reconstruction of multifocal structured illumination microscopy data. Methods Appl. Fluoresc. 3 (1), 014002 (2015).
- Mudry, E., et al. Structured illumination microscopy using unknown speckle patterns. Nat. Photonics. 6 (5), 312-315 (2012).
- Ayuk, R., et al. Structured illumination fluorescence microscopy with distorted excitations using a filtered blind-SIM algorithm. Opt. Lett. 38 (22), 4723 (2013).
- Ball, G., et al. SIMcheck: a Toolbox for Successful Super-resolution Structured Illumination Microscopy. Sci. Rep. 5, 15915 (2015).
- York, A. G., et al. Resolution doubling in live, multicellular organisms via multifocal structured illumination microscopy. Nat. Methods. 9 (7), 749-754 (2012).
- Li, D., et al. Extended-resolution structured illumination imaging of endocytic and cytoskeletal dynamics. Science. 349 (6251), (2015).
- York, A. G., et al. Resolution doubling in live, multicellular organisms via multifocal structured illumination microscopy. Nat. Methods. 9 (7), 749-754 (2012).

