Correlative אלקטרון מיקרוסקופ אור (קלם) עבור מעקב אחר והדמיה חלבון נגיפי הקשורים מבנים בתאים הקפאה. מרותק למיטה
Summary
שיטה correlative מיקרוסקופ אלקטרונים אור (קלם) מוחל על התמונה הנוצרות על-ידי וירוס תאיים מבנים באמצעות מיקרוסקופ אלקטרונים (EM) בתאים שנבחרו קודם לכן על ידי מיקרוסקופ אור (LM). באימות LM ו- EM משולבים כמו בגישה הדמיה היברידי להשיג תצלום המשולב של וירוס-פונדקאי אינטראקציות.
Abstract
בשל שלה ברזולוציה גבוהה, מיקרוסקופ אלקטרונים (EM) הוא כלי הכרחי עבור עשרים ושלוש. עם זאת, אחד הקשיים העיקריים בעת ניתוח תאים הנגועים בנגיף או transfected ויה EM הן היעילות נמוכה של זיהום או תרביות תאים, הפרעה הבחינה של תאים אלה. על מנת להתגבר על הקושי הזה, מיקרוסקופ אור (LM) ניתן לבצע קודם להקצות את subpopulation של תאים נגועים או transfected. לכן, מנצל השימוש פלורסנט חלבונים (FPs) התמזגו חלבונים נגיפיים, LM משמש כאן כדי להקליט את העמדות של תאי “transfected חיובי”, המבטאת FP וגדל על תמיכה עם דוגמת מילוי אלפאנומריים. כתוצאה מכך, תאי מעובדות נוספות עבור EM באמצעות לחץ גבוה קפוא (HPF), הקפאת שרף והטבעה של החלפת (FS). שלב ההקפאה אולטרה מהיר מבטיח ממברנה מעולה לשימור התאים שנבחרו מסוגל ואז לנתח ברמת ultrastructural על ידי במיקרוסקופ אלקטרונים הילוכים (TEM). . הנה, זרימת עבודה שלב אחר שלב correlative אלקטרון מיקרוסקופ אור (קלם) מסופק, המתארים הכנת הדוגמא, הדמיה, המתאם בפירוט. הנבחנים ניתן להחיל גם להתייחס הרבה שאלות בביולוגיה של התא.
Introduction
הרעיון של שילוב שתי שיטות מיקרוסקופ כדי לקבל תמונה טובה יותר של תהליך ביולוגי מסוים היא זקנה למדי. לפיכך, המחקר הראשון על וירוסים באמצעות “מיקרוסקופ correlative” פורסם בשנת 1960 שני פרסומים נפרד1,2. במחקר זה, המחברים ניתח את השינויים המורפולוגיה של גרעין שנגזרות adenoviruses באמצעות שתי טכניקות במיקרוסקופ. בפרסום הראשון, תצפיות מיקרוסקופ אלקטרונים (EM) המתאר את הפרטים מורפולוגי הקשורים אדנו זיהום היו דווח על1. בפרסום השני, המבנים שונים נצפה ע י EM היו בקורלציה עם מיקרוסקופ אור (LM) תמונות של דפוסי מכתימים פתולוגיה, להגדיר את מהות של המבנים נצפה בעבר ע י EM2.
במחקרים אלה מוקדם, עם זאת, שלהם תצפיות בוצעו באמצעות תאים נגועים שונים מוכנים כמו ניסויים עצמאית. “הקשר”, ואכן, נועד כמו השילוב של המידע שמגיע שתי שיטות הדמיה כדי להבין תופעה מסוימת, השוואת כל הממצאים אשר הושגו עם מבחני שונות על מנת להבין נתון ביולוגי תהליך.
כיום, המונח correlative מיקרוסקופ, הידוע גם בשם אור correlative ואלקטרון (קלם), חלה על מספר גדל והולך של שיטות (נבדקה הפניות3,4,5), עם המכנה המשותף כי שתי טכניקות הדמיה (LM ו- EM) מתבצעות על הדגימה אותו. השילוב של שתי השיטות תוצאות, ובכך, ניתוח ומשולבות, סולם רב, רב ממדית הזה מדגם3. היתרונות הם כי LM יכול לספק סקירה רחבה של תאים שונים רבים, המאפשרים זיהוי תא subpopulations חלבון או חלבונים עניין בתוך אוכלוסיה הטרוגנית התא. אם מתגבר על מגבלת רזולוציה של LM, מתן של תמונה ברזולוציה גבוהה יותר של אירוע מסוים תאיים. יתר על כן, EM מאפשר את הפריט החזותי של הקשר הלא-פלורסנט subcellular, לרבות כל organelles ממברנה מאוגדים, מתחמים גדולים macromolecular (למשל, ריבוזומים, centrioles, וכו ‘), אלמנטים cytoskeletal, ובכך מתן מידע מרחבי נוסף, שנקרא “מפנה שטח”6, ולתת בהקשר לנקודה פלורסנט זוהה על ידי LM.
במהלך השנים האחרונות, קלם הפך להיות כלי רב עוצמה תא ביולוגים5, אלא גם עבור עשרים ושלוש (נבדקה ב הפניה7) שרוצה להבין את האינטראקציות וירוס מורכבים-תא להוביל הפצת וירוסים מוצלחות. לפיכך, הבנה כיצד וירוסים לשנות קרום התא, organelles שלהם לטובת חיוני לפתח תרופות אנטי להשמיד וירוסים פתוגניים.
. הנה, שיטה קלם מתואר המאפשר הזיהוי על ידי LM של תאים המבטאים חלבונים ויראלי דבוקה חלבון פלואורסצנטי (FP). תאים אלה הם לאחר מכן משותק הקפאה נוספת מוכן לניתוח ultrastructural באמצעות מיקרוסקופ אלקטרונים הילוכים (TEM) כדי לקבל תובנות חדשות איך הביטוי של חלבונים אלה מחדש תאיים ממברנות (איור 1). קלם בוצעה עם תאים כימי קבוע ברוב המחקרים וירולוגיה פורסם תאריך8,9,10,11,12,13,14 ,15,16,17,18,19. זאת בעיקר בשל הצורך של inactivating חומר זיהומיות מסיבות אבטחה אבטחה ברמה 2 ו-3 (BSL-2 ו- BSL-3) מעבדות, איפה הקפאה-הנייח של תאים בדרך כלל אינה אפשרית. לשאלות אלה הדורשים שימור של האופטימלית לקרום התא, ויטריפיקציה באמצעות לחץ גבוה קפוא (HPF), עם זאת, מומלץ מאוד20. במקרים אלה, ניתן להחיל את פרוטוקול קלם המתוארים כאן. מעניין, במיוחד בעת עבודה עם דגימות זיהומיות, HPF יכול להתבצע על דגימות שהיו בעבר כימית מוחלש, לדוגמה במעבדות BSL-2 ו- BSL-3. השילוב של קיבוע כימי ואחריו HPF הוא אפשרות להרוויח לפחות חלקית היתרונות של שימור-הקפאה שיטות21,22.
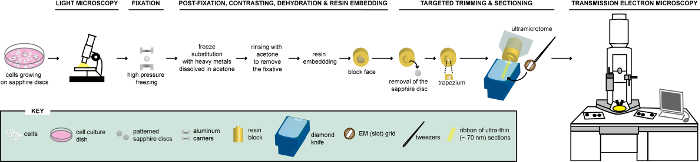
איור 1 : ייצוג סכמטי של זרימת העבודה עבור הניתוח של תאים דרך קלם. גדל דיסקים ספיר בדוגמת התאים מנותחים קודם על ידי LM כדי להתאים לשפה התאים לבטא FPs לפני העיבוד שלהם עבור EM. ברגע ממוקם, תאים מיד קבועים על ידי HPF FS להיות מוטבע לאחר מכן שרף. בעת הפילמור של השרף, התמיכה בו צמחו תאים (= דיסקים ספיר) יש להסיר מן הרחוב שרף. הרחוב המכילות את התאים מוטבע נחתך כיסוי trapezium קטן שממנו הם התאים הנותרים, המבטאת FPs, למחלקה עם סכין יהלום. סעיפים זגוגית נאספים על חריץ רשתות וכוח נוסף שבדק TEM לקבל מידע ultrastructural של תאים אלה. איור זה הותאם, ששינה באישור הפניה29. אנא לחץ כאן כדי להציג גירסה גדולה יותר של הדמות הזאת.
Protocol
Representative Results
Discussion
המתודולוגיה קלם המובאים כאן לחקור את ההשפעה של ביטוי חלבון נגיפי על קרום התא שימש בהצלחה לפני התירי את בזכות שכפול-הקשורים מבנים, בעיקר קרום כפול שלפוחית (DMVs)21, כמו גם לקבוע אבני הבניין קריטי הנדרש כדי ליצור אלה הנוצרות על-ידי בזכות מבנים23. שימו לב כי בעבודתנו הראשונים באמצעות קלם ללמוד בזכות שכפול21, גירסה קצת שונה של הפרוטוקול המתואר כאן יושם. באותו מחקר, דיסקים ספיר עבה מ מ 0.05 קונבנציונאלי, ללא דפוס אלפא-נומריים, שימשו שבו תבנית הפניה נוצר על ידי פחמן ציפוי אותם עם רשת finder למעלה (ראה טבלה של חומרים). גירסת פרוטוקול הנוכחי יכול להיות בסופו של דבר מיושם, עם יתרון כי המוביל “A” HPF ניתן להשתמש ישירות, ללא צורך כורתים אותו כמו איור 3א. לחלופין, כאמור בפרוטוקול, עבה “A” המוביל יכול להיות מנוצל (ראה טבלה של חומרים) עם דיסקים ספיר בדוגמת, ללא הצורך של חברת “B”.
מעניין, פרוטוקול זה יכול להיות מיושם לא רק ללמוד דגימות BSL-1, כגון תאים transfected עם חלבונים ויראלי כפי שמתואר כאן ושם19,23, אלא גם ללמוד תאים הנגועים בנגיף. למרות עבודה עם פתוגנים האנושית היא בדרך כלל מוגבלת למעבדות BSL-2 ו- BSL-3, במדינות מסוימות זה עדיין אפשרי לבצע הקפאה-הנייח בתנאים אלה אבטחה. אלה BSL-2, מעבדות BSL-3 איפה ויטריפיקציה אינה אפשרית, בשל תקנות מקומיות או העדר של מכונת HPF, תאים הנגועים בנגיף ניתן עדיין להכין בשיטה זו אם קיבוע כימי עם aldehydes יבוצע בתיאום מראש. כלומר לפני שעזב את המתקנים BSL-2 או BSL-3. יתר על כן, aldehydes צריך לכלותה מיד לאחר קיבוע לשמור את פלורסצנטיות, בעוד שאר הפרוטוקול היא זהה לזו המתוארת כאן. טכניקה זו יכולה להיחשב מיותר כי התאים קבועים פעמיים, מבחינה כימית, דרך ויטריפיקציה. עם זאת, פרוטוקול קיבוע זוגי זה מוביל אכן הרבה יותר טוב שימור DMVs בזכות-induced בהשוואה DMVs נמצאו תאים נתון קיבוע כימי לבד21.
עוד שינויים ולפתרון הקורא נקרא את הערות במהלך החלק פרוטוקול של כתב היד הזה. הערות אלו מתארים כדי למנוע pitfalls, וכן חלופות להתגבר על הקשיים בשם שעלולות להתעורר בעת ביצוע בשיטה זו.
המתחייב הראשי להחלת טכניקה זו היא מכונת HPF. מתי הקפאה-שיתק התאים באמצעות HPF הוא לא ריאלי (העדר מכונת HPF) או לא נדרש (כאשר שימור ממברנה אינו צריך להיות אופטימלי), תאים יכולים להיות כימי קבוע, לאחר מכן מוכן, נותחו על ידי EM8, 9,10,11,12,13,14,15,16,17,18 ,19. אפשרות זו אינה דורשת שימוש דיסקים ספיר, אבל התא מנות תרבות עם דפוסים gridded לרילוקיישן תאים או תא אשכולות. היתרון העיקרי של השימוש של הכלים האלה הוא שלהם בקוטר גדול יותר בהשוואה דיסקים ספיר, המאפשר הקרנת הסרט פני שטחים גדולים יותר. לפיכך, היישום של פרוטוקול קלם זה יושם בהצלחה כדי לחקור את ההשפעה של תרכובת אנטי נגד בזכות15 או לדמיין את rearrangements ממברנה שנגזרות החלבונים nonstructural של noroviruses19. על נושא אחר ניתן להגביל את הביצועים של שיטה זו הוא בהעדר מכשיר FS מסחרי. במקרה זה, מערכות בסיסי FS תוצרת בית יכול להיות מנוצל במקום. למרות מכונות ונדינג FS עשויים להפחית את התקלות טיפול, תוצרת בית, משמש בהצלחה למשל-קנט מקדונלדס30 ומעבדות פול. וולטר.
לגבי קיבוע כימי, הפרוטוקול המתואר כאן מבטיח של האופטימלית שימור מבנים תאיים20. לכן, במקרה המכשירים HPF ו- FS הנ ל זמינים, vitrifying את התאים עניין יהיה מועדף.
חלופות עתידי לגישה זו קלם כוללים את האפשרות להשתמש בשיטה זו לא רק לרכוש מידע 2D ברמת ultrastructural, אלא גם כדי לקבל נתוני תלת-ממד על הארכיטקטורה של הממברנה, אברון. שינויים שנגרמו על ידי וירוסים. השיטות 3D-EM, לרבות טומוגרפיה אלקטרון (ET) ואלקטרון יון ממוקד לסריקת קרן (שיקרתי-SEM) (שמתואר בהרחבה29), יכול להיות מיושם גם בתאים שלא הוכנו בעקבות זה הנוכחי פרוטוקול21, 31. בנוסף, 3D היתה אפשרות גם לקבל מידע ברמת LM, כאשר באמצעות מיקרוסקופ קונפוקלי, המאפשר הרכישה של z-במחסן. למעשה, אפשרות זו מומלצת מאוד כאשר מתאם מדויק בין datasets באימות LM ו- EM הוא הרצוי (ראה לדוגמה17). המידע הכלול z 3D-במחסן מסייע לשיפור הקשר עם תמונות TEM 2D. לפיכך, בתרחיש כזה, הכי מתאים תמונות LM ו- EM יכול להיות שנבחרו ונחשפו ואז לאחד התוכנה המתאם זמינים, כגון ה-ec-קלם plugin של אייסי (http://icy.bioimageanalysis.org/)32 או תוסף התכתבויות ציון דרך של תמונת J (http://imagej.net/Landmark_Correspondences), וכתוצאה מכך הדור של חופפים תמונות LM-EM.
כאשר מידע זמני יש צורך להבין את קינטיקה של אירוע מסוים, הדמיה בצילום מואץ ניתן לעקוב אחר הדינמיקה של תאים חיים, בשילוב עם EM. במהלך האירוע עניין תאים קבועים באופן מיידי, יצירת “תמונה קפואה” מסוגל לאחר מכן לנתח באמצעות EM, מתן מידע ultrastructural מפורט אודות בדיוק באותו רגע בזמנו של הנייח. על מנת לקבל את “בזק קפוא,” לאחר הצפייה בזמן אמת, תאים יכולים להיות כימי קבוע33 או הקפאה. מרותק למיטה6. מאז תהליכים תאיים רבים מתרחשים מהר יותר תהליכי דיפוזיה של קיבוע כימי, במידת האפשר, הקפאה מהירה במיוחד יש לבצעו. עם זאת, חשוב לקחת בחשבון כי המכונות HPF נבדלים שלהם ברזולוציה של זמן אפקטיבי34.
יתר על כן, אף על פי פרוטוקול זה תוכנן עבור ההטמעה של תאים שרף אפוקסי, התאים ניתן גם להטביע שרפים צמיגות נמוכה, כגון Lowicryls, LR לבן או זהב LR. בשימוש במדיה ההטבעה אלה מאפשר לשמר את antigenicity35,36, וכן קרינה פלואורסצנטית37,38 ו, לכן, משמשים בעיקר להטבעת פוסט-immunolabeling על סעיף39 , 40 ו—סעיף קלם41,42,43,44, שבו פרוטוקול LM נעשית לאחר ההטמעה. שתי הגישות (חיסונית-EM ו—סעיף קלם) חייב להיות מכריע לניסויים הללו שבה מבנים, מאפיין שאינו ניתן בקלות למצוא דרך TEM ו/או כפקד נגד miscorrelation בין באימות LM ו- EM אותות. באופן דומה, תיוג עם נוגדנים, ניתן לאבחן על ידי שתי שיטות הדמיה (LM ו- EM) יכול להתבצע45 כדי, למשל, לזהות תאים transfected LM (הטבעה מראש הבמה) ולהשיג על לוקליזציה הרבה יותר מדויק של האות ה-GFP ויה שלה תיוג ספציפית על ידי חיסונית-EM (שלב פוסט ההטבעה). יש לקחת בחשבון, עם זאת, permeabilization הזה מבוצע לפני LM כדי לאפשר את הגישה של הנוגדנים למרחב תאיים, אשר עלול לגרום שימור תת אופטימלית של האדריכלות תא ברמת EM. מעניין, פרוטוקול זה מתאימה מאוד גם עבור צבע רב הניסויים אשר יכולה להיות מושגת עם השימוש של תגיות פלורסנט אחרים, מלבד GFP (כפי שמוצג כאן). לסיכום, ישנן אפשרויות רבות בשם של התאמת פרוטוקול זה, הן על פרוטוקול LM ו/או בצדדים EM, תלוי השאלות להיות המטופלות. לקבלת תיאור מקיף של פרוטוקולים אחרים חלופי הקורא נקרא5,46. יחד ללא קשר כיצד שיטות מיקרוסקופ משולבים, התוצאה היא רווח של מידע, אשר מאפשר לנו להבין טוב יותר כיצד וירוסים וחלבונים שלהם אינטראקציה עם מארחיהם בחיים האמיתיים.
השלב הקריטי ביותר בתוך שיטה זו היא האוסף של קטעים טורי מתאי עניין. כפי שמודגש במקטע תוצאות נציג, הדבר דורש צוות מומחה, כמו גם הרבה סבלנות. חשוב לציין, שלב זה חיוני כדי לחפש את התאים חזרה באותה רמת EM משתי סיבות. ראשית, מעין פרוטוקול קלם באמצעות הטבעה מראש LM, נקודות הציון גלויים רק ברמה של LM, על פני בלוק שרף לאחר ההטמעה. עם זאת, הם לא יהיו גלויים על הסעיפים על ידי TEM. לכן, זמירה יישוב על פני בלוק למטה אל מחוזות ריבית (ROIs) חייב להתבצע בזהירות עם סכין גילוח כדי להבטיח כי הסעיפים שמושגות לאחר מכן מכילים התאים לבטא FP נתון. שנית, “סריקה” בכמה סעיפים יש צורך למצוא את הכיסוי הטוב ביותר בין פרוטוקול LM ורכישות EM. בניגוד לשיטות איפה LM מתבצע בשלב שלאחר ההטבעה, במקרה זה הכיסוי LM-EM הוא לא מדויק. דיוק כיסוי נמוך הוא ההבדלים ברזולוציה צירית בין באימות LM ו- EM, הצטמקות במהלך עיבוד הדגימה של EM ודחיסת במהלך חלוקתה42. יחד עם זאת, שיטות מעקב יעיל אחר, כגון השימוש של ציוני דרך, לעזור למצוא את התאים בחזרה. זה כולל את המיקום של תא אחד למשנהו, כמו גם את צורת התאים ואת הגרעין שלהם. בהקשר זה, כפי שהוסבר בפרוטוקול, DIC תמונות לספק מידע “אנטומיה” של התאים הם קריטיים כדי לשפר את המתאם. לחלופין, הגרעינים או אחרים האברונים טוב ניתן לזיהוי (כגון המיטוכונדריה או השומנים טיפות) יכול להיות מוכתם לפני LM ומשמש ציוני דרך.
לבסוף, ראוי לציין כי אף על פי כתב יד זה מתמקדת השימוש בטכניקה זו ללימודי וירולוגיה, היקף עיצוב ניסיוני זה ניתן להרחיב שאלות ביולוגיות כלליות יותר.
Divulgations
The authors have nothing to disclose.
Acknowledgements
. אנחנו מאוד אסירי תודה לחברי הצוות של מיקרוסקופ אלקטרונים הליבה מתקנים (EMCF) ב EMBL (היידלברג) וב אוניברסיטת היידלברג. גם ברצוננו להודות אולריקה Herian, סטפני Kallis, אנדראה Hellwig (אוניברסיטת היידלברג), כמו גם אברהרט שמידט רנטה קונץ (האוניברסיטה ההיסטורית אולם) לקבלת סיוע טכני מומחה. עבודה לפי R.B. וצוותו (U.H. ו לתעשיה-בי) נתמכה על ידי פתוח, SFB1129, TP11 TRR83, TP13.
Materials
| UV Crosslinker | Stratagene | 400072 | Stratalinker 1800, 230Vac, equipped with 254-nm UV light bulbs, 8-watts/each. |
| Patterned sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 627 | They have a 0.3-mm diameter and are 0.16-mm thick, as well as an an etched alphanumeric pattern to allow for re-location of the cells. They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Slim and long tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | 72919-SS | "Style SS", for handling sapphire discs. |
| Cell culture medium | Thermo Fisher Scientific, Waltham, MA, USA | 41965-062 | Dulbecco's modified Eagle medium (DMEM) supplemented with 2 mM L-glutamine, nonessential amino acids, 100 units penicillin per ml, 100 µg streptomycin per ml and 10% fetal calf serum (DMEM complete, see below). Package containing 10 bottles, 500 ml/each. |
| L-glutamine | Thermo Fisher Scientific, Waltham, MA, USA | 25030-123 | Package containing 20 bottles of 100 ml/each. |
| Nonessential amino acids | Thermo Fisher Scientific, Waltham, MA, USA | 11140-068 | Package containing 20 bottles of 100 ml/each. |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Waltham, MA, USA | 15140-163 | Package containing 20 bottles of 100 ml/each. |
| Fetal calf serum | Sigma Aldrich, St. Louis, MI, USA | F7524 | Bottle of 50 ml. |
| Inverted microscope | Olympus Deutschland, Hamburg, Germany | CKX41 | It is an inverted microscope with trinocular head options and fluorescence upgrade capability. |
| Huh7-Lunet cells stably expressing the T7 RNA-polymerase | Avaliable at Prof. Dr. Ralf Bartenschlager laboratory | Not available | Contact Prof. Bartenschlager at: ralf.bartenschlager@med.uni-heidelberg.de. |
| Mirus TransIT-LT1 Transfection Reagent | Mirus Bio LLC, Madison, USA | MIR 2304 | Broad spectrum, low toxicity, DNA transfection reagent. Vial of 0.4 ml. |
| Inverted widefield fluorescence microscope | Carl Zeiss Microscopy GmbH, Germany | Zeiss Observer.Z1 | Inverted fluorescence microscope for experiments involving living cell cultures. |
| 1-hexadecene | Merck, Darmstadt, Germany | 8220640100 | Bottle of 100 ml. |
| "A" aluminium holders for high pressure frezing (HPF) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 241 | This is the holder that has been used for this protocol and has 2 different depths of 0.1 and 0.2-mm. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "B" aluminium holders for HPF | Engineering Office M. Wohlwend, Sennwald, Switzerland | 242 | This is the holder that has been used for this protocol.It is 0.3-mm thick.They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "A" aluminium holder for HPF (special for working with patterned sapphire discs) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 737 | This is the holder than can be used alone with the patterned sapphire disc (as an alternative to the current protocol), without the need of a "B" holder or the edition of the "A" holder. It is 0.84-mm thick. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 405 | These sapphires discs are the "conventional" one, with a 0.3-mm diameter and a thickness of 0.05 mm . They can be also used for CLEM as an alternative instead of patterned sapphire discs. |
| Finder grids | Electron Microscopy Sciences, Hatfield, Philadelphia, USA | LF135-Cu | These 135 mesh grids are used to create an alphanumeric pattern on "conventional" sapphire discs (described above) via carbon coating, so that they can be used for CLEM. 100 grids/vial. |
| HPF machine | ABRA Fluid AG, Widnau, Switzerland | HPM 01 | This HPF machine has been used for this protocol. |
| HPF machine | Leica Microsystems, Vienna, Austria | EMPACT 2 | "EMPACT 2", as an alternative to the use of the HPM machine that it has been used in this protocol (described above). |
| Cryo-tubes | Thermo Fisher Scientific, Waltham, MA, USA | Z763667-500EA | For long term-storage of cryo-immobilized samples in liquid nitrogen. Package containing 500 cryovials. |
| Liquid nitrogen dewar | Cole-Parmer GmbH, Wertheim, Germany | GZ-05094-60 | For long term-storage of cryo-immobilized samples in liquid nitrogen, equipped with cryo-racks with a capacity of 1600 cryo-tubes. |
| Automatic freeze substitution (AFS) machine | Leica Microsystems, Vienna, Austria | EM AFS2 | This machine performs freeze substitution and progressive lowering of temperature (PLT) techniques and allows low temperature embedding and polymerization of resins. |
| Osmium tetroxide (OsO4) | Electron Microscopy Sciences, Hatfield, PA, USA | 19150 | 4% aqueous solution, one box containing 10 x 2 ml ampules. |
| Uranyl-Acetate (UA) | Serva, Heidelberg, Germany | 77879.01 | Bottle containing 25 grs of (UA)-2 H2O. |
| Sonicator | Bandelin Electronic, Berlin, Germany | 329 | "Sonorex Super RK 31" is a high-power ultrasonic cleaning bath for aqueous cleaning solution that is used in this protocol to mix OsO4 and Ua when preparing the FS medium. |
| Glass-distilled acetone | Electron Microscopy Sciences, Hatfield, PA, USA | 10015 | Bottle of 100 ml. |
| Stereomicroscope | Leica Microsystems, Vienna, Austria | Leica M80 | Routine stereomicroscope for daily inspections, equipped with a camera for capturing images. |
| Epoxy resin | Electron Microscopy Sciences, Hatfield, PA, USA | 14120 | Embed 812 is a kit containing several components that must be mix together in the proportions given by the manufacturers. |
| Flow through rings | Leica Microsystems, Vienna, Austria | 16707157 | Package containing 100 pieces. |
| Reagent baths | Leica Microsystems, Vienna, Austria | 16707154 | Package containing 100 pieces. |
| Ultramicrotome | Leica Microsystems, Vienna, Austria | Leica EM UC7 | Ultramicrotome for preparation of semi- and ultrathin sections at room temperature. |
| Ultra 35° diamond knife | Diatome Ltd., Nidau Switzerland |
AGG339-735 | This knife have an edge length of 3 mm. |
| Ultra fine tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | E78318 | "Style 3X", for handling EM grids. |
| EM slot grids | Electron Microscopy Sciences, Hatfield, PA, USA | G2010-Cu | 100 grids/vial. |
| EM grid storage box | Electron Microscopy Sciences, Hatfield, PA, USA | 71155 | It has capacity for 100 grids. |
References
- Morgan, C., Godman, G. C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. I. Electron microscopy. Journal of Experimental Medicine. 112, 373-382 (1960).
- Godman, G. C., Morgan, C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. II. Light microscopy. Journal of Experimental Medicine. 112, 383-402 (1960).
- Caplan, J., Niethammer, M., Taylor, R. M., Czymmek, K. J. The power of correlative microscopy: multi-modal, multi-scale, multi-dimensional. Current Opinion in Structural Biology. 21, 686-693 (2011).
- de Boer, P., Hoogenboom, J. P., Giepmans, B. N. Correlated light and electron microscopy: ultrastructure lights up. Nature Methods. 12, 503-513 (2015).
- Müller-Reichert, T., Verkade, P. . Correlative light and electron microscopy III, First edition. , (2017).
- Brown, E., Mantell, J., Carter, D., Tilly, G., Verkade, P. Studying intracellular transport using high-pressure freezing and Correlative Light Electron Microscopy. Seminars in Cell and Developmental Biology. 20, 910-919 (2009).
- Bykov, Y. S., Cortese, M., Briggs, J. A., Bartenschlager, R. Correlative light and electron microscopy methods for the study of virus-cell interactions. FEBS Letters. , (2016).
- Spuul, P., et al. Assembly of alphavirus replication complexes from RNA and protein components in a novel trans-replication system in mammalian cells. Journal of Virology. 85, 4739-4751 (2011).
- Nagel, C. H., Dohner, K., Binz, A., Bauerfeind, R., Sodeik, B. Improper tagging of the non-essential small capsid protein VP26 impairs nuclear capsid egress of herpes simplex virus. PLoS One. 7, 44177 (2012).
- Sharma, M., Kamil, J. P., Coughlin, M., Reim, N. I., Coen, D. M. Human cytomegalovirus UL50 and UL53 recruit viral protein kinase UL97, not protein kinase C, for disruption of nuclear lamina and nuclear egress in infected cells. Journal of Virology. 88, 249-262 (2014).
- Kallio, K., et al. Template RNA length determines the size of replication complex spherules for Semliki Forest virus. Journal of Virology. 87, 9125-9134 (2013).
- Martinez, M. G., Snapp, E. L., Perumal, G. S., Macaluso, F. P., Kielian, M. Imaging the alphavirus exit pathway. Journal of Virology. 88, 6922-6933 (2014).
- Lebrun, M., et al. Varicella-zoster virus induces the formation of dynamic nuclear capsid aggregates. Virology. 454-455, 311-327 (2014).
- Madela, K., et al. A simple procedure to analyze positions of interest in infectious cell cultures by correlative light and electron microscopy. Methods in Cell Biology. 124, 93-110 (2014).
- Berger, C., et al. Daclatasvir-like inhibitors of NS5A block early biogenesis of hepatitis C virus-induced membranous replication factories, independent of RNA replication. Gastroenterology. 147, 1094-1105 (2014).
- van der Schaar, H. M., et al. Illuminating the Sites of Enterovirus Replication in Living Cells by Using a Split-GFP-Tagged Viral Protein. mSphere. 1, (2016).
- Vale-Costa, S., et al. Influenza A virus ribonucleoproteins modulate host recycling by competing with Rab11 effectors. Journal of Cell Science. 129, 1697-1710 (2016).
- Wang, L., et al. Visualization of HIV T Cell Virological Synapses and Virus-Containing Compartments by Three-Dimensional Correlative Light and Electron Microscopy. Journal of Virology. 91, (2017).
- Doerflinger, S. Y., et al. Membrane alterations induced by nonstructural proteins of human norovirus. PLOS Pathogens. 13, 1006705 (2017).
- Dahl, R., Staehelin, L. A. High-pressure freezing for the preservation of biological structure: theory and practice. Journal of Electron Microscopy Technique. 13, 165-174 (1989).
- Romero-Brey, I., et al. Three-dimensional architecture and biogenesis of membrane structures associated with hepatitis C virus replication. PLOS Pathogens. 8, 1003056 (2012).
- Sosinsky, G. E., et al. The combination of chemical fixation procedures with high pressure freezing and freeze substitution preserves highly labile tissue ultrastructure for electron tomography applications. Journal of Structural Biology. 161, 359-371 (2008).
- Romero-Brey, I., et al. NS5A Domain 1 and Polyprotein Cleavage Kinetics Are Critical for Induction of Double-Membrane Vesicles Associated with Hepatitis C Virus Replication. MBio. 6, 00759 (2015).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36, 280-290 (2003).
- Jou, M. J., Jou, S. B., Guo, M. J., Wu, H. Y., Peng, T. I. Mitochondrial reactive oxygen species generation and calcium increase induced by visible light in astrocytes. Annals of the New York Academy of Sciences. 1011, 45-56 (2004).
- McDonald, K. L., Morphew, M., Verkade, P., Muller-Reichert, T. Recent advances in high-pressure freezing: equipment- and specimen-loading methods. Methods in Molecular Biology. 369, 143-173 (2007).
- Walther, P., Ziegler, A. Freeze substitution of high-pressure frozen samples: the visibility of biological membranes is improved when the substitution medium contains water. Journal of Microscopy. 208, 3-10 (2002).
- White, J. G., Southgate, E., Thomson, J. N., Brenner, S. The structure of the nervous system of the nematode Caenorhabditis elegans. Philosophical Transactions of the Royal Society B: Biological Sciences. 314, 1-340 (1986).
- Romero-Brey, I., Bartenschlager, R. Viral Infection at High Magnification: 3D Electron Microscopy Methods to Analyze the Architecture of Infected Cells. Viruses. 7, 6316-6345 (2015).
- McDonald, K. L., Webb, R. I. Freeze substitution in 3 hours or less. Journal of Microscopy. 243, 227-233 (2011).
- Villinger, C., Neusser, G., Kranz, C., Walther, P., Mertens, T. 3D Analysis of HCMV Induced-Nuclear Membrane Structures by FIB/SEM Tomography: Insight into an Unprecedented Membrane Morphology. Viruses. 7, 5686-5704 (2015).
- Paul-Gilloteaux, P., et al. eC-CLEM: flexible multidimensional registration software for correlative microscopies. Nature Methods. 14, 102-103 (2017).
- Polishchuk, R. S., Mironov, A. A. Correlative video light/electron microscopy. Current Protocols in Cell Biology Supplement. , 8 (2001).
- McDonald, K. L. A review of high-pressure freezing preparation techniques for correlative light and electron microscopy of the same cells and tissues. Journal of Microscopy. 235, 273-281 (2009).
- Newman, G. R., Jasani, B., Williams, E. D. A simple post-embedding system for the rapid demonstration of tissue antigens under the electron microscope. The Histochemical Journal. 15, 543-555 (1983).
- Schwarz, H., Humbel, B. M. Influence of fixatives and embedding media on immunolabelling of freeze-substituted cells. Scanning Microscopy. 3, 57-63 (1989).
- Luby-Phelps, K., Ning, G., Fogerty, J., Besharse, J. C. Visualization of identified GFP-expressing cells by light and electron microscopy. Journal of Histochemistry and Cytochemistry. 51, 271-274 (2003).
- Nixon, S. J., et al. A single method for cryofixation and correlative light, electron microscopy and tomography of zebrafish embryos. Traffic. 10, 131-136 (2009).
- McDonald, K. L. Rapid embedding methods into epoxy and LR White resins for morphological and immunological analysis of cryofixed biological specimens. Microscopy and Microanalysis. 20, 152-163 (2014).
- Webster, P., Schwarz, H., Griffiths, G. Preparation of cells and tissues for immuno EM. Methods in Cell Biology. 88, 45-58 (2008).
- Kukulski, W., et al. Correlated fluorescence and 3D electron microscopy with high sensitivity and spatial precision. Journal of Cell Biology. 192, 111-119 (2011).
- Peddie, C. J., et al. Correlative and integrated light and electron microscopy of in-resin GFP fluorescence, used to localise diacylglycerol in mammalian cells. Ultramicroscopy. 143, 3-14 (2014).
- Hampoelz, B., et al. Pre-assembled Nuclear Pores Insert into the Nuclear Envelope during Early Development. Cell. 166, 664-678 (2016).
- Lemercier, N., et al. Microtome-integrated microscope system for high sensitivity tracking of in-resin fluorescence in blocks and ultrathin sections for correlative microscopy. Scientific Reports. 7, 13583 (2017).
- Takizawa, T., Powell, R. D., Hainfeld, J. F., Robinson, J. M. FluoroNanogold: an important probe for correlative microscopy. Journal of Biological Chemistry. 8, 129-142 (2015).
- Romero-Brey, I., Yamauchi, Y. 3D electron microscopy (EM) and correlative light electron microscopy (CLEM) methods to study virus-host interactions. Methods in Molecular Biology: Influenza Virus Methods & Protocols. , (2018).

