En atferdsskjerm for varmeinduserte anfall i musemodeller av epilepsi
Summary
Målet med metoden er å screene for hypertermi eller varmeinduserte anfall i musemodeller. Protokollen beskriver bruken av et spesialbygd kammer med kontinuerlig overvåking av kroppstemperaturen for å avgjøre om forhøyet kroppstemperatur fører til anfall.
Abstract
Transgene musemodeller har vist seg å være kraftige verktøy for å studere ulike aspekter av menneskelige nevrologiske lidelser, inkludert epilepsi. SCN1A-assosierte genetiske epilepsier utgjør et bredt spekter av anfallsforstyrrelser med ufullstendig penetrans og klinisk variasjon. SCN1A-mutasjoner kan resultere i et stort utvalg av anfall fenotype som spenner fra enkle, selvbegrensede feberrelaterte feberrelaterte feberanfall (FS), genetisk epilepsi på moderat nivå med feberanfall pluss (GEFS+) til mer alvorlig Dravet syndrom (DS). Selv om FS ofte ses hos barn under 6-7 år som ikke har genetisk epilepsi, fortsetter FS hos GEFS+ pasienter å forekomme i voksen alder. Tradisjonelt har eksperimentell FS blitt indusert hos mus ved å utsette dyret for en strøm av tørr luft eller varmelamper, og endringshastigheten i kroppstemperaturen er ofte ikke godt kontrollert. Her beskriver vi et spesialbygd varmekammer, med en plexiglassfront, som er utstyrt med en digital temperaturregulator og en varmeapparatutstyrt elektrisk vifte, som kan sende oppvarmet tvungen luft inn i testarenaen på en temperaturkontrollert måte. Kroppstemperaturen til en mus plassert i kammeret, overvåket gjennom en rektal sonde, kan økes til 40-42 °C på en reproduserbar måte ved å øke temperaturen inne i kammeret. Kontinuerlig visuell overvåking av dyrene i oppvarmingsperioden viser induksjon av varmeinduserte anfall hos mus som bærer en FS-mutasjon ved en kroppstemperatur som ikke fremkaller atferdsmessige anfall hos villtype kullkamerater. Dyr kan enkelt fjernes fra kammeret og plasseres på en kjølepute for raskt å returnere kroppstemperaturen til normal. Denne metoden gir en enkel, rask og reproduserbar screeningprotokoll for forekomst av varmeinduserte anfall i epilepsimusmodeller.
Introduction
Epilepsi, den fjerde vanligste familien av nevrologiske lidelser i USA1, er preget av en ubalanse av eksitatorisk og hemmende drivkraft i CNS som fører til tilbakevendende anfall. Feberbeslag (FS) eller feberrelaterte anfall kan forekomme i befolkningen generelt, oftest hos barn så tidlig som 3 måneder opp til 6-7 år. Men hos enkelte individer med genetiske mutasjoner, oftest i et natriumkanalgen, kan FS vedvare utover 7 år i voksen alder. Denne tilstanden kalles feberanfall pluss eller FS+. Raske fremskritt innen genomsekvensering har identifisert over 1300 mutasjoner i det humane natriumionkanalgenet SCN1A, noe som gjør det til et hotspot for epilepsimutasjoner. SCN1A-mutasjoner har vært knyttet til et bredt spekter av anfallsforstyrrelser, inkludert feberbeslag (FS), genetisk epilepsi med feberanfall pluss (GEFS+) og Dravet syndrom (DS)2,3,4,5,6. Omtrent 20% av SCN1A missense mutasjoner fører til GEFS + 5,7,8. Pediatrisk historie med kompleks eller langvarig FS i barndommen kan senere utvikle seg til mer svekkende former for epilepsi som temporal lobe epilepsi (TLE)9,10,11. Dravet syndrom oppstår på grunn av avkortingsmutasjoner eller tap av funksjonsmutasjoner i SCN1A og er en alvorlig form for intractable epilepsi, med barndoms utbrudd av feberanfall som utvikler seg til ildfaste anfall, og er ofte forbundet med kognitive, utviklingsmessige og motoriske svekkelser2,5,12 . Siden mange individer med GEFS+ og/eller DS viser feberanfall, blir det viktig å utvikle nye terapier for bedre å bekjempe disse anfallsforstyrrelsene.
Dyremodeller av SCN1A assosiert epilepsi har vist seg uvurderlig i karakterisering av ulike typer anfall (febril vs generalisert) og dissekering av nevronmekanismen for anfallsgenerasjon13,14,15,16,17,18. Mens studien av spontane anfall via EEG / EMG-opptak i gnagerhjerner er godt etablert og er et veldig nyttig verktøy, har bare noen få studier forsøkt å etterligne feberbeslag i musemodeller14,16,19,20,21,22,23 . Tidligere studier har brukt en stråle med oppvarmet tørr luft, eller en metakrylatsylinder utstyrt med et termisk system, eller varmelamper med temperaturregulator i lukkede testarenaer9,16,21,22,23,24 for å indusere anfall via hypertermi. For å øke kroppstemperaturen i et mer kontrollert miljø, bruker protokollen som er beskrevet her et spesialbygget kammer med et temperaturkontrollert varmesystem som tillot reproduserbare økningshastigheter i kroppstemperaturen til en mus inne i kammeret. Varmekammeret ble konstruert av tre (lengde 40 cm x bredde 34 cm x høyde 31 cm) og ble utstyrt med en digital temperaturregulator med K termokobling. En liten aksialvifte utstyrt med en varmeapparat på baksiden av kammeret leder oppvarmet luft inn i kammeret regulert av en digital temperaturregulator. Dette tvungne luftvarmesystemet gjør det mulig å kontrollere hastigheten kammertemperaturen øker med. (Figur 1A,B). K-termoelementet inne i trevarmekammeret sender tilbakemelding til den digitale temperaturregulatoren for å opprettholde konstante temperaturer inne i esken under analysen. Hvis du stiller inn temperaturen på den digitale temperaturregulatoren, kan den elektriske viften sende oppvarmet tvungen luft gjennom ventiler for å varme opp kammeret jevnt (figur 1A). Frontpanelet på varmekammeret er et klart plexiglassark for å muliggjøre enkel videoopptak av forsøkene.
Voksne (P30-P40) mus, heterozygote for en missense mutasjon i SCN1A som får GEFS+ og et likt antall villtype kullkamerater til å fungere som kontrollgruppen, ble valgt for hvert eksperiment. Dyr, både menn og kvinner, som ble brukt i disse studiene veide minst 15 g, da villmus som veide mindre var mer følsomme for varmeinduserte anfall enn tyngre dyr i samme alder. I pilotstudien ble både mutant- og villtypemus observert for å oppsøke de kjøligere hjørnene av kammeret på baksiden og forble der i lengre perioder. For å omgå dette ble effektiv gulvstørrelse inne i varmekammerets testarena redusert til lengde 16,5 cm x bredde 21,5 cm x høyde 27,5 cm ved å plassere en treblokk B (mål 20 cm x 8 cm x 7,2 cm) på høyre side av kammeret (figur 1A). Varmekammeret ble konstruert av 1,9 cm tykt kryssfiner (lengde 40 cm x bredde 34 cm x høyde 31 cm) dekket med hvitt laminat og utstyrt med en digital temperaturregulator med K termokobling. Kammerveggenes laminatoverflate er ugjennomtrengelig og kan enkelt desinfiseres mellom forsøk ved å tørke av med 70% etanol. Temperaturen på varmekammeret ble i utgangspunktet satt til 50 °C og forvarmet i minst 1 time før starten av eksperimentet, for å sikre jevn oppvarming inne i kammeret. Hver mus var utstyrt med et rektal termometer for kontinuerlig overvåking av kroppstemperatur gjennom hele eksperimentet. En enkelt mus ble plassert i kammeret om gangen og temperaturen ble holdt ved 50 °C mellom 1.–10. Temperaturen ble deretter hevet til 55 °C i 11.-20. minutt, og til slutt hevet til 60 °C i 21.-30. Dette resulterte i en reproduserbar økning i musens kroppstemperatur (figur 2A). Hver prøveversjon ble filmet, og atferdsanalyse ble utført offline.
Varmeprotokollen kan enkelt modifiseres for å endre den opprinnelige temperaturen på varmekammeret og hastigheten som kammeret oppvarmes, noe som igjen endrer hvor raskt kroppstemperaturen til musen er forhøyet under analysen. Dermed gir denne metoden mer fleksibilitet i forhold til tradisjonelle metoder for å sette opp atferdsskjermer som involverer varmeinduserte anfall. Den varmeinduserte anfallsprotokollen kan også brukes til å screene for antiepileptika som gjør mutantmus mer motstandsdyktige mot varmeinduserte anfall eller øker terskeltemperaturen der anfall observeres. På samme måte kan gunstige effekter av restriktive diettregimer som keto-diett på varmeinduserte anfall undersøkes i normale chow-matet vs keto-matede mus.
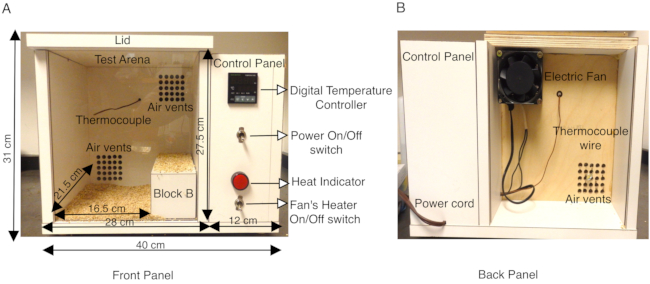
Figur 1: Beskrivelse av det spesialbygde musevarmekammeret. (A) Frontpanelet på tremusens varmekammer viser sidekontrollpanelet som inneholder Power ON/OFF-bryteren som slår på digital temperaturregulator, K-termokobling, vifteovnens PÅ/AV-bryter og varmeindikator. De ytre dimensjonene på boksen og den indre testarenaen vises i cm. En treblokk B som brukes til effektivt å redusere testarenaoverflaten, vises også. Bunnen av testarenaen er dekket med cob sengetøy for å forhindre at mus kommer direkte i kontakt med oppvarmede treflater. (B) Bakpanelet på varmekammeret viser viften montert på toppluftventilen og strømledningen for å levere strøm til kammeret. Dette tallet er modifisert fra figur 3 i Das et al., 2021, eNeuro14. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Vi beskriver en enkel og effektiv protokoll for å screene for forekomst av varmeinduserte anfall hos mus, atferdsekvivalenten til feberanfall hos menneskelige pasienter. Analysen evaluerer flere parametere – inkludert prosentandelen mus som viser anfall, anfallsterskel, alvorlighetsgrad av anfall på en Racine-skala, for å sammenligne følsomheten til kontroll- og testmusgrupper for å øke kroppstemperaturen.
Et kritisk skritt i denne protokollen innebærer å øke varmen i kammeret mens du kontinuerlig overvåker kroppstemperaturen til musen. Det er viktig at den maksimale kroppstemperaturen musene vil oppleve i disse analysene er 44 °C fordi villdyr kan gjennomgå varmeinduserte anfall ved kroppstemperaturer >44 °C. Forbehandling med generell anestesi eller smertestillende midler kan redusere kjernetemperaturen til dyr eller forstyrre termoregulering, noe som igjen vil forvirre innsamling av anfallsterskeltemperaturdata. Dermed kunne mus under denne screeningprotokollen ikke leveres med disse agentene i løpet av 30 min prøvevindu. Alle prosedyrer må godkjennes av institusjonens IACUC-komité. For å sikre kontinuerlig overvåking av musens kjernetemperatur under analysen, tape rektal temperatursonden sikkert til musenes hale. Hvis det under analysen viser seg at musens kroppstemperatur forblir uendret i lengre perioder, selv etter å ha økt temperaturen på musekammeret, må du sørge for at rektal temperatursonden ikke har kommet ut av musen eller er festet løst til halen.
Genetisk bakgrunn av musemodeller kan påvirke følsomheten for SCN1A-mutasjonen og farmakologisk induserte anfall18,25,26,27. Som diskutert i resultatene ovenfor, kan musenes genetiske bakgrunn påvirke deres følsomhet for varmeinduserte anfall. Scn1a K1270T GEFS+ mutantmus ble testet i to genetiske bakgrunner – 129X1 og B6NJ, og en liten prosentandel av villtype mus (33%) i den anfallsfølsomme B6NJ-bakgrunnen, ble også observert for å gjennomgå varmeinduserte anfall. Men sammenlignet med de heterozygote mutant scn1aKT /+ musene, opplevde B6NJ villtype mus varmeinduserte anfall med en betydelig høyere temperaturterskel. Dette bekrefter at den genetiske mutasjonen (Scn1a K1270T) som ble introdusert av CRISPR knock-in, gjør mutantmusene mer utsatt for hypertermiinduserte anfall.
Det er flere fordeler med å vedta denne protokollen, som er oppsummert nedenfor. For det første, i motsetning til bruk av strøm av tørr luft eller oppvarmede lamper, gir en temperaturkontrollert tvungen luft satt opp i et lukket rom eksperimentet mer kontroll over oppvarming av testarenaen til ønsket hastighet. Trinnene i varmeprotokollen kan enkelt endres for å øke / redusere starttemperaturen, varigheten av hvert trinn, etc. for å screene eldre mus som er tyngre eller større gnagere som rotter. For det andre gir kontinuerlig overvåking av musens kroppstemperatur via den vedlagte rektalsonden verdifull informasjon om kroppstemperaturendringen i individuell mus, gjennom hele analysen. Dette gjør at eksperimentet kan nøye observere at temperaturendringen i musen ikke overstiger 0,25-0,5 °C/min (noe som kan være stressende for dyrene), når du tilpasser denne protokollen til andre testarenaer. Viktigst, frekvensen av endring av kroppstemperatur over tid i forskjellige musgrupper kan kaste lys over deres evne til å termoregulering og kan være nyttig for å forstå om feberbeslag som forårsaker mutasjoner også endrer termoregulering hos mus. For det tredje sikrer kontinuerlig kroppstemperaturovervåking at anfallsterskeltemperaturmålingene ved hjelp av denne protokollen er nøyaktige, siden de registreres samtidig med den første anfallskampen som musen opplever. Hvis dyrets kroppstemperatur ikke overvåkes kontinuerlig eller anfallsterskeltemperaturen måles etter å ha tatt dyret ut av testarenaen, kan anfallsterskelverdiene variere på grunn av tiden det tar å håndtere musene etter anfall. Til slutt omgår denne metoden behovet for å bruke invasive metoder for å indusere feber (ved å injisere patogener) hos mus for å etterligne feberanfall hos menneskelige pasienter.
En av begrensningene i denne protokollen er at det er vanskelig å screene juvenile (mindre enn P30 i alderen) mus for varmeinduserte anfall. Protokollen ble utviklet for å screene for følsomhet for voksne mus (P30-P40 og over) til varme- eller hypertermiinduserte anfall. Etter vår erfaring er de yngre villtype musene, spesielt de som veier under 15 g, mer sannsynlig å gjennomgå varmeinduserte anfall, noe som kan skyldes underutviklede termoreguleringsmekanismer, fysiologisk termisk stress eller en kombinasjon av begge deler. Derfor er det ikke ideelt å utføre den varmeinduserte anfallsskjermen på juvenile mus ved hjelp av denne protokollen.
Fremtidige studier som kombinerer EEG-overvåking mens musen utsettes for varmeinduserte anfall, kan belyse EEG-anfallsmønstre for varmeinduserte anfall, tilsvarende en tidligere studie19. Nevronaktivitet i bestemte områder i musehjernen kan spores ved å kombinere optogenetiske tilnærminger og immunhiistokjemibaserte studier etter høsting av hjernevevet. Effektene av restriktive dietter som keto-diett på å redusere feberanfall kan også evalueres ved å utsette keto-matede mus og normale chow-matede mus for varmeindusert anfallsprotokoll. På samme måte kan epilepsi narkotika screening paradigmer utvikles for å teste og identifisere kandidat anti-epileptiske legemidler som ameliorate eller undertrykke varmeinduserte anfall i narkotika-matet eller behandlet mus sammenlignet med kjøretøy-matet eller kontroll mus.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Vi vil takke Connor J. Smith for hans hjelp til å bygge det tilpassede musevarmekammeret. Vi erkjenner hjelp fra O’Dowd labmedlemmer, Lisha Zeng og Andrew Salgado for standardisering av varmeprotokollen i de tidlige stadiene av analyseutviklingen. Vi takker også Danny Benavides og Kumar Perinbam for videoopptak av deler av den eksperimentelle prosedyren for manuskriptet. Dette arbeidet ble støttet av NIH-stipendet (NS083009) tildelt D.O.D.
Materials
| Axial fan | Farnam | AF20-200-120-xx10-3.1 | Farnam custom products -Axial Fan Heater with Fan |
| Digital temperature controller | Inkbird | ITC-100RH | Inkbird digital PID temperature controller ITC-100RH with K thermocouple |
| Mouse rectal temperature probe | ThermoWorks, Braintree Scientific, Inc | RET-3 | Mouse rectal temperature probe with thermometer |
References
- Hirtz, D., et al. How common are the ‘common’ neurologic disorders. Neurology. 68, 326-337 (2007).
- Catterall, W. A. Sodium Channel Mutations and Epilepsy. Jasper’s Basic Mechanisms of the Epilepsies. , (2012).
- Mantegazza, M., Broccoli, V. SCN 1A /Na V 1.1 channelopathies: Mechanisms in expression systems, animal models, and human iPSC models. Epilepsia. 60, (2019).
- Stafstrom, C. E. Persistent Sodium Current and Its Role in Epilepsy. Epilepsy Currents. 7, 15-22 (2007).
- Schutte, S. S., Schutte, R. J., Barragan, E. V., O’Dowd, D. K. Model systems for studying cellular mechanisms of SCN1A-related epilepsy. Journal of Neurophysiology. 115, 1755-1766 (2016).
- Wei, F., et al. Ion Channel Genes and Epilepsy: Functional Alteration, Pathogenic Potential, and Mechanism of Epilepsy. Neuroscience Bulletin. 33, 455-477 (2017).
- Abou-Khalil, B., et al. Partial and generalized epilepsy with febrile seizures plus and a novel SCN1A mutation. Neurology. 57, 2265-2272 (2001).
- Zhang, Y. -. H., et al. Genetic epilepsy with febrile seizures plus: Refining the spectrum. Neurology. 89, 1210-1219 (2017).
- Patterson, K. P., et al. Enduring memory impairments provoked by developmental febrile seizures are mediated by functional and structural effects of neuronal restrictive silencing factor. Journal of Neuroscience. 37, 3799-3812 (2017).
- Rossi, M. A. SCN1A and febrile seizures in mesial temporal epilepsy: An early signal to guide prognosis and treatment. Epilepsy Currents. 14, 189-190 (2014).
- Zhang, Y., et al. Altered gut microbiome composition in children with refractory epilepsy after ketogenic diet. Epilepsy Research. 145, 163-168 (2018).
- Meng, H., et al. The SCN1A mutation database: Updating information and analysis of the relationships among genotype, functional alteration, and phenotype. Human Mutation. 36, 573-580 (2015).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Das, A., et al. Interneuron dysfunction in a new mouse model of SCN1A GEFS. eNeuro. , (2021).
- Kalume, F., et al. Sudden unexpected death in a mouse model of Dravet syndrome. Journal of Clinical Investigations. 123, 1798-1808 (2013).
- Martin, M. S., et al. Altered function of the SCN1A voltage-gated sodium channel leads to gamma-aminobutyric acid-ergic (GABAergic) interneuron abnormalities. Journal of Biological Chemistry. 285, 9823-9834 (2010).
- Rubinstein, M., et al. Dissecting the phenotypes of Dravet syndrome by gene deletion. Brain. 138, 2219-2233 (2015).
- Yu, F. H., et al. Reduced sodium current in GABAergic interneurons in a mouse model of severe myoclonic epilepsy in infancy. Nature Neuroscience. 9, 1142-1149 (2006).
- Dutton, S. B. B., et al. Early-life febrile seizures worsen adult phenotypes in Scn1a mutants. Experimental Neurology. 293, 159-171 (2017).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Oakley, J. C., Cho, A. R., Cheah, C. S., Scheuer, T., Catterall, W. A. Synergistic GABA-enhancing therapy against seizures in a mouse model of Dravet Syndrome. Journal of Pharmacology and Experimental Therapeutics. 345, 215-224 (2013).
- Ricobaraza, A., et al. Epilepsy and neuropsychiatric comorbidities in mice carrying a recurrent Dravet syndrome SCN1A missense mutation. Scientific Reports. 9, (2019).
- Warner, T. A., Liu, Z., Macdonald, R. L., Kang, J. -. Q. Heat induced temperature dysregulation and seizures in Dravet Syndrome/GEFS+ Gabrg2+/Q390X mice. Epilepsy Research. 134, 1-8 (2017).
- Eun, B. -. L., Abraham, J., Mlsna, L., Kim, M. J., Koh, S. Lipopolysaccharide potentiates hyperthermia-induced seizures. Brain and Behavior. 5, 00348 (2015).
- Miller, A. R., Hawkins, N. A., McCollom, C. E., Kearney, J. A. Mapping genetic modifiers of survival in a mouse model of Dravet syndrome. Genes Brain and Behavior. 13, 163-172 (2013).
- Mistry, A. M., et al. Strain- and age-dependent hippocampal neuron sodium currents correlate with epilepsy severity in Dravet syndrome mice. Neurobiology of Disease. 65, 1-11 (2014).
- Ogiwara, I., et al. Nav1.1 localizes to axons of parvalbumin-positive inhibitory interneurons: a circuit basis for epileptic seizures in mice carrying an Scn1a gene mutation. Journal of Neuroscience. 27, 5903-5914 (2007).

