Una prueba conductual para las convulsiones inducidas por el calor en modelos de epilepsia en ratones
Summary
El objetivo del método es detectar hipertermia o convulsiones inducidas por el calor en modelos de ratón. El protocolo describe el uso de una cámara personalizada con monitoreo continuo de la temperatura corporal para determinar si la temperatura corporal elevada conduce a convulsiones.
Abstract
Los modelos de ratones transgénicos han demostrado ser herramientas poderosas en el estudio de diversos aspectos de los trastornos neurológicos humanos, incluida la epilepsia. Las epilepsias genéticas asociadas a SCN1A comprenden un amplio espectro de trastornos convulsivos con penetrancia incompleta y variabilidad clínica. Las mutaciones scn1A pueden dar lugar a una gran variedad de fenotipos convulsivos que van desde convulsiones febriles (FS) simples y autolimitadas asociadas a la fiebre, epilepsia genética de nivel moderado con convulsiones febriles más (GEFS +) hasta el síndrome de Dravet (DS) más grave. Aunque las FS se observan comúnmente en niños menores de 6-7 años de edad que no tienen epilepsia genética, la FS en pacientes con GEFS+ continúa ocurriendo en la edad adulta. Tradicionalmente, los FS experimentales se han inducido en ratones al exponer al animal a una corriente de aire seco o lámparas de calefacción, y la tasa de cambio en la temperatura corporal a menudo no está bien controlada. Aquí, describimos una cámara de calefacción hecha a medida, con un frente de plexiglás, que está equipada con un controlador de temperatura digital y un ventilador eléctrico equipado con calentador, que puede enviar aire forzado calentado a la arena de prueba de una manera controlada por temperatura. La temperatura corporal de un ratón colocado en la cámara, monitoreada a través de una sonda rectal, se puede aumentar a 40-42 ° C de manera reproducible aumentando la temperatura dentro de la cámara. El monitoreo visual continuo de los animales durante el período de calentamiento demuestra la inducción de convulsiones inducidas por el calor en ratones portadores de una mutación FS a una temperatura corporal que no provoca convulsiones conductuales en compañeros de camada de tipo salvaje. Los animales se pueden sacar fácilmente de la cámara y colocarlos en una almohadilla de enfriamiento para devolver rápidamente la temperatura corporal a la normalidad. Este método proporciona un protocolo de detección simple, rápido y reproducible para la aparición de convulsiones inducidas por el calor en modelos de ratón con epilepsia.
Introduction
La epilepsia, la cuarta familia más común de trastornos neurológicos en los Estados Unidos1, se caracteriza por un desequilibrio del impulso excitatorio e inhibitorio en el SNC que conduce a convulsiones recurrentes. Las convulsiones febriles (FS) o las convulsiones asociadas a la fiebre pueden ocurrir en la población general, con mayor frecuencia en niños desde los 3 meses hasta los 6 -7 años de edad. Sin embargo, en algunos individuos con mutaciones genéticas, con mayor frecuencia en un gen del canal de sodio, FS puede persistir más allá de la edad de 7 años en la edad adulta. Esta condición se conoce como convulsiones febriles plus o FS +. Los rápidos avances en la secuenciación del genoma han identificado más de 1.300 mutaciones en el gen del canal iónico de sodio humano SCN1A, lo que lo convierte en un punto caliente para las mutaciones de la epilepsia. Las mutaciones de SCN1A se han relacionado con un amplio espectro de trastornos convulsivos, incluidas las convulsiones febriles (FS), la epilepsia genética con convulsiones febriles plus (GEFS+) y el síndrome de Dravet (DS)2,3,4,5,6. Alrededor del 20% de las mutaciones sin sentido scN1A conducen a GEFS+5,7,8. Los antecedentes pediátricos de FS compleja o prolongada en la infancia pueden convertirse posteriormente en formas más debilitantes de epilepsia, como la epilepsia del lóbulo temporal (TLE)9,10,11. El síndrome de Dravet surge debido a mutaciones de truncamiento o mutaciones de pérdida de función en SCN1A y es una forma grave de epilepsia intratable, con inicio en la infancia de convulsiones febriles que se convierten en convulsiones refractarias, y a menudo se asocia con deficiencias cognitivas, de desarrollo y motoras2,5,12 . Dado que muchas personas con GEFS+ y/o DS exhiben convulsiones febriles, se vuelve imperativo desarrollar nuevas terapias para combatir mejor estos trastornos convulsivos.
Los modelos animales de epilepsia asociada a SCN1A han demostrado ser invaluables para caracterizar diferentes tipos de convulsiones (febril vs generalizada) y diseccionar el mecanismo neuronal de la generación de convulsiones13,14,15,16,17,18. Si bien el estudio de las convulsiones espontáneas a través de registros de EEG / EMG en cerebros de roedores está bien establecido y es una herramienta muy útil, solo unos pocos estudios han intentado imitar las convulsiones febriles en modelos de ratón14,16,19,20,21,22,23 . Estudios anteriores han utilizado un chorro de aire seco calentado, o un cilindro de metacrilato equipado con un sistema térmico, o lámparas de calor con un controlador de temperatura en arenas de prueba cerradas9,16,21,22,23,24 para inducir convulsiones a través de la hipertermia. Con el fin de aumentar la temperatura corporal en un entorno más controlado, el protocolo descrito aquí utiliza una cámara personalizada con un sistema de calefacción de temperatura controlada que permitió tasas reproducibles de aumento de la temperatura corporal de un ratón dentro de la cámara. La cámara de calor fue construida de madera (largo 40 cm x ancho 34 cm x alto 31 cm) y fue equipado con un controlador de temperatura digital con un termopar K. Un pequeño ventilador axial equipado con un calentador en el panel posterior de la cámara dirige el aire caliente a la cámara regulada por un controlador de temperatura digital. Este sistema de calentamiento de aire forzado permite controlar la velocidad a la que aumenta la temperatura de la cámara. (Figura 1A,B). El termopar K ubicado dentro de la cámara de calor de madera envía retroalimentación al controlador de temperatura digital, para mantener temperaturas constantes dentro de la caja durante el ensayo. El ajuste de la temperatura en el controlador de temperatura digital permite que el ventilador eléctrico envíe aire forzado calentado a través de las rejillas de ventilación para calentar uniformemente la cámara (Figura 1A). El panel frontal de la cámara de calor es una lámina de plexiglás transparente para permitir una fácil grabación de video de los ensayos.
Para cada experimento se seleccionaron ratones adultos (P30-P40), heterocigotos para una mutación sin sentido en SCN1A que causa GEFS+ y un número igual de compañeros de camada de tipo salvaje para servir como grupo de control. Los animales, tanto machos como hembras, utilizados en estos estudios pesaron al menos 15 g, ya que los ratones de tipo salvaje que pesaban menos eran más sensibles a las convulsiones inducidas por el calor que los animales más pesados de la misma edad. En el estudio piloto, se observó que tanto los ratones mutantes como los de tipo salvaje buscaban las esquinas más frías de la cámara en la parte posterior y permanecieron allí durante períodos prolongados de tiempo. Para evitar esto, el tamaño efectivo del piso dentro de la arena de prueba de la cámara de calor se redujo a la longitud de 16.5 cm x ancho 21.5 cm x altura 27.5 cm colocando un bloque de madera B (dimensiones 20 cm x 8 cm x 7.2 cm) en el lado derecho de la cámara (Figura 1A). La cámara de calor se construyó a partir de madera contrachapada de 1,9 cm de espesor (largo 40 cm x ancho 34 cm x altura 31 cm) cubierta con laminado blanco y equipada con un controlador de temperatura digital con un termopar K. La superficie laminada de las paredes de la cámara es impermeable y se puede desinfectar fácilmente entre ensayos limpiando con etanol al 70%. La temperatura de la cámara de calor se fijó inicialmente en 50 °C y se precalentó durante al menos 1 h antes del inicio del experimento, para garantizar un calentamiento uniforme dentro de la cámara. A cada ratón se le equipó un termómetro rectal para el monitoreo continuo de la temperatura corporal durante todo el experimento. Se colocó un solo ratón en la cámara a la vez y la temperatura se mantuvo a 50 ° C entre el minuto 1 y el 10. La temperatura se elevó a 55 ° C durante el minuto 11-20, y finalmente se elevó a 60 ° C durante el minuto 21-30. Esto resultó en una tasa reproducible de aumento en la temperatura corporal del ratón (Figura 2A). Cada ensayo se grabó en video y el análisis del comportamiento se realizó fuera de línea.
El protocolo de calentamiento se puede modificar fácilmente para cambiar la temperatura inicial de la cámara de calor y la velocidad a la que se calienta la cámara, lo que a su vez cambia la rapidez con que se eleva la temperatura corporal del ratón durante el ensayo. Por lo tanto, este método proporciona más flexibilidad sobre los métodos tradicionales en la configuración de las pantallas de comportamiento que implican convulsiones inducidas por el calor. El protocolo de convulsiones inducidas por calor también se puede usar para detectar medicamentos antiepilépticos que hacen que los ratones mutantes sean más resistentes a las convulsiones inducidas por el calor o aumentan la temperatura umbral a la que se observan las convulsiones. Del mismo modo, los efectos beneficiosos de los regímenes de dieta restrictiva como la dieta ceto en las convulsiones inducidas por el calor se pueden examinar en ratones normales alimentados con chow vs cetoalimentados.
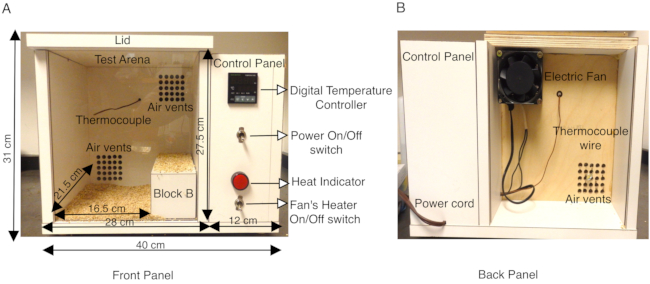
Figura 1: Descripción de la cámara de calor del ratón personalizada. (A) El panel frontal de la cámara de calor del ratón de madera muestra el panel de control lateral que contiene el interruptor de encendido / apagado que enciende el controlador de temperatura digital, el termopar K, el interruptor de encendido / apagado del calentador del ventilador y el indicador de calor. Las dimensiones exteriores de la caja y la arena de prueba interna se muestran en cm. También se muestra un bloque de madera B utilizado para reducir eficazmente la superficie de la arena de prueba. La parte inferior de la arena de prueba está cubierta con ropa de cama de mazorca para evitar que los ratones entren en contacto directo con las superficies de madera calentadas. (B) El panel posterior de la cámara de calor muestra el ventilador montado en la salida de aire superior y el cable de alimentación para suministrar electricidad a la cámara. Esta cifra se modifica de la Figura 3 en Das et al., 2021, eNeuro14. Haga clic aquí para ver una versión más grande de esta figura.
Protocol
Representative Results
Discussion
Describimos un protocolo simple y efectivo para detectar la aparición de convulsiones inducidas por el calor en ratones, el equivalente conductual de las convulsiones febriles en pacientes humanos. El ensayo evalúa varios parámetros, incluido el porcentaje de ratones que muestran convulsiones, el umbral de convulsiones, la gravedad de las convulsiones en una escala de Racine, para comparar la sensibilidad de los grupos de ratones de control y prueba con los aumentos de la temperatura corporal.
Un paso crítico en este protocolo implica aumentar el calor en la cámara mientras se monitorea continuamente la temperatura corporal del ratón. Es imperativo que la temperatura corporal máxima que los ratones experimentarán en estos ensayos sea de 44 ° C porque los animales de tipo salvaje pueden sufrir convulsiones inducidas por el calor a temperaturas corporales >44 ° C. El pretratamiento con anestesia general o analgésicos podría reducir la temperatura corporal central de los animales o interferir con la termorregulación, lo que a su vez confundiría la recopilación de datos de temperatura umbral de convulsiones. Por lo tanto, los ratones bajo este protocolo de detección no pudieron ser provistos de estos agentes durante la ventana de ensayo de 30 minutos. Todos los procedimientos deben ser aprobados por el comité IACUC de la institución. Para garantizar un monitoreo continuo de la temperatura corporal central del ratón durante el ensayo, pegue de forma segura la sonda de temperatura rectal a la cola de los ratones. Si durante el ensayo, se descubre que la temperatura corporal del ratón permanece sin cambios durante períodos prolongados de tiempo, incluso después de aumentar la temperatura de la cámara del ratón, asegúrese de que la sonda de temperatura rectal no haya salido del ratón o esté unida libremente a la cola.
Los antecedentes genéticos de los modelos de ratón pueden afectar la sensibilidad a la mutación SCN1A y las convulsiones inducidas farmacológicamente18,25,26,27. Como se discutió en los resultados anteriores, los antecedentes genéticos de los ratones pueden influir en su susceptibilidad a las convulsiones inducidas por el calor. Scn1a Los ratones mutantes K1270T GEFS + se probaron en dos antecedentes genéticos: 129X1 y B6NJ, y también se observó que un pequeño porcentaje de ratones de tipo salvaje (33%) en el fondo B6NJ sensible a las convulsiones sufría convulsiones inducidas por el calor. Sin embargo, en comparación con los ratones mutantes heterocigotos Scn1aKT / +, los ratones de tipo salvaje B6NJ experimentaron convulsiones inducidas por el calor a un umbral de temperatura significativamente más alto. Esto confirma que la mutación genética (Scn1a K1270T) que fue introducida por CRISPR knock-in hace que los ratones mutantes sean más susceptibles a las convulsiones inducidas por hipertermia.
Hay varias ventajas de adoptar este protocolo, que se resumen a continuación. En primer lugar, a diferencia del uso de corrientes de aire seco o lámparas calentadas, un aire forzado con temperatura controlada establecido dentro de un espacio cerrado proporciona al experimentador más control sobre el calentamiento de la arena de prueba a una velocidad deseada. Los pasos en el protocolo de calentamiento se pueden modificar fácilmente para aumentar / disminuir la temperatura inicial, la duración de cada paso, etc. para detectar ratones más viejos que son roedores más pesados o más grandes, como las ratas. En segundo lugar, el monitoreo continuo de la temperatura corporal del ratón a través de la sonda rectal adjunta, proporciona información valiosa sobre la tasa de cambio de temperatura corporal en ratones individuales, a lo largo del ensayo. Esto permite al experimentador observar de cerca que la tasa de cambio de temperatura en el ratón no supera los 0,25-0,5 °C/min (lo que podría ser estresante para los animales), al adaptar este protocolo a otros ámbitos de prueba. Es importante destacar que la tasa de cambio de la temperatura corporal a lo largo del tiempo en diferentes grupos de ratones puede arrojar luz sobre su capacidad para termorregular y podría ser útil para comprender si las convulsiones febriles que causan mutaciones que también alteran la termorregulación en ratones. En tercer lugar, el monitoreo continuo de la temperatura corporal garantiza que las mediciones de la temperatura del umbral de convulsiones utilizando este protocolo sean precisas, ya que se registran simultáneamente con el primer ataque de convulsiones experimentado por el ratón. Si la temperatura corporal del animal no se controla continuamente o se mide la temperatura del umbral de convulsión después de sacar al animal del campo de prueba, los valores del umbral de convulsión pueden variar debido al tiempo necesario para manejar a los ratones después de las convulsiones. Finalmente, este método evita la necesidad de utilizar métodos invasivos para inducir fiebre (mediante la inyección de patógenos) en ratones para imitar las convulsiones febriles en pacientes humanos.
Una de las limitaciones de este protocolo es que es difícil detectar ratones juveniles (menos de P30 de edad) para detectar convulsiones inducidas por el calor. El protocolo se desarrolló para detectar la sensibilidad de ratones adultos (P30-P40 y superiores) a las convulsiones inducidas por calor o hipertermia. En nuestra experiencia, los ratones de tipo salvaje más jóvenes, especialmente aquellos que pesan menos de 15 g, tienen más probabilidades de sufrir convulsiones inducidas por el calor, lo que podría deberse a mecanismos de termorregulación subdesarrollados, estrés térmico fisiológico o una combinación de ambos. Por lo tanto, no es ideal realizar la prueba de convulsiones inducidas por calor en ratones juveniles utilizando este protocolo.
Los estudios futuros que combinan la monitorización del EEG mientras someten al ratón a convulsiones inducidas por el calor pueden arrojar luz sobre los patrones de convulsiones del EEG de las convulsiones inducidas por el calor, similar a un estudio anterior19. La actividad neuronal en áreas específicas en el cerebro del ratón se puede rastrear combinando enfoques optogenéticos y estudios basados en inmunohistoquímica después de la recolección del tejido cerebral. Además, los efectos de las dietas restrictivas como la dieta ceto en la reducción de las convulsiones febriles se pueden evaluar sometiendo a los ratones alimentados con ceto y a los ratones normales alimentados con chow al protocolo de convulsiones inducidas por el calor. Del mismo modo, se pueden desarrollar paradigmas de detección de medicamentos para la epilepsia para probar e identificar fármacos antiepilépticos candidatos que mejoren o supriman las convulsiones inducidas por el calor en ratones alimentados con medicamentos o tratados en comparación con ratones alimentados con vehículos o de control.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Nos gustaría agradecer a Connor J. Smith por su ayuda en la construcción de la cámara de calor personalizada para ratones. Agradecemos la ayuda de los miembros del laboratorio O’Dowd, Lisha Zeng y Andrew Salgado, por estandarizar el protocolo de calentamiento durante las primeras etapas del desarrollo del ensayo. También agradecemos a Danny Benavides y Kumar Perinbam por grabar en video partes del procedimiento experimental para el manuscrito. Este trabajo fue apoyado por la subvención de los NIH (NS083009) otorgada a D.O.D.
Materials
| Axial fan | Farnam | AF20-200-120-xx10-3.1 | Farnam custom products -Axial Fan Heater with Fan |
| Digital temperature controller | Inkbird | ITC-100RH | Inkbird digital PID temperature controller ITC-100RH with K thermocouple |
| Mouse rectal temperature probe | ThermoWorks, Braintree Scientific, Inc | RET-3 | Mouse rectal temperature probe with thermometer |
References
- Hirtz, D., et al. How common are the ‘common’ neurologic disorders. Neurology. 68, 326-337 (2007).
- Catterall, W. A. Sodium Channel Mutations and Epilepsy. Jasper’s Basic Mechanisms of the Epilepsies. , (2012).
- Mantegazza, M., Broccoli, V. SCN 1A /Na V 1.1 channelopathies: Mechanisms in expression systems, animal models, and human iPSC models. Epilepsia. 60, (2019).
- Stafstrom, C. E. Persistent Sodium Current and Its Role in Epilepsy. Epilepsy Currents. 7, 15-22 (2007).
- Schutte, S. S., Schutte, R. J., Barragan, E. V., O’Dowd, D. K. Model systems for studying cellular mechanisms of SCN1A-related epilepsy. Journal of Neurophysiology. 115, 1755-1766 (2016).
- Wei, F., et al. Ion Channel Genes and Epilepsy: Functional Alteration, Pathogenic Potential, and Mechanism of Epilepsy. Neuroscience Bulletin. 33, 455-477 (2017).
- Abou-Khalil, B., et al. Partial and generalized epilepsy with febrile seizures plus and a novel SCN1A mutation. Neurology. 57, 2265-2272 (2001).
- Zhang, Y. -. H., et al. Genetic epilepsy with febrile seizures plus: Refining the spectrum. Neurology. 89, 1210-1219 (2017).
- Patterson, K. P., et al. Enduring memory impairments provoked by developmental febrile seizures are mediated by functional and structural effects of neuronal restrictive silencing factor. Journal of Neuroscience. 37, 3799-3812 (2017).
- Rossi, M. A. SCN1A and febrile seizures in mesial temporal epilepsy: An early signal to guide prognosis and treatment. Epilepsy Currents. 14, 189-190 (2014).
- Zhang, Y., et al. Altered gut microbiome composition in children with refractory epilepsy after ketogenic diet. Epilepsy Research. 145, 163-168 (2018).
- Meng, H., et al. The SCN1A mutation database: Updating information and analysis of the relationships among genotype, functional alteration, and phenotype. Human Mutation. 36, 573-580 (2015).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Das, A., et al. Interneuron dysfunction in a new mouse model of SCN1A GEFS. eNeuro. , (2021).
- Kalume, F., et al. Sudden unexpected death in a mouse model of Dravet syndrome. Journal of Clinical Investigations. 123, 1798-1808 (2013).
- Martin, M. S., et al. Altered function of the SCN1A voltage-gated sodium channel leads to gamma-aminobutyric acid-ergic (GABAergic) interneuron abnormalities. Journal of Biological Chemistry. 285, 9823-9834 (2010).
- Rubinstein, M., et al. Dissecting the phenotypes of Dravet syndrome by gene deletion. Brain. 138, 2219-2233 (2015).
- Yu, F. H., et al. Reduced sodium current in GABAergic interneurons in a mouse model of severe myoclonic epilepsy in infancy. Nature Neuroscience. 9, 1142-1149 (2006).
- Dutton, S. B. B., et al. Early-life febrile seizures worsen adult phenotypes in Scn1a mutants. Experimental Neurology. 293, 159-171 (2017).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Oakley, J. C., Cho, A. R., Cheah, C. S., Scheuer, T., Catterall, W. A. Synergistic GABA-enhancing therapy against seizures in a mouse model of Dravet Syndrome. Journal of Pharmacology and Experimental Therapeutics. 345, 215-224 (2013).
- Ricobaraza, A., et al. Epilepsy and neuropsychiatric comorbidities in mice carrying a recurrent Dravet syndrome SCN1A missense mutation. Scientific Reports. 9, (2019).
- Warner, T. A., Liu, Z., Macdonald, R. L., Kang, J. -. Q. Heat induced temperature dysregulation and seizures in Dravet Syndrome/GEFS+ Gabrg2+/Q390X mice. Epilepsy Research. 134, 1-8 (2017).
- Eun, B. -. L., Abraham, J., Mlsna, L., Kim, M. J., Koh, S. Lipopolysaccharide potentiates hyperthermia-induced seizures. Brain and Behavior. 5, 00348 (2015).
- Miller, A. R., Hawkins, N. A., McCollom, C. E., Kearney, J. A. Mapping genetic modifiers of survival in a mouse model of Dravet syndrome. Genes Brain and Behavior. 13, 163-172 (2013).
- Mistry, A. M., et al. Strain- and age-dependent hippocampal neuron sodium currents correlate with epilepsy severity in Dravet syndrome mice. Neurobiology of Disease. 65, 1-11 (2014).
- Ogiwara, I., et al. Nav1.1 localizes to axons of parvalbumin-positive inhibitory interneurons: a circuit basis for epileptic seizures in mice carrying an Scn1a gene mutation. Journal of Neuroscience. 27, 5903-5914 (2007).

