En adfærdsmæssig skærm for varmeinducerede anfald i musemodeller af epilepsi
Summary
Målet med metoden er at screene for hypertermi eller varmeinducerede anfald i musemodeller. Protokollen beskriver brugen af et specialbygget kammer med kontinuerlig overvågning af kropstemperaturen for at afgøre, om forhøjet kropstemperatur fører til anfald.
Abstract
Transgene musemodeller har vist sig at være kraftfulde værktøjer til at studere forskellige aspekter af menneskelige neurologiske lidelser, herunder epilepsi. De SCN1A-associerede genetiske epilepsier omfatter et bredt spektrum af anfaldsforstyrrelser med ufuldstændig penetrans og klinisk variabilitet. SCN1A-mutationer kan resultere i en lang række anfaldsfænotyper, der spænder fra enkle, selvbegrænsede feberrelaterede feberanfald (FS), genetisk epilepsi på moderat niveau med feberkramper plus (GEFS+) til mere alvorligt Dravet syndrom (DS). Selvom FS almindeligvis ses hos børn under 6-7 år, der ikke har genetisk epilepsi, fortsætter FS hos GEFS + -patienter med at forekomme i voksenalderen. Traditionelt er eksperimentel FS blevet induceret i mus ved at udsætte dyret for en strøm af tør luft eller varmelamper, og ændringshastigheden i kropstemperaturen er ofte ikke godt kontrolleret. Her beskriver vi et specialbygget varmekammer med plexiglasfront, der er udstyret med en digital temperaturregulator og en varmeudstyret elektrisk ventilator, som kan sende opvarmet tvungen luft ind i testarenaen på en temperaturstyret måde. Kropstemperaturen på en mus, der er anbragt i kammeret, overvåget gennem en rektal sonde, kan øges til 40-42 °C på en reproducerbar måde ved at øge temperaturen inde i kammeret. Kontinuerlig visuel overvågning af dyrene i opvarmningsperioden viser induktion af varmeinducerede anfald hos mus, der bærer en FS-mutation ved en kropstemperatur, der ikke fremkalder adfærdsmæssige anfald hos vildtype kuldkammerater. Dyr kan let fjernes fra kammeret og placeres på en kølepude for hurtigt at returnere kropstemperaturen til normal. Denne metode giver mulighed for en enkel, hurtig og reproducerbar screeningsprotokol for forekomsten af varmeinducerede anfald i epilepsimusemodeller.
Introduction
Epilepsi, den fjerde mest almindelige familie af neurologiske lidelser i USA1, er kendetegnet ved en ubalance af excitatorisk og hæmmende drev i CNS, der fører til tilbagevendende anfald. Feberkramper (FS) eller feberrelaterede anfald kan forekomme i den generelle befolkning, oftest hos børn så tidligt som 3 måneder op til 6-7 år. Men hos nogle personer med genetiske mutationer, oftest i et natriumkanalgen, kan FS fortsætte ud over 7 år i voksenalderen. Denne tilstand kaldes feberkramper plus eller FS +. Hurtige fremskridt inden for genomsekventering har identificeret over 1.300 mutationer i det humane natriumionkanalgen SCN1A, hvilket gør det til et hotspot for epilepsimutationer. SCN1A-mutationer har været forbundet med et bredt spektrum af anfaldsforstyrrelser, herunder feberkramper (FS), genetisk epilepsi med feberkramper plus (GEFS+) og Dravet syndrom (DS)2,3,4,5,6. Omkring 20% af SCN1A missense mutationer fører til GEFS + 5,7,8. Pædiatrisk historie af kompleks eller langvarig FS i barndommen kan efterfølgende udvikle sig til mere svækkende former for epilepsi såsom temporal lobe epilepsi (TLE)9,10,11. Dravet syndrom opstår på grund af afkortningsmutationer eller tab af funktionsmutationer i SCN1A og er en alvorlig form for uhåndterlig epilepsi, med barndomsdebut af feberkramper, der udvikler sig til ildfaste anfald, og er ofte forbundet med kognitive, udviklingsmæssige og motoriske svækkelser2,5,12 . Da mange personer med GEFS + og / eller DS udviser feberkramper, bliver det bydende nødvendigt at udvikle nye terapier for bedre at bekæmpe disse anfaldsforstyrrelser.
Dyremodeller af SCN1A-associeret epilepsi har vist sig uvurderlige til at karakterisere forskellige typer anfald (febril vs generaliseret) og dissekere neuronal mekanisme for anfaldsgenerering13,14,15,16,17,18. Mens undersøgelsen af spontane anfald via EEG / EMG-optagelser i gnaverhjerner er veletableret og er et meget nyttigt værktøj, har kun få undersøgelser forsøgt at efterligne feberkramper i musemodeller14,16,19,20,21,22,23 . Tidligere undersøgelser har brugt en stråle opvarmet tør luft eller en methacrylatcylinder udstyret med et termisk system eller varmelamper med en temperaturregulator i lukkede testarenaer9,16,21,22,23,24 til at fremkalde anfald via hypertermi. For at øge kropstemperaturen i et mere kontrolleret miljø bruger protokollen beskrevet her et specialbygget kammer med et temperaturstyret varmesystem, der tillod reproducerbare stigningshastigheder i kropstemperaturen på en mus inde i kammeret. Varmekammeret blev konstrueret af træ (længde 40 cm x bredde 34 cm x højde 31 cm) og var udstyret med en digital temperaturregulator med et K-termoelement. En lille aksial ventilator udstyret med en varmelegeme på kammerets bagpanel leder opvarmet luft ind i kammeret reguleret af en digital temperaturregulator. Dette tvungne luftvarmesystem gør det muligt for en at styre den hastighed, hvormed kammertemperaturen stiger. (Figur 1A,B). K-termoelementet, der er placeret inde i trævarmekammeret, sender feedback til den digitale temperaturregulator for at opretholde konstante temperaturer inde i kassen under analysen. Indstilling af temperaturen på den digitale temperaturregulator gør det muligt for den elektriske ventilator at sende opvarmet tvungen luft gennem ventilationsåbninger for ensartet opvarmning af kammeret (figur 1A). Varmekammerets frontpanel er en klar plexiglasplade, der muliggør nem videooptagelse af forsøgene.
Voksne (P30-P40) mus, heterozygote for en missense-mutation i SCN1A, der får GEFS+ og et lige antal vildtypekuldkammerater til at fungere som kontrolgruppe, blev udvalgt til hvert forsøg. Dyr, både han- og hundyr, der blev anvendt i disse undersøgelser, vejede mindst 15 g, da vildtypemus, der vejede mindre, var mere følsomme over for varmeinducerede anfald end tungere dyr i samme alder. I pilotstudiet blev både mutante og vildtypemus observeret for at opsøge de køligere hjørner af kammeret bagpå og forblev der i længere perioder. For at omgå dette blev den effektive gulvstørrelse inde i varmekammertestarenaen reduceret til længde 16,5 cm x bredde 21,5 cm x højde 27,5 cm ved at placere en træblok B (dimensioner 20 cm x 8 cm x 7,2 cm) i højre side af kammeret (figur 1A). Varmekammeret blev konstrueret af 1,9 cm tyk krydsfiner (længde 40 cm x bredde 34 cm x højde 31 cm) dækket af hvidt laminat og udstyret med en digital temperaturregulator med et K-termoelement. Laminatoverfladen på kammervæggene er uigennemtrængelig og kan let desinficeres mellem forsøg ved at tørre ned med 70% ethanol. Varmekammerets temperatur blev oprindeligt sat til 50 °C og forvarmet i mindst 1 time før forsøgets start for at sikre ensartet opvarmning inde i kammeret. Hver mus blev udstyret med et rektalt termometer til kontinuerlig overvågning af kropstemperaturen under hele eksperimentet. En enkelt mus blev placeret i kammeret ad gangen, og temperaturen blev holdt på 50 °C mellem 1.-10. minut. Temperaturen blev derefter hævet til 55 °C i det 11.-20. minut og til sidst hævet til 60 °C i det 21.–30. minut. Dette resulterede i en reproducerbar stigningshastighed i musens kropstemperatur (figur 2A). Hvert forsøg blev videofilmet, og adfærdsanalyse blev udført offline.
Opvarmningsprotokollen kan let ændres for at ændre varmekammerets starttemperatur og den hastighed, som kammeret opvarmes, hvilket igen ændrer, hvor hurtigt musens kropstemperatur hæves under analysen. Således giver denne metode mere fleksibilitet i forhold til traditionelle metoder til opsætning af adfærdsmæssige skærme, der involverer varmeinducerede anfald. Den varmeinducerede anfaldsprotokol kan også bruges til at screene for antiepileptiske lægemidler, der gør mutante mus mere modstandsdygtige over for varmeinducerede anfald eller øger tærskeltemperaturen, ved hvilken anfald observeres. Tilsvarende kan gavnlige virkninger af restriktive diætregimer såsom keto-diæt på varmeinducerede anfald undersøges hos normale chow-fodrede vs keto-fodrede mus.
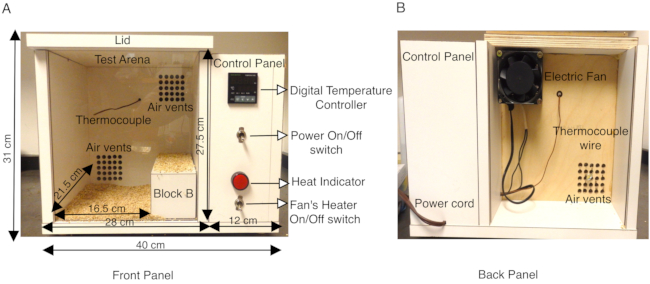
Figur 1: Beskrivelse af det specialbyggede musevarmekammer. (A) Frontpanelet på træmusens varmekammer viser sidekontrolpanelet, der indeholder tænd / sluk-kontakt, der tænder digital temperaturregulator, K-termoelement, ventilatorvarmerens ON / OFF-kontakt og varmeindikator. Kassens ydre dimensioner og den indre testarena er vist i cm. En træblok B, der bruges til effektivt at reducere testarenaoverfladen, er også vist. Bunden af testarenaen er dækket af kolbestrøelse for at forhindre mus i at komme direkte i kontakt med opvarmede træoverflader. (B) Varmekammerets bagpanel viser ventilatoren monteret på den øverste udluftning og netledningen for at levere elektricitet til kammeret. Dette tal er modificeret fra figur 3 i Das et al., 2021, eNeuro14. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Vi beskriver en enkel og effektiv protokol til at screene for forekomst af varmeinducerede anfald hos mus, den adfærdsmæssige ækvivalent af feberkramper hos humane patienter. Assayet evaluerer flere parametre – herunder procentdelen af mus, der viser anfald, anfaldstærskel, sværhedsgraden af anfald på en Racine-skala, for at sammenligne følsomheden af kontrol- og testmusgrupper til stigninger i kropstemperaturen.
Et kritisk trin i denne protokol indebærer at øge varmen i kammeret, mens musens kropstemperatur løbende overvåges. Det er bydende nødvendigt, at den maksimale kropstemperatur, musene vil opleve i disse analyser, er 44 °C, fordi vildtypedyr kan gennemgå varmeinducerede anfald ved kropstemperaturer >44 °C. Forbehandling med generel anæstesi eller smertestillende midler kan reducere dyrenes kropstemperatur eller forstyrre termoreguleringen, hvilket igen ville forvirre indsamlingen af data om anfaldstærskeltemperaturen. Således kunne mus under denne screeningsprotokol ikke forsynes med disse midler i løbet af 30 minutters forsøgsvinduet. Alle procedurer skal godkendes af institutionens IACUC-udvalg. For at sikre kontinuerlig overvågning af musens kernekropstemperatur under analysen skal du tape den rektale temperatursonde sikkert til musens hale. Hvis musens kropstemperatur under analysen viser sig at forblive uændret i længere perioder, selv efter at have øget temperaturen i musekammeret, skal du sørge for, at den rektale temperatursonde ikke er kommet ud af musen eller er fastgjort løst til halen.
Musemodellernes genetiske baggrund kan påvirke følsomheden over for SCN1A-mutationen og farmakologisk inducerede anfald18,25,26,27. Som diskuteret i resultaterne ovenfor kan musenes genetiske baggrund påvirke deres modtagelighed for varmeinducerede anfald. Scn1a K1270T GEFS+ mutante mus blev testet med to genetiske baggrunde – 129X1 og B6NJ, og en lille procentdel af vildtypemus (33 %) i den anfaldsfølsomme B6NJ-baggrund blev også observeret at gennemgå varmeinducerede anfald. I sammenligning med de heterozygote mutante Scn1aKT/+-mus oplevede B6NJ-vildtypemusene imidlertid varmeinducerede anfald ved en signifikant højere temperaturtærskel. Dette bekræfter, at den genetiske mutation (Scn1a K1270T), der blev introduceret ved CRISPR-knock-in, gør de mutante mus mere modtagelige for hypertermi-inducerede anfald.
Der er flere fordele ved at vedtage denne protokol, som er opsummeret nedenfor. For det første giver en temperaturstyret tvungen luft, der er oprettet i et lukket rum, i modsætning til brugen af strøm af tør luft eller opvarmede lamper eksperimentatoren mere kontrol over opvarmning af testarenaen med en ønsket hastighed. Trinene i opvarmningsprotokollen kan let ændres for at øge / mindske starttemperaturen, varigheden af hvert trin osv. For at screene ældre mus, der er tungere eller større gnavere, såsom rotter. For det andet giver kontinuerlig overvågning af musens kropstemperatur via den vedhæftede rektale sonde værdifuld information om hastigheden af kropstemperaturændringen i den enkelte mus gennem hele analysen. Dette gør det muligt for forsøgsdyrkeren nøje at observere, at musens temperaturændringshastighed ikke overstiger 0,25-0,5 °C/min (hvilket kan være stressende for dyrene), når denne protokol tilpasses til andre testarenaer. Det er vigtigt, at hastigheden af ændring af kropstemperaturen over tid i forskellige musegrupper kan kaste lys over deres evne til at termoregulere og kan være nyttigt at forstå, om feberkramper, der forårsager mutationer, også ændrer termoregulering hos mus. For det tredje sikrer kontinuerlig kropstemperaturovervågning, at målingerne af anfaldstærskeltemperaturen ved hjælp af denne protokol er nøjagtige, da de registreres samtidig med det første anfald, som musen oplevede. Hvis dyrets kropstemperatur ikke overvåges kontinuerligt, eller hvis anfaldstærskeltemperaturen måles efter at dyret er taget ud af testarenaen, kan anfaldstærskelværdierne variere på grund af den tid, det tager at håndtere musene efter anfald. Endelig omgår denne metode behovet for at anvende invasive metoder til at fremkalde feber (ved at injicere patogener) hos mus for at efterligne feberkramper hos humane patienter.
En af begrænsningerne ved denne protokol er, at det er vanskeligt at screene unge (mindre end P30 i alderen) mus for varmeinducerede anfald. Protokollen blev udviklet til at screene for følsomhed hos voksne mus (P30-P40 og derover) over for varme- eller hypertermi-inducerede anfald. Efter vores erfaring er de yngre vildtypemus, især dem, der vejer under 15 g, mere tilbøjelige til at gennemgå varmeinducerede anfald, hvilket kan skyldes underudviklede termoreguleringsmekanismer, fysiologisk termisk stress eller en kombination af begge. Derfor er det ikke ideelt at udføre den varmeinducerede anfaldsskærm på unge mus ved hjælp af denne protokol.
Fremtidige undersøgelser, der kombinerer EEG-overvågning, mens musen udsættes for varmeinducerede anfald, kan kaste lys over EEG-anfaldsmønstre af varmeinducerede anfald, svarende til en tidligere undersøgelse19. Neuronal aktivitet i bestemte områder i musehjernen kan spores ved at kombinere optogenetiske tilgange og immunhistokemibaserede undersøgelser efter høst af hjernevævet. Virkningerne af restriktive diæter såsom keto-diæt på reduktion af feberkramper kan også evalueres ved at udsætte keto-fodrede mus og normale chow-fodrede mus for varmeinduceret anfaldsprotokol. Tilsvarende kan epilepsilægemiddelscreeningsparadigmer udvikles til at teste og identificere kandidat anti-epileptiske lægemidler, der lindrer eller undertrykker varmeinducerede anfald hos lægemiddelfodrede eller behandlede mus sammenlignet med køretøjsfodrede eller kontrolmus.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Vi vil gerne takke Connor J. Smith for hans hjælp med at bygge det tilpassede musevarmekammer. Vi anerkender hjælp fra O’Dowd-laboratoriemedlemmer, Lisha Zeng og Andrew Salgado til standardisering af opvarmningsprotokollen i de tidlige stadier af assayudviklingen. Vi takker også Danny Benavides og Kumar Perinbam for videooptagelse af dele af den eksperimentelle procedure for manuskriptet. Dette arbejde blev støttet af NIH-bevillingen (NS083009), der blev tildelt D.O.D.
Materials
| Axial fan | Farnam | AF20-200-120-xx10-3.1 | Farnam custom products -Axial Fan Heater with Fan |
| Digital temperature controller | Inkbird | ITC-100RH | Inkbird digital PID temperature controller ITC-100RH with K thermocouple |
| Mouse rectal temperature probe | ThermoWorks, Braintree Scientific, Inc | RET-3 | Mouse rectal temperature probe with thermometer |
References
- Hirtz, D., et al. How common are the ‘common’ neurologic disorders. Neurology. 68, 326-337 (2007).
- Catterall, W. A. Sodium Channel Mutations and Epilepsy. Jasper’s Basic Mechanisms of the Epilepsies. , (2012).
- Mantegazza, M., Broccoli, V. SCN 1A /Na V 1.1 channelopathies: Mechanisms in expression systems, animal models, and human iPSC models. Epilepsia. 60, (2019).
- Stafstrom, C. E. Persistent Sodium Current and Its Role in Epilepsy. Epilepsy Currents. 7, 15-22 (2007).
- Schutte, S. S., Schutte, R. J., Barragan, E. V., O’Dowd, D. K. Model systems for studying cellular mechanisms of SCN1A-related epilepsy. Journal of Neurophysiology. 115, 1755-1766 (2016).
- Wei, F., et al. Ion Channel Genes and Epilepsy: Functional Alteration, Pathogenic Potential, and Mechanism of Epilepsy. Neuroscience Bulletin. 33, 455-477 (2017).
- Abou-Khalil, B., et al. Partial and generalized epilepsy with febrile seizures plus and a novel SCN1A mutation. Neurology. 57, 2265-2272 (2001).
- Zhang, Y. -. H., et al. Genetic epilepsy with febrile seizures plus: Refining the spectrum. Neurology. 89, 1210-1219 (2017).
- Patterson, K. P., et al. Enduring memory impairments provoked by developmental febrile seizures are mediated by functional and structural effects of neuronal restrictive silencing factor. Journal of Neuroscience. 37, 3799-3812 (2017).
- Rossi, M. A. SCN1A and febrile seizures in mesial temporal epilepsy: An early signal to guide prognosis and treatment. Epilepsy Currents. 14, 189-190 (2014).
- Zhang, Y., et al. Altered gut microbiome composition in children with refractory epilepsy after ketogenic diet. Epilepsy Research. 145, 163-168 (2018).
- Meng, H., et al. The SCN1A mutation database: Updating information and analysis of the relationships among genotype, functional alteration, and phenotype. Human Mutation. 36, 573-580 (2015).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Das, A., et al. Interneuron dysfunction in a new mouse model of SCN1A GEFS. eNeuro. , (2021).
- Kalume, F., et al. Sudden unexpected death in a mouse model of Dravet syndrome. Journal of Clinical Investigations. 123, 1798-1808 (2013).
- Martin, M. S., et al. Altered function of the SCN1A voltage-gated sodium channel leads to gamma-aminobutyric acid-ergic (GABAergic) interneuron abnormalities. Journal of Biological Chemistry. 285, 9823-9834 (2010).
- Rubinstein, M., et al. Dissecting the phenotypes of Dravet syndrome by gene deletion. Brain. 138, 2219-2233 (2015).
- Yu, F. H., et al. Reduced sodium current in GABAergic interneurons in a mouse model of severe myoclonic epilepsy in infancy. Nature Neuroscience. 9, 1142-1149 (2006).
- Dutton, S. B. B., et al. Early-life febrile seizures worsen adult phenotypes in Scn1a mutants. Experimental Neurology. 293, 159-171 (2017).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Oakley, J. C., Cho, A. R., Cheah, C. S., Scheuer, T., Catterall, W. A. Synergistic GABA-enhancing therapy against seizures in a mouse model of Dravet Syndrome. Journal of Pharmacology and Experimental Therapeutics. 345, 215-224 (2013).
- Ricobaraza, A., et al. Epilepsy and neuropsychiatric comorbidities in mice carrying a recurrent Dravet syndrome SCN1A missense mutation. Scientific Reports. 9, (2019).
- Warner, T. A., Liu, Z., Macdonald, R. L., Kang, J. -. Q. Heat induced temperature dysregulation and seizures in Dravet Syndrome/GEFS+ Gabrg2+/Q390X mice. Epilepsy Research. 134, 1-8 (2017).
- Eun, B. -. L., Abraham, J., Mlsna, L., Kim, M. J., Koh, S. Lipopolysaccharide potentiates hyperthermia-induced seizures. Brain and Behavior. 5, 00348 (2015).
- Miller, A. R., Hawkins, N. A., McCollom, C. E., Kearney, J. A. Mapping genetic modifiers of survival in a mouse model of Dravet syndrome. Genes Brain and Behavior. 13, 163-172 (2013).
- Mistry, A. M., et al. Strain- and age-dependent hippocampal neuron sodium currents correlate with epilepsy severity in Dravet syndrome mice. Neurobiology of Disease. 65, 1-11 (2014).
- Ogiwara, I., et al. Nav1.1 localizes to axons of parvalbumin-positive inhibitory interneurons: a circuit basis for epileptic seizures in mice carrying an Scn1a gene mutation. Journal of Neuroscience. 27, 5903-5914 (2007).

