Fabrication et utilisation d’échafaudages d’alginate macroporeux secs pour la transduction virale des lymphocytes T
Summary
Voici un protocole pour créer des échafaudages d’alginate macroporeux secs qui interviennent dans le transfert efficace de gènes viraux pour une utilisation dans le génie génétique des cellules T, y compris les cellules T pour la thérapie cellulaire CAR-T. Il a été démontré que les échafaudages transduisaient les lymphocytes T primaires activés avec une transduction de >85%.
Abstract
Le génie génétique des lymphocytes T pour la thérapie cellulaire CAR-T est devenu au premier plan du traitement du cancer au cours des dernières années. Les cellules CAR-T sont produites par transfert de gènes viraux dans les cellules T. L’étalon-or actuel du transfert de gènes viraux implique la spinoculation de plaques recouvertes de rétronectine, ce qui est coûteux et prend beaucoup de temps. Il existe un besoin important de méthodes efficaces et rentables pour générer des cellules CAR-T. La méthode décrite ici est une méthode de fabrication d’échafaudages d’alginate macroporeux secs et peu coûteux, connus sous le nom d’échafaudages Drydux, qui favorisent efficacement la transduction virale des cellules T activées. Les échafaudages sont conçus pour être utilisés à la place de la spinoculation de référence des plaques enrobées de rétronectine ensemencées avec des virus et simplifient le processus de transmission des cellules. L’alginate est réticulé avec du gluconate de calcium D et congelé pendant la nuit pour créer les échafaudages. Les échafaudages congelés sont lyophilisés dans un lyophilisateur pendant 72 h pour compléter la formation des échafaudages macroporeux secs. Les échafaudages servent de médiateur au transfert de gènes viraux lorsque le virus et les lymphocytes T activés sont ensemencés ensemble sur le dessus de l’échafaudage pour produire des cellules génétiquement modifiées. Les échafaudages produisent >85% de transduction primaire des lymphocytes T, ce qui est comparable à l’efficacité de transduction de la spinoculation sur des plaques recouvertes de rétronectine. Ces résultats démontrent que les échafaudages d’alginate macroporeux secs constituent une alternative moins coûteuse et plus pratique à la méthode de transduction conventionnelle.
Introduction
L’immunothérapie est devenue un paradigme révolutionnaire de traitement du cancer en raison de sa capacité à cibler spécifiquement les tumeurs, à limiter la cytotoxicité hors cible et à prévenir les rechutes. En particulier, la thérapie cellulaire à récepteur antigénique chimérique T (CAR-T) a gagné en popularité en raison de son succès dans le traitement des lymphomes et des leucémies. La FDA a approuvé la première thérapie cellulaire CAR-T en 2017 et, depuis lors, a approuvé quatre autres thérapies cellulaires CAR-T 1,2,3,4,5. Les CARs ont un domaine de reconnaissance d’antigène généralement constitué d’un fragment variable à chaîne unique d’un anticorps monoclonal spécifique d’un antigène associé à une tumeur 3,4. Lorsqu’un CAR interagit avec son antigène associé à la tumeur, les cellules CAR-T s’activent, entraînant une réponse antitumorale impliquant la libération de cytokines, la dégranulation cytolytique, l’expression du facteur de transcription et la prolifération des lymphocytes T. Pour produire des cellules CAR-T, le sang est prélevé sur le patient pour obtenir ses cellules T. Les CARs sont génétiquement ajoutés aux lymphocytes T du patient à l’aide d’un virus. Les cellules CAR-T sont cultivées in vitro et réinjectées au patient 2,3,4,6. La génération réussie de cellules CAR-T est déterminée par l’efficacité de transduction, qui décrit le nombre de cellules T génétiquement modifiées en cellules CAR-T.
Actuellement, l’étalon-or pour la génération de cellules CAR-T est la spinoculation des lymphocytes T activés et du virus sur des plaques recouvertes de rétronectine 7,8. La transduction commence lorsque les particules virales s’engagent à la surface des lymphocytes T. La rétronectine favorise la colocalisation du virus et des cellules en augmentant l’efficacité de liaison entre les particules virales et les cellules, améliorant la transduction 7,8. La rétronectine ne fonctionne pas bien seule et doit être accompagnée d’une spinoculation, qui améliore le transfert de gènes en concentrant les particules virales et en augmentant la perméabilité de surface de la cellule T, ce qui facilite l’infection virale8. Malgré le succès de la spinoculation sur des plaques recouvertes de rétronectine, il s’agit d’un processus complexe qui nécessite plusieurs cycles d’essorage et des réactifs coûteux. Par conséquent, d’autres méthodes de transfert de gènes viraux plus rapides et moins coûteuses sont hautement souhaitables.
L’alginate est un polysaccharide anionique naturel largement utilisé dans l’industrie biomédicale en raison de son faible coût, de son bon profil d’innocuité et de sa capacité à former des hydrogels lors du mélange avec des cations divalents 9,10,11,12. L’alginate est un polymère conforme aux BPF et est généralement reconnu comme sûr (GRAS) par la FDA13. L’alginate de réticulation avec les cations crée des hydrogels stables souvent utilisés dans la cicatrisation des plaies, l’administration de petits médicaments chimiques et de protéines, et le transport cellulaire 9,10,11,12,14,15,16. En raison de ses excellentes propriétés gélifiantes, l’alginate est le matériau préféré pour créer des échafaudages poreux par lyophilisation10,17. Ces caractéristiques de l’alginate en font un candidat attrayant pour la production d’un échafaudage capable de servir de médiateur au transfert de gènes viraux de cellules activées.
On décrit ici un protocole de fabrication d’échafaudages d’alginate macroporeux secs, connus sous le nom d’échafaudages Drydux, qui transduisent statiquement les lymphocytes T par transfert de gènes viraux17,18. Le processus de fabrication de ces échafaudages est illustré à la figure 1. Ces échafaudages éliminent le besoin de spinoculation des plaques recouvertes de rétronectine. Les échafaudages d’alginate macroporeux favorisent l’interaction des particules virales et des lymphocytes T pour permettre un transfert efficace des gènes en une seule étape sans affecter la fonctionnalité et la viabilité des lymphocytes T modifiés17. Lorsqu’ils sont suivis correctement, ces échafaudages d’alginate macroporeux ont une efficacité de transduction d’au moins 80%, ce qui simplifie et raccourcit le processus de transduction virale.
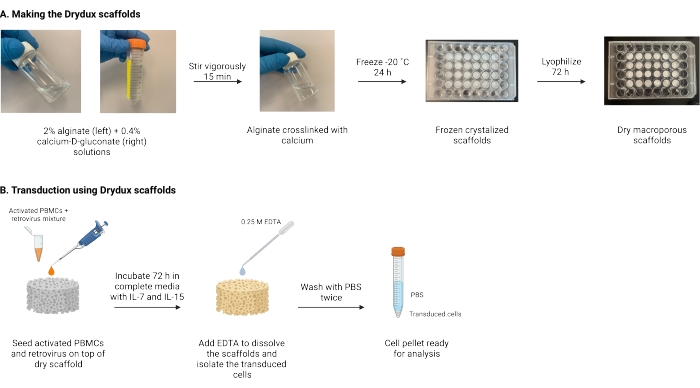
Figure 1 : Schéma et chronologie du protocole. (A) Calendrier de fabrication des échafaudages d’alginate macroporeux secs. L’alginate est réticulé avec le gluconate de calcium D et congelé pendant la nuit. Les échafaudages congelés sont lyophilisés pendant 72 h pour créer les échafaudages Drydux. (B) Chronologie de la transduction virale des cellules activées. Les cellules activées et le virus (MOI 2) sont ensemencés sur le dessus de l’échafaudage et incubés dans des milieux complets supplémentés en IL-7 et IL-15. Les échafaudages absorbent le mélange et favorisent le transfert de gènes viraux. L’EDTA est utilisé pour dissoudre les échafaudages et isoler les cellules transduites. Après avoir été lavé deux fois avec du PBS, le granulé de cellule peut être utilisé pour l’analyse. Abréviations : PBS = solution saline tamponnée au phosphate; PBMC = cellules mononucléées du sang périphérique. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Protocol
Representative Results
Discussion
La thérapie cellulaire CAR-T continue de susciter de l’intérêt pour la recherche et les applications commerciales. Malgré le succès de la thérapie cellulaire CAR-T dans le traitement des cancers du sang, le coût élevé de la procédure limite son utilisation. Le protocole présenté ici introduit une nouvelle méthode pour le transfert de gènes viraux de lymphocytes T sans avoir besoin de spinoculation de plaques recouvertes de rétronectine. La production d’échafaudages d’alginate macroporeux secs pour f…
Divulgations
The authors have nothing to disclose.
Acknowledgements
Ce travail a été soutenu par les National Institutes of Health par le biais des numéros d’attribution de subvention R37-CA260223, R21CA246414. Nous remercions le noyau de cytométrie en flux du NCSU pour sa formation et ses conseils sur l’analyse de cytométrie en flux. Les schémas ont été créés avec Biorender.com
Materials
| 0.5 M EDTA | Invitrogen | 15575-038 | UltraPure, pH 8.0 |
| 1x DPBS | Gibco | 14190-144 | No calcium chloride or magnesium chloride |
| 3% Acetic Acid with Methylene Blue | Stemcell Technologies Inc | 07060 | |
| Activated Periphreal Blood Mononuclear Cells | – | – | Fresh or frozen |
| Calcium-D-Gluconate | Alfa Aesar | A11649 | |
| CD28.2 Antibody | BD | 555725 | 1 mg/mL |
| CD3 Antibody | Miltenyi | 130-093-387 | 100 μg/mL |
| Click's Media | FUJIFILM IRVINE SCIENTIFIC MS | 9195 | |
| DI Water | – | – | |
| Glutamax | Gibco | 35-050-061 | |
| HyClone FBS | Cytvia | SH3039603 | |
| HyClone RPMI 1640 Media | Cytvia | SH3009601 | |
| Penicillin-streptomycin (P/S) | Gibco | 15-140-122 | |
| Peripheral Blood Mononuclear Cells | – | – | Fresh or frozen |
| PRONOVA UP MVG | NovaMatrix | 4200101 | Sodium alginate |
| Recombinant Human IL-15 | Peprotech | 200-15 | 5 ng/mL |
| Recombinant Human IL-7 | Peprotech | 200-07 | 10 ng/mL |
| Retrovirus | – | – | 1 x 106 TU/mL |
References
- Prinzing, B. L., Gottschalk, S. M., Krenciute, G. C. A. R. T-cell therapy for glioblastoma: ready for the next round of clinical testing. Expert Review of Anticancer Therapy. 18 (5), 451-461 (2018).
- Bagley, S. J., Desai, A. S., Linette, G. P., June, C. H., O’Rourke, D. M. CAR T-cell therapy for glioblastoma: recent clinical advances and future challenges. Neuro-oncology. 20 (11), 1429-1438 (2018).
- Nair, R., Westin, J. CAR T cells. Advances in Experimental Medicine and Biology. 1342, 297-317 (2021).
- Jackson, H. J., Rafiq, S., Brentjens, R. J. Driving CAR T-cells forward. Nature Reviews. Clinical Oncology. 13 (6), 370-383 (2016).
- Sterner, R. C., Sterner, R. M. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal. 11 (4), 69 (2021).
- Miliotou, A. N., Papadopoulou, L. C. CAR T-cell therapy: A new era in cancer immunotherapy. Current Pharmaceutical Biotechnology. 19 (1), 5-18 (2018).
- Lee, H. -. J., et al. Retronectin enhances lentivirus-mediated gene delivery into hematopoietic progenitor cells. Biologicals: Journal of the International Association of Biological Standardization. 37 (4), 203-209 (2009).
- Rajabzadeh, A., Hamidieh, A. A., Rahbarizadeh, F. Spinoculation and retronectin highly enhance the gene transduction efficiency of Mucin-1-specific chimeric antigen receptor (CAR) in human primary T cells. BMC Molecular and Cell Biology. 22 (1), 57 (2021).
- Sun, J., Tan, H. Alginate-based biomaterials for regenerative medicine applications. Materials. 6 (4), 1285-1309 (2013).
- Nayak, A. K., Mohanta, B. C., Hasnain, M. S., Hoda, M. N., Tripathi, G. Chapter 14 – Alginate-based scaffolds for drug delivery in tissue engineering. Alginates in Drug Delivery. , 359-386 (2020).
- Lee, K. Y., Mooney, D. J. Alginate: properties and biomedical applications. Progress in Polymer Science. 37 (1), 106-126 (2012).
- Kuo, C. K., Ma, P. X. Ionically crosslinked alginate hydrogels as scaffolds for tissue engineering: part 1. Structure, gelation rate and mechanical properties. Biomaterials. 22 (6), 511-521 (2001).
- Soccol, C., et al. Probiotic nondairy beverages. Handbook of Plant-Based Fermented Food and Beverage Technology, Second Edition. , 707-728 (2012).
- Moody, C. T., et al. Restoring carboxylates on highly modified alginates improves gelation, tissue retention and systemic capture. Acta Biomaterialia. 138, 208-217 (2022).
- Brudno, Y., et al. Replenishable drug depot to combat post-resection cancer recurrence. Biomaterials. 178, 373-382 (2018).
- Moody, C. T., Palvai, S., Brudno, Y. Click cross-linking improves retention and targeting of refillable alginate depots. Acta Biomaterialia. 112, 112-121 (2020).
- Agarwalla, P., et al. Scaffold-mediated static transduction of T Cells for CAR-T Cell therapy. Advanced Healthcare Materials. 9 (14), 2000275 (2020).
- Agarwalla, P., et al. Bioinstructive implantable scaffolds for rapid in vivo manufacture and release of CAR-T cells. Nature Biotechnology. 40 (8), 1250-1258 (2022).
- Vera, J., et al. T lymphocytes redirected against the kappa light chain of human immunoglobulin efficiently kill mature B lymphocyte-derived malignant cells. Blood. 108 (12), 3890-3897 (2006).
- . PRONOVA UP MVG. IFF Nutrition Norge AS Available from: https://novamatrix.biz/store/pronova-up-mvg/ (2022)
- Zappasodi, R., Budhu, S., Abu-Akeel, M., Merghoub, T. In vitro assays for effector T cell functions and activity of immunomodulatory antibodies. Methods in Enzymology. 631, 43-59 (2020).
- Kong, B. S., Lee, C., Cho, Y. M. Protocol for the assessment of human T cell activation by real-time metabolic flux analysis. STAR Protocols. 3 (1), 101084 (2022).
- Bio-Rad cell activation protocols. Bio-Rad Available from: https://www.bio-rad-antibodies.com/cell-activation.html?JSESSIONID_STERLING=D6E538F76818E53C29884D6CC7334F24 (2022)
- Lin, H. -. R., Yeh, Y. -. J. Porous alginate/hydroxyapatite composite scaffolds for bone tissue engineering: Preparation, characterization, andin vitro studies. Journal of Biomedical Materials Research. 71 (1), 52-65 (2004).
- Wu, J., Zhao, Q., Sun, J., Zhou, Q. Preparation of poly(ethylene glycol) aligned porous cryogels using a unidirectional freezing technique. Soft Matter. 8 (13), 3620 (2012).

