التحضير وتلطيخ التألق المناعي للحزم وخلايا الألياف المفردة من قشرة ونواة عدسة العين
Summary
يصف هذا البروتوكول طرقا لإعداد خلايا ألياف عدسة العين المحيطية والناضجة والنووية للتلطيخ المناعي لدراسة التداخل المعقد من خلية إلى أخرى وبنية الغشاء.
Abstract
العدسة عبارة عن عضو شفاف وبيضاوي الشكل في الحجرة الأمامية للعين يتغير شكله لتركيز الضوء بدقة على شبكية العين لتشكيل صورة واضحة. يتكون الجزء الأكبر من هذا النسيج من خلايا ليفية متخصصة ومتمايزة لها مقطع عرضي سداسي وتمتد من القطب الأمامي إلى القطب الخلفي للعدسة. هذه الخلايا الطويلة والنحيفة تعارض بشدة الخلايا المجاورة ولها تداخلات معقدة على طول الخلية. الهياكل المتشابكة المتخصصة مطلوبة للخصائص الميكانيكية الحيوية العادية للعدسة وقد تم وصفها على نطاق واسع باستخدام تقنيات المجهر الإلكتروني. يوضح هذا البروتوكول الطريقة الأولى للحفاظ على وتلوين المفرد وكذلك حزم خلايا ألياف عدسة الماوس للسماح بالتوطين التفصيلي للبروتينات داخل هذه الخلايا ذات الشكل المركب. توضح البيانات التمثيلية تلطيخ خلايا الألياف الطرفية والتمايزية والناضجة والنووية في جميع مناطق العدسة. يمكن استخدام هذه الطريقة على خلايا الألياف المعزولة من عدسات الأنواع الأخرى.
Introduction
العدسة عبارة عن نسيج شفاف وبيضاوي الشكل في الحجرة الأمامية للعين يتكون من نوعين من الخلايا ، الخلايا الظهارية والليفية 1 (الشكل 1). هناك طبقة أحادية من الخلايا الظهارية التي تغطي نصف الكرة الأمامي للعدسة. تتمايز الخلايا الليفية عن الخلايا الطلائية، وتشكل الجزء الأكبر من العدسة. تخضع خلايا الألياف عالية التخصص لبرمجة الاستطالة والتمايز والنضج ، والتي تتميز بتغيرات واضحة في مورفولوجيا غشاء الخلية من محيط العدسة إلى مركز العدسة2،3،4،5،6،7،8،9،10،11،12، المعروف أيضا باسم نواة العدسة. تعتمد وظيفة العدسة في التركيز الدقيق للضوء القادم من مسافات مختلفة على شبكية العين على خصائصها الميكانيكية الحيوية ، بما في ذلك الصلابة والمرونة13،14،15،16،17،18،19. تم افتراض التداخلات المعقدة لألياف العدسة20,21 وثبت مؤخرا أنها مهمة لصلابةالعدسة 22,23.
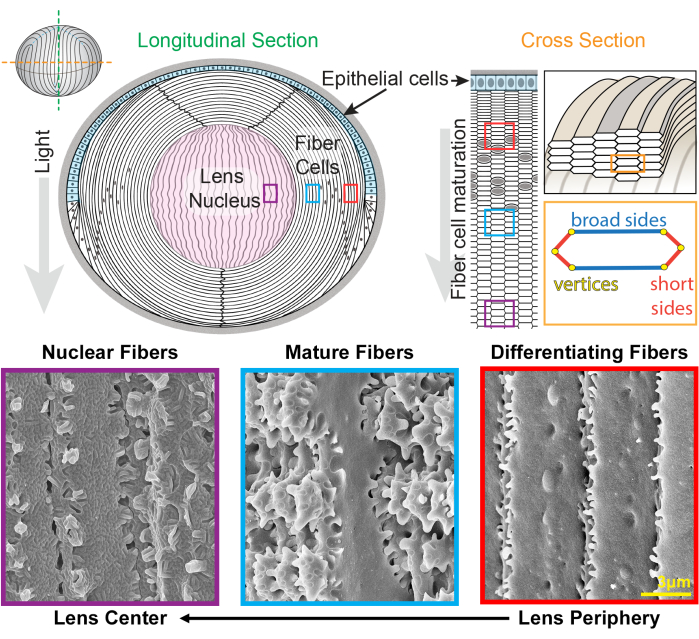
الشكل 1: مخططات تشريح العدسة وصور المجهر الإلكتروني الماسح التمثيلي (SEM) من ألياف العدسة. يظهر الرسم الكاريكاتوري منظرا طوليا (من الأمام إلى الخلف من الأعلى إلى الأسفل) للطبقة الأحادية الأمامية للخلايا الظهارية (مظللة باللون الأزرق الفاتح) وكتلة كبيرة من خلايا ألياف العدسة (بيضاء). يعرف مركز العدسة (المظلل باللون الوردي) باسم النواة ويتكون من خلايا ليفية مضغوطة للغاية. على اليمين ، يكشف رسم كاريكاتوري مقطع عرضي عن شكل الخلية السداسية الممدودة لألياف العدسة المعبأة في نمط قرص العسل. الخلايا الليفية لها جانبان عريضان وأربعة جوانب قصيرة. تظهر صور SEM التمثيلية على طول الجزء السفلي التداخل الغشائي المعقد بين خلايا ألياف العدسة على أعماق مختلفة من العدسة. من اليمين ، تحتوي ألياف العدسة المشكلة حديثا في محيط العدسة على نتوءات صغيرة على طول الجوانب القصيرة والكرات والمقابس على طول الجانب العريض (الصناديق الحمراء). أثناء النضج ، تطور ألياف العدسة مجالات مجداف كبيرة مزينة بنتوءات صغيرة على طول الجوانب القصيرة (الصناديق الزرقاء). تحتوي خلايا الألياف الناضجة على مجالات مجداف كبيرة موضحة بنتوءات صغيرة. هذه المجالات المتشابكة مهمة للخصائص الميكانيكية الحيوية للعدسة. تحتوي الخلايا الليفية في نواة العدسة على عدد أقل من النتوءات الصغيرة على طول جوانبها القصيرة ولها تداخلات معقدة بين اللسان والأخدود (مربعات أرجوانية). تعرض الجوانب العريضة للخلية مورفولوجيا غشاء كروي. تم تعديل الرسوم المتحركة من22,32 ولم يتم رسمها على نطاق واسع. شريط المقياس = 3 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
تنمو العدسة عن طريق إضافة أغلفة من خلايا الألياف الجديدة المتراكبة فوق الأجيال السابقة من الألياف24,25. الخلايا الليفية لها شكل مقطع عرضي سداسي ممدود مع جانبين عريضين وأربعة جوانب قصيرة. تمتد هذه الخلايا من القطب الأمامي إلى القطب الخلفي للعدسة ، واعتمادا على الأنواع ، يمكن أن يصل طول ألياف العدسة إلى عدة ملليمترات. لدعم بنية هذه الخلايا الممدودة والنحيفة ، تخلق التداخلات المتخصصة على طول الجانبين العريض والقصير هياكل متشابكة للحفاظ على شكل العدسة والخصائص الميكانيكية الحيوية. تم توثيق التغييرات في شكل غشاء الخلية أثناء تمايز الخلايا الليفية ونضجها على نطاق واسع من خلال دراسات المجهر الإلكتروني (EM)2،3،4،5،6،7،8،9،10،20،26،27،28،29. تحتوي الخلايا الليفية المشكلة حديثا على كرات ومآخذ على طول جوانبها العريضة مع نتوءات صغيرة جدا على طول جوانبها القصيرة ، بينما تحتوي الألياف الناضجة على نتوءات ومجاديف متشابكة على طول جوانبها القصيرة. تعرض الألياف النووية تداخلات اللسان والأخدود ومورفولوجيا الغشاء الكروي. لا يعرف سوى القليل عن البروتينات المطلوبة لهذه الأغشية المتشابكة المعقدة. اعتمدت الدراسات السابقة حول توطين البروتين في خلايا الألياف على أقسام أنسجة العدسة ، والتي لا تسمح بتصور واضح لبنية الخلية المعقدة.
ابتكر هذا العمل وأتقن طريقة جديدة لإصلاح خلايا ألياف العدسة المفردة والحزم للحفاظ على التشكل المعقد والسماح بتلطيخ المناعة للبروتينات في غشاء الخلية وداخل السيتوبلازم. تحافظ هذه الطريقة بأمانة على بنية غشاء الخلية ، مقارنة بالبيانات من دراسات EM ، وتسمح بتلطيخ الأجسام المضادة الأولية لبروتينات معينة. لقد سبق لنا أن خضعنا ألياف العدسات القشرية الملطخة بالمناعة والتي تخضع للتمايز والنضج22,23. في هذا البروتوكول ، هناك أيضا طريقة جديدة لتلطيخ خلايا الألياف من نواة العدسة. يفتح هذا البروتوكول الباب لفهم آليات التكوين والتغيرات في تداخل الغشاء أثناء نضوج الخلايا الليفية وضغط نواة العدسة.
Protocol
Representative Results
Discussion
وقد أظهر هذا البروتوكول طرق التثبيت والحفظ والمناعة التي تحافظ بأمانة على مورفولوجيا غشاء 3D للحزم أو خلايا ألياف العدسة المفردة من أعماق مختلفة في العدسة. تتم مقارنة ألياف العدسة الملطخة مع مستحضرات SEM التي تستخدم منذ فترة طويلة لدراسة مورفولوجيا خلايا ألياف العدسة. تظهر النتائج هياكل غش…
Divulgations
The authors have nothing to disclose.
Acknowledgements
تم دعم هذا العمل من خلال منحة R01 EY032056 (إلى CC) من المعهد الوطني للعيون. يشكر المؤلفون الدكتورة تيريزا فاسيل وكيمبرلي فاندربول في مرفق سكريبس للأبحاث المجهرية الأساسية لمساعدتهم في صور المجهر الإلكتروني.
Materials
| 100% Triton X-100 | FisherScientific | BP151-500 | |
| 60mm plate | FisherScientific | FB0875713A | |
| 16% paraformaldehyde | Electron Microscopy Sciences | 15710 | |
| 10X phosphate buffered saline | ThermoFisher | 70011-044 | |
| 1X phosphate buffered saline | ThermoFisher | 14190136 | |
| 48-well plate | CytoOne | CC7672-7548 | |
| Cover slips (22 x 40 mm) | FisherScientific | 12-553-467 | |
| Curved tweezers | World Precision Instruments | 501981 | |
| Dissection microscope | Carl Zeiss | Stereo Discovery V8 | |
| Fine tip straight tweezers | Electron Microscopy Sciences | 72707-01 | |
| Fisherbrand Superfrost Plus Microscope Slides | FisherScientific | 12-550-15 | |
| LSM 800 confocal microscope with Airyscan (63X) and Zen 3.5 Software | Carl Zeiss | ||
| Nail polish | |||
| Normal donkey serum | Jackson ImmunoResearch | 017-000-121 | |
| Phalloidin (rhodamine) | ThermoFisher | R415 | |
| Primary antibody | |||
| Scalpel Feather Disposable, steril, No. 11 | VWR | 76241-186 | |
| Secondary antibody | |||
| Straight forceps | World Precision Instruments | 11252-40 | |
| Thermo Scientific Nunc MicroWell MiniTrays (dissection tray) | FisherScientific | 12-565-154 | |
| Ultra-fine scissors | World Precision Instruments | 501778 | |
| VECTASHIELD Antifade Mounting Medium with DAPI | Vector Laboratories | H-1200 | |
| Wheat germ agglutinin (fluorescein) | Vector Laboratories | FL-1021-5 |
References
- Lovicu, F. J., McAvoy, J. W. Growth factor regulation of lens development. Biologie du développement. 280 (1), 1-14 (2005).
- Kuszak, J., Alcala, J., Maisel, H. The surface morphology of embryonic and adult chick lens-fiber cells. The American Journal of Anatomy. 159 (4), 395-410 (1980).
- Kuszak, J. R. The ultrastructure of epithelial and fiber cells in the crystalline lens. International Review of Cytology. 163, 305-350 (1995).
- Kuszak, J. R., Macsai, M. S., Rae, J. L. Stereo scanning electron microscopy of the crystalline lens. Scanning Electron Microscopy. , 1415-1426 (1983).
- Lo, W. K., Harding, C. V. Square arrays and their role in ridge formation in human lens fibers. Journal of Ultrastructure Research. 86 (3), 228-245 (1984).
- Taylor, V. L., et al. Morphology of the normal human lens. Investigative Ophthalmology & Visual Science. 37 (7), 1396-1410 (1996).
- Vrensen, G. F. Aging of the human eye lens-a morphological point of view. Comparative Biochemistry and Physiology. Part A, Physiology. 111 (4), 519-532 (1995).
- Vrensen, G. F., Duindam, H. J. Maturation of fiber membranes in the human eye lens. Ultrastructural and Raman microspectroscopic observations. Ophthalmic Research. 27, 78-85 (1995).
- Willekens, B., Vrensen, G. The three-dimensional organization of lens fibers in the rabbit. A scanning electron microscopic reinvestigation. Albrecht von Graefe’s Archive for Clinical and Experimental Opthalmology. 216 (4), 275-289 (1981).
- Willekens, B., Vrensen, G. The three-dimensional organization of lens fibers in the rhesus monkey. Graefe’s Archive for Clinical and Experimental Ophthalmology. 219 (3), 112-120 (1982).
- Zhou, C. J., Lo, W. K. Association of clathrin, AP-2 adaptor and actin cytoskeleton with developing interlocking membrane domains of lens fibre cells. Experimental Eye Research. 77 (4), 423-432 (2003).
- Kuwabara, T. The maturation of the lens cell: a morphologic study. Experimental Eye Research. 20 (5), 427-443 (1975).
- Weeber, H. A., Eckert, G., Pechhold, W., vander Heijde, R. G. Stiffness gradient in the crystalline lens. Graefe’s Archive for Clinical and Experimental Ophthalmology. 245 (9), 1357-1366 (2007).
- Weeber, H. A., et al. Dynamic mechanical properties of human lenses. Experimental Eye Research. 80 (3), 425-434 (2005).
- Weeber, H. A., vander Heijde, R. G. On the relationship between lens stiffness and accommodative amplitude. Experimental Eye Research. 85 (5), 602-607 (2007).
- Heys, K. R., Cram, S. L., Truscott, R. J. Massive increase in the stiffness of the human lens nucleus with age: the basis for presbyopia. Molecular Vision. 10, 956-963 (2004).
- Heys, K. R., Friedrich, M. G., Truscott, R. J. Presbyopia and heat: changes associated with aging of the human lens suggest a functional role for the small heat shock protein, alpha-crystallin, in maintaining lens flexibility. Aging Cell. 6 (6), 807-815 (2007).
- Glasser, A., Campbell, M. C. Biometric, optical and physical changes in the isolated human crystalline lens with age in relation to presbyopia. Vision Research. 39 (11), 1991-2015 (1999).
- Pierscionek, B. K. Age-related response of human lenses to stretching forces. Experimental Eye Research. 60 (3), 325-332 (1995).
- Biswas, S. K., Lee, J. E., Brako, L., Jiang, J. X., Lo, W. K. Gap junctions are selectively associated with interlocking ball-and-sockets but not protrusions in the lens. Molecular Vision. 16, 2328-2341 (2010).
- Lo, W. K., et al. Aquaporin-0 targets interlocking domains to control the integrity and transparency of the eye lens. Investigative Ophthalmology & Visual Science. 55 (3), 1202-1212 (2014).
- Cheng, C., et al. Tropomyosin 3.5 protects the F-actin networks required for tissue biomechanical properties. Journal of Cell Science. 131 (23), (2018).
- Cheng, C., et al. Tropomodulin 1 regulation of actin is required for the formation of large paddle protrusions between mature lens fiber cells. Investigative Ophthalmology & Visual Science. 57 (10), 4084-4099 (2016).
- Kuszak, J. R. The development of lens sutures. Progress in Retinal and Eye Research. 14 (2), 567-591 (1995).
- Bassnett, S., Costello, M. J. The cause and consequence of fiber cell compaction in the vertebrate lens. Experimental Eye Research. 156, 50-57 (2017).
- Biswas, S., Son, A., Yu, Q., Zhou, R., Lo, W. K. Breakdown of interlocking domains may contribute to formation of membranous globules and lens opacity in ephrin-A5(-/-) mice. Experimental Eye Research. 145, 130-139 (2016).
- Blankenship, T., Bradshaw, L., Shibata, B., Fitzgerald, P. Structural specializations emerging late in mouse lens fiber cell differentiation. Investigative Ophthalmology & Visual Science. 48 (7), 3269-3276 (2007).
- Cheng, C., et al. Age-related changes in eye lens biomechanics, morphology, refractive index and transparency. Aging. 11 (24), 12497-12531 (2019).
- Cheng, C., et al. EphA2 affects development of the eye lens nucleus and the gradient of refractive index. Investigative Ophthalmology & Visual Science. 63 (1), 2 (2022).
- Cheng, C., Gokhin, D. S., Nowak, R. B., Fowler, V. M. Sequential application of glass coverslips to assess the compressive stiffness of the mouse lens: strain and morphometric analyses. Journal of Visualized Experiments. (111), e53986 (2016).
- Forrester, J. V., Dick, A. D., McMenamin, P. G., Roberts, F., Pearlman, E., Saunders, W. B. Anatomy of the eye and orbit. The Eye (Fourth Edition). , 1 (2016).
- Cheng, C., Nowak, R. B., Fowler, V. M. The lens actin filament cytoskeleton: Diverse structures for complex functions. Experimental Eye Research. 156, 58-71 (2017).
- Goldberg, M. W., Fiserova, J. Immunogold labeling for scanning electron microscopy. Methods in Molecular Biology. 1474, 309-325 (2016).
- Goldberg, M. W. High-resolution scanning electron microscopy and immuno-gold labeling of the nuclear lamina and nuclear pore complex. Methods in Molecular Biology. 1411, 441-459 (2016).
- Hermann, R., Walther, P., Muller, M. Immunogold labeling in scanning electron microscopy. Histochemistry and Cell Biology. 106 (1), 31-39 (1996).
- Gokhin, D. S., et al. Tmod1 and CP49 synergize to control the fiber cell geometry, transparency, and mechanical stiffness of the mouse lens. PLoS One. 7 (11), e48734 (2012).

