Karakterisering af G-protein-koblede receptorer med en fluorescens-baserede calciummobilisering Assay
Summary
Den her beskrevne fluorescens-baserede calcium mobilisering analysen er en medium-throughput omvendt farmakologi screening til identifikation af funktionelt aktiverende ligand (r) af forældreløse G-protein-koblede receptorer (GPCR).
Abstract
For mere end 20 år har omvendt farmakologi været det mest fremtrædende strategi for at opdage de aktiverende ligander af forældreløse G-protein-koblede receptorer (GPCR). Starten af et omvendt farmakologi analysen er kloning og efterfølgende transfektion af en GPCR af interesse i et cellulært ekspressionssystem. Den heterologe udtrykte receptor derefter udfordret med en forbindelse bibliotek af kandidat-ligander til at identificere receptor-aktiverende ligand (s). Receptor-aktivering kan vurderes ved måling af ændringer i koncentrationen af den anden messenger reportermolekyler, såsom calcium-eller cAMP. Fluorescens-baserede calciummobilisering assay beskrevet her er et hyppigt anvendt medium-throughput omvendt farmakologi assay. Den forældreløse GPCR er udtrykt transient i humane embryonale nyre 293T (HEK293T) celler og en promiskuøs Ga 16 konstruktion er cotransficeres. Efter ligand binding, aktivering af Ga 16 underenheden inducerer frigivelsen af calcium fra det endoplasmatiske reticulum. Forud for ligand screening, er receptor-udtrykkende celler fyldt med en fluorescerende calciumindikator, Fluo-4 acetoxymethyl. Den fluorescerende signal Fluo-4 er ubetydelig i celler under hvilebetingelser, men kan forstærkes mere end en 100-fold ved interaktion med calciumioner, der frigives efter receptor-aktivering. Den beskrevne teknik kræver ikke tidskrævende etablering af stabilt transficerede cellelinjer, hvor det transficerede genetiske materiale er integreret i værtscellens genom. I stedet en transient transfektion, genererer midlertidige ekspression af målgenet, er tilstrækkeligt til at udføre screening assay. Opsætningen giver medium-throughput screening af hundredvis af forbindelser. Co-transfektion af promiskuøs Ga 16, som kobler til de fleste GPCRs, tillader intracellulær signalvej at blive omdirigeret til frigivelsen af calcium, uanset den indfødte signalvej i endogene settsomheder. De HEK293T celler er nemme at håndtere og har bevist deres effektivitet gennem årene i receptor deorphanization assays. Kan dog være nødvendigt at opretholde optimering af analysen for specifikke receptorer.
Introduction
G-protein-koblede receptorer (GPCR) udgør en af de største og mest forskelligartede familier blandt alle celleoverfladeproteiner. Deres tilstedeværelse i hvirveldyr, hvirvelløse dyr, planter, gær og slim skimmel samt i protozoer og den tidligste diploblastic Metazoa indikerer, at GPCRs er blandt de ældste molekylerne er forbundet med signaltransduktion 1. Deres naturlige aktiverende ligander omfatter en bred vifte af eksterne stimuli, herunder peptider, biogene aminer, lugtstoffer, glycoproteiner, og fotoner 2. Som sådan er disse receptor-ligand-signalsystemer er involveret i en lang række fysiologiske processer. Den brede funktionelle spektrum gør dem velegnet til udvikling af terapeutiske lægemidler, der dækker et bredt spektrum af humane sygdomme. Omkring 50-60% af de nuværende lægemiddelkandidater er repræsenteret ved GPCRs 3,4. Udover deres stor betydning i den farmaceutiske industri, GPCR'er er også i fokus for udviklingen af enny generation af artsspecifikke insekticider 5,6 og pesticider i almindelighed. Fordi de naturlige ligander af mange GPCRs er stadig uidentificeret, er de klassificeret som sjældne GPCRs. Den deorphanization af disse receptorer, vil forbedre forståelsen af deres fysiologiske roller i organismer, og kan afsløre formodede mål for nye lægemidler 7.
Da den genomiske æra, er det omvendte farmakologi strategi almindeligt anvendt til deorphanization af GPCRs 8. Tilgangen indebærer, at en forældreløs receptor bruges som en 'krog' til 'fisk ud' sin aktiverende ligand fra en biologisk ekstrakt eller fra et bibliotek af syntetiske forbindelser. GPCR'en af interesse er derfor klonet og efterfølgende transficeres i et cellulært ekspressionssystem. I de mest almindeligt anvendte metoder er receptoraktivering bestemmes ved at måle ændringer i koncentrationen af second messenger-molekyler 9 </sup>. De vigtigste receptor screeningassays stole på calcium-følsomme bioluminiscerende proteiner (f.eks aequorin) 10 eller fluorescerende calcium indikatorer (f.eks, Fluo-4) 11.. De fluorescens-baserede assays, hvor receptor-udtrykkende celler er fyldt med et fluorescerende calciumindikator før ligand screening, har den fordel, at de tillader højkapacitetsscreening grundet deres brugervenlighed, kort læsning tid, og fleksibiliteten af screening flere forældreløse receptorer på en enkelt plade 12.
Her fluorescens-baserede calciummobilisering assay grundigt beskrevet og illustreret ved deorphanization proces Drosophila melanogaster korte neuropeptid F (sNPF) receptoren. Dette neuropeptidergic signalsystem blev oprindeligt karakteriseret ved Mertens et al. i 2002, 13 med en calcium bioluminescens assay udføres i kinesisk hamsterovarie (CHO) celler14 og af Feng et al. I 2003 med en elektrofysiologisk assay hjælp Xenopus-oocytter 15. Tilstedeværelsen af sNPF signalsystem synes at være begrænset til phylum af Arthropoda, hvor det er impliceret i en lang række processer, herunder regulering af fodring, vækst, stressreaktioner, bevægelse og døgnrytmen 16.
Forskning i neuropeptidergic signalsystemer i insekter ikke blot kan føre til nye mål for udvikling af insekticider, men viden om deres funktion kan også ekstrapoleres til andre organismer så mange signalsystemer har generelt været godt bevaret gennem evolution 17. I det sidste årti er der gjort store fremskridt i deorphanization proces insekt neuropeptid GPCRs. På trods af disse bestræbelser, har kun et lille antal af receptorer blevet matchet til deres beslægtede ligand, og masser af sekvens information fornye forældreløse GPCRs er blevet tilgængelige på grund af den boomende genomforskning 18. Tilgængeligheden af medium / high-throughput screening tilgange, ligesom fluorescens-baserede calcium mobilisering analyse, der har vist sig at være et almindeligt anvendt teknik 9,18, er derfor uvurderlig.
Fluorescens-baserede calciummobilisering assay som beskrevet her udføres i humane embryonale nyre 293T (HEK293T) cellelinie og bruger en fluorescerende probe til at bestemme ændringer i intracellulære calciumkoncentrationer ved receptor-aktivering. For at sikre høj ekspression og oversættelse niveauer af receptoren, er en Kozak-konsensussekvens 19 tilføjes til 5'-enden af det receptorkodende sekvens, der efterfølgende klonet i en ekspressionsvektor (f.eks pcDNA vektor serie for mammale cellelinier). Da det er vanskeligt at forudsige den endogene G-protein-kobling af sjældne GPCR baseret på sekvens informationalene, second messenger-molekyler (fx calcium-eller cAMP), der er moduleret efter receptoraktivering ofte forbliver ukendt før ligand identifikation. For at omgå dette problem, promiskuøse G-proteiner af G q familien (fx murine Ga 15 eller humant Ga 16 [bruges her]) eller kimære G-proteiner (f.eks Ga qi5), der interagerer med de fleste GPCRs og inducere frigivelse af calcium kan co-udtrykt 20,21,22. Ved binding af ligand til dens receptor, GPCR undergår en konformationel ændring, der fører til aktivering af specifikke intracellulære signalveje. Den guanosin difosfat (BNP) molekyle bundet under hvile betingelser til Ga 16-underenheden, vil blive erstattet af en guanosintriphosphat (GTP) molekyle. Dette provokerer dissociation af heterotrimere G-protein i en Ga 16 og Gβγ underenhed. Den Ga 16 underenheden aktiverer phospholipase C &# 946; (PLCβ), som igen hydrolyserer membranbundet phosphatidylinositol bisphosphat (PIP2), hvilket resulterer i diacylglycerol (DAG) og inositoltriphosphat (IP3). IP3 vil sprede sig over hele cytoplasmaet og aktiverer IP 3-afhængige calciumkanaler er til stede i membranen af det endoplasmatiske reticulum, der inducerer frigivelse af calcium ind i cytoplasmaet.
Calcium-frigivelse ved receptor-aktivering sker inden for sekunder, og kan detekteres ved at fylde celler, før screeningsassayet med en calcium-sensitive farvestof, som Fluo-4 acetoxymethyl (AM) 11. AM estergruppe giver fluorofor til at krydse cellemembranen og fraspaltes af cytoplasmiske esteraser gang inde i cellen. Derfor er den negative ladning af det fluorescerende farvestof afsløret, forhindrer det i at diffundere ud af cellen og gør det muligt at interagere med calciumioner. Den fluorescerende signal of Fluo-4 er ubetydelig i celler under hvilebetingelser kun indeholder calcium koncentrationer i nanomolære område. Men når calcium frigives ved receptor-aktivering, kan signalet øge koncentrationsafhængigt til mere end 100 gange, herved sikres en stor signal-til-støj-forhold. Fluo-4 også udviser et stort dynamikområde for rapportering [calcium] omkring en Kd (calcium) på 345 nM, hvilket gør den velegnet til at måle fysiologisk relevante calcium ændringer i en bred vifte af celler. Excitation af Fluo-4 sker ved 488 nm og emission fluorescens måles ved 525 nm 11. Fluorimeters som fluorescensimagografi pladelæser (FLIPR) 23, Novostars eller FlexStation (station enhed) er 12 medium / high-throughput systemer, der tillader samtidig forbindelse tilsætning og påvisning af Fluo-4 signal ved receptor-aktivering til hver brønd i et assay plade. Den calciummobilisering assayet beskrevet her er baseret på stationenenhed 96-brønds mikroplade system.
Den Softmax Pro-software (software) bruges til at betjene stationen enheden samt til dataanalyse. Programmet viser straks resultaterne som grafer i 96-brønds format. Flere brønde kan vælges samtidigt for at sammenligne resultaterne af disse brønde på den samme graf. Den relative fluorescerende enhed (RFU) værdier af brønde i hver søjle samtidigt målt i en periode på to minutter, startende før tilsætning af forbindelser til brøndene, og fortsætter efter måling af fluorescenssignalet efter receptor-aktivering. Typisk tendensen i en agonist kurve flugter med grundlinjen indtil en aktiverende forbindelse tilsættes til cellerne, hvilket resulterer i en hurtig stigning af det fluorescerende signal. Den maksimale højde er korreleret med den endelige agonist koncentration i brønden. Efter højdepunktet det fluorescerende signal langsomt falder mod basisniveauet. RFU målinger can omdannes til koncentrations-respons-kurver for at bestemme EC50-værdi (halv maksimal effektiv koncentration) for en ligand. I almindelighed, mindst tre uafhængige skærme, hver med tre kopier af en fusion serie, bør foretages for at komponere en pålidelig koncentration-respons-kurve.
Det anbefales at omfatte flere positive og negative kontroller i den eksperimentelle design. Først og fremmest en transfektion kontrol, dvs gennemførelsen af en receptor med en kendt ligand, bør afprøves. Dette gør det muligt at kontrollere, om transfektion agent var i drift. Inkorporering af et kontrolforsøg med en agonist til en endogen receptor cellelinien og en negativ kontrol (fx vaskebuffer) anbefales også at overvåge sundheden og levedygtigheden af cellerne og at udelukke muligheden for, at vaskepufferen var forurenet med en faktor, der kan fremkalde en auto-fluoreduft respons. Ofte anvendte agonister er et peptid afledt af protease-aktiveret receptor-1 (PAR 1), der fungerer som et PAR-1 selektiv agonist eller carbachol, der aktiverer acetylcholinreceptoren. Celler transficeret med en tom ekspressionsvektor bør også testet for at udelukke, at aktive forbindelser interagerer med cellens endogene receptorer. Kan være påkrævet optimering af flere parametre, der er beskrevet i protokollen nedenfor for forskellige signalsystemer. En skematisk figur af den komplette fluorescens-baserede calciummobilisering assay er vist i figur 1.
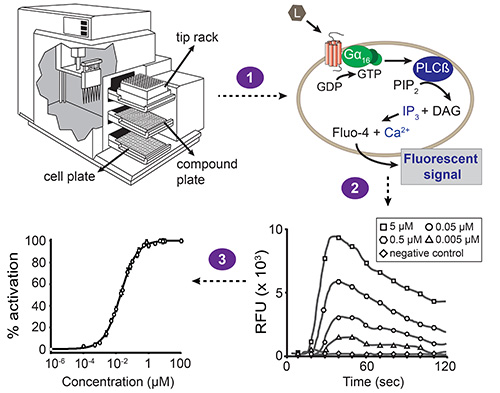
Figur 1.. Overordnet plan for fluorescens-baserede calcium mobilisering assay. Automatiseret væske håndtering og samtidig fluorescens målinger udføres med stationenenhed mikropladelæser, drevet af softwaren. Stationen Enheden indeholder tre skuffer: én for cellen plade, sammensatte plade og tip rack. De indbyggede pipettor overfører forbindelser fra én kolonne af den sammensatte plade til den tilsvarende kolonne af cellen plade (trin 1). Hver brønd i cellepladen indeholder et monolag af HEK293T celler, der er blevet co-transficeret med GPCR af interesse og promiskuøs Ga 16 underenhed. Når en forbindelse aktiverer receptoren, er Ga 16-bundet BNP erstattet af GTP. Den Ga 16 subunit efterfølgende dissocierer fra Gβγ kompleks og aktiverer phospholipase Cp (PLCβ), som igen hydrolyserer phosphatidylinositol-bisphosphat (PIP2), hvilket resulterer i diacylglycerol (DAG) og inositoltriphosphat (IP3). IP3 aktiverer IP 3 calciumkanaler er til stede i membranen af det endoplasmatiske reticulum, inducere frigivelsen af calcium into cytoplasmaet. Interaktionen af calcium med Fluo-4 (som cellerne lastes før sammensatte tilføjelse) resulterer i et fluorescerende signal (trin 2). Den software, viser resultaterne som relative fluorescerende enhed (RFU) værdier i funktion af tiden, og tophøjder korrelerer med liganden koncentration i en koncentrationsafhængig måde. Disse data kan derefter omdannes til en koncentration-respons-kurve for at bestemme EC50-værdi på en ligand-receptor-par (trin 3).
Protocol
Representative Results
Discussion
Fluorescens-baserede calciummobilisering assay blev anvendt med succes til at bekræfte den funktionelle karakterisering af Drosophila sNPF peptiderge signalsystem, som allerede blev udført ved Mertens et al. med en bioluminescens assay og Feng et al. med en elektrofysiologisk assay 13,15. EC 50 værdier opnået med fluorescensassay i HEK293T celler er omkring 10 gange mindre end dem, der opnås med bioluminescence assay udført i CHO-celler (Drome-sNPF-1: fluo = 2,04 nM, lumi = 51 nM, Drome-sNPF- 2: fluo = 5,89 nM, lumi = 42 nM, Drome-sNPF-3: fluo = 5.55 nM lumi = 31 nM, Drome-sNPF-4: fluo = 0.50 nM lumi = 75 Nm). Disse variationer kan forklares med flere faktorer, herunder det faktum, at en af de anvendte ekspressionssystemer kan være bedre egnet til funktionel ekspression af en given receptor eller foldningen af visse receptorer kan være mindre effektiv i Certain celletyper. EC50 værdier for alle fire Drome-sNPF peptider er i det nanomolære område, når de testes på deres receptor med både fluorescens og bioluminescens assay generelt støtte den fysiologiske relevans af deres peptid-receptor-interaktion in vivo.
Bemærk, at ingen transfektion kontrol med en receptor, for hvilken den aktiverende ligand er kendt var inkluderet på skærmen præsenteres her, fordi Drosophila sNPF signalsystem er normalt transfektion kontrol forsøgsopstillinger. Den positive kontrol med en endogen ligand af HEK293T celler (PAR 1) og den negative kontrol (vaskepuffer) blev inkluderet i skærmen. Resultaterne af PAR 1 viste, at cellerne var i god stand. Den negative kontrol (vaskepuffer) ikke fremkalde et fluorescerende signal, som indikerer, at det medium, hvori peptiderne opløses var fri for forureninger, der kan influence resultaterne.
Den tidligere karakteriserede Drosophila sNPF signalsystem blev her anvendt til at forklare den fluorescens-baserede calciummobilisering assay. Til dette formål blev koncentrationen serie af de aktiverende ligander testes umiddelbart. Men når sjældne receptor bragt til overekspression i et screeningsassay til at teste et bibliotek indeholder hundredvis af forbindelser, anbefales det at første skærm med relativt høje endelige koncentrationer af ligander (f.eks., 10 eller 1 uM). Efter påvisning af en aktiverende forbindelse, kan en fortyndingsserie af denne forbindelse skal screenes med henblik på at sammensætte en koncentration-respons-kurve og bestemme EC 50-værdi.
Når den aktiverende ligand af en receptor er bestemt, kan intracellulær signalvej undersøges yderligere ved at tilpasse protokollen. Assayet kan udføres som beskrevet ovenfor, men uden co-transfektion af G ^5, 16 underenhed. Når calcium reaktion måles, betyder det, at receptor par med en endogen Ga q underenhed af det cellulære ekspressionssystem. Når der ikke observeres fluorescerende signal, kan anvendes protokoller til at måle ændringer i koncentrationen af andre sekundære budbringere (f.eks., Camp).
Struktur-aktivitet relationer (SAR) undersøgelser kan også udføres for at definere peptid kerne sekvens kræves for receptor aktivering. Først trunkerede sekvenser vurderes at definere den minimale aminosyresekvens af peptidet, der stadig er i stand til at aktivere receptoren. Desuden kan peptider afprøves som systematisk hver aminosyre er erstattet af en alaninrest. Test syntetiske alanin-substitution serie om receptoren gør det muligt at bestemme betydningen af hver af de aminosyrer for receptor-aktivering 24,25.
På trods af sin hyppige brug og gennemprøvede effektivitetcacy, skal det understreges, at analysen er beskrevet her kan have brug for nogle tilpasninger for at opnå optimale resultater for specifikke receptorer af interesse. Den Ga 16 subunit har den fordel, at det binder sig til de fleste GPCRs, men kan også have en dominant negativ effekt på receptorer, der endogent par via Ga q 22. I dette tilfælde kan det være nyttigt at afprøve forskellige kombinationer af G-proteiner under optimering af en roman calcium assay og sammenligne resultaterne for Ga q-koblede receptorer i fraværet eller tilstedeværelsen af Ga 16. Alternative analyser, der er uafhængige af interagerende G-protein til at detektere receptor-aktivering kan også udføres, såsom translokationen af GFP-mærket arrestin, eller påvisning af ændringer i membranpotentiale (f.eks. Ved FLIPR Membrane Potential Assay Kit). Udover Fluo-4 er vant her, en bred vifte af andre calcium-følsomme fluorophores, hver med sin egen spektrale og chemical egenskaber, er til rådighed. Den mest hensigtsmæssige fluorofor kan vælges baseret på GPCR celletype og den tilgængelige pladelæser, men eksperimentel verifikation er nødvendig. Mængderne af transficeret DNA og DNA / transfektionsreagens forholdet behov for at bestemmes for hver receptor-transfektionsreagens-cellelinje kombination. Endelig skal det holdes for øje, at celler i kontinuerlig kultur tillader kun 20-25 brugbare passager for at udføre screeningsassayene.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Forfatterne anerkender Research Foundation Flandern (FWO-Vlaanderen, Belgien, G.0601.11) og KU Leuven Research Foundation GOA/11/002. IB, TJ og LT gavn af et stipendium fra FWO-Vlaanderen.
Materials
| HEK293T cells | |||
| Dulbecco's Phosphate Buffered Saline (PBS) | Sigma-Aldrich | D8537 | |
| Trypsin-EDTA solution (0.25%) | Sigma-Aldrich | T4049 | |
| Ethylenediaminetetraacetic acid disodium salt dihydrate (EDTA) | MP Biomedicals | 195173 | |
| Dulbecco's Modified Eagle's Medium – high glucose (DMEM) | Sigma-Aldrich | D5796 | |
| Fetal Bovine Serum (FBS) | Sigma-Aldrich | F7524 | |
| Penicillin-Streptomycin (P-S) | Sigma-Aldrich | P4333 | |
| jetPRIME | Polyplus transfection | 114-01 | FuGENE HD Transfection Reagent (Promega); Lipofectamine LTX & Plus Reagent (Life technologies) |
| Dialyzed Fetal Bovine Serum (FBS) | Sigma-Aldrich | F0392 | |
| Fibronectin from human plasma | Sigma-Aldrich | F0895 | |
| Reagent A100, Lysis buffer | Chemometec | 910-0003 | |
| Reagent B, Stabilizing buffer | Chemometec | 910-0002 | |
| CaCl2 | Sigma-Aldrich | C3881 | |
| HEPES | Sigma-Aldrich | H4034 | |
| Bovine Serum Albumin (BSA) | Sigma-Aldrich | A4503 | |
| HBSS buffer: Hank's Balanced Salt Solution | Sigma-Aldrich | H8264 | |
| Probenecid | Sigma-Aldrich | P8761 | |
| NaOH (1 M) | Vel | 2781 | |
| Pluronic acid | Invitrogen | P-3000MP | |
| Dimethyl-sulfoxide (DMSO) | Sigma-Aldrich | D8418 | |
| Fluo-4 AM | Invitrogen | F14201 | Fluo-3, Rhod-2, Fluo-5, Calcium Green-1,.. (Invitorgen) |
| TPP tissue culture flasks (T-75 and T-150) | Sigma-Aldrich | Z707503 and Z707554 | |
| FlexStation device | Molecular Devices | NOVOstar (BMG Labtechnologies); FLIPR (Fluorometric Imaging Plate Reader) (Molecular Devices) | |
| Black-walled polystyrene plates (96 wells) with clear bottom | Greiner Bio-One | 655090 | Corning 96 well flat clear bottom black polystyrene poly-D-lysine coated microplates |
| NucleoCassette | Chemometec | 941-0001 | |
| NucleoCounter NC-100 | Chemometec | ||
| Microcentrifuge tubes, siliconized | BioCision | BCS-2470 | |
| Polystyrene V-shaped 96-well plates | Greiner Bio-One | 651101 | |
| 96-Well, FlexStation Pipet Tips | Molecular Devices | 9000-0912 | |
| Soft Max Pro software | Molecular Devices |
Riferimenti
- Bockaert, J., Pin, J. P. Molecular tinkering of G protein-coupled receptors an evolutionary success. EMBO J. 18 (7), 1723-1729 (1999).
- Gether, U. Uncovering molecular mechanisms involved in activation of G protein-coupled receptors. Endocr Rev. 21 (1), 90-113 (2000).
- Drews, J. Drug discovery a historical perspective. Science. 287 (5460), 1960-1964 (2000).
- Marinissen, M. J., Gutkind, J. S. G-protein-coupled receptors and signaling networks emerging paradigms. Trends Pharmacol Sci. 22 (7), 368-376 (2001).
- Bendena, W. G. Neuropeptide physiology in insects. Adv Exp Med Biol. 692, 166-191 (2010).
- Van Hiel, M. . B., et al. Neuropeptide receptors as possible targets for development of insect pest control agents. Adv Exp Med Biol. 692, 211-226 (2010).
- Tang, X. . L., Wang, Y., Li, D. . L., Luo, J., Liu, M. . Y. Orphan G protein-coupled receptors (GPCRs): biological functions and potential drug targets. Acta Pharmacol Sin. 33 (3), 363-371 (2012).
- Civelli, O., Reinscheid, R. K., Zhang, Y., Wang, Z., Fredriksson, R., Schiöth, H. B. G protein-coupled receptor deorphanizations. Annu Rev Pharmacol Toxicol. 53, 127-146 (2013).
- Mertens, I., Vandingenen, A., Meeusen, T., De Loof, A., Schoofs, L. Postgenomic characterization of G-protein-coupled receptors. Pharmacogenomics. 5 (6), 657-672 (2004).
- Brough, S. J., Shah, P. Use of aequorin for G protein-coupled receptor hit identification and compound profiling. Methods Mol Biol. 552, 181-198 (2009).
- Gee, K. R., Brown, K. A., Chen, W. N. U., Bishop-Stewart, J., Gray, D., Johnson, I. Chemical and physiological characterization of fluo-4 Ca2+-indicator dyes. Cell Calcium. 27 (2), 97-106 (2000).
- Beets, I., Lindemans, M., Janssen, T., Verleyen, P. Deorphanizing G protein-coupled receptors by a calcium mobilization assay. Methods Mol Biol. 789, 377-391 (2011).
- Mertens, I., Meeusen, T., Huybrechts, R., De Loof, A., Schoofs, L. Characterization of the short neuropeptide F receptor from Drosophila melanogaster. Biochem Biophys Res Commun. 297 (5), 1140-1148 (2002).
- Lu, H. -. L., Kersch, C. N., Taneja-Bageshwar, S., Pietrantonio, P. V. A calcium bioluminescence assay for functional analysis of mosquito (Aedes aegypti) and tick (Rhipicephalus microplus) G protein-coupled receptors. J. Vis. Exp. (50), e2732 (2011).
- Feng, G., et al. Functional characterization of a neuropeptide F-like receptor from Drosophila melanogaster. Eur. J. Neurosci. 18 (2), 227-238 (2003).
- Nässel, D. R., Wegener, C. A comparative review of short and long neuropeptide F signaling in invertebrates any similarities to vertebrate neuropeptide Y signaling. Peptides. 32 (6), 1335-1355 (2011).
- Grimmelikhuijzen, C. J. P., Hauser, F. Mini-review The evolution of neuropeptide signaling. Regul Pept. 177, S6-S9 (2012).
- Caers, J., Verlinden, H., Zels, S., Vandersmissen, H. P., Vuerinckx, K., Schoofs, L. More than two decades of research on insect neuropeptide GPCRs an overview. Front Endocrinol (Lausanne. 3 (151), 1-30 (2012).
- Kozak, M. An analysis of 5’-noncoding sequences from 699 vertebrate messenger RNAs). Nucleic Acids Res. 15 (20), 8125-8148 (1987).
- Offermanns, S., Simon, M. I. Gα15 and Gα16 couple a wide variety of receptors to phospholipase. CJ Biol Chem. 270 (25), 15175-15180 (1995).
- Ral Conklin, B., et al. Carboxyl-terminal mutations of Gqα and Gsα that alter the fidelity of receptor activation. Mol Pharmacol. 50 (4), 885-890 (1996).
- Kostenis, E. Is Gα16 the optimal tool for fishing ligands of orphan G-protein-coupled receptors. Trends Pharmacol Sci. 22 (11), 560-564 (2001).
- Robas, N. M., Fidock, M. D. Identification of orphan G protein-coupled receptor ligands using FLIPR assays. Methods Mol Biol. 306, 17-26 (2005).
- Caers, J., Peeters, L., Janssen, T., De Haes, W., Gäde, G., Schoofs, L. Structure-activity studies of Drosophila adipokinetic hormone (AKH) by a cellular expression system of dipteran AKH receptors. Gen Comp Endocrinol. 177 (3), 332-337 (2012).
- Peeters, L., et al. A pharmacological study of NLP-12 neuropeptide signaling in free-living and parasitic nematodes. Peptides. 34 (1), 82-87 (2012).

