שיטה כללית לגילוי Nitrosamide היווצרות בחילוף החומרים במבחנה של Nitrosamines מאת ציטוכרום P450s
Summary
Α-hydroxylation של nitrosamines מסרטנים מאת ציטוכרום P450s הוא מסלול מטבולי מקובל שמייצר מזיקות-DNA intermediates, לגרום מוטציות. עם זאת, נתונים חדשים מציין עוד חמצון כדי nitrosamides יכול להתרחש. אנו מתארים גנרל שיטה לגילוי nitrosamides המופק במבחנה ציטוכרום P450 מזורז מטבוליזם של nitrosamines.
Abstract
N-nitrosamines הם קבוצת חומרים מסרטנים סביבתי, אשר דורשים ציטוכרום P450 חמצון להפגין פעילות ומבוססת. המנגנון המקובל של הפעלת מטבולית כרוך היווצרות α-hydroxynitrosamines המפרקות באופן ספונטני לסוכנים החומר הדנ א. הצטברות של נזק לדנ א של מוטציות וכתוצאה מכך יכול בסופו של דבר להוביל לסרטן. ראיות חדשות מציין כי α-hydroxynitrosamines יכול להיות עוד יותר מחומצן כדי nitrosamides processively על-ידי ציטוכרום P450s. מאחר nitrosamides הם בדרך כלל יציבים יותר α-hydroxynitrosamines אפשר גם alkylate ה-DNA, nitrosamides עשוי לשחק תפקיד carcinogenesis. בדו ח זה, אנו מתארים פרוטוקול כללי עבור הערכת ייצור nitrosamide מ במבחנה ציטוכרום P450 מזורז חילוף החומרים של nitrosamines. פרוטוקול זה מנצל הגישה הכללית של הסינתזה בין את nitrosamides הרלוונטי של במבחנה ציטוכרום P450 חילוף החומרים assay באמצעות ספקטרומטר מסה של טנדם יינון שגובהו ברזולוציה של כרומטוגרפיה נוזלית-nanospray לצורך זיהוי. שיטה זו מתגלה N′– nitrosonorcotinine כמו מטבוליט מינור של N′– nitrosonornicotine במחקר דוגמה. השיטה יש רגישות גבוהה וזיהוי המוני בשל באופן סלקטיבי מדויק. יישום השיטה הזאת למגוון רחב של מערכות nitrosamine-ציטוכרום P450 יעזרו לקבוע את הכלליות של השינוי הזה. הבנה טובה יותר של היווצרות nitrosamide יכול לסייע מכיוון ציטוכרום P450s הן רב-צורתיות משתנות בפעילות, להערכת הסיכון לסרטן בודדים.
Introduction
N-nitrosamines הם קבוצה גדולה של חומרים מסרטנים נמצאו הדיאטה, מוצרי טבק, ואיכות הסביבה הכללית; הם יכולים גם להיות הקימו endogenously גוף האדם1. יותר מ-300 N –nitroso תרכובות נבדקו, > 90% הוערכו מסרטנים כמו בחיה מודלים2,3. להפגין את carcinogenicity שלהם, תרכובות אלו צריך קודם להיות מופעל על ידי ציטוכרום P450s1,2,3. מחקרים מראים כי ציטוכרום P450s ברצון נישחק nitrosamines כדי α-hydroxynitrosamines (איור 1), אשר הם תרכובות תגובתי עם מחצית החיים של ~ 5 s לפני נרקב באופן ספונטני כדי alkyldiazohydroxides. האחרון יכול alkylate דנ א לאחר ההפסד של H2O ו- N2. ה-DNA שנוצר adducts, אם לא מתוקן, יכול לגרום מוטציות, במקרה של onco קריטי – או גנים משתיק קול של גידול, להוביל לפיתוח סרטן1. מסיבה זו, יש כבר שהושקעו מאמצים להשיג הבנה מלאה מסלולים מטבוליים, אן adducts, ואת הזרם מטבוליטים של ציטוכרום P450 חמצון של nitrosamines מסרטנים. הידע הזה יש פוטנציאל היישום הערכת סיכון סרטן בודדים4.
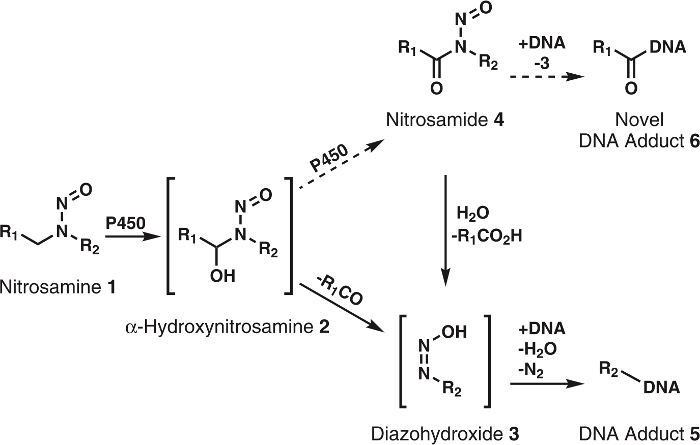
איור 1: גנרל וחילוף החומרים המוצע של nitrosamines.
Nitrosamines (1) הם תחמוצת על-ידי P450s כדי α-hydroxynitrosamines (2) המפרקות באופן ספונטני כדי alkyldiazohydroxides (3). תרכובות אלו יכולים לאגד הדנ א על טופס שה-DNA adducts. זה המשוערות הזה 2 יש נוספת תחמוצת על-ידי P450s nitrosamides 4. אלה ניתן ישירות לאגד ל- DNA טופס DNA הרומן adducts או להיות הידרוליזה ל 3 לטופס ש-DNA הידוע adducts. R1 ו- R2 מייצגים כל אלקיל קבוצה. אנא לחץ כאן כדי להציג גירסה גדולה יותר של הדמות הזאת.
למרות ההנחה α-hydroxynitrosamine נתמך באופן יציב על ידי נתונים מקיפים, יש כמה סתירות; אחד גדול הוא זמן מחצית החיים הקצר של α-hydroxynitrosamines5,6. ידוע כי תרכובות אלו מיוצרים בחברת קרום רשתית תוך-פלזמית, אחר כך alkylate DNA גרעיני. בהתחשב חייהם של כמה שניות, זה הוא תמוה איך intermediates האלה לשרוד המסע הנדרש אבל את ציטוזול. אחת ההשערות היא כי חלק של α-hydroxynitrosamines הם processively מחומצן nitrosamides7,8, אשר יציבים למדי השוואה9. זה ככל הנראה להתרחש דרך השמירה של α-hydroxynitrosamines ציטוכרום P450 פעילה באתר. כבר ראיתי תקדים עבור סוג זה של חמצון עם ניקוטין10, כהלים11ו12,alkylnitrosamines פשוט13. בנוסף, nitrosamides הם ישיר אקטינג מסרטנים2,3. על סמך שלהם תגובתיות9, תרכובות אלו הם האמינו להפקת DNA adducts זהים לאלו הנובעות α-hydroxynitrosamines יחד עם חדש, ה-DNA נחקרו adducts (איור 1). לכן, השערה זו לא רק מסביר התחבורה באמצעות ציטוזול, אלא גם היווצרות של ה-DNA נזק מוצרים.
בנייר זה, מתואר פרוטוקול כללי להערכת במבחנה ציטוכרום P450 בתיווך המרה של nitrosamines ל- nitrosamides. ההמרה שדווחה בעבר של N′– nitrosonornicotine (NNN) N′– nitrosonorcotinine (NNC) על ידי ציטוכרום P450 2A6 הצור דוגמה14. יישום של פרוטוקול זה על מגוון רחב של מערכות אנזים-סובסטרט יעזרו לקבוע את החשיבות של nitrosamides בחילוף החומרים nitrosamine הכללית.
Protocol
Representative Results
Discussion
שחקרתי את חילוף החומרים של nitrosamines הוא מרכיב קריטי להבנת carcinogenicity שלהם. מאז ציטוכרום מעורב P450s, אנזימים מטבוליים אחרים רב-צורתיות, יישום של ידע זה יכול באופן פוטנציאלי לזהות בסיכון גבוה-יחידים-1,–4. נתונים חדשים המציין את חמצון נוסף של α-hydroxynitrosamines, מטבוליטים הג…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
מחקר זה נתמך על ידי מענק אין. CA-81301 מן המכון הלאומי לסרטן. אנו מודים בוב קרלסון לסיוע העריכה, ד ר פיטר Villalta, מינג Xun לסיוע ספקטרומטר מסה אנליטי ביוכימיה משותפים משאב של מרכז הסרטן הבונים החופשיים, ואת ד ר אדם טי Zarth ד ר אנה ק מישל לדיונים החשובים שלהם קלט. למשאב משותף ביוכימיה אנליטי נתמכת באופן חלקי על ידי נבחרת סרטן המכון סרטן מרכז תמיכה גרנט CA-77598
Materials
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
Riferimenti
- Rom, W. N., Markowitz, S. . Environmental and Occupational Medicine. , 1226-1239 (2007).
- Preussmann, R., Stewart, B. W., Searle, C. E. . Chemical Carcinogens, ACS Monograph 182. 2, 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R., Searle, C. E. . Chemical Carcinogens. ACS monograph 173. , 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. . ACS Symposium Series. 101, 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5′(1′)iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochimica. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N’-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N’-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).

