En General metode til påvisning af Nitrosamide dannelse i In Vitro metabolismen af nitrosaminer af cytokrom P450s
Summary
Α-hydroxylering af kræftfremkaldende nitrosaminer af cytokrom P450s er den accepterede stofskiftevej, der producerer DNA-skader mellemprodukter, som forårsager mutationer. Men nye data viser yderligere oxidation til nitrosamides kan forekomme. Vi beskriver en generel metode til påvisning af nitrosamides fremstillet af in vitro- cytokrom P450-katalyseret metabolisme af nitrosaminer.
Abstract
N-nitrosaminer er en veletableret gruppe af miljømæssige kræftfremkaldende stoffer, som kræver cytokrom P450 oxidation at udstille aktivitet. Accepteret mekanisme af metabolisk aktivering omfatter dannelsen af α-hydroxynitrosamines, der spontant nedbrydes til DNA alkylerende stoffer. Ophobning af DNA-skader og de deraf følgende mutationer kan i sidste ende føre til kræft. Nye tyder på, at α-hydroxynitrosamines kan yderligere oxideres til nitrosamides processively af cytokrom P450s. Fordi nitrosamides er generelt mere stabile end α-hydroxynitrosamines og kan også alkylatbenzin DNA, kan nitrosamides spille en rolle i carcinogenese. I denne betænkning beskriver vi en generel protokol for at vurdere nitrosamide produktion fra in vitro- cytokrom P450-katalyseret metabolisme af nitrosaminer. Denne protokol udnytter en generel tilgang til syntesen af de relevante nitrosamides og en in vitro- cytokrom P450 stofskifte analyse ved hjælp af liquid chromatography-nanospray ionisering-høj opløsning tandem massespektrometri til påvisning. Denne metode fundet N′– nitrosonorcotinine som en mindre metabolit af N′– nitrosonornicotine i eksempel undersøgelse. Metoden har høj følsomhed og selektivt behørigt at nøjagtigt masse påvisning. Anvendelse af denne metode på en bred vifte af Nitrosamin-cytokrom P450 systemer vil hjælpe med at bestemme det generelle indhold af denne transformation. Fordi cytokrom P450s er polymorfe og varierer i aktivitet, kunne en bedre forståelse af nitrosamide dannelse støtte i enkelte kræft risikovurdering.
Introduction
N-nitrosaminer er en stor klasse af kræftfremkaldende stoffer fundet i kosten, tobaksvarer og det generelle miljø; de kan også dannes endogent i den menneskelige krop1. Mere end 300 N –nitroso forbindelser er blevet testet og > 90% blev evalueret som kræftfremkaldende i dyre modeller2,3. Til at udstille deres carcinogenicitet, skal disse forbindelser først aktiveres af cytokrom P450s1,2,3. Forskning viser, at cytokrom P450s let oxiderer nitrosaminer til α-hydroxynitrosamines (figur 1), som er meget reaktive forbindelser med halveringstider ~ 5 s før spontant nedbrydes til alkyldiazohydroxides. Sidstnævnte kan alkylatbenzin DNA efter tabet af H2O og N2. Den resulterende DNA adukter, hvis skadevirkningen, kan forårsage mutationer, der i kritiske Kræftpsykologisk- eller tumor suppressor gener, fører til kræft udvikling1. Af denne grund, meget indsats har blevet brugt for at opnå en fuld forståelse af de metaboliske reaktionsveje, DNA adukter, og downstream metabolitter af cytokrom P450 oxidation af kræftfremkaldende nitrosaminer. Denne viden har potentielle anvendelse i enkelte cancer risiko vurdering4.
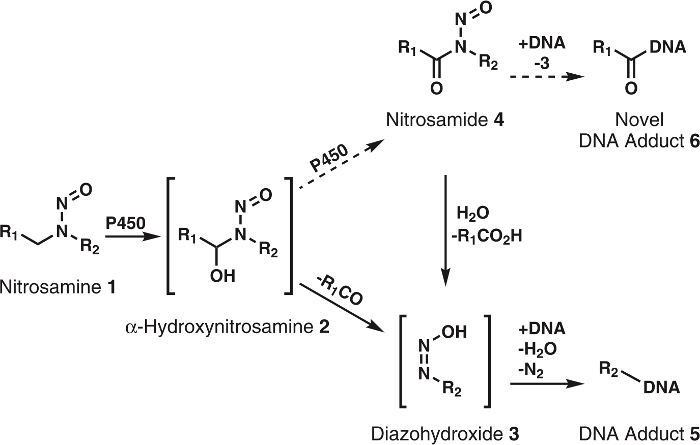
Figur 1: General og foreslåede metabolisme af nitrosaminer.
Nitrosaminer (1) oxideres af P450s til α-hydroxynitrosamines (2) der spontant nedbrydes til alkyldiazohydroxides (3). Disse forbindelser kan binde til DNA til at danne DNA adukter. Det er en hypotese at 2 oxideres videre af P450s til nitrosamides 4. Disse kan direkte binde til DNA til at danne nye DNA adukter eller være hydrolyseret 3 -form kendt DNA adukter. F1 og F2 repræsenterer enhver alkyl gruppen. Venligst klik her for at se en større version af dette tal.
Selv om α-hydroxynitrosamine hypotese er solidt understøttet af omfattende data, er der et par uoverensstemmelser; en større man er den korte half-life af α-hydroxynitrosamines5,6. Det er kendt, at disse forbindelser er produceret på endoplasmatiske reticulum membran og senere alkylatbenzin nukleare DNA. I betragtning af deres levetid af et par sekunder, det forvirrende, hvordan disse mellemprodukter overleve den nødvendige rejse selv i cytosol. En hypotese er, at en del af α-hydroxynitrosamines processively er oxideret til nitrosamides7,8, hvilket er ret stabilt i sammenligning9. Dette vil formentlig ske via fastholdelse af α-hydroxynitrosamines i cytokrom P450 aktive site. Præcedens for denne form for oxidering har været set med nikotin10, alkoholer11og enkle alkylnitrosamines12,13. Derudover er nitrosamides direkte virkende kræftfremkaldende2,3. Baseret på deres reaktivitet9, menes disse forbindelser at producere DNA adukter identiske med dem som følge af α-hydroxynitrosamines sammen med nye, uudforskede DNA adukter (figur 1). Således, denne hypotese ikke kun forklarer transport gennem i cytosol, men også dannelsen af DNA skade produkter.
I dette papir, er en generel protokol for at vurdere in vitro- cytokrom P450-medieret konvertering af nitrosaminer til nitrosamides beskrevet. Den tidligere rapporteret konvertering af N′– nitrosonornicotine (NNN) til N′– nitrosonorcotinine (NNC) af cytokrom P450 2A6 er fremvist som et eksempel14. Anvendelse af denne protokol på en bred vifte af substrat-enzym systemer vil hjælpe med at bestemme betydningen af nitrosamides i overordnede Nitrosamin stofskifte.
Protocol
Representative Results
Discussion
Belyse metabolismen af nitrosaminer er et afgørende element til at forstå deres kræftfremkaldende egenskaber. Da de involverede cytokrom P450s og andre metaboliske enzymer er polymorfe, kunne yderligere anvendelse af denne viden potentielt identificere høj risiko personer1,4. Nye data viser, at yderligere oxidation af α-hydroxynitrosamines, de formodede vigtigste metabolitter af nitrosaminer involveret i DNA bindende, at nitrosamides er muligt; men dette har…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Denne undersøgelse blev støttet af tilskud ikke. CA-81301 fra National Cancer Institute. Vi takker Bob Carlson for redaktionelle bistand, Dr. Peter Villalta og Xun Ming for massespektrometri bistand i den analytisk biokemi delt ressource af frimurerisk Cancer Center, og Dr. Adam T. Zarth og Dr. Anna K. Michel for deres værdifulde drøftelser og input. Analytisk biokemi delt ressource understøttes delvist af National Cancer Institute kræft Center støtte Grant CA-77598
Materials
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
Riferimenti
- Rom, W. N., Markowitz, S. . Environmental and Occupational Medicine. , 1226-1239 (2007).
- Preussmann, R., Stewart, B. W., Searle, C. E. . Chemical Carcinogens, ACS Monograph 182. 2, 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R., Searle, C. E. . Chemical Carcinogens. ACS monograph 173. , 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. . ACS Symposium Series. 101, 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5′(1′)iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochimica. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N’-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N’-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).

