Potenciación de la eficacia del anticuerpo contra el cáncer por fármacos antineoplásicos: detección de anticuerpos-droga sinergia utilizando la ecuación de índice de combinación
Summary
Este protocolo describe cómo evaluar sinergismo entre un anticuerpo contra el cáncer y fármacos antineoplásicos en modelos preclínicos mediante la ecuación de índice de combinación de Chou y Talalay.
Abstract
Potenciación de la hostiles anticuerpos monoclonales (mAb) por agentes quimioterapéuticos constituye una estrategia valiosa para el diseño de una terapia eficaz y segura contra el cáncer. Aquí proporcionamos un protocolo para identificar una combinación racional en la etapa preclínica. En primer lugar, se describe un ensayo basado en células para evaluar el sinergismo entre mAb contra el cáncer y las drogas citotóxicas, que utiliza la ecuación de índice de combinación de Chou y Talalay1. Esto incluye la medición del tumor celular drogas y anticuerpos-sensibilidad usando un análisis MTT, seguido de un análisis automatizado de la computadora para calcular los valores de índice (CI) de combinación. Valores de CI de < 1 indican sinergismo entre mAbs probado y agentes citotóxicos1. Para corroborar la en vitro resultados en vivo, además se describe un método para evaluar la eficacia del régimen de combinación en un modelo de xenoinjerto tumoral. En este modelo, el régimen combinado retrasa significativamente el crecimiento del tumor, que se traduce en una significativa supervivencia extendida en comparación con controles de agente único. Lo importante es la experimentación en vivo revela que el régimen de combinación es bien tolerado. Este protocolo permite la evaluación eficaz de combinaciones de fármacos contra el cáncer en modelos preclínicos y la identificación de una combinación racional para evaluar en ensayos clínicos.
Introduction
El enfoque convencional en el tratamiento de un gran número de diferentes tipos de cáncer se basaba en monoterapia. Aunque todavía se utiliza en muchos casos, este método reunieron varios obstáculos lleva a optar por terapias combinadas2. Particularmente, las células cancerosas son más susceptibles a desarrollar resistencia cuando se tratan con un solo medicamento por inducir supervivencia alternativos mecanismos3, resultando en fracaso terapéutico de pacientes4. Por otra parte, en monoterapia, medicamentos generalmente son administrados en una dosis alta. Esta situación a menudo resulta en la ocurrencia de fuertes efectos secundarios de dosis dependiente que puede ser intolerable y obligar a los médicos para detener el tratamiento2. Por estas razones, la Asociación de moléculas contra el cáncer ahora es preferido a la monoterapia.
Combinaciones de medicamentos ideal serían las que actúan en sinergia contra células tumorales, sin aumento de la toxicidad contra las células normales. Sinergia se refiere a la interacción de dos o más medicamentos que produce un efecto terapéutico mayor que la suma de cada droga individual actuando por separado. Estas interacciones pueden resultar en mayor eficacia terapéutica clínica2. Límites de la resistencia al tratamiento, aumenta la eficacia y también puede reducir la toxicidad2. De hecho, puede reducirse la dosis de cada medicamento para disminuir sus efectos secundarios apuntando a distintas vías. Además, una de las moléculas también puede servir como un agente de sensibilización contra las células cancerosas. El efecto de la segunda droga puede mejorarse en las células sensibilizadas y menos de la dosis puede ser utilizado5.
La terapia combinada puede incluir dos o más medicamentos quimioterapéuticos o biológicos, como anticuerpos monoclonales6. Estos mAbs apuntar específicamente las células que expresaban un antígeno de superficie de la célula de interés y son capaces de matar células tumorales a través de vías inmunológicas incluyendo la citotoxicidad mediada por células dependiente de anticuerpo (ADCC), con la participación de las células efectoras inmunes 7y la citotoxicidad dependiente del complemento (CDC)6. También puede actuar a través de un mecanismo no inmunológico mediado por apoptosis8,9,10,11. En este caso, la inducción del proceso de muerte celular programada puede sensibilizar las células de cáncer, debilitan su función y hacer el fármaco quimioterápico asociado más eficaz en una dosis más baja. Como tal, proapoptotic mAb son buenos candidatos para el diseño de regímenes de combinación con fármacos antineoplásicos.
Se han descrito diferentes modelos matemáticos para evaluar sinergismo de drogas; uno de ellos se basa en la combinación del método de índice1. Este método se basa en el principio de efecto mediano desarrollado por Chou1. La ecuación de la mediana-efecto correlaciona la dosis de droga y el efecto de la droga como sigue.
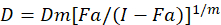
Aquí, D es la dosis de la droga; DM es la dosis mediana-efecto; FA es la fracción afectada por la dosis; m es un exponente que indica la forma de la dosis-efecto parcela1. La dosis mediana de efecto se utiliza para calcular la dosis de Dx de un fármaco que inhibe o mata a “x” por ciento de las células. Luego se calcula el valor de CI para evaluar el efecto aditivo de la combinación de drogas, de la siguiente manera1.
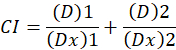
CI el valor de 1 indica un efecto aditivo y un valor de CI de 1 indica antagonismo1. La aplicación de este método se facilita aún más la disponibilidad de un programa de computadora, CompuSyn, que determina el sinergismo y el antagonismo en las dosis o los niveles de efecto simularon automáticamente12.
Nuestro grupo ha desarrollado el mAb 8B6 específico del antígeno O-acetil-GD2 para neuroblastoma gangliósido (OAcGD2)13 y otros demostraron que esta mAb es capaz de inducir la muerte celular con atributos de apoptosis11. Para probar si mAb 8B6 puede sensibilizar las células del neuroblastoma en el topotecán agente antineoplásico, adaptamos el método antedicho, desarrollado por Chou1. En primer lugar, determinamos los dosis efectiva 50 (ED50) los valores de mAb 8B6 y topotecán. A continuación, las células de neuroblastoma con equipotente relaciones de los dos compuestos basados en ED50 valores están expuestas para determinar los valores de CI con el software de simulación antes mencionados. Este método nos permite demostrar sinergismo entre mAb 8B6 y topotecan in vitro. A continuación, se describe un protocolo para evaluar aún más la potencia y la seguridad de esta combinación régimen en vivo. Este protocolo se puede aplicar fácilmente para seleccionar combinaciones de agente quimioterapéutico y mAb anticáncer potente y seguro en estudios preclínicos. Una representación esquemática de este estudio se proporciona en la figura 1.
Protocol
Representative Results
Discussion
Para predecir el efecto de la interacción con otros medicamentos, pueden utilizarse tres métodos: la metodología de isobologram17, la mezcla no lineal modelo18y la combinación índice1. Análisis de índice de combinación es el más comúnmente utilizado ya que su aplicación se simplifica por la disponibilidad de un programa informático fácil de usar. Para ello, primero hemos caracterizado la respuesta de dosis-efecto de cada agente utilizado…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Concesión de la ayuda: Fondation de Projet de L ‘Université de Nantes, les Bagouz’ à Manon, La Ligue contre le cáncer comité de Loire-Atlantique, comité de Morbihan y comité de Vendée, une rose pour S.A.R.A.H, L’Etoile de Martin y la Société Française de Lutte contre les Los cánceres et les leucémies de l ‘ enfant et de L’adolescent (SFCE). M.B. y J.F. son apoyados por La Ligue Contre Le cáncer. Los autores agradecen a la UTE-instalación de la estructura Fédérative de Recherche François Bonamy. Los autores también agradecen el Dr. S. Suzin (Inserm, París) para proporcionar las células IMR5 y Sra. H. Estéphan su asistencia técnica.
Materials
| Cell Proliferation kit (MTT) | Roche | 11-465-007-001 | |
| CompuSyn software | ComboSyn | Combosyn can be downloaded for free at http://www.combosyn.com | |
| Electric shaver | Bioseb | BIO-1556 | |
| Fetal calf serum | Eurobio | CVFSVFF00-01 | 10% heat-inactivated fetal calf serum in RPMI 1640 |
| Firefox | Mozilla Corporation | Firefox can be downloaded for free at http://www.mozilla.org/en-US/firefox/ | |
| Heat lamp | Verre&Quartz | 4003/1R | |
| Human neuroblastoma IMR-5 cell line | Accegen Biotechnology | ABC-TC0450 | IMR-5 is a clone of the human neuroblastoma cell line IMR32 5459762. IMR-5 cells were generously provided by Dr. Santos Susin (U.872, Paris, France) |
| L-glutamine | Gibco | 25030-024 | 2 mM in RPMI 1640 |
| Lysis solution | Roche | 11-465-007-001 | |
| mAb 8B6 | University of Nantes | N/A | |
| Matrigel | Corning | 354248 | |
| Multiskan FC | Thermofischer Scientific | N08625 | |
| Needle 21G 1 ½ | BD Microlance | 304432 | |
| Needle 25G 1 | Terumo | NN-2525R | |
| NSG mice | Charles River Laboratories | 5557 | |
| Nunc MicroWell 96-well microplates | Thermofisher | 167008 | |
| PBS | VWR | L182-10 | |
| PBS, 0,05% EDTA | Sigma-Aldrich | E9884 | |
| PC that runs windows 7 | Microsoft | Windows 7 can be purchased at http://www.microsoft.com/en-gb/software-download/windows7 | |
| Penicillin-Streptomycin | Gibco | 15140-122 | 100 units/mL penicillin and 100 mg/mL streptomycin in RPMI 1640 |
| Reagent reservoir | Thermofischer Scientific | 8094 | |
| Rodent restrainer | Bioseb | TV-150-SM | |
| RPMI 1640 | Gibco | 31870-025 | |
| Syringe 1 mL | Henke Sass Wolf | 5010.200V0 | |
| Topotecan | Sigma-Aldrich | T2705 |
Riferimenti
- Chou, T. C. Theoretical basis, experimental design, and computerized simulation of synergism and antagonism in drug combination studies. Pharmacological Reviews. 58 (3), 621-681 (2006).
- Bayat Mokhtari, R., et al. Combination therapy in combating cancer. Oncotarget. 8 (23), 38022-38043 (2017).
- Zahreddine, H., Borden, K. L. Mechanisms and insights into drug resistance in cancer. Frontiers in Pharmacology. 4, 28 (2013).
- Martin, T. P., Baguley, D., et al. Re: “Postoperative validation of bone-anchored implants in the single-sided deafness population.” Snapp et al. Otol Neurotol 2012: 33;291-6. Otol Neurotol. 34 (4), 777-778 (2013).
- Choi, B., et al. Sensitization of lung cancer cells by altered dimerization of HSP27. Oncotarget. 8 (62), 105372-105382 (2017).
- Weiner, L. M., Surana, R., Wang, S. Monoclonal antibodies: versatile platforms for cancer immunotherapy. Nature Reviews Immunology. 10 (5), 317-327 (2010).
- Mellor, J. D., Brown, M. P., Irving, H. R., Zalcberg, J. R., Dobrovic, A. A critical review of the role of Fc gamma receptor polymorphisms in the response to monoclonal antibodies in cancer. Journal of Hematology & Oncology. 6, 1 (2013).
- Kowalczyk, A., et al. The GD2-specific 14G2a monoclonal antibody induces apoptosis and enhances cytotoxicity of chemotherapeutic drugs in IMR-32 human neuroblastoma cells. Cancer Letters. 281 (2), 171-182 (2009).
- Retter, M. W., et al. Characterization of a proapoptotic antiganglioside GM2 monoclonal antibody and evaluation of its therapeutic effect on melanoma and small cell lung carcinoma xenografts. Ricerca sul cancro. 65 (14), 6425-6434 (2005).
- Nakamura, K., et al. Apoptosis induction of human lung cancer cell line in multicellular heterospheroids with humanized antiganglioside GM2 monoclonal antibody. Ricerca sul cancro. 59 (20), 5323-5330 (1999).
- Cochonneau, D., et al. Cell cycle arrest and apoptosis induced by O-acetyl-GD2-specific monoclonal antibody 8B6 inhibits tumor growth in vitro and in vivo. Cancer Letters. 333 (2), 194-204 (2013).
- Chou, T. C., Martin, N. . CompuSyn for drug combinations: PC software and user’s guide: a computer program for quantitation of synergism and antagonism in drug combinations, and the determination of IC50 and ED50 and LD50 values. , (2005).
- Alvarez-Rueda, N., et al. A monoclonal antibody to O-acetyl-GD2 ganglioside and not to GD2 shows potent anti-tumor activity without peripheral nervous system cross-reactivity. PLoS One. 6 (9), e25220 (2011).
- Faraj, S., et al. Neuroblastoma chemotherapy can be augmented by immunotargeting O-acetyl-GD2 tumor-associated ganglioside. Oncoimmunology. 7 (1), e1373232 (2017).
- Ishikawa, F., et al. Development of functional human blood and immune systems in NOD/SCID/IL2 receptor {gamma} chain(null) mice. Blood. 106 (5), 1565-1573 (2005).
- Ullman-Cullere, M. H., Foltz, C. J. Body condition scoring: a rapid and accurate method for assessing health status in mice. Laboratory Animal Science. 49 (3), 319-323 (1999).
- Teicher, B. A. Assays for in vitro and in vivo synergy. Methods in Molecular Medicine. 85, 297-321 (2003).
- White, D. B., Slocum, H. K., Brun, Y., Wrzosek, C., Greco, W. R. A new nonlinear mixture response surface paradigm for the study of synergism: a three drug example. Current Drug Metabolism. 4 (5), 399-409 (2003).
- Mosmann, T. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. Journal of Immunological Methods. 65 (1-2), 55-63 (1983).
- Huyck, L., Ampe, C., Van Troys, M. The XTT cell proliferation assay applied to cell layers embedded in three-dimensional matrix. Assay and Drug Development Technologies. 10 (4), 382-392 (2012).
- Thompson, J., et al. Synergy of topotecan in combination with vincristine for treatment of pediatric solid tumor xenografts. Clinical Cancer Research. 5 (11), 3617-3631 (1999).
- Tan, M., Fang, H. B., Tian, G. L., Houghton, P. J. Experimental design and sample size determination for testing synergism in drug combination studies based on uniform measures. Statistic in Medicine. 22 (13), 2091-2100 (2003).
- Tang, X. X., et al. Implications of EPHB6, EFNB2, and EFNB3 expressions in human neuroblastoma. Proceding of the National Academy of Sciences of the United States of America. 97 (20), 10936-10941 (2000).
- Mehta, R. R., Graves, J. M., Hart, G. D., Shilkaitis, A., Das Gupta, T. K. Growth and metastasis of human breast carcinomas with Matrigel in athymic mice. Breast Cancer Research and Treatment. 25 (1), 65-71 (1993).
- Mullen, P., Ritchie, A., Langdon, S. P., Miller, W. R. Effect of Matrigel on the tumorigenicity of human breast and ovarian carcinoma cell lines. International Journal of Cancer. 67 (6), 816-820 (1996).
- Feng, C., Tang, S., Wang, J., Liu, Y., Yang, G. Topotecan plus cyclophosphamide as maintenance chemotherapy for children with high-risk neuroblastoma in complete remission: short-term curative effects and toxicity. Nan Fang Yi Ke Da Xue Xue Bao. 33 (8), 1107-1110 (2013).
- Cheung, N. K., et al. Ganglioside GD2 specific monoclonal antibody 3F8: a phase I study in patients with neuroblastoma and malignant melanoma. Journal of Clininical Oncology. 5 (9), 1430-1440 (1987).
- Nair, A. B., Jacob, S. A simple practice guide for dose conversion between animals and human. Journal of Basic Clinical Pharmacy. 7 (2), 27-31 (2016).
- Dayde, D., et al. Tumor burden influences exposure and response to rituximab: pharmacokinetic-pharmacodynamic modeling using a syngeneic bioluminescent murine model expressing human CD20. Blood. 113 (16), 3765-3772 (2009).
- Racki, W. J., et al. NOD-scid IL2rgamma(null) mouse model of human skin transplantation and allograft rejection. Transplantation. 89 (5), 527-536 (2010).
- Sherif, A., Winerdal, M., Winqvist, O. Immune Responses to Neoadjuvant Chemotherapy in Muscle Invasive Bladder Cancer. Bladder Cancer. 4 (1), 1-7 (2018).

