Nanopartikler Tracking Analyse for kvantificering og størrelse bestemmelse af ekstracellulære vesikler
Summary
Vi demonstrerer, hvordan man bruger et nyt nanopartikler tracking analyseinstrument til at estimere størrelsesfordelingen og den samlede partikelkoncentration af ekstracellulære vesikler isoleret fra mus perigonadal fedtvæv og human plasma.
Abstract
De fysiologiske og patofysiologiske roller ekstracellulære vesikler (elbiler) er blevet mere og mere anerkendt, hvilket gør EV-feltet til et hurtigt udviklende forskningsområde. Der er mange forskellige metoder til EV isolation, hver med forskellige fordele og ulemper, der påvirker downstream udbytte og renhed af elbiler. Således er det vigtigt at karakterisere EV-prep isoleret fra en given kilde ved en valgt metode for fortolkning af downstream-resultater og sammenligning af resultater på tværs af laboratorier. Der findes forskellige metoder til bestemmelse af elbilers størrelse og mængde, som kan ændres af sygdomstilstande eller som reaktion på eksterne forhold. Nanopartikler tracking analyse (NTA) er en af de fremtrædende teknologier, der anvendes til high-throughput analyse af individuelle elbiler. Her præsenterer vi en detaljeret protokol til kvantificering og størrelsesbestemmelse af elbiler isoleret fra musesyigonadal fedtvæv og humant plasma ved hjælp af en banebrydende teknologi til NTA, der repræsenterer store fremskridt på området. Resultaterne viser, at denne metode kan levere reproducerbare og gyldige samlede partikelkoncentrations- og størrelsesfordelingsdata for elbiler isoleret fra forskellige kilder ved hjælp af forskellige metoder, som bekræftet af transmissionselektronmikroskopi. Tilpasningen af dette instrument til NTA vil tage fat på behovet for standardisering i NTA-metoder for at øge strengheden og reproducerbarheden i ev-forskning.
Introduction
Ekstracellulære vesikler (elbiler) er små (0,03-2 μm) membranbundne vesikler, der udskilles af næsten alle celletyper1. De omtales ofte som “exosomer”, “mikrovesicles” eller “apoptotiske kroppe” afhængigt af deres frigivelsesmekanisme og størrelse2. Mens det oprindeligt blev antaget, at elbiler simpelthen var et middel til at fjerne affald fra cellen for at opretholde homøostase3, ved vi nu, at de også kan deltage i intercellulær kommunikation via overførsel af molekylært materiale – herunder DNA, RNA (mRNA, microRNA), lipider og proteiner4,5 – og at de er vigtige regulatorer af normal fysiologi samt patologiske processer1, 5,6,7,8.
Der findes mange forskellige metoder til at isolere og kvantificere elbiler, som er beskrevet andetsteds9,10,11,12. Den anvendte isolationsprotokol samt kilden til elbiler kan i høj grad påvirke EV udbytte og renhed. Selv differentieret centrifugering, der længe har været betragtet som “guldstandardmetoden” for eksosome isolation, kan være genstand for betydelig variation, der efterfølgende påvirker den opnåede EV-population, og downstream-analyser13. Således gør de forskellige forskellige metoder til EV isolation og kvantificering det vanskeligt at sammenligne, reproducere og fortolke resultaterne af eksperimenter rapporteret i litteraturen14. Desuden kan EV-frigivelse reguleres af cellulære forhold eller forskellige eksterne faktorer. Det er blevet foreslået, at elbiler spiller en rolle i at opretholde cellulære homøostase ved at beskytte celler mod intracellulær stress15, som flere undersøgelser har vist, at cellulær stress stimulerer EV sekretion. For eksempel er øget EV-frigivelse blevet rapporteret efter cellulær eksponering for hypoxi, endoplasmisk reticulum stress, oxidativ stress, mekanisk stress, cigaretrøg ekstrakt, og partikler luftforurening16,17,18,19,20,21,22. Ev frigivelse har også vist sig at være ændret in vivo; mus, der er udsat for en kost med højt fedtindhold eller faste i seksten timer, frigav flere adipocyt-elbiler23. For at undersøge, om en bestemt behandling eller tilstand ændrer EV-frigivelsen, skal antallet af elbiler bestemmes nøjagtigt. Vurderingen af fordelingen af ev-størrelsen kan også indikere den fremherskende subcellulære oprindelse af elbiler (f.eks. fusion af sene endoomer/multivesikulære organer med plasmamembranen vs. spirende plasmamembran)24. Der er således behov for robuste metoder til nøjagtigt at måle den samlede koncentration og størrelsesfordelingen af den EV-forberedelse, der undersøges.
En hurtig og meget følsom metode til visualisering og karakterisering af elbiler i opløsning er nanopartikler tracking analyse (NTA). En detaljeret forklaring af principperne i denne metode og sammenligning med alternative metoder til vurdering af EV’s størrelse og koncentration er tidligere blevet beskrevet25,26,27,28. Kort sagt, under NTA måling, elbiler visualiseres af lyset spredt, når de er bestrålet med en laserstråle. Det spredte lys er fokuseret af et mikroskop på et kamera, der registrerer partikelbevægelsen. NTA-softwaren sporer den tilfældige termiske bevægelse af hver partikel, kendt som Brownian motion, for at bestemme diffusionskoefficienten, der bruges til at beregne størrelsen af hver partikel ved hjælp af Stokes-Einstein-ligningen. NTA blev første gang anvendt til måling af elbiler i en biologisk prøve i 201125. Indtil for nylig var der kun to mainstream virksomheder, der tilbyder kommercielle NTA instrumenter29 indtil indførelsen af ViewSizer 3000 (i det følgende benævnt partikel tracking instrument), som bruger en kombination af nye hardware og softwareløsninger til at overvinde betydelige begrænsninger af andre NTA teknikker.
Partikelsporingsinstrumentet karakteriserer nanopartikler i flydende prøver ved at analysere deres Brownian bevægelse og karakteriserer større mikron-størrelse partikler ved at analysere gravitationel afregning. Dette instruments unikke optiske system, som omfatter multispektral belysning med tre laserlyskilder (ved 450 nm, 520 nm og 635 nm), gør det muligt for forskere at analysere en bred vifte af partikelstørrelser (f.eks. exosomer, mikrovesicles) samtidigt. Der vises et skema over instrumentopsætningen i figur 1.
Her demonstrerer vi, hvordan man udfører partikelstørrelsesfordeling og koncentrationsmålinger af isolerede mus og menneskelige elbiler ved hjælp af et nyt NTA-instrument.
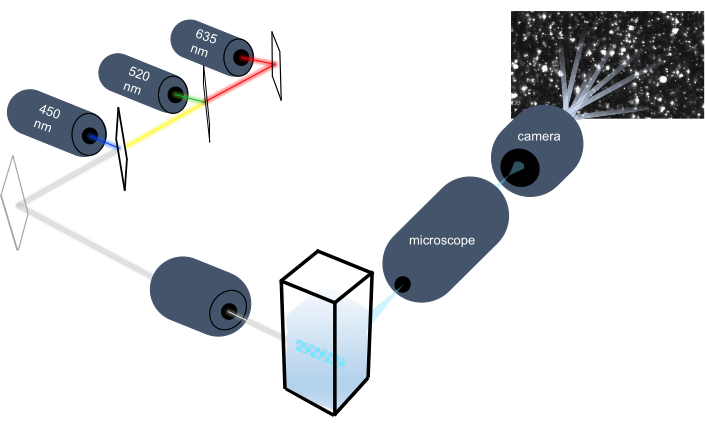
Figur 1: Partikelsporingsinstrument optisk system. NTA-instrumentet belyser partikler ved hjælp af tre lasere med følgende bølgelængder: 450 nm, 520 nm, 635 nm. Videooptagelse af det spredte lys fra individuelle partikler registreres og spores af et digitalt videokamera orienteret 90° fra cuvette. Klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Her demonstrerer vi en protokol for NTA af elbiler for at måle størrelsesfordelingen af en bred vifte af partikelstørrelser samtidigt og måle den samlede EV-koncentration i en polydispersprøve. I denne undersøgelse blev musemaigonadal fedtvæv og humant plasma brugt som kilde til elbiler. Men, Elbiler isoleret fra andre væv eller biologiske væsker såsom serum, urin, spyt, modermælk, fostervand, og celle kultur supernatant kan også anvendes til NTA. Målinger af polystyrenperlestandarder sikrede, at instrumente…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Dette arbejde blev støttet af National Institutes of Health (ES030973-01A1, R01ES025225, R01DK066525, P30DK026687, P30DK063608). Vi anerkender Jeffrey Bodycomb, Ph.D. af HORIBA Instruments Incorporated for hans hjælp kalibrere instrumentet.
Materials
| 1X dPBS | VWR | 02-0119-1000 | To dilute samples |
| 100 nm bead standard | Thermo Scientific | 3100A | To test ViewSizer 3000 calibration |
| 400 nm bead standard | Thermo Scientific | 3400A | To test ViewSizer 3000 calibration |
| Centrifugal Filter Unit | Amicon | UFC901024 | To filter PBS diluent |
| Collection tubes, 2 mL | Qiagen | 19201 | For isolation of human plasma extracellular vesicles |
| Compressed air duster | DustOff | DPSJB-12 | To clean cuvettes |
| Cuvette insert | HORIBA Scientific | – | Provided with purchase of ViewSizer 3000 |
| Cuvette jig | HORIBA Scientific | – | To align magnetic stir bar while placing inserts inside cuvette; Provided with purchase of ViewSizer 3000 |
| De-ionized water | VWR | 02-0201-1000 | To clean cuvettes |
| Desktop computer with monitor, keyboard, mouse, and all necessary cables | Dell | – | Provided with purchase of ViewSizer 3000 |
| Ethanol (70-100%) | Millipore Sigma | – | To clean cuvettes |
| ExoQuick ULTRA | System Biosciences | EQULTRA-20A-1 | For isolation of human plasma extracellular vesicles |
| Glass scintillation vials with lids | Thermo Scientific | B780020 | To clean cuvettes |
| "Hook" tool | Excelta | – | Provided with purchase of ViewSizer 3000 |
| Lint-free microfiber cloth | Texwipe | TX629 | To clean cuvettes and cover work surface |
| Microcentrifuge tubes, 2 mL | Eppendorf | 22363344 | For isolation of human plasma extracellular vesicles |
| Stir bar | Sp Scienceware | F37119-0005 | |
| Suprasil Quartz cuvette with cap | Agilent Technologies | AG1000-0544 | Initially provided with purchase of ViewSizer 3000 |
| ViewSizer 3000 | HORIBA Scientific | – | Nanoparticle tracking instrument |
Riferimenti
- Colombo, M., Raposo, G., Théry, C. Biogenesis, secretion, and intercellular interactions of exosomes and other extracellular vesicles. Annual Review of Cell and Developmental Biology. 30, 255-289 (2014).
- Hessvik, N. P., Llorente, A. Current knowledge on exosome biogenesis and release. Cellular and molecular life sciences: CMLS. 75, 193-208 (2018).
- Johnstone, R. M., Adam, M., Hammond, J. R., Orr, L., Turbide, C. Vesicle formation during reticulocyte maturation. Association of plasma membrane activities with released vesicles (exosomes). The Journal of Biological Chemistry. 262, 9412-9420 (1987).
- Théry, C., Ostrowski, M., Segura, E. Membrane vesicles as conveyors of immune responses. Nature Reviews Immunology. 9, 581-593 (2009).
- Yáñez-Mó, M., et al. Biological properties of extracellular vesicles and their physiological functions. Journal of Extracellular Vesicles. 4, 27066 (2015).
- Lo Cicero, A., Stahl, A., Raposo, G. Extracellular vesicles shuffling intercellular messages: for good or for bad. Current Opinion in Cell Biology. 35, 69-77 (2015).
- Raposo, G., Stoorvogel, W. Extracellular vesicles: exosomes, microvesicles, and friends. The Journal of Cell Biology. 200, 373-383 (2013).
- Mathivanan, S., Ji, H., Simpson, R. J. Exosomes: extracellular organelles important in intercellular communication. Journal of Proteomics. 73, 1907-1920 (2010).
- Zhang, M., et al. Methods and technologies for exosome isolation and characterization. Small Methods. 2, 1800021 (2018).
- Szatanek, R., et al. The methods of choice for extracellular vesicles (EVs) characterization. International Journal of Molecular Sciences. 18, (2017).
- Erdbrügger, U., Lannigan, J. Analytical challenges of extracellular vesicle detection: A comparison of different techniques. Cytometry. Part A: The Journal of the International Society for Analytical Cytology. 89, 123-134 (2016).
- Konoshenko, M. Y., Lekchnov, E. A., Vlassov, A. V., Laktionov, P. P. Isolation of Extracellular Vesicles: General Methodologies and Latest Trends. BioMed Research International. 2018, 1-27 (2018).
- Cvjetkovic, A., Lötvall, J., Lässer, C. The influence of rotor type and centrifugation time on the yield and purity of extracellular vesicles. Journal of Extracellular Vesicles. 3, (2014).
- Taylor, D. D., Shah, S. Methods of isolating extracellular vesicles impact down-stream analyses of their cargoes. Methods. 87, 3-10 (2015).
- Desdín-Micó, G., Mittelbrunn, M. Role of exosomes in the protection of cellular homeostasis. Cell Adhesion & Migration. 11, 127-134 (2017).
- Kanemoto, S., et al. Multivesicular body formation enhancement and exosome release during endoplasmic reticulum stress. Biochemical and Biophysical Research Communications. 480, 166-172 (2016).
- Benedikter, B. J., et al. Cigarette smoke extract induced exosome release is mediated by depletion of exofacial thiols and can be inhibited by thiol-antioxidants. Free Radical Biology & Medicine. 108, 334-344 (2017).
- Saeed-Zidane, M., et al. Cellular and exosome mediated molecular defense mechanism in bovine granulosa cells exposed to oxidative stress. PloS One. 12, 0187569 (2017).
- Wang, K., et al. Mechanical stress-dependent autophagy component release via extracellular nanovesicles in tumor cells. ACS Nano. 13, 4589-4602 (2019).
- King, H. W., Michael, M. Z., Gleadle, J. M. Hypoxic enhancement of exosome release by breast cancer cells. BMC Cancer. 12, 421 (2012).
- Bonzini, M., et al. Short-term particulate matter exposure induces extracellular vesicle release in overweight subjects. Environment Research. 155, 228-234 (2017).
- Neri, T., et al. Particulate matter induces prothrombotic microparticle shedding by human mononuclear and endothelial cells. Toxicology In Vitro. 32, 333-338 (2016).
- Flaherty, S. E., et al. A lipase-independent pathway of lipid release and immune modulation by adipocytes. Science. 363, 989-993 (2019).
- van Niel, G., D’Angelo, G., Raposo, G. Shedding light on the cell biology of extracellular vesicles. Nature Reviews. Molecular Cell Biology. 19, 213-228 (2018).
- Dragovic, R. A., et al. Sizing and phenotyping of cellular vesicles using Nanoparticle Tracking Analysis. Nanomedicine: Nanotechnology, Biology, and Medicine. 7, 780-788 (2011).
- Saveyn, H., et al. Accurate particle size distribution determination by nanoparticle tracking analysis based on 2-D Brownian dynamics simulation. Journal of Colloid and Interface Science. 352, 593-600 (2010).
- Vander Meeren, P., Kasinos, M., Saveyn, H. Relevance of two-dimensional Brownian motion dynamics in applying nanoparticle tracking analysis. Methods in Molecular Biology. , 525-534 (2012).
- Filipe, V., Hawe, A., Jiskoot, W. Critical evaluation of Nanoparticle Tracking Analysis (NTA) by NanoSight for the measurement of nanoparticles and protein aggregates. Pharmaceutical Research. 27, 796-810 (2010).
- Bachurski, D., et al. Extracellular vesicle measurements with nanoparticle tracking analysis – An accuracy and repeatability comparison between NanoSight NS300 and ZetaView. Journal of Extracellular Vesicles. 8, 1596016 (2019).
- Varga, Z., et al. Hollow organosilica beads as reference particles for optical detection of extracellular vesicles. Journal of Thrombosis and Haemostasis. 16, 1646-1655 (2018).
- Serrano-Pertierra, E., et al. Extracellular vesicles: Current analytical techniques for detection and quantification. Biomolecules. 10, (2020).
- Maguire, C. M., Rösslein, M., Wick, P., Prina-Mello, A. Characterisation of particles in solution – a perspective on light scattering and comparative technologies. Science and Technology of Advanced Materials. 19, 732-745 (2018).
- Bohren, C. F., Huffman, D. R. . Absorption and Scattering of Light by Small Particles. , (1983).

