Et eksperiment ved hjelp av funksjonell nær-infrarød spektroskopi og robotassisterte flerledds pekebevegelser i underekstremiteten
Summary
Det er anslått at 1 av 6 individer over hele verden vil få et slag i livet, noe som forårsaker langvarig funksjonshemming, hvis rehabiliteringsmekanismer fortsatt er dårlig forstått. Denne studien foreslår en protokoll for å evaluere hjerneaktivering ved funksjonell nær-infrarød spektroskopi (fNIRS) under en robotterapi-økt i underekstremitetene.
Abstract
Stroke påvirker ca 17 millioner individer over hele verden hvert år og er en ledende årsak til langvarig funksjonshemming. Robotterapi har vist løfte om å hjelpe slagpasienter til å gjenvinne tapte motorfunksjoner. En potensiell avenue for å øke forståelsen av hvordan motorisk utvinning oppstår, er å studere hjerneaktivering under bevegelsene som er målrettet av terapi hos friske individer. Funksjonell nær-infrarød spektroskopi (fNIRS) har dukket opp som en lovende neuroimaging teknikk for å undersøke nevrale grunnlaget for motorisk funksjon. Denne studien hadde som mål å undersøke fNIRS nevrale korrelater av komplekse bevegelser i underekstremitetene hos friske personer. Deltakerne ble bedt om å utføre sykluser av hvile og bevegelse i 6 minutter ved hjelp av en robotenhet for motorrehabilitering. Oppgaven krevde koordinerte kne- og ankelleddbevegelser for å peke på mål som vises på en dataskjerm. To eksperimentelle forhold med ulike nivåer av bevegelsesassistanse fra roboten ble utforsket. Resultatene viste at fNIRS-protokollen effektivt oppdaget hjernegrupper assosiert med motorstyring under oppgaven. Spesielt viste alle forsøkspersonene større aktivering i det kontralaterale premotoriske området under ikke-assistansetilstanden sammenlignet med den assisterte tilstanden. Avslutningsvis synes fNIRS å være en verdifull tilnærming for å oppdage endringer i oksyhemoglobinkonsentrasjon assosiert med multi-joint pointing bevegelser av underekstremiteten. Denne forskningen kan bidra til forståelsen av slagmotoriske gjenopprettingsmekanismer og kan bane vei for forbedrede rehabiliteringsbehandlinger for slagpasienter. Imidlertid er det behov for ytterligere forskning for å fullt ut belyse potensialet til fNIRS i å studere motorisk funksjon og dens anvendelser i kliniske omgivelser.
Introduction
Epidemiologiske data indikerer at det på verdensbasis er ~ 17 millioner nye tilfeller av hjerneslag hvert år, med en økning i forekomst i lav- og mellominntektsland1. Antall nye tilfeller anslås å øke til 77 millioner innen 20302. Motorisk svekkelse på grunn av hjerneslag påvirker ofte pasientens mobilitet og deltakelse i dagliglivets aktiviteter, noe som bidrar til lav livskvalitet. Tradisjonell motorrehabilitering inkluderer manuell terapi, men i løpet av de siste tiårene har robotsystemer for rehabilitering blitt utviklet. Disse systemene kan levere behandling med høy intensitet, dose, kvantifiserbarhet, pålitelighet, repeterbarhet og fleksibilitet3 og har vist potensial som effektive rehabiliteringsbehandlinger for både akutte og kroniske slagpasienter 4,5,6. I tillegg til å levere terapi, kan robotsystemer for rehabilitering brukes som evalueringsverktøy, da de kan utstyres med sensorer som kan måle pasientbevegelser kinematiske/kinetiske data 7,8. For motorrehabilitering i øvre ekstremiteter har slike data ikke bare vist seg å være nyttige for å vurdere nivået av pasientens motoriske utvinning fremkalt av robotbehandling og tjent som et supplerende verktøy til tradisjonelle kliniske vurderinger 9,10, men det har også bidratt til å fremme forståelsen av prosessen med motorisk gjenoppretting fra slag11, 12 samt nevral kontroll av bevegelse og motorisk læring hos friske forsøkspersoner 3,13,14. Som et resultat har disse funnene gitt grunnlag for å styrke rehabiliteringsbehandlinger15.
I løpet av de siste to tiårene har mange robotinnretninger for nevrorehabilitering i underekstremitetene blitt foreslått, alt fra eksoskjeletter som støtter pasientens kroppsvekt under gange (f.eks. Over tredemølle, som Lokomat16) til stasjonære robotsystemer som tillater pasienten å trene ankelen, kneet eller foten uten å gå (som Rutgers Ankle17, High-Performance Ankel Rehabilitation Robot18, og Gwangju Institute of Science and Technology (GIST) ankel / fotrehabiliteringsrobot19) eller aktive fotortoser som er aktiverte eksoskjeletter som bæres av pasienten for å gå over bakken eller over en tredemølle (for eksempel Powered Gait Orthosis20 og MIT Anklebot21). Se 22,23,4 for en gjennomgang av roboter for rehabilitering av underekstremiteter.
Resultater av kliniske studier av robotinnretninger for rehabilitering av underekstremiteter på slagpasienter har vært oppmuntrende og har vist at disse systemene kan forbedre leddenes bevegelsesområde (ROM), muskelstyrke eller gange, avhengig av den spesifikke enheten og klinisk protokoll (se 24,25 for en gjennomgang av effekten av underekstremitetsroboter for rehabilitering). Mens det har blitt postulert at robotassistert terapi fremmer nevroplastiske forandringer, noe som til slutt resulterer i forbedrede motoriske evner26, hvordan prosessen med motorisk gjenoppretting fra hjerneslag nøyaktig oppstår og hvilke robottreningsprotokoller optimaliserer prosessen med gjenoppretting av motoriske evner i underekstremitetene, forblir for det meste uklart. Faktisk er det en betydelig, økende forskjell mellom den økende utviklingen av rehabiliteringsroboter (enten av akademiske forskere eller kommersielle enheter) og den begrensede forståelsen av de nevrofysiologiske mekanismene som ligger til grunn for motorisk gjenoppretting4. Målinger av bevegelseskinmatikk eller leddmomenter tatt med innebygde sensorer har bidratt til kvantitativt å beskrive motoriske atferdsendringer som oppstår når pasienter gjenoppretter motoriske evneri underekstremitetene 27,28,29, og delvis fyller dette gapet. Imidlertid har de nevrale korrelatene som ligger til grunn for slike endringer blitt mindre undersøkt. Dette skyldes flere grunner.
Hjernefunksjonell bildebehandling er tidkrevende og noen ganger vanskelig å fullføre i sammenheng med kliniske studier, som ofte krever å holde pasientbyrden minimal for å maksimere sannsynligheten for pasienttilslutning til studien. Dette gjelder spesielt for personer som har hatt et slag, gitt det faktum at tretthet etter slag og muskelsvakhet ofte observeres30. Også bildebehandlingsmodaliteter som er basert på magnetfelt, for eksempel funksjonell magnetisk resonansavbildning (fMRI), krever at både pasient- og robotmaskinvare er magnetsikker.
Blant ikke-invasive bildebehandlingsmodaliteter er funksjonell nær-infrarød spektroskopi (fNIRS) en avbildningsteknikk spesielt egnet for å vurdere områder av hjerneaktivering hos personer som gjennomgår robotbehandling. På samme måte som fMRI måler fNIRS oksygenering/deoksygenering i blodet i hjernen. Imidlertid, i motsetning til fMRI, er fNIRS fullt kompatibel med robotmaskinvare, og den er ofte bærbar, selv om den kan brukes ved sengen. Dessuten har fNIRS lave kostnader og mindre følsomhet for bevegelsesartefakter 31,32,33.
Til tross for sine klare fordeler og utbredt bruk i mange kliniske innstillinger siden den første introduksjonen på slutten av 70-tallet34, har bare noen få studier brukt fNIRS til å kvantifisere hjerneaktivering assosiert med bevegelser i underekstremitetene og slagmotorisk gjenoppretting. FNIRS-studier rettet mot å belyse mekanismer for nevral kontroll av bevegelse og / eller mekanismer eller evaluering av motorisk utvinning fra hjerneslag har for det meste undersøkt enkeltleddsbevegelser (f.eks. Dorsifleksjon, plantarfleksjon eller kneekstensjonsbevegelser35,36,37), gange 38,39,40,41,42,43 eller sykling44. Se45 for en gjennomgang. Tilsvarende har fNIRS-studier på robotassistert terapi for underekstremiteten hovedsakelig fokusert på robotassistert gangrehabilitering; Se46 for en gjennomgang. Noen få studier har fokusert på å bruke fNIRS som en del av et Brain-Computer Interface (BCI) -system for å utlede kontrollsignaler for robotenheter47,48; Selv om dette forskningsområdet også er avhengig av behandling av fNIRS-signaler, er målet annerledes og hovedsakelig fokusert på å dekode pasientens intensjoner (f.eks. Pasienter med alvorlige motoriske funksjonshemninger).
Pilotstudien som presenteres her, er en del av en innledende innsats for å undersøke effekten av et robotsystem for rehabilitering av underekstremiteter. Roboten kan levere målorientert rehabilitering av underekstremiteter som involverer trening i hverdagslige flerleddsbevegelser, samt levere terapi til enkeltledd (f.eks. kne eller ankel) i underekstremiteten (dvs. implementere et rehabiliteringsprogram nedenfra og opp).
Studien hadde som mål å undersøke muligheten for en eksperimentell protokoll som krevde oppkjøp av fNIRS-data under utførelsen av pekebevegelser i underekstremitetene. Varigheten av datainnsamlingsperioden i denne studien, som var begrenset til 6 minutter, er kortere enn typiske fNIRS-protokoller. Dette var et bevisst valg gjort med sikte på å forbedre den praktiske og kliniske anvendeligheten av denne forskningen, spesielt hos pasienter med begrenset mobilitet eller styrke. Identifisering av fNIRS korrelater av slike komplekse flerleddsbevegelser og innsikt i hvordan hjerneaktivering ble modulert av robotassistanse var også interessante punkter. For dette formålet ble det gjennomført to økter med eksperimenter med de samme deltakerne: en uten robotassistanse og en med robotassistanse. Til slutt er det viktig å merke seg at denne studien fokuserte på friske personer for å etablere et grunnlag for fremtidig forskning når det gjelder registrering av protokollgjennomførbarhet og evaluering av hjerneaktivering under bevegelser målrettet av robotterapi.
Apparat
En bærbar robot designet for å levere rehabilitering av underekstremiteter (se figur 1) ble brukt til å utføre våre eksperimenter. Roboten har et 3D-tilgjengelig arbeidsområde og er kompakt og lett, veier omtrent 35 lb., noe som gjør det enkelt å transportere og installere.
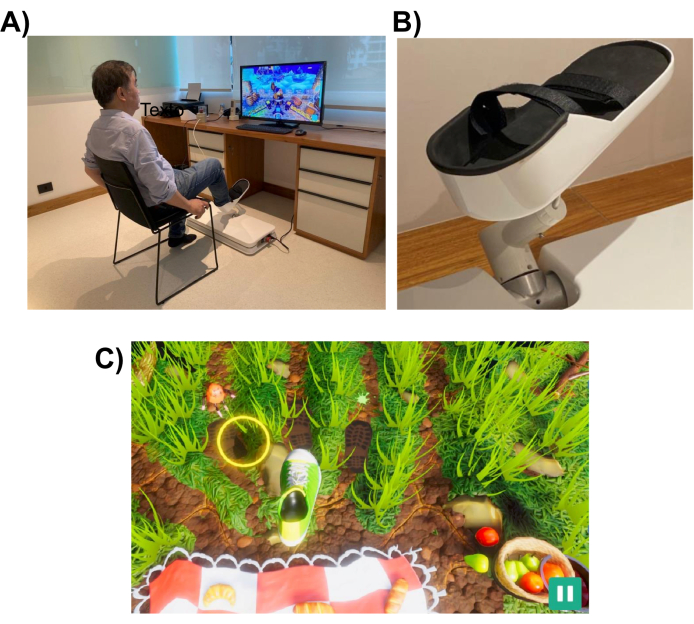
Figur 1: Eksperimentelt oppsett. (A) Robotsystemet (installert på gulvet) designet for underekstremiteten. En frivillig vises ved hjelp av grensesnittet med høyre fot. (B) Støttestruktur for forsøkspersonens fot som muliggjør festing til robotsystemet. (C) Et skjermbilde av piknikspillet. Målet med spillet er å flytte foten (grønn og hvit sko) til målet (gul sirkel). Klikk her for å se en større versjon av denne figuren.
Robotsystemet er designet for å hjelpe en pasient med å utføre bevegelser i underekstremitetene som ligner de som utføres i hverdagslige oppgaver, for eksempel å peke eller sparke. Den bruker interaktive virtuelle virkelighetsspill, som vises på en dataskjerm eller en TV-skjerm plassert foran robotenheten (se figur 1). Robotendens effektor er festet til pasientens underekstremitet (f.eks. ankel), og posisjonen er kartlagt til posisjonen til en markør på skjermen. Et typisk spill viser pasientens bevegelsesmål (f.eks. objektet å peke på eller hvor du skal sparke ballen).
For å fullføre bevegelsesoppgaven kan roboten hjelpe pasienten med et nivå av assistanse som kan variere fra full assistanse til ingen. Nivået på robotassistanse velges i begynnelsen av hver rehabiliteringsøkt basert på pasientens grad av motorisk funksjonsnedsettelse. Bevegelsene som utføres av motivet, brukes av spillet til å score pasientens ytelse og gi dem tilbakemelding på deres ytelse (f.eks. ROM, antall bevegelser og nivå av robothjelp). Spillene er designet for å være interaktive og underholdende for å opprettholde pasientens interesse og oppmerksomhet. I denne studien spilte deltakerne “Picnic-spillet”, der spilleren måtte stoppe insektene fra å nå håndkleet og stjele maten (se figur 1, nederste panel, for et skjermbilde).
Datainnsamlingen ble utført med et bærbart fNIRS-innsamlingssystem med to forskjellige kontinuerlige bølgeoptoder (760 nm og 850 nm), 8 dual-tip LED-kilder og 8 dual-tip aktive detektorer. Signalene ble samlet inn ved hjelp av en samplingsfrekvens på 10,17 Hz. En bærbar PC ble brukt til kalibreringsoptimalisering og signalopptak ved hjelp av et Wi-Fi-nettverk opprettet av fNIRS-systemet.
En hette ble brukt til å holde optodene på de forhåndsbestemte stedene. Kildene og detektorene ble plassert i henhold til det 10-10 internasjonale EEG-systemet i en rutenettsromlig fordeling. Hver fNIRS-kanal ble definert av et kildedetektorpar med interoptodeavstander på ca. 30 mm. Optodene ble plassert over de supplerende motor-, premotor- og motorområdene på stedene vist i figur 2. Totalt antall kanaler var 28, hvor 8 var kortdistansekanaler som ble koblet til hver kilde ved hjelp av en fiberoptikkadapter til en enkelt detektor. Gitt maskinvarens multipleksingsoppsett, er det mulig å skaffe kortdistanseinformasjon fra alle kilder ved hjelp av bare en detektor.
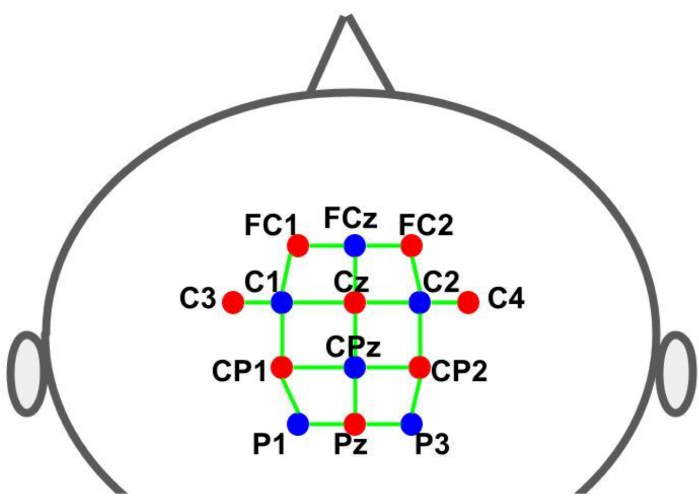
Figur 2: Montasjeoppsett med 10-10 EEG-systemet. Bokstavene og tallene angir kilde-/detektorplasseringene. De røde og blå prikkene representerer henholdsvis kilde- og detektoroptodene. De grønne linjene representerer fNIRS-kanalene som består av kilde- og detektorpar. Klikk her for å se en større versjon av denne figuren.
Eksperimentelt design
Eksperimentet ble utført under to forskjellige eksperimentelle forhold, forskjellig i nivået av assistanse fra roboten for fagets bevegelser. I den første tilstanden var roboten programmert til ikke å gi noen hjelp til fagets bevegelser, mens i den andre tilstanden styrte roboten motivets fot- og benbevegelser (robotassistert bevegelse).
Hvert eksperiment fulgte et blokkdesignparadigme som involverte vekslende sykluser av en motoroppgave (å spille spillet – 30 s) og hvile (30 s), som illustrert i figur 3. Starten og avslutningen av hver fase (spill / spill eller hvile) ble visuelt signalisert til motivet gjennom dataskjermen. I hvilefasen ble det vist en melding som indikerte en pause. Hver syklus (lek/spill + hvile) hadde en varighet på 60 s og ble gjentatt seks ganger, noe som resulterte i en total kjøretid på 360 s (6 min).
Deltakerne spilte “Picnic game”, hvor målet var å hindre insekter i å nå håndkleet og stjele mat. Denne kampen involverte en sekvens av bevegelser i underekstremitetene, som startet fra et utpekt hjemmemål (startposisjon) og strakte seg mot ett av tre ytre mål før det returnerte til hjemmemålet. På skjermen var de ytre målene visuelt representert som animerte bevegelige insekter, som deltakerne måtte nå og gå på. Det var tre ytre mål, hvert tilfeldig presentert like mange ganger, sammen med et felles hjemmemål for hver bevegelse. Avstanden som foten trengte for å reise fra hjemmemålet til posisjonen til de ytre målene dannet en bue, omtrent 26 cm. Den motoriske oppgaven krevde utførelse av flerleddsbevegelser, krevende koordinering mellom knefleksjon / ekstensjon, plantarfleksjon og dorsifleksjonsbevegelser.
FNIRS-dataopptakene ble synkronisert med de visuelle stimuli presentert av spillet til motivet gjennom en transistor-transistor-logikk (TTL) puls generert av roboten. Pulser ble generert i begynnelsen av hver fase (lek/spill og hvile). Dermed ble all timingkontroll utført av spillet, som ga visuelle signaler (mål) til deltakeren for å starte hver bevegelse, sendte TTL-signaler til fNIRS-systemet for å markere hjerneaktivitetsopptakene, og, hvis eksperimentet krevde det, sendte signaler til robotstyringssystemet for å initiere bevegelseshjelp.
Protocol
Representative Results
Discussion
I denne proof-of-concept-studien ble muligheten for å gjøre slutninger om hjerneaktiveringskartlegging ved hjelp av fNIRS-data fra friske personer mens de trente med forskjellige typer bevegelser ved hjelp av en robot for rehabilitering av underekstremiteter undersøkt. Typiske fNIRS-registreringsøkter hos voksne er lengre enn 6 min54. For å gjøre opptak gjennomførbare i forbindelse med en rehabiliteringsinnstilling, må imidlertid den totale varigheten av eksperimentet minimeres for å unng…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Meningene, hypotesene, konklusjonene og anbefalingene fra denne studien er forfatternes og representerer ikke nødvendigvis finansieringsorganets meninger. JRS takker Sao Paulo Research Foundation (FAPESP, stipendnummer 2021/05332-8, 2018/04654-9, 2018/21934-5 og 2023/02538-0) og Jackson Cionek for teknologisk støtte. AMM og Vivax Ltda er takknemlige for FAPESP (São Paulo Research Foundation) og FINEP (Brazilian Innovation Agency). Dette prosjektet ble finansiert med tilskudd fra FAPESP (tilskuddsnummer 2018/09559-4) og FINEP (tilskuddsnummer 2019/09933-6).
Materials
| 32 inch Smart TV | Samsung | N/A | TV connected to robot via HDMI cable |
| 8-detector silicon photodiode (SiPD) optodes for optical detection with dual tip | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| 8-source optodes bundle for optical illumination with dual tip | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| Aurora acquisition software | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| Laptop Precision XPS 13 | Dell Technologies (Round Rock, TX, USA) | ||
| nirsLAB fNIRS Analysis software | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| NIRSports2 fNIRS acquisition system | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | It has two different continuous wave optics (760 and 850 nm), 8 dual-ended LED sources and 8 dual-ended active detectors. |
| R | R-project.org (open source software) | https://www.r-project.org/ | |
| Standard cut cap, black color for up to 128 holders. | Easycap GmbH (Wörthsee, Germany) | https://www.easycap.de/ | |
| Vivax Assistive Rehabilitation Machine (ARM) | Vivax Ltda (São Paulo, Brazil) | https://vivaxbr.com/home/ | It is a portable robot designed to deliver lower limb rehabilitation. It has a 3D reachable workspace and is compact and light, weighing about 35 lb., which makes it easy to transport and to install. |
Riferimenti
- GBD 2016 Stroke Collaborators. Global, regional, and national burden of stroke, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. The Lancet. Neurology. 18 (5), 439-458 (2019).
- GBD 2019 Stroke Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. The Lancet. Neurology. 20 (10), 795-820 (2021).
- Huang, V. S., Krakauer, J. W. Robotic neurorehabilitation: a computational motor learning perspective. Journal of NeuroEngineering and Rehabilitation. 6, 5 (2009).
- Hobbs, B., Artemiadis, P. A Review of Robot-Assisted Lower-Limb Stroke Therapy: Unexplored Paths and Future Directions in Gait Rehabilitation. Frontiers in neurorobotics. 14, 19 (2020).
- Bertani, R., Melegari, C., De Cola, M. C., Bramanti, A., Bramanti, P., Calabrò, R. S. Effects of robot-assisted upper limb rehabilitation in stroke patients: a systematic review with meta-analysis. Neurological Sciences. 38 (9), 1561-1569 (2017).
- Warutkar, V., Dadgal, R., Mangulkar, U. R. Use of robotics in gait rehabilitation following stroke: A review. Cureus. 14 (11), e31075 (2022).
- Dipietro, L., et al. Changing motor synergies in chronic stroke. Journal of Neurophysiology. 98 (2), 757-768 (2007).
- Dipietro, L., et al. Learning, not adaptation, characterizes stroke motor recovery: evidence from kinematic changes induced by robot-assisted therapy in trained and untrained task in the same workspace. IEEE Trans Neural Syst Rehabil Eng. 20 (1), 48-57 (2012).
- Bosecker, C., Dipietro, L., Volpe, B., Krebs, H. I. Kinematic robot-based evaluation scales and clinical counterparts to measure upper limb motor performance in patients with chronic stroke. Neurorehabilitation and Neural Repair. 24 (1), 62-69 (2010).
- Krebs, H. I., et al. Robotic measurement of arm movements after stroke establishes biomarkers of motor recovery. Stroke. 45 (1), 200-204 (2014).
- Volpe, B. T., et al. Robotic devices as therapeutic and diagnostic tools for stroke recovery. Archives of Neurology. 66 (9), 1086-1090 (2009).
- Hogan, N., et al. Motions or muscles? Some behavioral factors underlying robotic assistance of motor recovery. Journal of Rehabilitation Research and Development. 43 (5), 605-618 (2006).
- Shadmehr, R., Wise, S. P. . The Computational Neurobiology of Reaching and Pointing: A Foundation for Motor Learning. , (2005).
- Dipietro, L., Poizner, H., Krebs, H. I. Spatiotemporal dynamics of online motor correction processing revealed by high-density electroencephalography. J Cogn Neurosci. 26 (9), 1966-1980 (2014).
- Krebs, H., et al. Rehabilitation robotics: Performance-based progressive robot-assisted therapy. Autonomous Robots. 15, 7-20 (2003).
- Colombo, G., Joerg, M., Schreier, R., Dietz, V. Treadmill training of paraplegic patients using a robotic orthosis. Journal of Rehabilitation Research and Development. 37 (6), 693-700 (2000).
- Girone, M., et al. A Stewart platform-based system for ankle telerehabilitation. Autonomous Robots. 10, 203-212 (2001).
- Saglia, J. A., Tsagarakis, N. G., Dai, J. S., Caldwell, D. G. A high-performance redundantly actuated parallel mechanism for ankle rehabilitation. The International Journal of Robotics Research. 28 (9), 1216-1227 (2009).
- Yoon, J., Ryu, J. A novel reconfigurable ankle/foot rehabilitation robot. , 2290-2295 (2005).
- Ruthenberg, B. J., Wasylewski, N. A., Beard, J. E. An experimental device for investigating the force and power requirements of a powered gait orthosis. Journal of Rehabilitation Research and Development. 34 (2), 203-213 (1997).
- Forrester, L. W., et al. Clinical application of a modular ankle robot for stroke rehabilitation. NeuroRehabilitation. 33 (1), 85-97 (2013).
- Díaz, I., Gil, J. J., Sánchez, E. Lower-limb robotic rehabilitation: Literature review and challenges. Journal of Robotics. 2011, 759764 (2011).
- Zhang, X., Yue, Z., Wang, J. Robotics in lower-limb rehabilitation after stroke. Behavioural Neurology. 2017, 3731802 (2017).
- Zhang, M., Davies, T. C., Xie, S. Effectiveness of robot-assisted therapy on ankle rehabilitation – a systematic review. Journal of NeuroEngineering and Rehabilitation. 10, 30 (2013).
- Lo, K., Stephenson, M., Lockwood, C. Effectiveness of robotic assisted rehabilitation for mobility and functional ability in adult stroke patients: a systematic review protocol. JBI Database of Systematic Reviews and Implementation Reports. 15 (1), 39-48 (2017).
- Belda-Lois, J. M., et al. Rehabilitation of gait after stroke: a review towards a top-down approach. Journal of NeuroEngineering and Rehabilitation. 8, 66 (2011).
- Bortole, M., et al. The H2 robotic exoskeleton for gait rehabilitation after stroke: early findings from a clinical study. Journal of NeuroEngineering and Rehabilitation. 12, 54 (2015).
- Banala, S. K., Kim, S. H., Agrawal, S. K., Scholz, J. P. Robot assisted gait training with active leg exoskeleton (ALEX). IEEE Transactions on Neural Systems and Rehabilitation Engineering. 17 (1), 2-8 (2009).
- Bartenbach, V., Wyss, D., Seuret, D., Riener, R. A lower limb exoskeleton research platform to investigate human-robot interaction. 2015 IEEE International Conference on Rehabilitation Robotics (ICORR). 2015, 600-605 (2015).
- Hinkle, J. L., et al. Poststroke fatigue: Emerging evidence and approaches to management: A scientific statement for healthcare professionals from the American heart association. Stroke. 48 (7), e159-e170 (2017).
- Balardin, J. B., Zimeo Morais, G. A., Furucho, R. A., Trambaiolli, L. R., Sato, J. R. Impact of communicative head movements on the quality of functional near-infrared spectroscopy signals: negligible effects for affirmative and negative gestures and consistent artifacts related to raising eyebrows. Journal of Biomedical Optics. 22 (4), 4601 (2017).
- Nazeer, H., Naseer, N., Mehboob, A., Khan, M. J., Khan, R. A., Khan, U. S., Ayaz, Y. Enhancing classification performance of fNIRS-BCI by identifying cortically active channels using the z-score method. Sensors. 20 (23), 6995 (2020).
- Ayaz, H., et al. Optical imaging and spectroscopy for the study of the human brain: status report. Neurophotonics. 9, S24001 (2022).
- Chen, W. L., et al. Functional near-infrared spectroscopy and its clinical application in the field of neuroscience: Advances and future directions. Frontiers in Neuroscience. 14, 724 (2020).
- Yamamoto, K., Miyata, T., Onozuka, A., Koyama, H., Ohtsu, H., Nagawa, H. Plantar flexion as an alternative to treadmill exercise for evaluating patients with intermittent claudication. European Journal of Vascular and Endovascular Surgery. 33 (3), 325-329 (2007).
- Formenti, D., et al. Effects of knee extension with different speeds of movement on muscle and cerebral oxygenation. PeerJ. 6, 5704 (2018).
- Miyai, I., et al. Cortical mapping of gait in humans: a near-infrared spectroscopic topography study. NeuroImage. 14 (5), 1186-1192 (2001).
- Miyai, I., et al. Premotor cortex is involved in restoration of gait in stroke. Annals of Neurology. 52 (2), 188-194 (2002).
- Mihara, M., et al. Sustained prefrontal activation during ataxic gait: a compensatory mechanism for ataxic stroke?. NeuroImage. 37 (4), 1338-1345 (2007).
- Rea, M., et al. Lower limb movement preparation in chronic stroke: A pilot study toward an fNIRS-BCI for gait rehabilitation. Neurorehabilitation and Neural Repair. 28 (6), 564-575 (2014).
- Holtzer, R., Verghese, J., Allali, G., Izzetoglu, M., Wang, C., Mahoney, J. R. Neurological gait abnormalities moderate the functional brain signature of the posture first hypothesis. Brain Topography. 29 (2), 334-343 (2016).
- Kim, H. Y., Yang, S. P., Park, G. L., Kim, E. J., You, J. S. Best facilitated cortical activation during different stepping, treadmill, and robot-assisted walking training paradigms and speeds: A functional near-infrared spectroscopy neuroimaging study. NeuroRehabilitation. 38 (2), 171-178 (2016).
- Khan, H., Nazeer, H., Engell, H., Naseer, N., Korostynska, O., Mirtaheri, P. Prefrontal cortex activation measured during different footwear and ground conditions using fNIRS-A case study. 2021 IEEE International Conference on Artificial Intelligence and Mechatronics Systems (AIMS). , 1-6 (2021).
- Lin, P. Y., Chen, J. J., Lin, S. I. The cortical control of cycling exercise in stroke patients: an fNIRS study). Human Brain Mapping. 34 (10), 2381-2390 (2013).
- Yang, M., Yang, Z., Yuan, T., Feng, W., Wang, P. A systemic review of functional near-infrared spectroscopy for stroke: Current application and future directions. Frontiers in Neurology. 10, 58 (2019).
- Berger, A., Horst, F., Müller, S., Steinberg, F., Doppelmayr, M. Current state and future prospects of EEG and fNIRS in robot-assisted gait rehabilitation: A brief review. Frontiers in Human Neuroscience. 13, 172 (2019).
- Khan, R. A., Naseer, N., Qureshi, N. K., et al. fNIRS-based Neurorobotic Interface for gait rehabilitation. J NeuroEngineering Rehabil. 15 (1), 7 (2018).
- Khan, H., Naseer, N., Yazidi, A., Eide, P. K., Hassan, H. W., Mirtaheri, P. Analysis of Human Gait Using Hybrid EEG-fNIRS-Based BCI System: A Review. Front. Hum. Neurosci. 14, (2020).
- Delpy, D. T., Cope, M. Quantification in tissue near-infrared spectroscopy. Philosophical Transactions of the Royal Society B: Biological Sciences. 352 (1354), 649-659 (1997).
- Huppert, T. J. Commentary on the statistical properties of noise and its implication on general linear models in functional near-infrared spectroscopy. Neurophotonics. 3, 010401 (2016).
- Alexandre, F., Heraud, N., Oliver, N., Varray, A. Cortical implication in lower voluntary muscle force production in non-hypoxemic COPD patients. PLoS One. 9 (6), 100961 (2014).
- Yoon, T., Vanden Noven, M. L., Nielson, K. A., Hunter, S. K. Brain areas associated with force steadiness and intensity during isometric ankle dorsiflexion in men and women. Experimental Brain Research. 232 (10), 3133-3145 (2014).
- Ciccarelli, O., et al. Identifying brain regions for integrative sensorimotor processing with ankle movements. Experimental Brain Research. 166 (1), 31-42 (2005).
- Udina, C., et al. Functional near-infrared spectroscopy to study cerebral hemodynamics in older adults during cognitive and motor tasks: A review. Frontiers in Aging Neuroscience. 11, 367 (2020).
- Thickbroom, G. W., Phillips, B. A., Morris, I., Byrnes, M. L., Mastaglia, F. L. Isometric force-related activity in sensorimotor cortex measured with functional MRI. Experimental Brain Research. 121 (1), 59-64 (1998).
- Derosière, G., Alexandre, F., Bourdillon, N., Mandrick, K., Ward, T. E., Perrey, S. Similar scaling of contralateral and ipsilateral cortical responses during graded unimanual force generation. NeuroImage. 85 (1), 471-477 (2014).
- Shi, P., Li, A., Yu, H. Response of the cerebral cortex to resistance and non-resistance exercise under different trajectories: A functional near-infrared spectroscopy study. Frontiers in Neuroscience. 15, 685920 (2021).
- Dettmers, C., et al. Relation between cerebral activity and force in the motor areas of the human brain. Journal of Neurophysiology. 74 (2), 802-815 (1995).
- Keisker, B., Hepp-Reymond, M. C., Blickenstorfer, A., Kollias, S. S. Differential representation of dynamic and static power grip force in the sensorimotor network. The European Journal of Neuroscience. 31 (8), 1483-1491 (2010).
- Harada, T., Miyai, I., Suzuki, M., Kubota, K. Gait capacity affects cortical activation patterns related to speed control in the elderly. Experimental Brain Research. 193 (3), 445-454 (2009).
- Saleh, S., et al. The role of premotor areas in dual tasking in healthy controls and persons with multiple sclerosis: An fNIRS imaging study. Frontiers in Behavioral Neuroscience. 12, 296 (2018).
- Bonnal, J., et al. Relation between cortical activation and effort during robot-mediated walking in healthy people: A functional near-infrared spectroscopy neuroimaging study (fNIRS). Sensors. 22 (15), 5542 (2022).
- Shibuya, K., Sadamoto, T., Sato, K., Moriyama, M., Iwadate, M. Quantification of delayed oxygenation in ipsilateral primary motor cortex compared with contralateral side during a unimanual dominant-hand motor task using near-infrared spectroscopy. Brain Research. 1210, 142-147 (2008).
- Dai, T. H., Liu, J. Z., Sahgal, V., Brown, R. W., Yue, G. W. Relationship between muscle output and functional MRI-measured brain activation. Experimental brain research. 140 (3), 290-300 (2001).
- Cabibel, V., Hordacre, B., Perrey, S. Implication of the ipsilateral motor network in unilateral voluntary muscle contraction: the cross-activation phenomenon. Journal of Neurophysiology. 123 (5), 2090-2098 (2020).
- Akselrod, M., Martuzzi, R., Serino, A., vander Zwaag, W., Gassert, R., Blanke, O. Anatomical and functional properties of the foot and leg representation in areas 3b, 1 and 2 of primary somatosensory cortex in humans: A 7T fMRI study. NeuroImage. 159, 473-487 (2017).
- Brigadoi, S., Cooper, R. J. How short is short? Optimum source-detector distance for short-separation channels in functional near-infrared spectroscopy. Neurophotonics. 2 (2), 025005 (2015).
- Funahashi, S. Prefrontal contribution to decision-making under free-choice conditions. Frontiers in Neuroscience. 11, 431 (2017).
- Simon, S. R., Meunier, M., Piettre, L., Berardi, A. M., Segebarth, C. M., Boussaoud, D. Spatial attention and memory versus motor preparation: premotor cortex involvement as revealed by fMRI. Journal of Neurophysiology. 88 (4), 2047-2057 (2002).
- Desmurget, M., Sirigu, A. A parietal-premotor network for movement intention and motor awareness. Trends in Cognitive Sciences. 13 (10), 411-419 (2009).
- Nachev, P., Kennard, C., Husain, M. Functional role of the supplementary and pre-supplementary motor areas. Nature reviews. Neuroscience. 9 (11), 856-869 (2008).
- Thoenissen, D., Zilles, K., Toni, I. Differential involvement of parietal and precentral regions in movement preparation and motor intention. The Journal of neuroscience: the official journal of the Society for Neuroscience. 22 (20), 9024-9034 (2002).
- Al-Quraishi, M. S., Elamvazuthi, I., Tang, T. B., Al-Qurishi, M., Adil, S. H., Ebrahim, M. Bimodal data fusion of simultaneous measurements of EEG and fNIRS during lower limb movements. Brain Sciences. 11 (6), 713 (2021).
- Bishnoi, A., Holtzer, R., Hernandez, M. E. Brain Activation Changes While Walking in Adults with and without Neurological Disease: Systematic Review and Meta-Analysis of Functional Near-Infrared Spectroscopy Studies. Brain sciences. 11 (3), 291 (2021).
- Oh, S., Song, M., Kim, J. Validating attentive locomotion training using interactive treadmill: an fNIRS study. Journal of NeuroEngineering and Rehabilitation. 15 (1), 122 (2018).

