- 00:00개요
- 01:28Principles of Soil Nutrient Analysis
- 04:12Extraction of Nutrients
- 06:21Analyzing Samples for Nitrate
- 07:52Analyzing Samples for Phosphate
- 09:16Analyzing Samples for Potassium
- 11:13Applications
- 13:08Summary
Análise de Nutrientes do Solo: Nitrogênio, Fósforo e Potássio
English
소셜에 공유하기
개요
Fonte: Laboratórios de Margaret Workman e Kimberly Frye – Universidade Depaul
Neste experimento, três macronutrientes do solo são extraídos quimicamente, combinados com reagentes baseados em cores, e analisados usando cor para determinar a concentração de nutrientes presente na amostra do solo.
Nitrogênio, fósforo e potássio são os principais componentes do fertilizante do solo. Esses métodos isolam cada nutriente do solo em uma solução que pode ser analisada usando turbidez e cor para determinar a concentração de nutrientes presentes na amostra do solo. Conhecer a concentração atual informa os cientistas ambientais de uma deficiência de nutrientes ou excedente em solos usados para apoiar a produção vegetal, e também fornece uma visão geral sobre os ciclos biogeoquímicos básicos de um ecossistema.
Principles
Quando quimicamente isolados do solo, nutrientes podem ser detectados usando essa técnica. Nitrogênio e fósforo, tipicamente encontrados na forma de nitratos e fosfatos, são extraídos com um extrator químico que ligará o nutriente do interesse. Uma vez extraído do solo, cada nutriente pode ser combinado com um reagente conhecido que faz com que a solução de nutrientes mude para uma cor específica de nutrientes em uma relação linear, com uma cor mais escura indicando maior concentração do nutriente. Para analisar a concentração de cada nutriente, um reagente químico será usado para colorir cada amostra com um aumento na intensidade da cor indicando aumento da concentração do nutriente.
Nos testes de nitrato de alta e média distância, o metal cádmio é usado para reduzir nitratos (NO3–) para nitritos (NO2–). O cádmio está contido nos travesseiros de pó Nitraver 5 (alta e média faixa) adquiridos e Nitraver 6 (baixa gama).
NO3– + Cd + 2 H+ → NO2– + Cd2+ + H2O
Íons de nitrito então reagem com ácido sulfanílico (em um meio ácido contido no pó NitraVer 5) para formar um sal intermediário de diazonium. Quando juntamente com ácido gentisico (também contido no NitraVer 5), uma solução cor âmbar é formada. A intensidade de cor deste composto é diretamente proporcional à concentração de nitrato da amostra de água e pode ser quantificada usando a caixa de comparador de nitrato com um disco de cor âmbar de nitrato contínuo.
Para fósforo, molise de sódio e pirossulfato de potássio no pó de reagente PhosVer 3 comprado reagem com os fosfatos reativos solúveis para formar um complexo fosfo-molipdato.
H2PO4– + 12 Na2MoO4 + → PMo12O403-
O complexo é então reduzido por ácido ascórbico (também contido em pó PhosVer 3) para formar uma cor azul molhênio. A cor azul é quantificada usando uma caixa comparativa de cor fosfato com um disco de cor azul fosfato contínuo.
Uma caixa comparativa de cores é usada para este método. Esta ferramenta opera com base em intensidades de cores conhecidas para cada concentração entre 0-50 mg/L. Um disco de cor na caixa é virado até que a cor em ambas as janelas de visualização (em branco e amostra) corresponda. Uma vez que as cores sejam combinadas, a concentração de nutrientes correspondente (mg/L) será exibida em uma janela inferior separada na caixa do comparador de cores. Essas caixas são robustas o suficiente para serem usadas com estudantes em qualquer nível até cursos universitários introdutórios e podem ser facilmente transportadas como parte de um kit de teste de solo de campo que pode ser usado em um local de amostragem. Esses métodos permitem testes básicos de nutrientes no laboratório de sala de aula sem exigir equipamentos caros que podem não estar disponíveis. Para garantir a precisão do teste, as soluções padrão de nitrato e fosfato podem ser usadas no lugar de uma amostra nos procedimentos antes de viajar para o local de campo ou iniciar a análise de amostras de solo no laboratório.
Nos testes de potássio, os íons de potássio combinam-se com tetrafenilborato de sódio contido no pó de reagente de potássio 3 comprado para formar tetrafenilborato de potássio, um precipitado branco. O precipitado permanece em suspensão em amostras, causando um aumento da turbidez.
NO3– + Cd + 2 H+ NaB(C6H5)4 + K+ → KB(C6H5)4 + Na+
Uma vareta de medição de potássio é usada para quantificar a quantidade de turbidez que é convertida em concentração de potássio. A vareta tem um ponto preto em uma extremidade que é colocado na amostra até que o ponto não seja mais visível através do precipitado branco. A vareta é incrementalmente marcada para indicar uma escala de visibilidade que é então convertida em concentração de potássio com um gráfico de conversão. Este método é um procedimento barato com equipamento mínimo que pode ser transportado para um local de amostragem ao ar livre e robusto o suficiente para ser usado com alunos em qualquer nível até cursos universitários introdutórios.
Procedure
Results
Each nutrient analysis will result in a concentration reported in mg/L.
Nitrate and Phosphate concentrations will be determined with the color comparator boxes and display the result in the window.

Figure 1. Example color disks for nitrate (left) and phosphate (right) color comparator boxes. Color intensities are on the outer edge of the disks and nutrient concentration (mg/L) are on the inner edge of the disks.
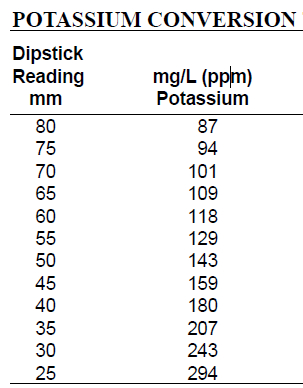
Table 1. Potassium Conversion Table used to convert dipstick potassium reading into mg/L. Locate the dipstick reading on the left column and record the corresponding mg/L concentration on the right column.
| Nitrogen | Phosphorus | Potassium | |
| Nutrient level range in ppm | |||
| Low | 0-15 | 0-25 | 0-60 |
| Medium | 15-30 | 25-50 | 60-100 |
| High | 30+ | 50+ | 100+ |
Table 2. Table of nutrient ranges arranged by categories.
Applications and Summary
Determining the nutrient concentrations for nitrate, phosphates, and potassium can reveal how a soil is functioning in regards to its intended use and how nutrients are cycling through a soil. A nutrient test provides a report of average nutrient concentration (mg/L) for all nutrients tested. In an agricultural setting, knowing the concentration of nutrients can help food producers know when to add fertilizer, how much to add, and which nutrients need supplemented and in what amount. Consistently high nitrogen soils, for instance, would be good for growing nitrogen-demanding crops such as soy and corn. High nitrogen levels are also particularly useful for non-flowering plants because nitrogen is required for any green part of plants. High nitrogen levels can suppress flowering however, if they remain higher than phosphorus levels. Phosphorus controls flowering in plants and is important to any plant production involving flowering or fruiting plants and phosphorus is often added to soils or directly to plants before and during flowering and fruiting life-cycle stages to increase agricultural yields in larger crop size and increased amounts of fruit production per plant. Potassium is involved in catalyzing many chemical reactions required to support plant life including drought tolerance and moisture regulation. Low potassium soils will likely need to be irrigated if soil amendment is not possible. Nutrient concentration can also inform of nutrient deficiencies or surpluses that can be detrimental to plant growth. If a nutrient is too high, amendments can be performed to reduce a surplus, such as adding mulch or tilling the soil. If nutrients are too low to support plant production, fertilization can be used to add nutrients in an amount needed for a specific crop. Low nutrient soil may also have more applicable uses to land managers for recreational or developed (paved surfaces or building construction) spaces.
내레이션 대본
Soil nutrient analyses can be carried out to extract three major soil macronutrients, nitrogen, phosphorus, and potassium, and combine them with color-based reagents to determine their concentration.
Nitrogen, phosphorus, and potassium are major components of soil fertilizer. Knowing their concentration in soils can inform environmental scientists of nutrient deficiency or surplus in soils used to support plant production, and provide a general insight into the basic biogeochemical cycles of an ecosystem.
Soil nutrient analysis can be carried out using chemicals to bind the macronutrient of interest. For nitrogen or phosphorus, reagents are added which react to the presence of the specific macronutrient and produce colored products. Potassium concentration is determined by forming precipitates in an amount proportional to potassium concentration.
These methods are simple, inexpensive, require minimal equipment, and can be carried out in a field setting if desired. This video will illustrate the techniques used to extract and quantify these common soil macronutrients.
To begin analysis, macronutrients are first extracted from collected soil samples. Nitrogen is extracted using calcium sulfate; phosphorus and potassium are extracted using Mehlich 2 solution, a solution of acetic acid, ammonium chloride, hydrochloric acid, hydrofluoric acid, and demineralized water.Boundmacronutrients present in suspension can then be separated from the remaining solid soil components by vacuum filtration.
Once macronutrients have been extracted, their concentration can be determined. For nitrogen, cadmium metal is used to reduce nitrates to nitrites. This cadmium is present in pre-packaged pillows that are added to the soil filtrate. The nitrite ions react with sulfanilic acid to form diazonium salt. This couples with gentisic acid and an amber solution is formed.
For phosphorus, sodium molybdate reacts with the soluble reactive phosphate to form a phospho-molybdate complex. This is then reduced by ascorbic acid to form a molybdenum blue color.
The color intensity of both solutions is proportional to the nutrient concentration. Color comparator boxes are used for analysis of nitrate and phosphate. Samples are compared to a blank, and the color disk is turned until both viewing windows match. The corresponding nutrient concentration in mg/L will be displayed in a separate window. The color intensity of both solutions is proportional to the nutrient concentration.
To quantify potassium, the ions from the soil filtrate combine with sodium tetraphenylborate to form potassium tetraphenylborate, a white precipitate. The precipitate remains in suspension, causing an increase in turbidity.
A potassium dipstick is used to quantify turbidity caused by the precipitate. The dipstick is placed in the sample and lowered until the black dot at the end is no longer visible. The stick is incrementally marked, and readings on this scale can be converted to potassium concentration using a conversion chart.
Now that we are familiar with the principles behind extraction and quantification of soil macronutrients, let’s take a look at how the procedures are carried out in the laboratory.
Once the soil samples have been collected, correctly transported, and stored, they can be brought into the laboratory for analysis, beginning with the nitrogen extraction. First, turn on the balance, set a weigh boat on top, and tare.
Using a spatula, weigh out 10 g of dried, sieved soil sample and transfer to a labeled 100-mL beaker. Next, weigh 0.1 g of calcium sulfate and transfer it to the beaker.
Measure out 20 mL of deionized water with a graduated cylinder and transfer to the beaker. Thoroughly mix the contents of the beaker with a stirring rod. Repeat these additions for each test soil sample. Secure samples on a tabletop shaker and agitate for 1 min.
To begin extraction of phosphorus and potassium from the soils, use a spatula to weigh out 2 g of dried, sieved soil sample, and transfer to a labeled 100-mL beaker. With a graduated cylinder, measure 20 mL of Mehlich 2 soil extractant and transfer to the beaker. Thoroughly mix the contents of the beaker with a stir rod. Secure samples on a tabletop shaker and agitate for 5 min. After extraction, all three nutrient sample sets should be vacuum filtered using a vacuum flask and Büchner funnel.
First, turn on the vacuum jet and slowly pour the soil extract solution into the funnel. Extract should drain from the funnel, into the flask. Pour the filtrate into a clean, labeled 50-mL beaker. Remove the funnel, discard filter paper, and rinse funnel and flask with deionized water. Use an air jet to dry the funnel and flask.
Now the nutrient samples have been filtered, content analysis can begin. For each nutrient test, begin by labeling a color viewing tube with an “S”, for sample. Label a second with a “B” for blank.
Thoroughly rinse both color viewing tubes with deionized water, then shake to remove the remaining rinse water. Add the sample extract to a depth of ¼ inch in the color viewing tube marked “S”. Cap the tube with a rubber stopper and shake for 3 s, then discard the solution.
Next, add the sample extract to both tubes until the meniscus is even with the 5-mL mark on the tubes, at the bottom of the frosted area. Add the contents of one nitrogen reagent pillow to the tube marked “S”. Cap and shake the tube vigorously for 1 min. Immediately place both tubes into the comparator, with tube “B” in the outside hole, and tube “S” on the inside. Leave for 5 min.
Hold the comparator up to a light source and rotate the disc until the color in the window for tube “B” matches that in the window for tube “S”. Record the concentration value displayed in the lower window of the color comparator box.
Samples can also be analyzed for phosphate content using the color comparator. Using a dropper, add 2.5 mL of the filtered phosphorus sample extract to a 25 mL graduated cylinder. Add deionized water to the 25 mL mark, cap with a stopper, and invert to mix. Add the diluted sample extract to about ¼ inch deep in the color viewing tube marked “S” to rinse the tube. Cap with a rubber stopper, and shake for a few seconds before discarding the solution.
Into both tubes, add the sample extract until the meniscus is even with the 5 mL mark. Add the contents of one phosphorus reagent pillow to the “S” tube, cap, and shake vigorously for 1 min. Immediately place the color tubes into the color comparator, with the blank tube in the outside hole, and the sample tube in the inside hole. Leave for 3 min. Hold the comparator up to a light source, and rotate the disc until the window for tube “B” matches the color in the window for tube “S”. Record the value displayed in the window.
Finally, samples can be analyzed for potassium content. Using a dropper, add 3 mL of potassium sample extract to a 25 mL cylinder. Add deionized water to the 21 mL mark on the cylinder, cap firmly with a rubber stopper, and invert. Next, add one potassium 2 reagent pillow to the cylinder. Add 3 mL of an alkaline EDTA solution to the cylinder, cap with a rubber stopper, and invert several times to mix. Let the solution stand for 3 min. Add the contents of one potassium reagent pillow, cap the cylinder and shake vigorously for 10 s. Allow the solution to stand for 3 min as a white turbidity develops.
Looking straight down into the cylinder, slowly insert the potassium dipstick vertically into the solution until the black dot is no longer visible from above. Hold the dipstick in position and rotate the cylinder to view the scale. Record the number on the dipstick scale where the surface of the sample meets the dipstick. Refer to the potassium conversion table to determine the concentration of samples in mg/L. Locate the dipstick reading in the left hand column, and record the corresponding mg/L concentration reported in the right hand column.
Once concentrations are obtained, a table of nutrient ranges can be used to assess sample quality and determine whether sampled soil needs nutrient amendment, and if so, how much. Nutrient amendment can be carried out by application of specific fertilizers.
The ability to analyze the soil nutrient composition of soils has a wide variety of applications, with potential implications for human populations or agricultural ecosystems.
Different crop plants will have different potential nutrient requirements for optimal growing. For example, high nitrogen levels are needed for growing nitrogen-demanding crops, such as soy and corn. High levels of phosphorus can stimulate and enhance flower or fruit production. The ability to measure soil nutrient composition in an intended crop growing area can therefore allow farmers or land managers to supplement the soil with necessary nutrients to grow their intended crop successfully.
The composition of soil can also have implications for its ability to retain water, which can in turn influence its ability to support different flora or fauna. For example, low potassium soils have poor drought tolerance, and may require nutrient amendment, by fertilization of the soil with appropriate amounts of the missing nutrient. Alternatively, irrigation may be necessary to grow any plants that do not display high drought tolerance.
Soil composition and nutrient quality can also help inform land managers to designate appropriate land-use. In areas where the soil has poor nutrient quality, that would require heavy modification or supplementation to grow crop plants, setting aside land for development of buildings or structures may be more appropriate. Alternatively, areas with ideal composition for intended crop growing can be earmarked and set aside, protected from development.
You’ve just watched JoVE’s introduction to Soil Nutrient Analysis. You should now understand the importance of soil macronutrients, how to extract them from soils, and how to determine their concentrations. Thanks for watching!




