Massespektrometrisk Approaches å studere Proteinstruktur og interaksjoner i Lyofiliserte Pulver
Summary
Here, we present detailed protocols for solid-state amide hydrogen/deuterium exchange mass spectrometry (ssHDX-MS) and solid-state photolytic labeling mass spectrometry (ssPL-MS) for proteins in solid powders. The methods provide high-resolution information on protein conformation and interactions in the amorphous solid-state, which may be useful in formulation design.
Abstract
Amid hydrogen / deuterium-utveksling (ssHDX-MS) og sidekjede fotolytisk merking (SSPL-MS), etterfulgt av massespektrometrisk analyse kan være verdifulle for karakterisering av lyofiliserte preparater av protein-terapeutika. Merking etterfulgt av egnet proteolytisk nedbrytning gjør at proteinstruktur og interaksjoner som skal kartlegges med peptid-nivå oppløsning. Siden proteinstrukturelementene er stabilisert ved hjelp av et nettverk av kjemiske bindinger fra sidekjeder av aminosyrer, spesifikk merking av atomer i aminosyrerestene gir innsikt i strukturen og konformasjon av proteinet hovedkjeder og. I motsetning til rutinemessige metoder som brukes for å studere proteiner i frysetørkede faste stoffer (f.eks FTIR), ssHDX-MS og SSPL-MS gi kvantitative og stedsspesifikke informasjon. Omfanget av deuterium inkorporering og kinetiske parametre kan være relatert til hurtig og langsomt utveksling amid bassenger (N raskt, N sakte) og reflekterer de grader direkteree av proteinfolding og struktur i frysetørkede formuleringer. Stabil fotolytisk merking gjennomgår ikke back-utveksling, en fordel over ssHDX-MS. Her gir vi detaljerte protokoller for både ssHDX-MS og SSPL-MS, ved hjelp av myoglobin (Mb) som modell protein i frysetørkede formuleringer som inneholder enten trehalose eller sorbitol.
Introduction
Protein narkotika er den raskest voksende delen av biofarmasøytiske industrien og har lovende nye behandlinger for hittil har vært vanskelige sykdommer, inkludert hormonelle lidelser, kreft og autoimmune sykdommer 1. I 2012 nådde den globale biotherapeutics markedet $ 138 000 000 000, og er forventet å nå $ 179 000 000 000 innen år 2018 2. Proteiner er større og mer skjør enn konvensjonelle små molekyl narkotika og så er mer utsatt for mange typer nedbrytning tre. For å sikre tilstrekkelig holdbarhet og stabilitet, er protein-medikamenter ofte formulert som lyofiliserte (dvs, fryse-tørket) faste pulvere. Imidlertid kan et protein fremdeles gjennomgår nedbrytning i fast tilstand, spesielt hvis den opprinnelige struktur ikke er bevart under lyofiliseringsprosessen 4,5. Sikre at strukturen er beholdt er mulig bare hvis det er analytiske metoder som kan detektere protein konformasjon i solid-state med sufficient oppløsning.
NMR-spektroskopi 6 og røntgenkrystallografi 7 er de som vanligvis brukes med høy oppløsning metoder for å vurdere proteinstruktur i oppløsning og krystallinske faststoffer 8. På grunn av innholdet av hjelpestoffer og bearbeidingsmetoder som benyttes, frysetørkede protein formuleringer er vanligvis amorfe snarere enn krystallinsk 9. Mangelen på homogenitet og mikroskopisk rekkefølge gjør de ovennevnte teknikker upraktisk for proteiner i amorfe, faste stoffer. Fourier transform infrarød spektroskopi (FTIR) 10, Raman-spektroskopi 11 og nær infrarød spektroskopi (NIR) 12 er regelmessig brukt av biofarmasøytiske industrien for å sammenligne protein sekundærstruktur i lyofiliserte pulvere som i den native løsningstilstand struktur. Men disse metodene er lav oppløsning og kan bare gi informasjon om globale endringer i sekundærstruktur. Solid-state strukturell karakterisering ved hjelp av FTIRhar vist enten svak 13,14 eller dårlig 15 korrelasjon med langtidslagringsstabilitet. Disse begrensningene aktualiserer behovet for egnede høyoppløselige metoder for å identifisere protein strukturelle forstyrrelser i solid-state.
Kjemisk merking kombinert med proteolyse og massespektrometrisk analyse har dukket opp som en kraftig tilnærming til overvåking proteinstruktur og molekylære interaksjoner i vandig løsning. I farmasøytisk utvikling, har HDX-MS blitt brukt for epitopkartlegging i antigen-antistoff interaksjoner 16,17, for å kartlegge reseptor-interaksjoner 18, for å overvåke effekten av post-translasjonelle modifikasjoner på konformasjon av protein narkotika 19, og for å sammenligne batch-til-batch variasjon i utviklingen biosimilars 20. Tilsvarende har photoactivatable ligander blitt brukt for å identifisere medikament mål og å bestemme bindingsaffinitet og spesifisitet av medikament-reseptor interaksjoner 21,22. Til eXtend anvendelsen av disse metodene til frysetørkede formuleringer, har vår gruppe utviklet solid-state hydrogen deuterium utveksling massespektrometri (ssHDX-MS) og solid-state fotolytisk merking massespektrometri (SSPL-MS) for å studere protein conformations og eksipienspartikler interaksjoner i frysetørkede prøver med høy oppløsning.
I begge ssHDX-MS og SSPL-MS, blir protein merket under ideelle reaksjonsbetingelser i lyofiliserte faste stoffer, og prøvene blir deretter rekonstituert og analysert ved massespektrometri med eller uten proteolytisk fordøyelse. ssHDX-MS gir informasjon om hovedkjeden eksponering for deuterium damp, mens SSPL-MS gir informasjon om miljøet av sidekjeder (figur 1). De to metodene kan dermed gi utfyllende informasjon om protein konformasjon i solid-state. Her gir vi en generell protokoll for å studere proteiner i frysetørkede faste stoffer ved hjelp ssHDX-MS og SSPL-MS (figur 2), ved hjelp av Mb somen modell protein. Vi viser evnen av de to fremgangsmåter for å skille forskjeller i formuleringene med to forskjellige hjelpestoffer.
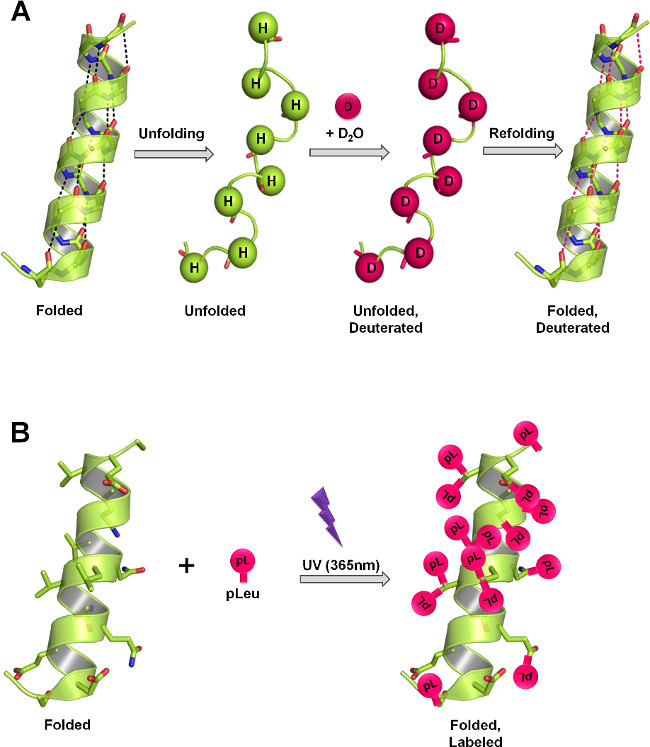
Fig. 1: ssHDX og SSPL måle proteinstrukturen i lyofiliserte faste stoffer gjennom forskjellige merkingsmekanismer (A) I HDX, hydrogenatomer i ryggraden amid utveksling med deuterium som en funksjon av proteinstruktur og D 2 O tilgjengelighet. I fast tilstand, hastighet og grad av deuterium-utveksling avhenge av nivået av D 2 O sorpsjon, protein mobilitet (utfolding og refolding hendelser) og arten av hjelpestoffene er til stede i den faste matriks. (B) I PL, UV-bestråling ved 365 nm initierer dannelse av et reaktivt mellomprodukt karben fra diazirine funksjonell gruppe pLeu og settes inn ikke-spesifikt inn i en hvilken som helst XH bindingen (X = en hvilken som helst atom), eller added tvers av en C = C-binding i dens umiddelbare nærhet. I fast tilstand, hastigheten og graden av merking avhenge av den lokale konsentrasjonen av merkemiddel, bestrålingstiden, proteinstruktur og arten av hjelpestoffene er til stede i den faste matriks. Panelene A og B viser den maksimale teoretiske merking som kan oppstå på ryggraden, og sidekjeder i henholdsvis protein.
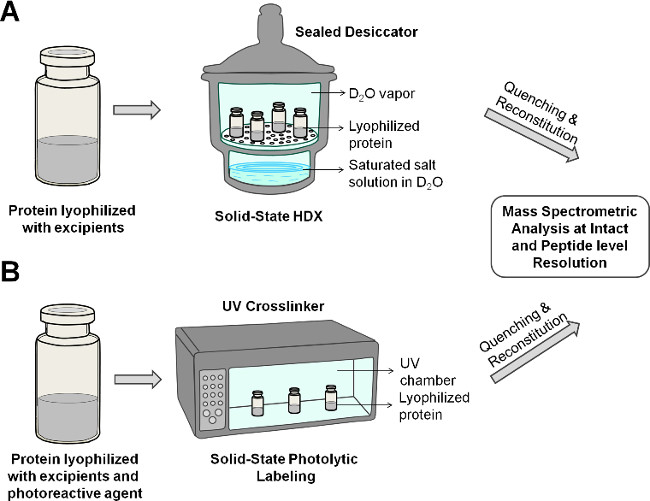
Figur 2: Skjematisk viser solid-state HDX-MS (A) og PL-MS (B) for protein i lyofilisert formulering.
Protocol
Representative Results
Discussion
Flere studier har antydet at det lokale miljøet i frysetørkede prøver påvirker proteinnedbrytingen 5,29,30. Imidlertid, å etablere en direkte sammenheng mellom proteinstruktur og stabilitet i fast tilstand ikke har vært mulig på grunn av mangel på høy oppløsning analytiske metoder. Anvendelsen av eksisterende høyoppløselige metoder som HDX og PL til frysetørkede pulver krever endring av løsnings protokoller og forsiktig tolking. HDX-MS og PL-MS har blitt suksessivt vedtatt å overvåke protein conformations i solid-state. Resultatene presenteres her og andre steder 27,28,31-33 har vist evne av disse metodene for å overvåke protein konformasjon med høy oppløsning i solid miljø. Selv om de kritiske trinn i dataanalyse ikke varierer fra merking i løsning 34-36, er viktige hensyn under eksperimentelle oppsettet og data tolkning nødvendig for solid-state kjemical merking.
Valg av merkingsreagens må være basert på størrelse og mekanismen for merking. Den lille størrelsen på deuterium tillater peptidryggraden til å bli analysert lett, mens den relativt store størrelsen av pLeu begrenser merking til sidekjeder. Både ssHDX og SSPL viser ingen preferanse for en hvilken som helst aminosyre, slik at merking bare avhenger av ryggraden, og sidekjedeeksponering til matriksen. Å effektivt sondere protein conformations i solid-state, må de eksterne faktorer som påvirker merkeprosessen kontrolleres nøye. Den totale mengde og den romlige fordelingen av merkemiddel i lyofiliserte faste stoffer er forskjellig fra vandige løsninger.
I ssHDX, kan mengden av D 2 O i den faste matriks påvirke graden av protein utfolding (eller delvis utfolding), refolding og deuterium-utveksling. Dette er ikke tilfelle med løsningen HDX, hvor proteinprøven blir vanligvis fortynnet med et stort volum av D 2 O.Nøye screening av effektene av hydrering på ssHDX hastigheten kan informere utvalget av ideelle RH forhold. For å kontrollere hastigheten av fuktighet sorpsjon og unngå kollaps av pulveret i formuleringer inneholdende hygroskopiske hjelpestoffer (for eksempel sukrose og trehalose), kan ssHDX utføres under kjølebetingelser (2-8 ° C). Vår tidligere studie på hydration effekter viste økt hastighet og grad av utveksling med økning i vanninnhold, som forventet. I store deler av vårt arbeid, en mellom RH på 43% ved 5 ° C har vist seg å være ideelt å skille formuleringer i en rimelig tid 24. Reaksjonen utføres vanligvis inntil et platå blir nådd. Dette sikrer at fuktighet absorpsjon og diffusjon til solid ikke kontrollere HDX rate. Bruk av små faste utvalgsstørrelser med pre-frysetørking volum på ≤2 ml bidrar også til å sikre at D 2 O damp absorpsjon er hovedsakelig fullført tidlig i utvekslingsperioden. Selv ssHDX-MS girkvantitativ informasjon om konformasjon av protein i solid-state, er det visse forhold der tolkning av data ikke kan være helt basert på ssHDX studien alene. Det er mulig at den reduserte deuterium opptak observert i en prøve (i forhold til kontroll) kan være på grunn av den høyere retensjon av proteinstrukturen eller den betydelige mengde av proteinaggregater som er tilstede i prøven. I et slikt tilfelle, tolkning av data ssHDX trenger resultater fra andre komplementære fremgangsmåter. Peak utvidelse i deuterert massespektra ble observert for flere Mb formuleringer 27,28. Dette kan være på grunn av forskjellige faktorer, som tilstedeværelsen av delvis ufoldet protein befolkningen, romlig heterogenitet i prøven, eller de romlige gradienter i D 2 O konsentrasjon. Men disse faktorene ikke skilt i ssHDX-MS og trenger videre etterforskning.
Som SSPL-MS er relativt ny i forhold til andre metoder, kontinuerlig læring abut dens anvendelser og begrensninger er nødvendig. I SSPL, blir den fototverrbinder lyofilisert med proteinet. Mangel på fuktighet begrenser mobiliteten av komponentene i den faste matriks, og den partielle strukturelle avslapning som kan forekomme med fuktighet sorpsjon i ssHDX er ikke et fenomen i SSPL. Dette begrenser merking i SSPL til umiddelbar nærhet av foto-cross-linker. Imidlertid, i motsetning til HDX-MS, MS / MS-analyse av det kovalent merket protein kan gi restnivå strukturell informasjon. Siden SSPL merking er kovalente og irreversible, tilbake utveksling ikke oppstår og prøver kan være forberedt og analysert uten bekymring for tap av etiketten. For å lette diffusjon av merkemiddel og forbedre merking effektivitet i faststoff-matrisen, kan SSPL utføres med økende% RH. pLeu opptak kan også forbedres ved å øke konsentrasjonen av fotoreaktivt middel. Det molare forhold av protein til pLeu kan varieres etter ønske. Generelt, en 100x molar overskudd av pLeu til protein vil sikre tilstrekkelig merking. Imidlertid kan høy konsentrasjon pLeu resultere i tap av proteintertiærstruktur i den faste matriks. Derfor, i tillegg til å merke kinetikk og formuleringssammensetning, valg av pLeu konsentrasjon må også være basert på å opprettholde strukturell integritet protein. Som pLeu ikke-selektivt etiketter XH (der X = C, N, O) gruppe, er det mulig at hjelpestoffer med lignende merke nettsteder i stor grad kan påvirke nivået av protein merking. Forstyrrelser av hjelpestoffene i tilgjengeligheten av pLeu for protein merking er ennå å bli karakterisert. Det er kjent at karben genereres fra diazirine aktivering ikke er rest-spesifikk, men en undersøkelse rapporterer forspenning mot Asp og Glu 36. Selv om det er godt å lære om rest-spesifikke vekselvirkninger, er peptid-nivå informasjon også nyttig og kan brukes til å utforme hjelpestoffer for å blokkere områder med stor matrise eksponering i fast tilstand. SSPL-MS gir detaljert kvalitativ informasjon, menkvantitative data må innhentes og robuste beregninger må utvikles for å analysere formulering forskjeller på tvers av en rekke frysetørrede systemer.
Bruken av en rest-spesifikt merket kombinert med MS / MS-analyse kan ytterligere øke oppløsningen til den amino-syrenivået. Merking reagenser som 2,3-butandion å merke Arg, kan N hydroksysuccinimid derivater for Lys og N -alkylmaleimide derivater for Cys brukes til nettopp å kartlegge molekylære interaksjoner i lyofilisert pulver. Men disse reagenser er pH-avhengig, og reaksjonene kan ikke være så godt kontrollert som fotolytisk merking i fast tilstand. En alternativ fremgangsmåte er å innlemme den fototverrbinder inn i proteinsekvensen med bruk av auxotrofe cellelinjer, seterettet mutagenese, eller sidekjede derivatisering.
Våre tidligere ssHDX-MS- og SSPL-MS-undersøkelser har vist at merking av proteiner er avhengig av arten og mengden av hjelpestoffenebrukt 24,27,28,31-33,37,38. ssHDX-MS av Mb co-lyofilisert med guanidinhydroklorid (Gdn.HCl) viste større deuterium opptak enn Mb co-lyofilisert med lav molekylvekt 32 sukkerarter. I en separat SSPL-MS studie, Mb co-frysetørket med Gdn.HCl viste større beskyttelse mot fotolytisk merking enn Mb med sukrose 33. Videre har kvantitative målinger fra ssHDX-MS vært høyt korrelert med stabiliteten av protein ved langtidslagring 28. Disse studiene tyder på at ssHDX eller SSPL protein reflekterer graden av strukturell retensjon av proteinet i lyofilisert pulver. Vi tror at retensjonen av sekundærstruktur i lyofiliserte pulvere gir gunstig miljø for sidekjede merking med pLeu og beskyttelse av amid hydrogen fra deuterium-utveksling. Imidlertid må detaljert sammenligning av informativt innhold av disse metodene for å bli utført i fremtiden. Selv etablere nytten av ssHDX-MS og SSPL-MSsom en formulering screening verktøy til slutt vil kreve at det brukes på mange proteiner, resultater fra våre nyere studier støtter sin bredere adopsjon. Med videreutvikling, er disse metoder forventet å være mye nyttig for å karakterisere faststoffproteinformuleringer i det biofarmasøytiske industrien.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors gratefully acknowledge financial support from NIH R01 GM085293 (PI: E. M. Topp) and from the College of Pharmacy at Purdue University.
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| Equine myoglobin | Sigma-Aldrich | M0630-5G | |
| D-(+)-Trehalose dihydrate | Sigma Aldrich | #T9531 | |
| D-Sorbitol | Sigma Aldrich | #240850 | |
| L-Photo-leucine | Thermo Scientific | #22610 | |
| Potassium phosphate monobasic | Sigma-Aldrich | #P0662 | |
| Potassium phosphate dibasic | Sigma-Aldrich | #P3786 | |
| Deuterium Oxide | Cambridge Isotope Laboratories | #DLM-4-PK | Alternate (Cat. No.: 151882, Sigma-Aldrich) |
| Immobilized pepsin | Applied Biosystems | #2-3132-00 | |
| Trypsin | Promega | #V511A | Chymotrypsin (Cat. No.: #V1062, Promega) can be additionally used |
| Water, Optima LC/MS grade | Fisher Chemical | #7732-18-5 | |
| Acetonitrile | Sigma-Aldrich | #34998 | |
| Formic acid | Thermo Scientific | #28905 | |
| ESI-TOF Calibrant | Agilent Technologies | #G1969-85000 | Highly flammable liquid |
| Protein microtrap | Michrom Bioresources | TR1/25108/03 | |
| Peptide microtrap | Michrom Bioresources | TR1/25109/02 | |
| Analytical column | Agilent Technologies | Zorbax 300SB-C18 | |
| Freeze dryer | VirTis AdVantage Plus | ||
| Stratalinker equipped with five 365 nm lamps | Stratagene Corp. | Stratalinker 2400 | |
| HPLC | Agilent Technologies | 1200 series LC | Refrigerated LC system for HDX-MS |
| ESI-qTOF MS | Agilent Technologies | 6520 qTOF | |
| HDExaminer (HDX-MS data analysis software) | Sierra Analytics | http://www.massspec.com/HDExaminer.html |
References
- Lawrence, S. Billion dollar babies–biotech drugs as blockbusters. Nat. Biotechnol. 25 (4), 380-382 (2007).
- . . Global Markets and Manufacturing Technologies for Protein Drugs. , BIO021D (2013).
- Lai, M. C., Topp, E. M. Solid-state chemical stability of proteins and peptides. J. Pharm. Sci. 88 (5), 489-500 (1999).
- Carpenter, J. F., Pikal, M. J., Chang, B. S., Randolph, T. W. Rational design of stable lyophilized protein formulations: some practical advice. Pharm. Res. 14 (8), 969-975 (1997).
- Carpenter, J. F., Chang, B. S., Garzon-Rodriguez, W., Randolph, T. W. Rational design of stable lyophilized protein formulations: theory and practice. Pharm. Biotechnol. 13, 109-133 (2002).
- Wüthrich, K. Protein structure determination in solution by NMR spectroscopy. J. Biol. Chem. 265 (36), 22059-22062 (1990).
- Ilari, A., Savino, C. Protein structure determination by x-ray crystallography. Methods. Mol. Biol. 452, 63-87 (2008).
- Brunger, A. T. X-ray crystallography and NMR reveal complementary views of structure and dynamics. Nat. Struct. Biol. 4, 862-865 (1997).
- Yu, L. Amorphous pharmaceutical solids: preparation, characterization and stabilization. Adv Drug. Deliv. Rev. 48 (1), 27-42 (2001).
- Manning, M. C. Use of infrared spectroscopy to monitor protein structure and stability. Expert. Rev. Proteomics. 2 (5), 731-743 (2005).
- Grohganz, H., Gildemyn, D., Skibsted, E., Flink, J. M., Rantanen, J. Rapid solid-state analysis of freeze-dried protein formulations using NIR and Raman spectroscopies. J. Pharm. Sci. 100 (7), 2871-2875 (2011).
- Bai, S., Nayar, R., Carpenter, J. F., Manning, M. C. Noninvasive determination of protein conformation in the solid state using near infrared (NIR) spectroscopy. J. Pharm. Sci. 94 (9), 2030-2038 (2005).
- Pikal, M. J., et al. Solid state chemistry of proteins: II. The correlation of storage stability of freeze-dried human growth hormone (hGH) with structure and dynamics in the glassy solid. J. Pharm. Sci. 97 (12), 5106-5121 (2008).
- Wang, B., Tchessalov, S., Cicerone, M. T., Warne, N. W., Pikal, M. J. Impact of sucrose level on storage stability of proteins in freeze-dried solids: II. Correlation of aggregation rate with protein structure and molecular mobility. J. Pharm. Sci. 98 (9), 3145-3166 (2009).
- Schule, S., Friess, W., Bechtold-Peters, K., Garidel, P. Conformational analysis of protein secondary structure during spray-drying of antibody/mannitol formulations. Eur. J. Pharm. Biopharm. 65 (1), 1-9 (2007).
- Baerga-Ortiz, A., Hughes, C. A., Mandell, J. G., Komives, E. A. Epitope mapping of a monoclonal antibody against human thrombin by H/D-exchange mass spectrometry reveals selection of a diverse sequence in a highly conserved protein. Protein. Sci. 11 (6), 1300-1308 (2002).
- Coales, S. J., Tuske, S. J., Tomasso, J. C., Hamuro, Y. Epitope mapping by amide hydrogen/deuterium exchange coupled with immobilization of antibody, on-line proteolysis, liquid chromatography and mass spectrometry. Rapid. Commun. Mass. Spectrom. 23 (5), 639-647 (2009).
- Pacholarz, K. J., Garlish, R. A., Taylor, R. J., Barran, P. E. Mass spectrometry based tools to investigate protein-ligand interactions for drug discovery. Chem. Soc. Rev. 41 (11), 4335-4355 (2012).
- Houde, D., Peng, Y., Berkowitz, S. A., Engen, J. R. Post-translational modifications differentially affect IgG1 conformation and receptor binding. Mol. Cell. Proteomics. 9 (8), 1716-1728 (2010).
- Houde, D., Berkowitz, S. A., Engen, J. R. The utility of hydrogen/deuterium exchange mass spectrometry in biopharmaceutical comparability studies. J. Pharm. Sci. 100 (6), 2071-2086 (2011).
- Dorman, G., Prestwich, G. D. Using photolabile ligands in drug discovery and development. Trends. Biotechnol. 18 (2), 64-77 (2000).
- Robinette, D., Neamati, N., Tomer, K. B., Borchers, C. H. Photoaffinity labeling combined with mass spectrometric approaches as a tool for structural proteomics. Expert. Rev. Proteomics. 3 (4), 399-408 (2006).
- Greenspan, L. Humidity fixed points of binary saturated aqueous solutions. Journal of Research of the National Bureau of Standards. 81A (1), 8 (1977).
- Sophocleous, A. M., Zhang, J., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 1. Exchange mapping. Mol. Pharm. 9 (4), 718-726 (2012).
- Keppel, T. R., Jacques, M. E., Young, R. W., Ratzlaff, K. L., Weis, D. D. An efficient and inexpensive refrigerated LC system for H/D exchange mass spectrometry. J. Am. Soc. Mass. Spectrom. 22 (8), 1472-1476 (2011).
- Gasteiger, E., et al. ExPASy: The proteomics server for in-depth protein knowledge and analysis. Nucleic. Acids. Res. 31 (13), 3784-3788 (2003).
- Sophocleous, A. M., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 2. Exchange kinetics. Mol. Pharm. 9 (4), 727-733 (2012).
- Moorthy, B. S., Schultz, S. G., Kim, S. G., Topp, E. M. Predicting Protein Aggregation during Storage in Lyophilized Solids Using Solid State Amide Hydrogen/Deuterium Exchange with Mass Spectrometric Analysis (ssHDX-MS). Mol. Pharm. 11 (6), 1869-1879 (2014).
- Wang, W. Lyophilization and development of solid protein pharmaceuticals. Int. J. Pharm. 203 (1-2), 1-60 (2000).
- Sarciaux, J. M., Mansour, S., Hageman, M. J., Nail, S. L. Effects of buffer composition and processing conditions on aggregation of bovine IgG during freeze-drying. J. Pharm. Sci. 88 (12), 1354-1361 (1999).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Characterizing protein structure in amorphous solids using hydrogen/deuterium exchange with mass spectrometry. Anal. Biochem. 366 (1), 18-28 (2007).
- Sinha, S., Li, Y., Williams, T. D., Topp, E. M. Protein conformation in amorphous solids by FTIR and by hydrogen/deuterium exchange with mass spectrometry. Biophys. J. 95 (12), 5951-5961 (2008).
- Iyer, L. K., Moorthy, B. S., Topp, E. M. Photolytic labeling to probe molecular interactions in lyophilized powders. Mol. Pharm. 10 (12), 4629-4639 (2013).
- Hentze, N., Mayer, M. P. Analyzing protein dynamics using hydrogen exchange mass spectrometry. J. Vis. Exp. (81), e50839 (2013).
- Kaltashov, I. A., Bobst, C. E., Abzalimov, R. R. H/D exchange and mass spectrometry in the studies of protein conformation and dynamics: is there a need for a top-down approach. Anal. Chem. 81 (19), 7892-7899 (2009).
- Jumper, C. C., Schriemer, D. C. Mass spectrometry of laser-initiated carbene reactions for protein topographic analysis. Anal. Chem. 83 (8), 2913-2920 (2011).
- Li, Y., Williams, T. D., Topp, E. M. Effects of excipients on protein conformation in lyophilized solids by hydrogen/deuterium exchange mass spectrometry. Pharm. Res. 25 (2), 259-267 (2008).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Trehalose and calcium exert site-specific effects on calmodulin conformation in amorphous solids. Biotechnol. Bioeng. 97 (6), 1650-1653 (2007).

