Mass Spectrometric Abordagens para estudar a estrutura das proteínas e interacções em liofilizados Pós
Summary
Here, we present detailed protocols for solid-state amide hydrogen/deuterium exchange mass spectrometry (ssHDX-MS) and solid-state photolytic labeling mass spectrometry (ssPL-MS) for proteins in solid powders. The methods provide high-resolution information on protein conformation and interactions in the amorphous solid-state, which may be useful in formulation design.
Abstract
Amida de hidrogénio / troca de deutério (ssHDX-MS) e da cadeia lateral fotolítica rotulagem (SSPL-MS) seguido de análise por espectrometria de massa pode ser valiosa para a caracterização de formulações liofilizadas de proteínas terapêuticas. Labeling seguido de digestão proteolítica adequado permite que a estrutura das proteínas e interacções a ser mapeada com resolução de nível peptídeo. Uma vez que a proteína de elementos estruturais são estabilizados por uma rede de ligações químicas entre as cadeias principais e cadeias laterais de aminoácidos, de marcação específica dos átomos nos resíduos de aminoácidos fornece informações sobre a estrutura e a conformação da proteína. Em contraste com os métodos de rotina usados para estudar as proteínas liofilizadas em sólidos (por exemplo, FTIR), ssHDX-MS-MS e SSPL fornecer informação quantitativa e específica de sítio. A extensão da incorporação de deutério e parâmetros cinéticos pode ser relacionado com a troca rápida e lentamente piscinas amida (N rápido, lento N) e reflecte directamente os grausree de dobramento de proteínas e estrutura em formulações liofilizadas. Rotulagem photolytic Estável não sofre back-troca, uma vantagem sobre ssHDX-MS. Aqui, nós fornecemos protocolos detalhados para ambos ssHDX-MS e SSPL-MS, utilizando mioglobina (Mb) como uma proteína modelo em formulações liofilizadas contendo trealose ou sorbitol.
Introduction
Drogas de proteína são o setor que mais cresce na indústria biofarmacêutica e oferecer novos tratamentos promissores para doenças antes incuráveis, incluindo distúrbios hormonais, câncer e doenças auto-imunes 1. Em 2012, o mercado mundial biotherapeutics atingiu 138.000 milhões dólar e deve chegar a 179 bilião dólares até o ano de 2018 2. As proteínas são maiores e mais frágil do que convencionais drogas de pequenas moléculas e por isso são mais suscetíveis a muitos tipos de degradação 3. Para assegurar a vida de prateleira e estabilidade adequadas, fármacos de proteína são muitas vezes formuladas como liofilizada (isto é, seco por congelação) pós sólidos. No entanto, uma proteína pode ainda sofrer degradação no estado sólido, particularmente se a sua estrutura nativa não é preservada durante o processo de liofilização 4,5. Assegurando que a estrutura foi mantida só é viável se houver métodos analíticos que podem sondar conformação da proteína no estado sólido com sufficienresolução t.
Espectroscopia de RMN 6 e cristalografia de raios X 7 são os métodos de alta resolução vulgarmente utilizados na avaliação da estrutura da proteína na solução e sólidos cristalinos 8. Devido à natureza dos excipientes e os métodos de processamento utilizadas, formulações de proteínas liofilizadas são geralmente amorfo cristalino em vez de 9. A falta de homogeneidade e de ordem microscópica faz com que as técnicas acima mencionadas impraticável para proteínas em sólidos amorfos. Espectroscopia de infravermelho com transformada de Fourier (FTIR) de 10, a espectroscopia de Raman 11 e espectroscopia de infravermelho próximo (NIR) 12 ter sido regularmente utilizadas pela indústria biofarmacêutica comparar a estrutura secundária da proteína de pós liofilizados para que a estrutura de solução de estado nativo. No entanto, estes métodos são de baixa resolução e só pode fornecer informações sobre as mudanças globais na estrutura secundária. Caracterização estrutural de estado sólido usando FTIRtem mostrado tanto fraco 13,14 ou pobre 15 correlação com a estabilidade de armazenamento a longo prazo. Estas limitações destacam a necessidade de métodos de alta resolução apropriada para identificar perturbações estruturais de proteína no estado sólido.
Marcação química acoplado à proteólise e análise de espectrometria de massa emergiu como uma abordagem poderosa para monitorar a estrutura das proteínas e interacções moleculares em solução aquosa. No desenvolvimento farmacêutico, HDX-MS foi utilizada para o mapeamento de epitopo de interacções antigénio-anticorpo 16,17, para mapear as interacções receptor-fármaco 18, para monitorizar os efeitos de modificações pós-traducionais sobre a conformação da proteína drogas 19, e para comparar variação no desenvolvimento biosimilars 20 de lote para lote. Do mesmo modo, os ligandos fotoactiv�eis têm sido utilizados para identificar alvos de drogas e para determinar a afinidade de ligação e especificidade de interacções receptor-fármaco 21,22. Dedo do péde estado sólido espectrometria xtend a aplicação destes métodos para formulações liofilizadas, o nosso grupo tem desenvolvido massa troca de deutério de hidrogênio (ssHDX-MS) e de estado sólido espectrometria de massa rotulagem photolytic (SSPL-MS) para estudar conformações de proteína e interações do excipiente em amostras liofilizadas com alta resolução.
Em ambos ssHDX-MS-MS e SSPL, a proteína é marcada em condições de reacção ideais em sólidos liofilizados, e as amostras são então reconstituídas e analisados por espectrometria de massa, com ou sem digestão proteolítica. ssHDX-MS fornece informações sobre a exposição da cadeia principal de vapor deutério, enquanto SSPL-MS fornece informações sobre o ambiente de cadeias laterais (Figura 1). Os dois métodos, portanto, pode fornecer informação complementar sobre a conformação da proteína no estado sólido. Aqui, nós fornecemos um protocolo geral para o estudo de proteínas em sólidos liofilizados utilizando ssHDX-MS-MS e SSPL (Figura 2), utilizando como Mbuma proteína modelo. Mostramos a capacidade dos dois métodos para distinguir diferenças em duas formulações com excipientes diferentes.
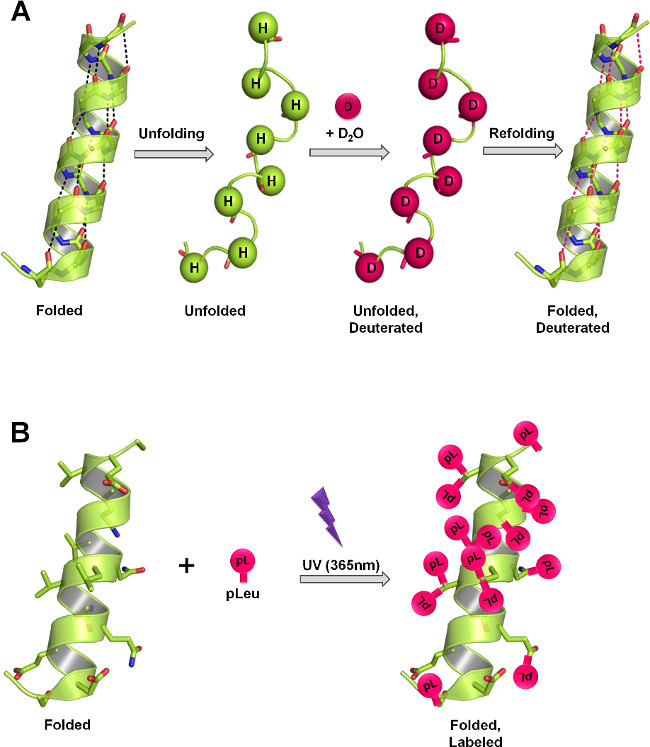
Figura 1:. SsHDX e SSPL estrutura proteica medida em sólidos liofilizados por meio de diferentes mecanismos de rotulagem (A) Em HDX, a espinha dorsal de amida hidrogénios troca com deutério como uma função da estrutura da proteína e D 2 O acessibilidade. No estado sólido, a taxa e extensão de troca de deutério depender do nível de D 2 O sorção, a mobilidade da proteína (desdobramento e redobragem eventos) e da natureza dos excipientes presentes na matriz sólida. (B) Em PL, irradiação UV a 365 nm, inicia a formação de um intermediário reactivo de carbeno do grupo funcional de diazirina pleu e está inserido de forma não específica em qualquer ligação de XH (X = qualquer átomo), ou added através de uma ligação C = C na sua vizinhança imediata. No estado sólido, a velocidade e extensão da marcação depende da concentração local do agente de marcação, o tempo de irradiação, a estrutura da proteína e da natureza dos excipientes presentes na matriz sólida. Os painéis A e B mostram a marcação máxima teórica que pode ocorrer na espinha dorsal e cadeias laterais, respectivamente, na proteína.
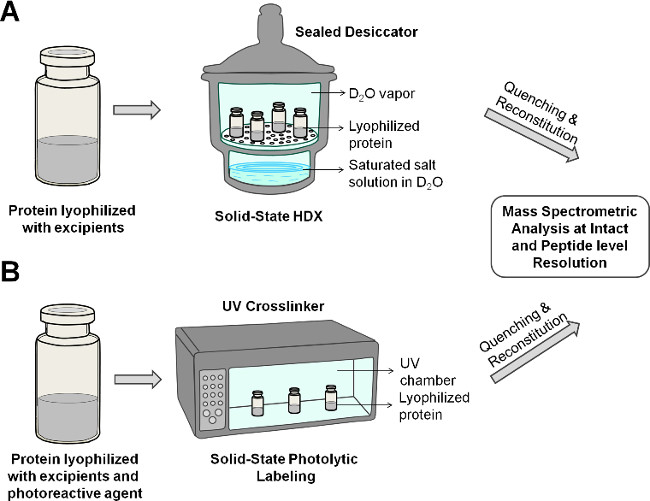
Figura 2: Diagrama esquemático mostrando em estado sólido HDX-MS (A) e PL-MS (B) para a proteína na formulação liofilizada.
Protocol
Representative Results
Discussion
Vários estudos têm sugerido que o ambiente local em amostras liofilizadas afecta a degradação da proteína 5,29,30. No entanto, o estabelecimento de uma relação directa entre a estrutura da proteína e estabilidade no estado sólido não tem sido possível, devido à falta de métodos analíticos de alta resolução. A aplicação de métodos de alta resolução já existentes, como HDX e PL para pós liofilizados requer a modificação de protocolos de solução e interpretação de dados cuidadosa. HDX-MS e PL-MS foram sucessivamente adoptadas para monitorar conformações de proteínas no estado sólido. Os resultados apresentados aqui e noutros lugares 27,28,31-33 demonstraram a capacidade destes métodos para controlar a conformação da proteína com alta resolução no ambiente sólido. Embora as etapas críticas na análise de dados não variam de rotulagem em solução 34-36, considerações importantes durante a configuração experimental e interpretação dos dados são necessários para o químico de estado sólidorotulagem cal.
A selecção do reagente de marcação deve ser baseada no tamanho e mecanismo de rotulagem. O pequeno tamanho de deutério permite que o esqueleto peptídico a ser sondado facilmente, ao passo que o tamanho relativamente maior de pleu limita rotulagem para as cadeias laterais. Ambos ssHDX SSPL e não mostram nenhuma preferência por qualquer aminoácido, de modo que a rotulagem depende apenas da espinha dorsal e cadeias laterais de exposição à matriz. Para sondar efetivamente conformações de proteínas em estado sólido, os fatores externos que afetam o processo de rotulagem deve ser cuidadosamente controlada. O montante total e da distribuição espacial de agente de marcação em sólidos liofilizados é diferente a partir de soluções aquosas.
Em ssHDX, a quantidade de D 2 O na matriz sólida pode afectar a taxa de desdobramento da proteína (ou desdobramento parcial), redobragem, e troca de deutério. Este não é o caso com solução HDX, em que a amostra de proteína é normalmente diluída com um amplo volume de D 2 O.Rastreio cuidadoso dos efeitos de hidratação na taxa ssHDX pode informar a selecção das condições ideais RH. Para controlar a taxa de humidade de sorção e evitar o colapso do pó em formulações contendo excipientes higroscópicas (por exemplo sacarose e trealose), ssHDX pode ser realizado sob condições de refrigeração (2-8 ° C). Nosso estudo anterior sobre os efeitos de hidratação mostrou velocidade e extensão da troca aumentou com o aumento do teor de umidade, como esperado. Em grande parte do nosso trabalho, um RH intermediário de 43% a 5 ° C provou ser ideal para distinguir formulações em um tempo razoável 24. A reacção é geralmente levada a cabo até um patamar é atingido. Isso garante que a sorção de umidade e difusão para o sólido não controlam a taxa HDX. A utilização de tamanhos de amostra pequenos sólidos com um volume pré-liofilização de ≤2 ml também ajuda a assegurar que a D 2 O sorção de vapor é essencialmente completa no início do período de intercâmbio. Embora ssHDX-MS ofereceInformação quantitativa sobre a conformação da proteína no estado sólido, há certas condições em que a interpretação de dados não podem ser inteiramente feitos apenas com o estudo ssHDX. É possível que a absorção de deutério diminuição observada em uma amostra (quando comparado com o controlo), pode ser devido a uma maior retenção de estrutura de proteína ou a montante significativo de agregados de proteínas presentes na amostra. Em tal caso, a interpretação de dados ssHDX requer resultados de outros métodos complementares. Ampliação Peak no espectro de massa deuterado foi observado para várias formulações Mb 27,28. Isto pode ser devido a vários factores, tais como a presença da população de proteína parcialmente desdobrada, a heterogeneidade espacial na amostra, ou os gradientes espaciais na concentração de D 2 O. No entanto, esses fatores não foram distinguidos em ssHDX-MS e precisa de uma investigação mais aprofundada.
Como SSPL-MS é relativamente novo, quando comparado com outros métodos, a aprendizagem contínua abas suas aplicações e limitações é necessário. Em SSPL, o foto-reticulante é liofilizada com a proteína. A falta de humidade limita a mobilidade dos componentes no interior da matriz sólida, e a relaxação estrutural parcial que pode ocorrer com a adsorção de humidade em ssHDX não é um fenómeno em SSPL. Isso limita a rotulagem em SSPL à vizinhança imediata da foto-cross-ligante. No entanto, ao contrário de HDX-MS, análise por MS / MS da proteína covalentemente marcada pode fornecer informações sobre a estrutura de nível resíduo. Desde rotulagem SSPL é covalente e irreversível, de volta de câmbio não ocorre e as amostras podem ser preparadas e analisadas sem se preocupar com a perda de rótulo. Para facilitar a difusão do agente de marcação e melhorar a eficiência de marcação em forma sólida de matriz, SSPL pode ser realizada com o aumento da% de HR. pleu captação também pode ser melhorada aumentando a concentração do agente fotor reactivo. A razão molar da proteína de pleu pode ser variada como desejado. Em geral, um excesso molar de 100 vezes de pró pleutein irá garantir uma rotulagem adequada. No entanto, de alta concentração pleu pode resultar em perda da estrutura terciária de proteína na matriz sólida. Assim, em adição à cinética de rotulagem e composição das formulações, a selecção de pleu concentração deve basear-se também a manutenção da integridade estrutural da proteína. Como pleu não selectiva etiquetas XH (em que X = C, N, O), é possível que os excipientes semelhantes com sítios de rotulagem podem afectar grandemente o grau de marcação da proteína. A interferência dos excipientes na disponibilidade de pleu para marcação de proteínas é ainda a ser caracterizado. Sabe-se que o gerado a partir de carbeno activação diazirina resíduo não é específica, no entanto, um estudo relata tendência para Asp e Glu 36. Embora seja bom para aprender sobre interacções específicas de resíduos, as informações-péptido nível também é útil e pode ser utilizado para desenhar excipientes para bloquear regiões com elevada exposição a matriz no estado sólido. SSPL-MS fornece informação qualitativa detalhada, porémquantitativa dos dados tem de ser obtido e métricas robustos precisa ser desenvolvido para analisar as diferenças de formulação através de uma variedade de sistemas liofilizados.
O uso de uma etiqueta específica do resíduo combinado com análise por MS / MS pode aumentar ainda mais a resolução ao nível de aminoácidos. Reagentes de marcação, tais como 2,3-butanodiona para rotular Arg, derivados de N-hidroxissuccinimida e N para Lys derivados -alkylmaleimide para Cys pode ser utilizado para mapear precisamente interacções moleculares em pó liofilizada. No entanto, estes reagentes são dependentes do pH e as reacções podem não ser tão bem controlado como rotulagem fotolítica no estado sólido. Uma abordagem alternativa consiste em incorporar o foto-reticulante para a sequência de proteína com a utilização de linhas de células auxotróficas, mutagénese dirigida ao local ou cadeia lateral de derivatização.
Nossos estudos anteriores ssHDX-MS e SSPL-MS mostraram que a marcação da proteína depende da natureza e quantidade de excipientesusado 24,27,28,31-33,37,38. ssHDX-MS de Mb co-liofilizado com guanidina (Gdn.HCl) mostrou uma maior absorção de deutério do que Mb co-liofilizado com baixo peso molecular 32 açúcares. Em um estudo SSPL-MS separado, Mb co-liofilizado com Gdn.HCl apresentaram maior proteção contra rotulagem photolytic que Mb com sacarose 33. Além disso, medições quantitativas de ssHDX-MS foram altamente correlacionada com a estabilidade da proteína durante a armazenagem de longo prazo 28. Estes estudos sugerem que ssHDX ou SSPL de proteína reflete a extensão da retenção estrutural da proteína em pó liofilizada. Acreditamos que a manutenção da estrutura secundária em pó liofilizado fornece ambiente favorável para a rotulagem cadeia lateral com pleu e proteção de amida de hidrogênio a partir de troca de deutério. No entanto, a comparação detalhada do conteúdo informativo a partir destes métodos tem de ser realizado no futuro. Embora institui a utilidade de ssHDX-MS e SSPL-MScomo ferramenta de triagem formulação acabará por exigir que ele seja aplicado a muitas proteínas, os resultados de nossos estudos recentes apoia a sua adoção mais ampla. Com a continuação do desenvolvimento, estes métodos deverão ser amplamente útil para a caracterização de formulações de proteínas de estado sólido na indústria biofarmacêutica.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors gratefully acknowledge financial support from NIH R01 GM085293 (PI: E. M. Topp) and from the College of Pharmacy at Purdue University.
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| Equine myoglobin | Sigma-Aldrich | M0630-5G | |
| D-(+)-Trehalose dihydrate | Sigma Aldrich | #T9531 | |
| D-Sorbitol | Sigma Aldrich | #240850 | |
| L-Photo-leucine | Thermo Scientific | #22610 | |
| Potassium phosphate monobasic | Sigma-Aldrich | #P0662 | |
| Potassium phosphate dibasic | Sigma-Aldrich | #P3786 | |
| Deuterium Oxide | Cambridge Isotope Laboratories | #DLM-4-PK | Alternate (Cat. No.: 151882, Sigma-Aldrich) |
| Immobilized pepsin | Applied Biosystems | #2-3132-00 | |
| Trypsin | Promega | #V511A | Chymotrypsin (Cat. No.: #V1062, Promega) can be additionally used |
| Water, Optima LC/MS grade | Fisher Chemical | #7732-18-5 | |
| Acetonitrile | Sigma-Aldrich | #34998 | |
| Formic acid | Thermo Scientific | #28905 | |
| ESI-TOF Calibrant | Agilent Technologies | #G1969-85000 | Highly flammable liquid |
| Protein microtrap | Michrom Bioresources | TR1/25108/03 | |
| Peptide microtrap | Michrom Bioresources | TR1/25109/02 | |
| Analytical column | Agilent Technologies | Zorbax 300SB-C18 | |
| Freeze dryer | VirTis AdVantage Plus | ||
| Stratalinker equipped with five 365 nm lamps | Stratagene Corp. | Stratalinker 2400 | |
| HPLC | Agilent Technologies | 1200 series LC | Refrigerated LC system for HDX-MS |
| ESI-qTOF MS | Agilent Technologies | 6520 qTOF | |
| HDExaminer (HDX-MS data analysis software) | Sierra Analytics | http://www.massspec.com/HDExaminer.html |
References
- Lawrence, S. Billion dollar babies–biotech drugs as blockbusters. Nat. Biotechnol. 25 (4), 380-382 (2007).
- . . Global Markets and Manufacturing Technologies for Protein Drugs. , BIO021D (2013).
- Lai, M. C., Topp, E. M. Solid-state chemical stability of proteins and peptides. J. Pharm. Sci. 88 (5), 489-500 (1999).
- Carpenter, J. F., Pikal, M. J., Chang, B. S., Randolph, T. W. Rational design of stable lyophilized protein formulations: some practical advice. Pharm. Res. 14 (8), 969-975 (1997).
- Carpenter, J. F., Chang, B. S., Garzon-Rodriguez, W., Randolph, T. W. Rational design of stable lyophilized protein formulations: theory and practice. Pharm. Biotechnol. 13, 109-133 (2002).
- Wüthrich, K. Protein structure determination in solution by NMR spectroscopy. J. Biol. Chem. 265 (36), 22059-22062 (1990).
- Ilari, A., Savino, C. Protein structure determination by x-ray crystallography. Methods. Mol. Biol. 452, 63-87 (2008).
- Brunger, A. T. X-ray crystallography and NMR reveal complementary views of structure and dynamics. Nat. Struct. Biol. 4, 862-865 (1997).
- Yu, L. Amorphous pharmaceutical solids: preparation, characterization and stabilization. Adv Drug. Deliv. Rev. 48 (1), 27-42 (2001).
- Manning, M. C. Use of infrared spectroscopy to monitor protein structure and stability. Expert. Rev. Proteomics. 2 (5), 731-743 (2005).
- Grohganz, H., Gildemyn, D., Skibsted, E., Flink, J. M., Rantanen, J. Rapid solid-state analysis of freeze-dried protein formulations using NIR and Raman spectroscopies. J. Pharm. Sci. 100 (7), 2871-2875 (2011).
- Bai, S., Nayar, R., Carpenter, J. F., Manning, M. C. Noninvasive determination of protein conformation in the solid state using near infrared (NIR) spectroscopy. J. Pharm. Sci. 94 (9), 2030-2038 (2005).
- Pikal, M. J., et al. Solid state chemistry of proteins: II. The correlation of storage stability of freeze-dried human growth hormone (hGH) with structure and dynamics in the glassy solid. J. Pharm. Sci. 97 (12), 5106-5121 (2008).
- Wang, B., Tchessalov, S., Cicerone, M. T., Warne, N. W., Pikal, M. J. Impact of sucrose level on storage stability of proteins in freeze-dried solids: II. Correlation of aggregation rate with protein structure and molecular mobility. J. Pharm. Sci. 98 (9), 3145-3166 (2009).
- Schule, S., Friess, W., Bechtold-Peters, K., Garidel, P. Conformational analysis of protein secondary structure during spray-drying of antibody/mannitol formulations. Eur. J. Pharm. Biopharm. 65 (1), 1-9 (2007).
- Baerga-Ortiz, A., Hughes, C. A., Mandell, J. G., Komives, E. A. Epitope mapping of a monoclonal antibody against human thrombin by H/D-exchange mass spectrometry reveals selection of a diverse sequence in a highly conserved protein. Protein. Sci. 11 (6), 1300-1308 (2002).
- Coales, S. J., Tuske, S. J., Tomasso, J. C., Hamuro, Y. Epitope mapping by amide hydrogen/deuterium exchange coupled with immobilization of antibody, on-line proteolysis, liquid chromatography and mass spectrometry. Rapid. Commun. Mass. Spectrom. 23 (5), 639-647 (2009).
- Pacholarz, K. J., Garlish, R. A., Taylor, R. J., Barran, P. E. Mass spectrometry based tools to investigate protein-ligand interactions for drug discovery. Chem. Soc. Rev. 41 (11), 4335-4355 (2012).
- Houde, D., Peng, Y., Berkowitz, S. A., Engen, J. R. Post-translational modifications differentially affect IgG1 conformation and receptor binding. Mol. Cell. Proteomics. 9 (8), 1716-1728 (2010).
- Houde, D., Berkowitz, S. A., Engen, J. R. The utility of hydrogen/deuterium exchange mass spectrometry in biopharmaceutical comparability studies. J. Pharm. Sci. 100 (6), 2071-2086 (2011).
- Dorman, G., Prestwich, G. D. Using photolabile ligands in drug discovery and development. Trends. Biotechnol. 18 (2), 64-77 (2000).
- Robinette, D., Neamati, N., Tomer, K. B., Borchers, C. H. Photoaffinity labeling combined with mass spectrometric approaches as a tool for structural proteomics. Expert. Rev. Proteomics. 3 (4), 399-408 (2006).
- Greenspan, L. Humidity fixed points of binary saturated aqueous solutions. Journal of Research of the National Bureau of Standards. 81A (1), 8 (1977).
- Sophocleous, A. M., Zhang, J., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 1. Exchange mapping. Mol. Pharm. 9 (4), 718-726 (2012).
- Keppel, T. R., Jacques, M. E., Young, R. W., Ratzlaff, K. L., Weis, D. D. An efficient and inexpensive refrigerated LC system for H/D exchange mass spectrometry. J. Am. Soc. Mass. Spectrom. 22 (8), 1472-1476 (2011).
- Gasteiger, E., et al. ExPASy: The proteomics server for in-depth protein knowledge and analysis. Nucleic. Acids. Res. 31 (13), 3784-3788 (2003).
- Sophocleous, A. M., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 2. Exchange kinetics. Mol. Pharm. 9 (4), 727-733 (2012).
- Moorthy, B. S., Schultz, S. G., Kim, S. G., Topp, E. M. Predicting Protein Aggregation during Storage in Lyophilized Solids Using Solid State Amide Hydrogen/Deuterium Exchange with Mass Spectrometric Analysis (ssHDX-MS). Mol. Pharm. 11 (6), 1869-1879 (2014).
- Wang, W. Lyophilization and development of solid protein pharmaceuticals. Int. J. Pharm. 203 (1-2), 1-60 (2000).
- Sarciaux, J. M., Mansour, S., Hageman, M. J., Nail, S. L. Effects of buffer composition and processing conditions on aggregation of bovine IgG during freeze-drying. J. Pharm. Sci. 88 (12), 1354-1361 (1999).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Characterizing protein structure in amorphous solids using hydrogen/deuterium exchange with mass spectrometry. Anal. Biochem. 366 (1), 18-28 (2007).
- Sinha, S., Li, Y., Williams, T. D., Topp, E. M. Protein conformation in amorphous solids by FTIR and by hydrogen/deuterium exchange with mass spectrometry. Biophys. J. 95 (12), 5951-5961 (2008).
- Iyer, L. K., Moorthy, B. S., Topp, E. M. Photolytic labeling to probe molecular interactions in lyophilized powders. Mol. Pharm. 10 (12), 4629-4639 (2013).
- Hentze, N., Mayer, M. P. Analyzing protein dynamics using hydrogen exchange mass spectrometry. J. Vis. Exp. (81), e50839 (2013).
- Kaltashov, I. A., Bobst, C. E., Abzalimov, R. R. H/D exchange and mass spectrometry in the studies of protein conformation and dynamics: is there a need for a top-down approach. Anal. Chem. 81 (19), 7892-7899 (2009).
- Jumper, C. C., Schriemer, D. C. Mass spectrometry of laser-initiated carbene reactions for protein topographic analysis. Anal. Chem. 83 (8), 2913-2920 (2011).
- Li, Y., Williams, T. D., Topp, E. M. Effects of excipients on protein conformation in lyophilized solids by hydrogen/deuterium exchange mass spectrometry. Pharm. Res. 25 (2), 259-267 (2008).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Trehalose and calcium exert site-specific effects on calmodulin conformation in amorphous solids. Biotechnol. Bioeng. 97 (6), 1650-1653 (2007).

