Masspektrometrisk Approaches att studera protein struktur och interaktioner i frystorkad Pulver
Summary
Here, we present detailed protocols for solid-state amide hydrogen/deuterium exchange mass spectrometry (ssHDX-MS) and solid-state photolytic labeling mass spectrometry (ssPL-MS) for proteins in solid powders. The methods provide high-resolution information on protein conformation and interactions in the amorphous solid-state, which may be useful in formulation design.
Abstract
Amid väte / deuterium utbyte (ssHDX-MS) och sidokedjan fotolytisk märkning (SSPL-MS) följt av masspektrometrisk analys kan vara värdefullt för att karakterisera frystorkade formuleringar av proteinläkemedel. Märkning följt av lämplig proteolytisk matsmältning gör proteinstrukturen och interaktioner som ska kartläggas med peptid-nivå upplösning. Eftersom proteinet strukturella element är stabiliserade av ett nätverk av kemiska bindningar från huvudkedjor och sidokedjor av aminosyror, specifik märkning av atomer i aminosyraresterna ger insikt i strukturen och konformationen av proteinet. I motsats till rutinmetoder används för att studera proteiner i frystorkade fasta ämnen (t.ex. FTIR), ssHDX-MS och SSPL-MS ger kvantitativa och platsspecifik information. Omfattningen av deuterium inkorporering och kinetiska parametrar kan relateras till snabbt och långsamt utbyta amid pooler (N snabb, N långsam) och reflekterar direkt på degree av proteinveckning och struktur i frystorkade formuleringar. Stabil fotolytisk märkning genomgår inte back-utbyte, en fördel över ssHDX-MS. Här ger vi detaljerade protokoll för både ssHDX-MS och SSPL-MS, med hjälp av myoglobin (Mb) som modell protein i frystorkade formuleringar innehållande antingen trehalos eller sorbitol.
Introduction
Proteinläkemedel är den snabbast växande sektorn i den biofarmaceutiska industrin och erbjuder lovande nya behandlingar för tidigare svåra sjukdomar, däribland hormonella störningar, cancer och autoimmuna sjukdomar 1. År 2012, den globala proteinläkemedel marknaden nådde $ 138.000.000.000 och förväntas nå $ 179.000.000.000 fram till år 2018 2. Proteiner är större och mer ömtålig än konventionella småmolekylära läkemedel och så är mer mottagliga för många typer av nedbrytning 3. För att säkerställa en tillräcklig hållbarhet och stabilitet, är proteinläkemedel ofta formuleras som frystorkat (dvs, frystorkade) fasta pulver. Dock kan ett protein fortfarande genomgår nedbrytning i fast tillstånd, särskilt om dess naturliga struktur inte bevaras under lyofiliseringsförfarandet 4,5. Säkerställa att strukturen har behållits är genomförbart endast om det finns analysmetoder som kan sondera proteinkonforma i solid-state med sufficient upplösning.
NMR-spektroskopi 6 och röntgenkristallografi 7 är de vanligen använda högupplösta metoder för att bedöma proteinstruktur i lösning och kristallina fastämnen 8. På grund av arten av hjälpämnen och de bearbetningsmetoder som används, frystorkade proteinformuleringar är vanligtvis amorfa snarare än kristallint 9. Bristen på homogenitet och mikroskopisk ordning gör de ovan nämnda teknikerna opraktiskt för proteiner i amorfa fasta ämnen. FTIR (FTIR) 10, Ramanspektroskopi 11 och nära infraröd spektroskopi (NIR) 12 har regelbundet används av biofarmaceutiska industrin att jämföra protein sekundär struktur i frystorkade pulver med den för det nativa lösningen-statsstruktur. Men dessa metoder är låg upplösning och kan bara ge information om globala förändringar i sekundärstruktur. Solid-state strukturell karakterisering med hjälp FTIRhar visat antingen svaga 13,14 eller dålig 15 korrelation med långtidslagringsstabilitet. Dessa begränsningar belyser behovet av lämpliga högupplösta metoder för att identifiera protein strukturella störningar i fast tillstånd.
Kemisk märkning i kombination med proteolys och masspektrometrisk analys har vuxit fram som en kraftfull metod för att övervaka proteinstruktur och molekylära interaktioner i vattenlösning. I läkemedelsutveckling, har HDX-MS använts epitopkartläggning i antigen-antikroppsinteraktioner 16,17, för att kart receptor-läkemedelsinteraktioner 18, för att övervaka effekterna av posttranslationella modifieringar på konforma av proteinläkemedel 19, och att jämföra sats till sats variationer i utvecklingen biosimilars 20. Likaså har fotoaktiverbara ligander använts för att identifiera mål för läkemedel och för att bestämma bindningsaffinitet och specificitet av narkotikareceptorinteraktioner 21,22. Till eXtend tillämpningen av dessa metoder till frystorkade formuleringar, har vår grupp utvecklat solid-state väte deuterium utbyte masspektrometri (ssHDX-MS) och solid-state fotolytisk märkning masspektrometri (SSPL-MS) för att studera proteinkonformationer och excipientpartiklarna interaktioner i frystorkade prover med hög upplösning.
I både ssHDX-MS och Sspl-MS proteinet märkt under ideala reaktionsbetingelser i lyofiliserade fasta substanser, och proverna rekonstituerades därefter och analyserades genom masspektrometri med eller utan proteolytisk spjälkning. ssHDX-MS ger information om huvudkedjan exponering för deuterium ånga, medan SSPL-MS ger information om miljön i sidokedjor (Figur 1). De två metoderna därmed kan ge kompletterande information om proteinkonforma i fast tillstånd. Här ger vi en allmän protokoll för att studera proteiner i frystorkade partiklar med ssHDX-MS och SSPL-MS (Figur 2), med hjälp av Mb somen modellprotein. Vi visar förmågan hos de två metoderna för att särskilja skillnader i formuleringar med två olika excipienter.
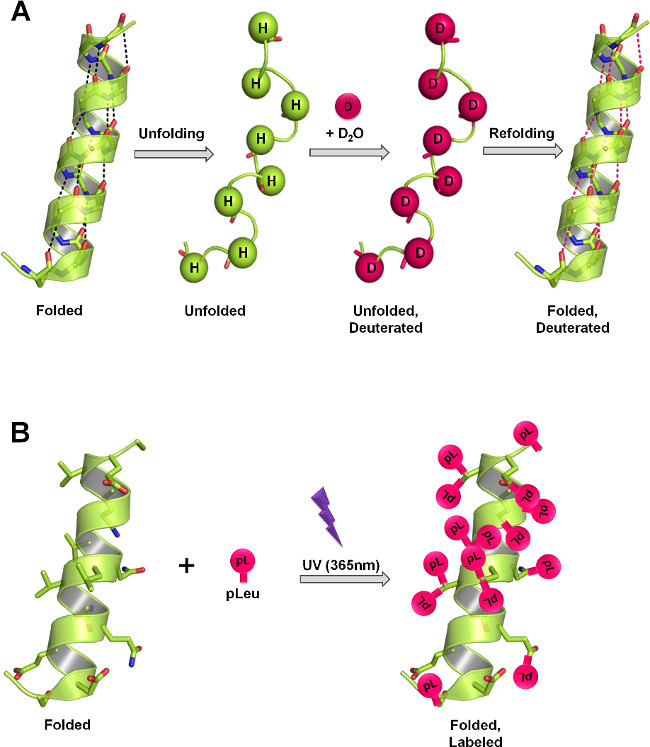
Figur 1:. SsHDX och Sspl åtgärd proteinstruktur i lyofiliserade fasta substanser genom olika system för märkning (A) På HDX, väten ryggraden amid utbyte med deuterium som en funktion av proteinstruktur och D2O tillgänglighet. I fast tillstånd, hastigheten och omfattningen av deuterium utbyte beror på graden av D 2 O sorption, protein rörlighet (utspelas och återveck händelser) och arten av hjälpämnena som finns i den fasta matrisen. (B) På PL, UV-bestrålning vid 365 nm initierar bildandet av en reaktiv karben intermediär från diazirine funktionella gruppen hos pLeu och införes ospecifikt i någon XH bindning (X = vilken atom), eller added över en C = C-bindning i dess omedelbara närhet. I fast tillstånd, är hastigheten och graden av märkning beror på den lokala koncentrationen av märkningsmedlet, bestrålningstiden, proteiners struktur och typen av hjälpämnen som föreligger i den fasta matrisen. Paneler A och B visar den maximala teoretiska märkning som kan uppstå på ryggraden och sidokedjor respektive protein.
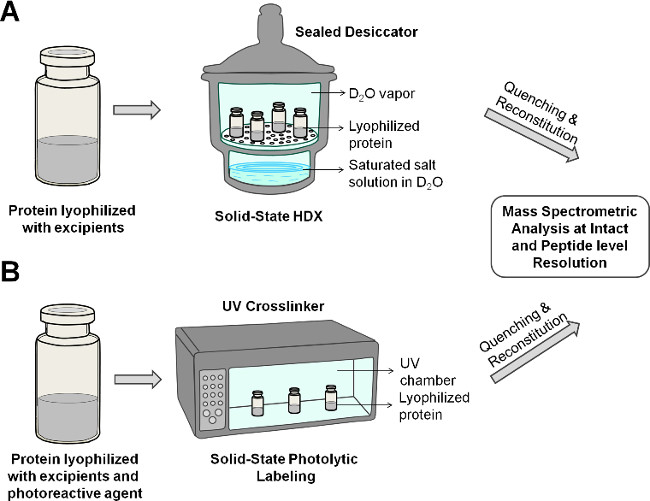
Figur 2: Schematisk visning solid-state HDX-MS (A) och PL-MS (B) för protein i lyofiliserad formulering.
Protocol
Representative Results
Discussion
Flera studier har antytt att den lokala miljön i frystorkade prover påverkar proteinnedbrytning 5,29,30. Att fastställa ett direkt samband mellan proteinstruktur och stabilitet i det fasta tillståndet har inte varit möjligt på grund av bristen på högupplösta analysmetoder. Tillämpningen av befintliga högupplösta metoder såsom HDX och PL till frystorkade pulver kräver modifiering av lösnings protokoll och noggrann tolkning av data. HDX-MS och PL-MS har successivt antagit att övervaka proteinkonformationer i fast tillstånd. Resultaten som presenteras här och på andra håll 27,28,31-33 ha visat förmåga av dessa metoder för att övervaka proteinkonforma med hög upplösning i den fasta miljön. Även de kritiska stegen i dataanalys inte varierar från märkning i lösning 34-36, är viktiga överväganden under experimentuppställning och tolkning av data som krävs för halvledar mekanocal märkning.
Val av märkningsreagens måste baseras på storlek och mekanismen för märkning. Den lilla storleken på deuterium tillåter peptid ryggraden som ska sonderas lätt, medan den relativt större storlek pLeu begränsar märkning till sidokedjorna. Både ssHDX och Sspl visar ingen preferens för någon aminosyra, så att märkningen endast beroende ryggrad och sidokedja exponering till matrisen. För att effektivt söka proteinkonformationer i solid-state, måste de externa faktorer som påverkar märkningsprocessen kontrolleras noggrant. Det totala beloppet och den geografiska fördelningen av märkningsmedel i frystorkade fasta skiljer sig från vattenlösningar.
I ssHDX, kan mängden D 2 O i den fasta matrisen påverkar graden av protein utspelas (eller partiell utspelas), återveck och deuterium utbyte. Detta är inte fallet med lösning HDX, i vilken proteinprovet normalt utspädes med en riklig volym av D 2 O.Noggrann genomgång av effekterna av hydrering på ssHDX hastigheten kan informera urval av ideala RH villkor. För att kontrollera hastigheten för fukt sorption och undvika kollaps av pulvret i formuleringar innehållande hygroskopiska konstituenser (t.ex. sackaros och trehalos), kan ssHDX utföras under kylda betingelser (2-8 ° C). Vår tidigare studie om hydrering effekter visade ökad hastighet och omfattning utbyte med ökad fukthalt, som förväntat. I mycket av vårt arbete, en mellan RH på 43% vid 5 ° C har visat sig vara idealisk för att skilja formuleringar i rimlig tid 24. Reaktionen utförs vanligtvis tills en platå uppnåtts. Detta säkerställer att fukt sorption och diffusion i den fasta inte styra HDX hastigheten. Användningen av små storlekar fasta prov med pre-frystorkning volym ≤2 ml bidrar också till att säkerställa att D 2 O ånga sorption är i huvudsak klar tidigt i utbytesperioden. Även ssHDX-MS gerkvantitativ information om konforma av protein i solid-state, det finns vissa förutsättningar där tolkning av data inte kan helt baserat på ssHDX studien ensam. Det är möjligt att den minskade deuterium upptag observerades i ett prov (jämfört med kontroll) kan bero på den högre retention av proteinstruktur eller den betydande mängden av proteinaggregat som finns i provet. I ett sådant fall, tolkning av ssHDX data kräver resultat från andra kompletterande metoder. Toppbreddning i deutererad masspektra observerades för flera Mb formuleringar 27,28. Detta kan bero på olika faktorer som närvaron av partiellt utvikta proteinpopulationen, rumslig heterogenitet i provet, eller de spatiala gradienterna i D 2 O koncentration. Men dessa faktorer inte särskiljas i ssHDX-MS och behöver utredas ytterligare.
Som SSPL-MS är relativt ny i jämförelse med andra metoder, kontinuerligt lärande absina tillämpningar och begränsningar krävs. I SSPL är fototvärbindningsfrystorkas med proteinet. Bristen på fukt begränsar rörligheten av komponenter inom den fasta matrisen, och den partiella strukturella avkoppling som kan förekomma med fukt sorption i ssHDX är inte ett fenomen i SSPL. Detta begränsar märkning i SSPL till omedelbar närhet av den fototvärbindaren. Men till skillnad från HDX-MS, MS / MS-analys av den kovalent märkta proteinet kan ge rester-nivå strukturell information. Eftersom SSPL märkning är kovalent och irreversibel, tillbaka utbytet inte inträffar och prover kan förberedas och analyseras utan oro för förlust av etiketten. För att underlätta spridning av märkningsmedel och förbättra märkningen effektiviteten i fast-matrisen, kan SSPL utföras med ökande% RH. pLeu upptag kan också förbättras genom att öka koncentrationen av fotoreaktiva medel. Det molära förhållandet av protein till pLeu kan varieras såsom önskas. I allmänhet, en 100x molärt överskott av pLeu till proTein kommer att säkerställa tillräcklig märkning. Dock får höga pLeu koncentration resultera i förlust av Tertiärstruktur i den fasta matrisen. Därför Förutom märknings kinetik och formulering sammansättning, val av pLeu koncentrationen måste också grundas på att bibehålla protein strukturell integritet. Som pLeu etiketter nonselectively XH (där X = C, N, O) grupp, är det möjligt att hjälpämnen med liknande märkning platser kan kraftigt påverka nivån på proteinmärkning. Störningen av hjälpämnen i tillgången på pLeu för proteinmärkning ännu präglas. Det är känt att karben genereras från diazirine aktivering inte rest specifik, men en studie redovisar inriktning mot Asp och Glu 36. Även om det är bra att lära sig om restspecifika interaktioner, är peptid-nivå informationen även användbar och kan användas för att utforma hjälpämnen för att blockera regioner med hög matris exponering i fast tillstånd. SSPL-MS ger detaljerad kvalitativ information, menkvantitativa data måste erhållas och robusta mått behöver utvecklas för att analysera formuleringsskillnader inom en rad frystorkade system.
Användningen av en återstod specifik etikett kombinerat med MS / MS-analys kan ytterligare förbättra upplösningen till amino-syranivå. Märkningsreagens såsom 2,3-butandion att märka Arg, N-hydroxisuccinimid-derivat för Lys och N -alkylmaleimide derivat för Cys kan användas för att exakt kartlägga molekylära interaktioner i lyofiliserat pulver. Men dessa reagenser pH-beroende och reaktionerna kanske inte är så välkontrollerad som fotolytisk märkning i fast tillstånd. Ett alternativt tillvägagångssätt är att införliva den fototvärbindningsmedel in i proteinsekvensen med användning av auxotrofa cellinjer, ställesriktad mutagenes eller sidokedja derivatisering.
Våra tidigare ssHDX-MS och SSPL-MS studier har visat att märkningen av protein beror på typen och mängden av hjälpämnenanvänds 24,27,28,31-33,37,38. ssHDX-MS i Mb samarfrystorkas med guanidinhydroklorid (Gdn.HCl) visade större deuterium upptag än Mb samarfrystorkat med låg molekylvikt sockerarter 32. I en separat SSPL-MS studie Mb samarfrystorkas med Gdn.HCl visade större skydd mot fotolytisk märkning än Mb med sackaros 33. Vidare kvantitativa mätningar från ssHDX-MS har starkt korrelerade med stabiliteten hos proteinet vid långtidslagring 28. Dessa studier tyder på att ssHDX eller SSPL protein återspeglar omfattningen av strukturell retention av proteinet i lyofiliserat pulver. Vi tror att bibehållandet av sekundär struktur i frystorkade pulver ger gynnsamma förutsättningar för sidokedja märkning med pLeu och skydd av amid väte från deuterium utbyte. Emellertid behöver detaljerad jämförelse av informativt innehåll från dessa metoder för att utföras i framtiden. Även upprättandet nyttan av ssHDX-MS och SSPL-MSsom en formulering screeningmetod i slutändan kommer att kräva att den tillämpas på många proteiner, resultat från våra nya studier stöder dess bredare införande. Med ytterligare utveckling, är dessa metoder förväntas vara allmänt användbar för att karakterisera halvledarproteinformuleringar i den biofarmaceutiska industrin.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors gratefully acknowledge financial support from NIH R01 GM085293 (PI: E. M. Topp) and from the College of Pharmacy at Purdue University.
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| Equine myoglobin | Sigma-Aldrich | M0630-5G | |
| D-(+)-Trehalose dihydrate | Sigma Aldrich | #T9531 | |
| D-Sorbitol | Sigma Aldrich | #240850 | |
| L-Photo-leucine | Thermo Scientific | #22610 | |
| Potassium phosphate monobasic | Sigma-Aldrich | #P0662 | |
| Potassium phosphate dibasic | Sigma-Aldrich | #P3786 | |
| Deuterium Oxide | Cambridge Isotope Laboratories | #DLM-4-PK | Alternate (Cat. No.: 151882, Sigma-Aldrich) |
| Immobilized pepsin | Applied Biosystems | #2-3132-00 | |
| Trypsin | Promega | #V511A | Chymotrypsin (Cat. No.: #V1062, Promega) can be additionally used |
| Water, Optima LC/MS grade | Fisher Chemical | #7732-18-5 | |
| Acetonitrile | Sigma-Aldrich | #34998 | |
| Formic acid | Thermo Scientific | #28905 | |
| ESI-TOF Calibrant | Agilent Technologies | #G1969-85000 | Highly flammable liquid |
| Protein microtrap | Michrom Bioresources | TR1/25108/03 | |
| Peptide microtrap | Michrom Bioresources | TR1/25109/02 | |
| Analytical column | Agilent Technologies | Zorbax 300SB-C18 | |
| Freeze dryer | VirTis AdVantage Plus | ||
| Stratalinker equipped with five 365 nm lamps | Stratagene Corp. | Stratalinker 2400 | |
| HPLC | Agilent Technologies | 1200 series LC | Refrigerated LC system for HDX-MS |
| ESI-qTOF MS | Agilent Technologies | 6520 qTOF | |
| HDExaminer (HDX-MS data analysis software) | Sierra Analytics | http://www.massspec.com/HDExaminer.html |
References
- Lawrence, S. Billion dollar babies–biotech drugs as blockbusters. Nat. Biotechnol. 25 (4), 380-382 (2007).
- . . Global Markets and Manufacturing Technologies for Protein Drugs. , BIO021D (2013).
- Lai, M. C., Topp, E. M. Solid-state chemical stability of proteins and peptides. J. Pharm. Sci. 88 (5), 489-500 (1999).
- Carpenter, J. F., Pikal, M. J., Chang, B. S., Randolph, T. W. Rational design of stable lyophilized protein formulations: some practical advice. Pharm. Res. 14 (8), 969-975 (1997).
- Carpenter, J. F., Chang, B. S., Garzon-Rodriguez, W., Randolph, T. W. Rational design of stable lyophilized protein formulations: theory and practice. Pharm. Biotechnol. 13, 109-133 (2002).
- Wüthrich, K. Protein structure determination in solution by NMR spectroscopy. J. Biol. Chem. 265 (36), 22059-22062 (1990).
- Ilari, A., Savino, C. Protein structure determination by x-ray crystallography. Methods. Mol. Biol. 452, 63-87 (2008).
- Brunger, A. T. X-ray crystallography and NMR reveal complementary views of structure and dynamics. Nat. Struct. Biol. 4, 862-865 (1997).
- Yu, L. Amorphous pharmaceutical solids: preparation, characterization and stabilization. Adv Drug. Deliv. Rev. 48 (1), 27-42 (2001).
- Manning, M. C. Use of infrared spectroscopy to monitor protein structure and stability. Expert. Rev. Proteomics. 2 (5), 731-743 (2005).
- Grohganz, H., Gildemyn, D., Skibsted, E., Flink, J. M., Rantanen, J. Rapid solid-state analysis of freeze-dried protein formulations using NIR and Raman spectroscopies. J. Pharm. Sci. 100 (7), 2871-2875 (2011).
- Bai, S., Nayar, R., Carpenter, J. F., Manning, M. C. Noninvasive determination of protein conformation in the solid state using near infrared (NIR) spectroscopy. J. Pharm. Sci. 94 (9), 2030-2038 (2005).
- Pikal, M. J., et al. Solid state chemistry of proteins: II. The correlation of storage stability of freeze-dried human growth hormone (hGH) with structure and dynamics in the glassy solid. J. Pharm. Sci. 97 (12), 5106-5121 (2008).
- Wang, B., Tchessalov, S., Cicerone, M. T., Warne, N. W., Pikal, M. J. Impact of sucrose level on storage stability of proteins in freeze-dried solids: II. Correlation of aggregation rate with protein structure and molecular mobility. J. Pharm. Sci. 98 (9), 3145-3166 (2009).
- Schule, S., Friess, W., Bechtold-Peters, K., Garidel, P. Conformational analysis of protein secondary structure during spray-drying of antibody/mannitol formulations. Eur. J. Pharm. Biopharm. 65 (1), 1-9 (2007).
- Baerga-Ortiz, A., Hughes, C. A., Mandell, J. G., Komives, E. A. Epitope mapping of a monoclonal antibody against human thrombin by H/D-exchange mass spectrometry reveals selection of a diverse sequence in a highly conserved protein. Protein. Sci. 11 (6), 1300-1308 (2002).
- Coales, S. J., Tuske, S. J., Tomasso, J. C., Hamuro, Y. Epitope mapping by amide hydrogen/deuterium exchange coupled with immobilization of antibody, on-line proteolysis, liquid chromatography and mass spectrometry. Rapid. Commun. Mass. Spectrom. 23 (5), 639-647 (2009).
- Pacholarz, K. J., Garlish, R. A., Taylor, R. J., Barran, P. E. Mass spectrometry based tools to investigate protein-ligand interactions for drug discovery. Chem. Soc. Rev. 41 (11), 4335-4355 (2012).
- Houde, D., Peng, Y., Berkowitz, S. A., Engen, J. R. Post-translational modifications differentially affect IgG1 conformation and receptor binding. Mol. Cell. Proteomics. 9 (8), 1716-1728 (2010).
- Houde, D., Berkowitz, S. A., Engen, J. R. The utility of hydrogen/deuterium exchange mass spectrometry in biopharmaceutical comparability studies. J. Pharm. Sci. 100 (6), 2071-2086 (2011).
- Dorman, G., Prestwich, G. D. Using photolabile ligands in drug discovery and development. Trends. Biotechnol. 18 (2), 64-77 (2000).
- Robinette, D., Neamati, N., Tomer, K. B., Borchers, C. H. Photoaffinity labeling combined with mass spectrometric approaches as a tool for structural proteomics. Expert. Rev. Proteomics. 3 (4), 399-408 (2006).
- Greenspan, L. Humidity fixed points of binary saturated aqueous solutions. Journal of Research of the National Bureau of Standards. 81A (1), 8 (1977).
- Sophocleous, A. M., Zhang, J., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 1. Exchange mapping. Mol. Pharm. 9 (4), 718-726 (2012).
- Keppel, T. R., Jacques, M. E., Young, R. W., Ratzlaff, K. L., Weis, D. D. An efficient and inexpensive refrigerated LC system for H/D exchange mass spectrometry. J. Am. Soc. Mass. Spectrom. 22 (8), 1472-1476 (2011).
- Gasteiger, E., et al. ExPASy: The proteomics server for in-depth protein knowledge and analysis. Nucleic. Acids. Res. 31 (13), 3784-3788 (2003).
- Sophocleous, A. M., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 2. Exchange kinetics. Mol. Pharm. 9 (4), 727-733 (2012).
- Moorthy, B. S., Schultz, S. G., Kim, S. G., Topp, E. M. Predicting Protein Aggregation during Storage in Lyophilized Solids Using Solid State Amide Hydrogen/Deuterium Exchange with Mass Spectrometric Analysis (ssHDX-MS). Mol. Pharm. 11 (6), 1869-1879 (2014).
- Wang, W. Lyophilization and development of solid protein pharmaceuticals. Int. J. Pharm. 203 (1-2), 1-60 (2000).
- Sarciaux, J. M., Mansour, S., Hageman, M. J., Nail, S. L. Effects of buffer composition and processing conditions on aggregation of bovine IgG during freeze-drying. J. Pharm. Sci. 88 (12), 1354-1361 (1999).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Characterizing protein structure in amorphous solids using hydrogen/deuterium exchange with mass spectrometry. Anal. Biochem. 366 (1), 18-28 (2007).
- Sinha, S., Li, Y., Williams, T. D., Topp, E. M. Protein conformation in amorphous solids by FTIR and by hydrogen/deuterium exchange with mass spectrometry. Biophys. J. 95 (12), 5951-5961 (2008).
- Iyer, L. K., Moorthy, B. S., Topp, E. M. Photolytic labeling to probe molecular interactions in lyophilized powders. Mol. Pharm. 10 (12), 4629-4639 (2013).
- Hentze, N., Mayer, M. P. Analyzing protein dynamics using hydrogen exchange mass spectrometry. J. Vis. Exp. (81), e50839 (2013).
- Kaltashov, I. A., Bobst, C. E., Abzalimov, R. R. H/D exchange and mass spectrometry in the studies of protein conformation and dynamics: is there a need for a top-down approach. Anal. Chem. 81 (19), 7892-7899 (2009).
- Jumper, C. C., Schriemer, D. C. Mass spectrometry of laser-initiated carbene reactions for protein topographic analysis. Anal. Chem. 83 (8), 2913-2920 (2011).
- Li, Y., Williams, T. D., Topp, E. M. Effects of excipients on protein conformation in lyophilized solids by hydrogen/deuterium exchange mass spectrometry. Pharm. Res. 25 (2), 259-267 (2008).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Trehalose and calcium exert site-specific effects on calmodulin conformation in amorphous solids. Biotechnol. Bioeng. 97 (6), 1650-1653 (2007).

