-HPLC baseado Ensaio para monitorar Extracelular Nucleotide / nucleosídeos Metabolismo em crônicas células de leucemia linfocítica Humanos
Summary
The protocol described here represents an easy and reproducible method that employs reverse phase high-performance liquid chromatography (RP-HPLC) to measure purine metabolism on chronic lymphocytic leukemia (CLL) cells cultured under different conditions.
Abstract
Este método descreve uma cromatografia sensível, específico, fiável e reprodutível de fase inversa de alto desempenho líquida (RP-HPLC) desenvolvido e validado para a quantificação de nucleótidos extracelulares de purina e nucleósidos produzidos por purificada da leucemia linfocítica crónica (CLL) células, sob diferentes condições de cultura . A separação cromatográfica de adenosina 5'-monofosfato (AMP), a adenosina (ADO) e inosina (NOi) é realizada a temperatura ambiente numa coluna à base de sílica, de fase inversa que é usada para a retenção de composto polar. O método inclui uma fase móvel binária, que consiste em acetato de amónio 7 mM e acetonitrilo com um caudal de 1,00 ml / min. Os eluatos são monitorizadas utilizando um detector de UV de fotodíodos ajustado a 260 nm. Uma curva de calibração padrão é gerada para calcular a equação para a quantificação analítica de cada composto de purina. controle do sistema, aquisição e análise de dados são então realizadas. Aplicando este protocolo, AMP, INO e ADO eluir aos 7, 11 e 11,9 min, respectivamente, eo tempo total de execução para cada amostra é de 20 min. Este protocolo pode ser aplicado a diferentes tipos de células e linhas celulares (ambos de suspensão e aderentes), utilizando meios de cultura como matriz. As vantagens são a preparação da amostra fácil e rápido e a exigência de uma pequena quantidade de sobrenadante para análise. Além disso, a utilização de um meio isento de soro permite saltando a etapa de precipitação de proteínas com acetoni trilo que os impactos a concentração final dos compostos de purina. Uma das limitações do método é a exigência de a coluna de equilíbrio executado antes de cada corrida única amostra, fazendo com que o tempo total de funcionamento do experimento mais tempo e evitando aplicações rastreio de alto rendimento.
Introduction
A adenosina (ADO) é um nucleósido de purina com uma molécula de adenina ligado a uma molécula porção de açúcar ribose através de uma ligação glicosídica. Quando presente no meio extracelular, que protege as células de danos excessivos pela acção do sistema imune. Este papel tem sido destacada usando diferentes modelos de doenças, tais como a colite 1, 2 diabetes, asma 3, sepse 4 e lesão isquêmica 5. Uma das principais funções ADO é a inibição de respostas imunitárias no microambiente tumoral, contribuindo para a evasão do tumor imune 6. Por esta razão, os mecanismos envolvidos na formação de ADO e de sinalização são de considerável interesse terapêutico 7.
ADO níveis no microambiente do tecido são relativamente baixas, em condições fisiológicas normais e, certamente, inferior ao limiar de sensibilidade das células imunes. No entanto, durante a hipoxia, isquemia, inflamação, infecção, metabólicastress e transformação do tumor eles aumentam rapidamente 8. Os elevados níveis ADO extracelular em resposta a sinais de perturbação do tecido tem uma dupla função: relatar lesão do tecido de uma maneira autócrina e parácrina e gerar respostas de tecido que pode ser geralmente visto como citoprotetor.
ADO extracelular pode ser formada através de uma variedade de mecanismos, que incluem a libertação a partir de compartimentos intracelulares mediadas por transportadores de nucleosídeos 9 ou acumulação por causa da degradação auditivos operado pela adenosina-desaminase. A principal via que conduz ao aumento dos níveis extracelulares ADO envolve a acção de uma cascata de ectonucleotidases, que são ectoenzimas associadas à membrana, gerando ADO phosphohydrolysis de nucleótidos libertados a partir de células mortas ou a morrer. Esta via prossegue através da ação sequencial de CD39 (trifosfato de ectonucleoside difosfohidrolase-1) que converte extracelular de adenosina 5'-trifosfato (ATP) ou adenosina 5'-difosfato (ADP) em adenosina-5'-monofosfato (AMP) e de CD73 (5'-nucleotidase), que converte a AMP ADO 10.
Extracelular ADO provoca suas respostas fisiológicas pela ligação a quatro transmembrana ADO receptores, ou seja, A1, A2A, A2B e A3. Cada receptor tem diferentes afinidades para ADO e distribuição do tecido específico. Todos os receptores possuem sete domínios transmembranares e são a proteína G acoplado a proteínas de ligação de GTP intracelular (proteínas G), que pode induzir a (proteína Gs) ou inibir a actividade da adenilato ciclase (proteína Gi) e, subsequentemente, a produção de AMPc intracelular. Portanto, mudanças no citoplasmática impacto níveis acampamento na atividade da proteína quinase intracelular durante as respostas fisiológicas 11. Sob condições fisiológicas ADO extracelular é abaixo de 1 uM, que podem activar indiscriminadamente A1, A2A e A3 receptores. No entanto, a activação de subtipo A2B requer consideravelmente maiorAs concentrações de nucleósido, tais como os gerados sob condições fisiopatológicas. Alternativamente, o ADO extracelular pode ser degradada de inosina (NOi) por adenosina-desaminase (ADA) e de CD26, uma proteína complexante da ADA localizar ADA na superfície da célula. Outra possibilidade é que o ADO é internalizado pela célula através dos transportadores de nucleosídeos equilibrative (ENT) e fosforilado em AMP por ADO proteína quinase 12,13.
O objectivo deste protocolo é descrever um método analítico de cromatografia líquida de alta eficiência de fase inversa (RP-HPLC) para quantificar num único ensaio AMP substrato e dos produtos de ADO e Ino, como gerado por linfócitos humanos. A experiência foi inicialmente obtida usando células de pacientes com leucemia linfocítica crónica (LLC), que são caracterizados pela expansão de uma população madura de linfócitos CD19 + / B CD5 + constitutivamente expressam CD39 14,15. Mostrámos cerca de 30%de CLL pacientes expressam a ectoenzima CD73 e que este fenótipo correlaciona-se com um mau prognóstico 16. Esta subpopulação de células leucêmicas co-expressam CD39 e CD73 pode produzir ativamente ADO extracelular a partir de ADP e / ou AMP. A pré-incubação de células CD73 + de CLL com α, síntese ADO extracelular β-metileno-ADP (APCP), um conhecido inibidor da actividade enzimica de CD73, que bloqueia completamente confirmando CD73 representa o enzima gargalo de que cascata 16.
células CLL expressam também a ADA e a ADA complexação proteína CD26, que são responsáveis pela conversão de ADO dentro INO. Ao utilizar inibidores específicos de ADA, como eritro-9- (2-hidroxi-3-nonil) eu wiadenine (EHNA) e cloridrato de desoxicoformicina (DCF), é possível bloquear a degradação ADO extracelular em INO. Além disso, o pré-tratamento com um inibidor da ADA em combinação com dipiridamol, que bloqueia os transportadores de nucleosídeos, aumenta a acumulação ADO na célulasobrenadantes.
Temos, em seguida, estendeu este protocolo para células derivadas de outros linhagens, incluindo linfócitos T e células mielóides, confirmando produção ADO dependente de CD73. Estes resultados sugerem que este protocolo de HPLC é altamente versátil e que pode ser aplicado a diferentes linhagens celulares e para diferentes condições de cultura (Figura 1).
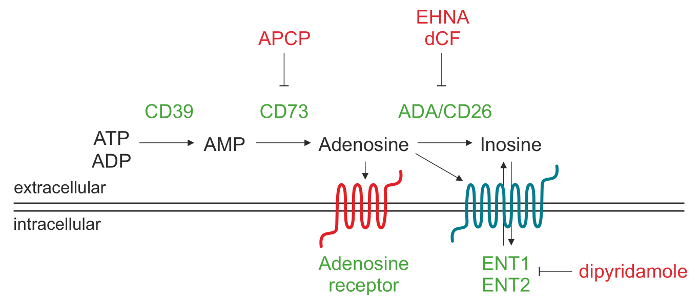
Figura 1. Representação esquemática da maquinaria enzimática responsável pela produção de ADO extracelular. A adenosina 5'-trifosfato (ATP) e / ou da adenosina-5'-difosfato (ADP) pode ser degradado pela CD39 de adenosina 5'-monofosfato (AMP), a qual por sua vez, é convertido por CD73 para o nucleosídeo adenosina (ADO). Uma vez ADO é produzida no espaço extracelular, pode reinserir a célula através dos transportadores de nucleosídeos (ENT), ser convertidos em inosina (NOi) ouligam-se a diferentes tipos de receptores P1 ADO. Por favor clique aqui para ver uma versão maior desta figura.
Protocol
Representative Results
Discussion
O protocolo aqui descrito permite avaliar a actividade do CD39 / CD73 máquinas adenosinérgico em meios de cultura de células a partir de células leucémicas humanas purificadas. Através deste método HPLC podemos seguir e medir quantitativamente a geração enzimática de ADO (dependente de CD73-) e sua posterior degradação INO (CD26 / ADA dependente). O uso de inibidores da enzima permite controlar o protocolo e ter controles internos. As vantagens e novidades deste protocolo são de que i) pode ser aplicada a c…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Este trabalho é apoiado pela Associazione Italiana Ricerca Cancro (IG # 12754).
Materials
| Human blood | |||
| Milli-Q water | Millipore | double deionised water | |
| Ficoll-Paque Plus | GE-Healthcare | 17-1440-03 | |
| purified anti-CD3, -CD14, -CD16 | made in-house | mouse monoclonal | |
| PE-labeled anti-CD19 | Miltenyi Biotec | 120-014-229 | |
| FITC-labeled anti-CD5 | Miltenyi Biotec | 130-096-574 | |
| Dynabeads sheep anti-mouse IgG | Invitrogen | 11031 | |
| Phosphate-buffered saline (PBS) | Amresco | E404-200TABS | tablets |
| bovine serum albumin (BSA) | ID bio | 1000-70 | standard grade |
| isolation buffer | PBS 0.1 % BSA 2 mM EDTA, pH 7.4 | ||
| AIM V serum free medium | GIBCO | 12055-091 | liquid (research grade) |
| adenosine 5’-diphosphate (ADP) | Sigma-Aldrich | A2754 | |
| adenosine 5’-monosphate (AMP) | Sigma-Aldrich | A1752 | |
| adenosine (ADO) | Sigma-Aldrich | A9251 | |
| inosine (INO) | Sigma-Aldrich | I4125 | |
| α,β-methylene-ADP (APCP) | Sigma-Aldrich | M8386 | CD73 inhibitor |
| EHNA hydrochloride | Sigma-Aldrich | E114 | adenosine deaminase inhibitor |
| Deoxycoformycin (dCF) | Tocris | 2033 | adenosine deaminase inhibitor |
| Dimethyl sulfoxide (DMSO) | Sigma-Aldrich | D2650 | |
| Dipyridamole | Sigma-Aldrich | D9766 | nucleoside transporter inhibitor |
| acetonitrile (CHROMASOLV Plus) | Sigma-Aldrich | 34998 | HPLC-grade |
| ammonium acetate | Sigma-Aldrich | 9688 | 7 mM, pH 3.0 |
| hydrochloric acid | Sigma-Aldrich | 30721-1L | min. 37 % |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Bürker cell counter | VWR | 631-0920 | hemocytometer |
| DynaMag-15 Magnet | Invitrogen | 12301D | Dynal magnetic bead separator |
| microcentrifuge safe-lock tubes | Eppendorf | 030-120-0086 | 1.5 ml |
| PET centrifuge tubes | Corning | 430053/430304 | 15 – 50 ml |
| Minisart RC4 syringe filters | Sartorius Stedim Biotech | 17821 | membrane 0.2 µm |
| short thread vials | VWR | 548-0029 | 1.5 ml/glass |
| micro-inserts | VWR | 548-0006 | 0.1 ml/glass |
| screw caps | VWR | 548-0085 | 9 mm/PP blue |
| Atlantis dC18 Column | Waters | 186001344 | 5 µm, 4.6 x 150 mm |
| Atlantis dC18 Guard Column | Waters | 186001323 | 5 µm, 4.6 x 20 mm |
| Waters Alliance 2965 Separations Module | Waters | HPLC separation module | |
| Waters 2998 Photodiode Array (PDA) Detector | Waters | UV detector | |
| Waters Empower2 software | Waters |
References
- Naganuma, M., Wiznerowicz, E. B., Lappas, C. M., Linden, J., Worthington, M. T., Ernst, P. B. Cutting edge: Critical role for A2A adenosine receptors in the T cell-mediated regulation of colitis. J Immunology. 177 (5), 2765-2769 (2006).
- Nemeth, Z. H., et al. Adenosine receptor activation ameliorates type 1 diabetes. FASEB J. 21 (10), 2379-2388 (2007).
- Fan, M., Jamal Mustafa, S. Role of adenosine in airway inflammation in an allergic mouse model of asthma. Int Immunopharmacol. 6 (1), 36-45 (2006).
- Csoka, B., et al. A2B adenosine receptors protect against sepsis-induced mortality by dampening excessive inflammation. J Immunol. 185 (1), 542-550 (2010).
- Peart, J. N., Headrick, J. P. Adenosinergic cardioprotection: multiple receptors, multiple pathways. Pharmacol Ther. 114 (2), 208-221 (2007).
- Ohta, A., et al. A2A adenosine receptor protects tumors from antitumor T cells. Proc Natl Acad Sci U S A. 103 (35), 13132-13137 (2006).
- Hasko, G., Linden, J., Cronstein, B., Pacher, P. Adenosine receptors: therapeutic aspects for inflammatory and immune diseases. Nat Rev Drug Discov. 7 (9), 759-770 (2008).
- Cronstein, B. N. Adenosine, an endogenous anti-inflammatory agent. J Appl Physiol (1985). 76 (1), 5-13 (1994).
- Molina-Arcas, M., Casado, F. J., Pastor-Anglada, M. Nucleoside transporter proteins. Curr Vasc Pharmacol. 7 (4), 426-434 (2009).
- Deaglio, S., et al. Adenosine generation catalyzed by CD39 and CD73 expressed on regulatory T cells mediates immune suppression. J Exp Med. 204 (6), 1257-1265 (2007).
- Linden, J. Regulation of leukocyte function by adenosine receptors. Adv Pharmacol. 61, 95-114 (2011).
- Antonioli, L., Blandizzi, C., Pacher, P., Hasko, G. Immunity, inflammation and cancer: a leading role for adenosine. Nat Rev Cancer. 13 (12), 842-857 (2013).
- Antonioli, L., Csoka, B., Fornai, M., et al. Adenosine and inflammation: what’s new on the horizon. Drug Discov Today. 19 (8), 1051-1068 (1051).
- Chiorazzi, N., Rai, K. R., Ferrarini, M. Chronic lymphocytic leukemia. N Engl J Med. 352 (8), 804-815 (2005).
- Abousamra, N. K., Salah El-Din, M., Hamza Elzahaf, E., Esmael, M. E. Ectonucleoside triphosphate diphosphohydrolase-1 (E-NTPDase1/CD39) as a new prognostic marker in chronic lymphocytic leukemia. Leuk Lymphoma. 56 (1), 113-119 (2015).
- Serra, S., et al. CD73-generated extracellular adenosine in chronic lymphocytic leukemia creates local conditions counteracting drug-induced cell death. Blood. 118 (23), 6141-6152 (2011).
- Chen, L. S., Keating, M. J., Gandhi, V. Blood collection methods affect cellular protein integrity: implications for clinical trial biomarkers and ZAP-70 inn CLL. Blood. 124 (7), 1192-1195 (2014).
- Kalina, T., et al. EuroFlow standardization of flow cytometer instrument settings and immunophenotyping protocols. Leukemia. 26 (9), 1986-2010 (2012).
- Deaglio, S., et al. CD38 and ZAP-70 are functionally linked and mark CLL cells with high migratory potential. Blood. 110 (12), 4012-4021 (2007).
- Sachsenmeier, K. F., et al. Development of a novel ectonucleotidase assay suitable for high-throughput screening. J Biomol Screen. 17 (7), 993-998 (2012).

