Syntes av RGD-funktion Hydrogeler som ett verktyg för terapeutiska tillämpningar
Summary
We present a protocol for the synthesis of RGD-functionalized hydrogels as devices for cell and drug delivery. The procedure involves copper catalyzed alkyne-azide cycloaddition (CuAAC) between alkyne-modified polyacrylic acid (PAA) and a RGD-azide derivative. The hydrogels are formed using microwave-assisted polycondensation and their physicochemical properties are investigated.
Abstract
The use of polymers as biomaterials has provided significant advantages in therapeutic applications. In particular, the possibility to modify and functionalize polymer chains with compounds that are able to improve biocompatibility, mechanical properties, or cell viability allows the design of novel materials to meet new challenges in the biomedical field. With the polymer functionalization strategies, click chemistry is a powerful tool to improve cell-compatibility and drug delivery properties of polymeric devices. Similarly, the fundamental need of biomedicine to use sterile tools to avoid potential adverse-side effects, such as toxicity or contamination of the biological environment, gives rise to increasing interest in the microwave-assisted strategy.
The combination of click chemistry and the microwave-assisted method is suitable to produce biocompatible hydrogels with desired functionalities and improved performances in biomedical applications. This work aims to synthesize RGD-functionalized hydrogels. RGD (arginylglycylaspartic acid) is a tripeptide that can mimic cell adhesion proteins and bind to cell-surface receptors, creating a hospitable microenvironment for cells within the 3D polymeric network of the hydrogels. RGD functionalization occurs through Huisgen 1,3-dipolar cycloaddition. Some PAA carboxyl groups are modified with an alkyne moiety, whereas RGD is functionalized with azido acid as the terminal residue of the peptide sequence. Finally, both products are used in a copper catalyzed click reaction to permanently link the peptide to PAA. This modified polymer is used with carbomer, agarose and polyethylene glycol (PEG) to synthesize a hydrogel matrix. The 3D structure is formed due to an esterification reaction involving carboxyl groups from PAA and carbomer and hydroxyl groups from agarose and PEG through microwave-assisted polycondensation. The efficiency of the gelation mechanism ensures a high degree of RGD functionalization. In addition, the procedure to load therapeutic compounds or biological tools within this functionalized network is very simple and reproducible.
Introduction
Hydrogeler är tredimensionella nätverk som bildats av hydrofila tvärbundna polymerer, som är naturliga eller syntetiska, och kännetecknas av en distinkt tredimensionell struktur. Dessa enheter är alltmer attraktiva i biomedicinska områdena drug delivery, vävnadsteknik, genbärare och smarta sensorer 1,2. Faktum är att deras höga vattenhalt, liksom deras reologiska och mekaniska egenskaper gör dem lämpliga kandidater att efterlikna mjukdelsmikromiljöer och göra dem effektiva verktyg för vattenlösligt cytokin eller tillväxtfaktor leverans. En av de mest lovande användning är som ett injicerbart biomaterial bärande celler och bioaktiva föreningar. Hydrogeler kan förbättra cellöverlevnad och kontroll stamcells öde genom att hålla och exakt leverera stamcellsregleringssignaler i ett fysiologiskt relevant sätt, såsom observerats i in vitro- och i in vivo-experiment 3,4. Den ledande Fördelen med detta är möjlighetenatt upprätthålla injicerade cellerna inom zonen av inokulering (in situ), vilket minimerar den mängd celler som lämnar området och extravasates i cirkulations flöde, migrerar över hela kroppen och förlora målet mål 5. Stabiliteten hos de tre-dimensionella hydrogelpartiklar nätverk beror på dess tvärbindningsställen, bildade genom kovalenta bindningar eller kohesiva krafter mellan polymerkedjorna 6.
I detta sammanhang tillämpas ortogonala selektiv kemi till polymerkedjor är ett mångsidigt verktyg kan förbättra hydrogel föreställningar 7. I själva verket modifiering av polymerer med lämpliga kemiska grupper kan bidra till att tillhandahålla lämplig kemiska, fysikaliska och mekaniska egenskaper för att förbättra cellviabilitet och deras användning i vävnadsbildning. På samma sätt, bland de tekniker för att ladda celler eller tillväxtfaktorer inom gelmatrisen, användningen av RGD-peptiden medger förbättringar i celladhesion och överlevnad. RGD är en tripeptid sammansattarginin, glycin och asparaginsyra, som är den i särklass mest effektiva och ofta anställda tripeptid på grund av dess förmåga att adressera mer än en cell adhesion receptor och dess biologiska effekter på cell förankring, beteende och överlevnad 8,9. I detta arbete studeras syntesen av RGD-funktion hydrogeler i syfte att utforma nätverk som kännetecknas av tillräckliga biokemiska egenskaper för en gäst cell mikromiljö.
Användningen av mikrovågsstrålning i hydrogel syntes ger ett enkelt förfarande för att minimera bireaktioner och få högre reaktionshastigheter och utbyten på kortare tid jämfört med konventionella termiska processer 10. Denna metod kräver inte reningssteg och ger sterila hydrogeler på grund av de interaktioner mellan polymererna och frånvaron av organiska lösningsmedel i reaktionssystemet 11. Därför ser det höga procentandelar av RGD kopplade till polymera nätverket eftersom ingen modfikationerna är skyldiga att polymer kemiska grupper som är inblandade i gelbildning. Karboxylgrupper, från PAA och karbomer, och hydroxylgrupper, från PEG och agaros, ge upphov till hydrogelen tredimensionella strukturen genom en polykondensationsreaktion. De nämnda polymerer användes för syntes av hydrogeler i ryggmärgsskada reparation behandlingar 12. Dessa enheter, som rapporterats i tidigare verk 13,14, visar hög biokompatibilitet samt mekaniska och fysikalisk-kemiska egenskaper som liknar de hos många levande vävnader och tixotrop natur. Dessutom förblir de lokaliserad in situ, vid zonen för injektionen.
I detta arbete är PAA karboxylgrupper modifierad med en alkyn molekyldel (figur 1), och en RGD-azid förening syntetiseras utnyttjar reaktiviteten hos tripeptid terminala gruppen -NH2 med en förberedd kemisk förening med strukturen (CH2) n – N 3 (<strong> Figur 2). Därefter reagerar den modifierade PAA med RGD-azidderivat genom CuAAC klick reaktion 15-17 (Figur 3). Användningen av en koppar (I) katalysator leder till stora förbättringar i både reaktionshastigheten och regioselektivitet. Den CuAAC reaktion används ofta i organisk syntes och polymervetenskap. Den kombinerar hög effektivitet och hög tolerans mot de funktionella grupperna, och det är opåverkad av användningen av organiska lösningsmedel. En hög selektivitet, en snabb reaktionstid och en enkel procedur renings tillåter erhållandet av stjärnpolymerer, segmentsampolymerer eller kedjor ympning önskade delar 18. Denna klick strategi gör det möjligt att modifiera polymerer efter polymerisation att anpassa fysikalisk-kemiska egenskaper enligt den slutliga biokemiska ansökan. De CuAAC experimentella betingelser är lätt reproducerbar (reaktionen är okänslig för vatten, medan koppar oxidation kan förekomma minimalt), och naturen avbildade triazol säkerställer produktens stabilitet. Användningen av kopparmetall kan anses vara en kritisk punkt, på grund av dess potentiella toxiska effekt mot celler och i den biologiska mikromiljö, men dialys används som en reningsmetod för att tillåta fullständigt avlägsnande av katalysatorrester. Slutligen PAA modifierad RGD används i hydrogel-syntes (Figur 4) och de fysikalisk-kemiska egenskaperna hos de erhållna näten undersöks, i syfte att kontrollera den potentiella funktionaliteten hos dessa system som celler eller droger bärare.
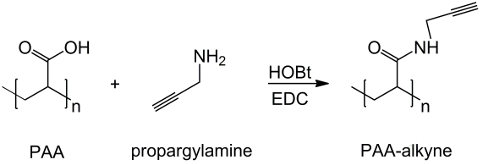
Figur 1: PAA modifierad alkyn syntes Ett system av PAA funktionalisering med alkyn grupp;. "n" anger monomerer med karboxylgrupp reagera med propargylamin. Klicka här för att seen större version av denna siffra.
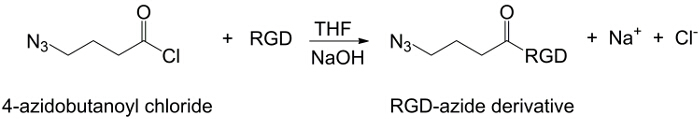
Figur 2:.. RGD-azid syntes Syntesen av RGD-azidderivat Klicka här för att se en större version av denna siffra.
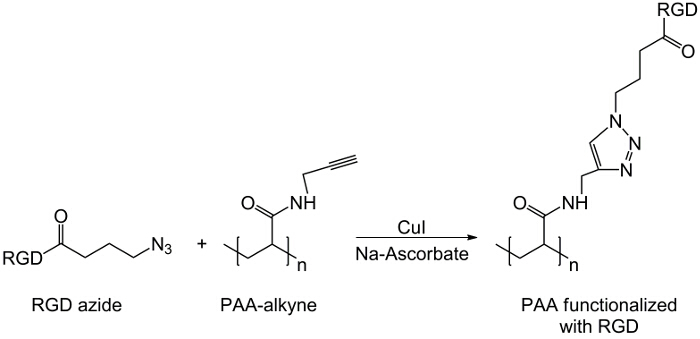
Figur 3: Klicka på reaktionsschema klick reaktion mellan RGD-azidderivat och alkyn-PAA.. Klicka här för att se en större version av denna siffra.
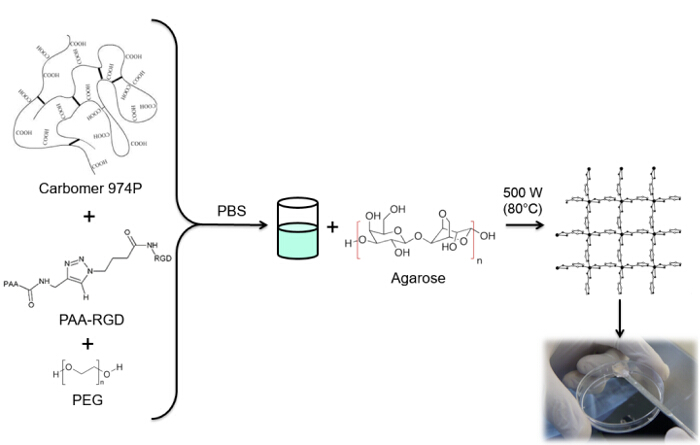
Figur 4: hydrogel Synthesis. RGD funktion hydrogel syntesförfarandet. Klicka här för att se en större version av denna siffra.
Protocol
Representative Results
Discussion
The PAA post-polymerization modification with alkyne moieties and the RGD functionalization with the azide group guarantee the formation of a stable bond between the polymer and the peptide. Indeed, triazole serves as a rigid linking unit among the carbon atoms, attached to the 1,4 positions of the 1,2,3-triazole ring and it cannot be cleaved hydrolytically or otherwise. In addition, triazole is extremely difficult to oxidize and reduce, unlike other cyclic structures such as benzenoids and related aromatic heterocycles<…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna vill tacka professor Maurizio Masi för givande diskussion och Miss Chiara Allegretti för språkgranskning. Författarnas forskning stöds av Bando Giovani Ricercatori 2010 (Minis della Salute GR-2010- 2.312.573).
Materials
| Poly(acrylic acid) solution average Mw ~ 100,000, 35 wt % in H2O | Sigma Aldrich | 523925 | CAS 9003-01-4 |
| Poly(ethylene glycol) 2,000 | Sigma Aldrich | 84797 | CAS 25322-68-3 |
| Carbomeer 974P | Fagron | 1387083 | |
| Agarose | Invitrogen Corp. | 16500-500 | UltraPure Agarose |
| RGD peptide | abcam | ab142698 | |
| 4-azidobutanoic acid | Aurum Pharmatech | Z-2421 | CAS 54447-68-6 |
| Oxalyl chloride | Sigma Aldrich | O8801 | CAS 79-37-8 |
| Propargylamine hydrochloride 95% | Sigma Aldrich | P50919 | CAS 15430-52-1 |
| Copper(I) iodide | Sigma Aldrich | 3140 | CAS 7681-65-4 |
| Sodium ascorbate | Sigma Aldrich | Y0000039 | CAS 134-03-2 |
| Phosphate buffered saline | Sigma Aldrich | P4417 | |
| Dialysis Membrane | Spectrum Laboratories, Inc. | 132725 | Spectra/Por 3 Dialysis Membrane Standard RC Tubing MWCO: 3,5 kD |
References
- Slaughter, B. V., Khurshid, S. S., Fisher, O. Z., Khademhosseini, A., Peppas, N. A. Hydrogels in Regenerative Medicine. Adv. Mater. 21 (32-33), 3307-3329 (2009).
- Rossi, F., Perale, G., Papa, S., Forloni, G., Veglianese, P. Current options for drug delivery to the spinal cord. Expert Opin. Drug Deliv. 10 (3), 385-396 (2013).
- Huebsch, N., et al. Harnessing traction-mediated manipulation of the cell/matrix interface to control stem-cell fate. Nat. Mater. 9 (6), 518-526 (2010).
- Mothe, A. J., Tam, R. Y., Zahir, T., Tator, C. H., Shoichet, M. S. Repair of the injured spinal cord by transplantation of neural stem cells in a hyaluronan-based hydrogel. Biomaterials. 34 (15), 3775-3783 (2013).
- Khetan, S., et al. Degradation-mediated cellular traction directs stem cell fate in covalently crosslinked three-dimensional hydrogels. Nat. Mater. 12 (5), 458-465 (2013).
- Ashley, G. W., Henise, J., Reid, R., Santi, D. V. Hydrogel drug delivery system with predictable and tunable drug release and degradation rates. Proc. Natl. Acad. Sci. U S A. 110 (6), 2318-2323 (2013).
- Rossi, F., van Griensven, M. Polymer Functionalization as a Powerful Tool to Improve Scaffold Performances. Tissue Eng. Part A. 20 (15-16), 2043-2051 (2014).
- Gould, S. T., Darling, N. J., Anseth, K. S. Small peptide functionalized thiol-ene hydrogels as culture substrates for understanding valvular interstitial cell activation and de novo tissue deposition. Acta Biomater. 8 (9), 3201-3209 (2012).
- Azagarsamy, M. A., Anseth, K. S. Wavelength-Controlled Photocleavage for the Orthogonal and Sequential Release of Multiple Proteins. Angew. Chem. Int. Edit. 52 (51), 13803-13807 (2013).
- Larrañeta, E., et al. Microwave-Assisted Preparation of Hydrogel-Forming Microneedle Arrays for Transdermal Drug Delivery Applications. Macromol. Mater. Eng. 300 (6), 586-595 (2015).
- Cook, J. P., Goodall, G. W., Khutoryanskaya, O. V., Khutoryanskiy, V. V. Microwave-Assisted Hydrogel Synthesis: A New Method for Crosslinking Polymers in Aqueous Solutions. Macromol. Rapid Comm. 33 (4), 332-336 (2012).
- Perale, G., et al. Multiple drug delivery hydrogel system for spinal cord injury repair strategies. J. Control. Release. 159 (2), 271-280 (2012).
- Rossi, F., Perale, G., Storti, G., Masi, M. A Library of Tunable Agarose Carbomer-Based Hydrogels for Tissue Engineering Applications: The Role of Cross-Linkers. J. Appl. Polym. Sci. 123 (4), 2211-2221 (2012).
- Frith, J. E., et al. An injectable hydrogel incorporating mesenchymal precursor cells and pentosan polysulphate for intervertebral disc regeneration. Biomaterials. 34 (37), 9430-9440 (2013).
- Kolb, H. C., Finn, M. G., Sharpless, K. B. Click chemistry: Diverse chemical function from a few good reactions. Angew. Chem. Int. Edit. 40 (11), (2001).
- Sacchetti, A., Mauri, E., Sani, M., Masi, M., Rossi, F. Microwave-assisted synthesis and click chemistry as simple and efficient strategy for RGD functionalized hydrogels. Tetrahedron Lett. 55 (50), 6817-6820 (2014).
- Ossipov, D. A., Hilborn, J. Poly(vinyl alcohol)-based hydrogels formed by "click chemistry". Macromolecules. 39 (5), 1709-1718 (2006).
- Truong, V., Blakey, I., Whittaker, A. K. Hydrophilic and Amphiphilic Polyethylene Glycol-Based Hydrogels with Tunable Degradability Prepared by "Click" Chemistry. Biomacromolecules. 13 (12), 4012-4021 (2012).
- Hou, R. Z., et al. New synthetic route for RGD tripeptide. Prep. Biochem. Biotechnol. 36 (3), 243-252 (2006).
- Rossi, F., Chatzistavrou, X., Perale, G., Boccaccini, A. R. Synthesis and Degradation of Agar-Carbomer Based Hydrogels for Tissue Engineering Applications. J. Appl. Polym. Sci. 123 (1), 398-408 (2012).
- Mauri, E., Rossi, F., Sacchetti, A. Tunable drug delivery using chemoselective functionalization of hydrogels. Mater. Sci. Eng. C. 61, 851-857 (2016).
- Joaquin, A., Peppas, N. A., Zoldan, J. Hydrogel Polymer Library for Developing Induced Pluripotent Stem Cell Derived Cardiac Patches. Tissue Eng. Part A. 20, S55-S55 (2014).
- Rossi, F., et al. Tunable hydrogel-Nanoparticles release system for sustained combination therapies in the spinal cord. Colloids Surf. B Biointerfaces. 108, 169-177 (2013).
- Kolb, H. C., Sharpless, K. B. The growing impact of click chemistry on drug discovery. Drug Discov. Today. 8 (24), 1128-1137 (2003).
- Ossipov, D. A., Yang, X., Varghese, O., Kootala, S., Hilborn, J. Modular approach to functional hyaluronic acid hydrogels using orthogonal chemical reactions. Chem. Commun. 46 (44), 8368-8370 (2010).
- Anderson, S. B., Lin, C. C., Kuntzler, D. V., Anseth, K. S. The performance of human mesenchymal stem cells encapsulated in cell-degradable polymer-peptide hydrogels. Biomaterials. 32 (14), 3564-3574 (2011).
- Caron, I., et al. A new three dimensional biomimetic hydrogel to deliver factors secreted by human mesenchymal stem cells in spinal cord injury. Biomaterials. 75, 135-147 (2016).
- Lee, J. W., Kim, H., Lee, K. Y. Effect of spacer arm length between adhesion ligand and alginate hydrogel on stem cell differentiation. Carbohyd. Polym. 139, 82-89 (2016).
- Liu, Y., Fan, Z., Wang, Y., Yu, L. Controlled Release of Low Molecular Protein Insulin-like Growth Factor-1 through Self-Assembling Peptide Hydrogel with Biotin Sandwich Approach. J.Biomed. Eng. 32 (2), 387-392 (2015).

