のフェーズI代謝コンピテンシーを特徴づけるために質量分析とルミネベースのアプローチ<em>インビトロ</em>細胞培養
Summary
in vitro系の代謝能力は、薬物や毒物の生体内変化及び処分のための重要な要件です。このプロトコルでは、我々は、私は細胞培養で代謝相を評価するための基準の代謝プローブのアプリケーションを記述します。
Abstract
生体異物代謝酵素は、溶解度を増加し、排泄を促進する官能基を追加することにより、医薬品や毒物の生体内変化における重要な機能を果たしています。いくつかの場面で、それらの構造変更は、新毒性産物の形成につながります。動物実験を低減するために、化学的リスクは、代謝コンピテント細胞を用いて評価することができます。代謝酵素の発現は、しかしながら、 インビトロでの初代培養系において多くの時間にわたって安定ではなく、多くの場合、細胞株において部分的または不在です。したがって、in vitroでの薬品、添加物、および環境汚染物質代謝の研究は、理想的に代謝活性を特徴づけされた細胞系で実施されるべきです。ここではUPLC質量分析法による定量化化学プローブおよびそれらの代謝産物を使用して、2D細胞株および初代3D培養における代謝酵素(ヒトフェーズI)のクラスの活性を測定する手法を説明しルミノメトリー。この方法は、細胞株および種々の組織に由来する一次細胞における代謝活性を試験するために実施することができます。
Introduction
生体異物代謝は身体に対して外来の化学物質は、それらの排泄1を容易にするために親水性基とのコンジュゲートの付加によって修飾されるプロセスです。典型的には、生体異物の代謝は、Iは、1つまたは複数のヒドロキシル基1、2を添加した酸化の大部分からなる相との二段階プロセスです。例えばグルクロニドまたは硫酸部分1,2のような親水性結合体のための受容体として、フェーズIIにおいて、ヒドロキシル基が使用されます。受容体基が分子にすでに存在する場合、結合ステップは、独立して、フェーズI代謝の発生する可能性があります。各反応は、ヒドロキシル化( 図1)及び化学基板3の脱アルキル化を触媒する酵素の特定の群、 例えば 、のCYP(シトクロムP450類)により行われます。 ConjugatioNスルホトランスフェラーゼによって触媒される、UDP-グルクロノシルトランスフェラーゼ( 図1)、グルタチオン-S-トランスフェラーゼおよびN-アセチルトランスフェラーゼ4。各組織及び臓器は、肝臓はこれらのタンパク質のほとんどを発現すると、特定の代謝酵素の発現プロファイルを有することになります。
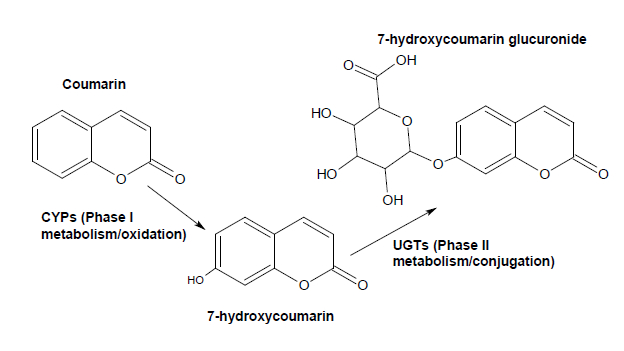
図1:クマリンためのフェーズIおよびフェーズII代謝の例。 CYP2A6 / CYP2A13クマリンの7 – 水酸化を触媒します。 7-ヒドロキシクマリンは、UGT1A6及びUGT1A9が最も高い活性を示すと、第II相酵素UGTsによってグルクロニド部分に結合されています。
生体異物の代謝を理解することは、二つの理由のための医薬品の安全性の評価では、化学的リスク評価のために重要である:反応速度は、薬物や化学物質がアクティブまたは非アクティブのB型で体内に残存する期間を決定しますEFORE排泄。親化合物は、代謝酵素によって、より反応性不安定で有毒種に変更することができます。また、「生物活性」として知られているような反応は、主相II抱合5によって位相I CYP酵素によっても稀な機会に駆動されます。
これに基づいて、正確に薬剤または化学的に関連するリスクを予測するためのインビトロモデルの能力は、細胞系の代謝能力に大きく依存します。罹患組織から、または正常細胞の形質転換に由来する細胞株は、多くの場合、一部でない場合起源6のそれらの組織の代謝酵素プロファイル代表のすべてを失います。正常な代謝酵素プロファイルのメンテナンスは、(少なくとも短期培養において)、一次細胞培養物におけるより良い表示され、組織は、その3次元構造体1を保持することを可能にするマトリックスで培養した場合に、さらに改善されます。したがって、CHARインビトロ細胞系の代謝能力のacterizationは、細胞モデルは、化学的安全性評価を実施することが適切であるに関する決定を導く上で重要な予備的なステップです。
本稿では、肝細胞ライン7と3D原発性肺細胞培養8とのそれらのアプリケーションの例を用いてインビトロでフェーズI CYP酵素の活性および発現をプロファイリングするためのプロトコルを提示します。 CYP特異的基質、それらの代謝産物及び阻害剤対照を質量spectrometry-およびルミネセンスに基づく定量方法と共に記載されています。いくつかのCYP誘導性であり、他のものは構成的であるので、実施例はまた、これらの2つのシナリオについて説明します。
Protocol
Representative Results
Discussion
現在、多くの標準化された毒物学的試験システムは、正常なヒト代謝1の代表的ではない操作細菌、細胞株、または胚細胞を使用します。これは、化学物質や薬の潜在的な毒性活性の不正確な予測につながることができます。このようなチップ上の3D細胞培養および器官などのin vitroモデル 、 革新的な、より良い人間の組織21、22、23の正常な形態および代謝活性を再現する試みで開発されています。代謝能力は、毒性学的評価と薬物生体内変化の研究のために最も適しているモデル解読するために使用することができる1つの基準です。
本稿で概説されているプロトコルは、生細胞を用いたCYP酵素の活性を測定するために設計されています。それは柔軟であり、2Dまたは3D culturにおける異なる細胞系のために使用することができますESと発光性プローブ – または質量分析ベースのアプローチのいずれかを使用するためのオプションを提供しています。両方の方法は、材料のナノグラム量を検出してのみマルチウェル形式で増殖させた細胞の小さな数を必要とするのに十分な感度です。彼らはまた、複雑なマトリックスで栽培回転楕円体または細胞に適用できます。プローブ基板の選択は、明らかに、プロトコルの重要な要素です。アッセイの特異性は、CYP酵素の選択的であるプローブに依存していると保証の別の層は、選択的CYP阻害剤を使用することによって得ることができます。この論文に記載された基質および阻害剤は、ほんの一例ですが、他は文献に見出すことができます。
酵素が低レベルで発現されることに起因する可能性が負CYP活性の結果として新たな細胞型で作業する場合、複数のインキュベーション時間を考慮することが重要です。陽性対照として使用することができる細胞型の添加は、Aを確保することが望ましいです否定結果が技術的な問題にリンクされていないと、トラブルシューティングを支援します。一次肝細胞が代謝的に有能であり、コントロールとして使用することができ、例えば、懸濁液中の初代肝細胞を使用することは非常に容易であるが、それらの生存率は、時間的に限られています。肝細胞株は、このプロトコルに記載のように使用することが比較的容易である可能な代替であるが、一部は代謝活性6、21の点で他のものより優れています。
アッセイは、総タンパク質が定量されていない限り、非破壊的であるため、長期的な研究20時間にわたってCYP活性を追従することが可能です。いくつかの細胞は、培養液中で時間をかけて、可変CYP活性を持つことになりますので、これは重要なポイントです。負の結果は、in vitroでの分化または脱分化との密集度の欠如、進行に伴うかもしれません。その場合には、アプローチは、半quantitatiありますデータは、各細胞培養物中のタンパク質の総量によって正規化されていないのでまし。 TCDDの場合のように組織に対する毒性効果を有することができるプローブ、インヒビターまたはインデューサーへの曝露のようなCYP活性を測定した後、組織を再利用することは常に可能または推奨されません。
例えばミクロソームのような細胞画分はまた、所定の細胞型のCYP活性を特徴付けるために使用することができます。ミクロソーム調製物は、しかし、細胞材料、十分な補因子の添加を多く必要とし、酵素が活性のままであることを保証するためのバッファ。生きた細胞を使用すると、トリッキーなミクロソーム調製工程を排除し、最高の仕事どのバッファおよび補因子ワークアウト。
一般的な推奨事項として、さらにそれが酵素活性と一致することを確認するために、細胞培養物中のCYPの発現プロファイルを特徴づけるためのベストプラクティスです。検証のこの追加のレベルは、代謝プローブがentiないことをお勧め与えられ、単一CYPに固有依存しており、それが測定された代謝活性は、対応する酵素発現によって一致していることを増加確信を与えます。 CYPが膜タンパク質であるので、したがって、それらは、定量的RT-PCRは、これらの酵素20をプロファイリングするための好ましいアプローチであった、ウェスタンブロットのために準備するのが比較的困難です。
このプロトコルが唯一重要なものはあるが、代謝酵素の一のファミリーを表すアッセイCYP酵素活性の方法を記載していることに留意することが重要です。質量分析アプローチの柔軟性がプローブ基板の他の代謝変換の取得方法の開発を可能にします。しかし、それらは、一度に1つを開発する必要があり、現在、少数の知られている特定のプローブおよび他の代謝酵素の家族のための選択的阻害剤です。このギャップは、in vitro細胞systeの代謝能力を総合的に評価を可能にするために取り組むべきですミズ。
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors thank Epithelix Sarl and Biopredic International for providing the airway cells and hepatic cells micrographies and Neil Smith for the figure illustrating the experimental procedure.
Materials
| Reagent & Cells | |||
| 2 μm syringe filter | Whatman | UN203NPEORG | |
| 24 well plate | Corning | 3524 | |
| 4-methylumbelliferone | Sigma Aldrich | M1381 | |
| 5-phenyl pentyne | Sigma Aldrich | CD5001437 | |
| 6-hydroxybupropion | Sigma Aldrich | H3167 | |
| 6-hydroxychlorzoxazone | Sigma Aldrich | UC148 | |
| 7-ethoxycoumarin | Sigma Aldrich | 195642 | |
| 7-hydroxycoumarin | Sigma Aldrich | H24003 | |
| 8-methoxypsoralen | Sigma Aldrich | M3501 | |
| acetic acid | Sigma Aldrich | 695092 | |
| acetonitrile | Fisher | A/0626/17 | |
| α-naphthoflavone | Sigma Aldrich | N5757 | |
| BCA kit | Thermo Scientific | 23227 | |
| b-glucuronidase/arylsulfatase | Sigma Aldrich | G0876 | |
| Bupropion | Sigma Aldrich | B102 | |
| Carbamazepine | Sigma Aldrich | C4024 | |
| chlorzoxasone | Sigma Aldrich | C4397 | |
| collagen | Cell Systems | 5005-B | |
| coumarin | Sigma Aldrich | C4261 | |
| disulfiram | Sigma Aldrich | 86720 | |
| fluvoxamine | Sigma Aldrich | F2802 | |
| Glutamax (Glutamine supplement) | Fisher | 35050061 | |
| HepaRG metabolism supplement | Merck | MMAD621 | |
| HepaRG thaw media supplement | Merck | MMADD671 | |
| HepaRG | Merck | MMHPR116 | |
| Luciferin-CEE | Promega | V8751 | |
| methanol | Fisher | M/4056/17 | |
| MucilAir airway cells | Epithelix | EP01 | |
| MucilAir airway cells maintenance media | Epithelix | EP04MM | |
| Phenomenex Kinetex 2.6μm, PFP 100A | Phenomenex | 00B-4477-AN | |
| TCDD | Sigma Aldrich | 48599 | |
| thioTEPA | Sigma Aldrich | T6069 | |
| Waters Acquity UPLC HSS T3 1.8µm 2.1 x 50mm | Waters | 86003538 | |
| Williams’ E media | Fisher | 17704-024 | |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| UPLC | Waters | Acquity | |
| QTRAP MS | Sciex | ABI Sciex 4000 | |
| QTRAP MS software | Sciex | Analyst 1.4.2 | |
| luminometer | Molecular Devices | SpectraMax M3 | |
| spectrophotometer | Molecular Devices | SpectraMax M3 | |
| cell counter | Beckman Coulter | Vi-Cell XR | |
| rotary evaporator | Eppendorf | Eppendorf-5301 |
References
- Garcia-Canton, C., Minet, E. Metabolic Characterization of Cell Systems Used in In Vitro Toxicology Testing. Encyclopedia of Drug Metabolism and Interactions. , 1-31 (2016).
- Croom, E. Metabolism of xenobiotics of human environments. Prog. Mol. Biol. Transl. Sci. 112, 31-88 (2012).
- Lewis, D. F. 57 varieties: the human cytochromes P450. Pharmacogenomics. 5, 305-318 (2004).
- Jancova, P., Anzenbacher, P., Anzenbacherova, E. Phase II drug metabolizing enzymes. Biomed. Pap. Med. Fac. Univ Palacky. 154, 103-116 (2010).
- Dekant, W. The role of biotransformation and bioactivation in toxicity. EXS. 99, 57-86 (2009).
- Donato, M. T., Lahoz, A., Castell, J. V., Gomez-Lechon, M. J. Cell lines: a tool for in vitro drug metabolism studies. Curr. Drug Metab. 9, 1-11 (2008).
- Guillouzo, A., et al. The human hepatoma HepaRG cells: a highly differentiated model for studies of liver metabolism and toxicity of xenobiotics. Chem. Biol. Interact. 168, 66-73 (2007).
- Huang, S., Wiszniewski, L., Constant, S., Roggen, E. Potential of in vitro reconstituted 3D human airway epithelia (MucilAir) to assess respiratory sensitizers. Toxicol. In Vitro. 27, 1151-1156 (2013).
- Sisson, J. H., Stoner, J. A., Ammons, B. A., Wyatt, T. A. All-digital image capture and whole-field analysis of ciliary beat frequency. J. Microsc. 211, 103-111 (2003).
- Kuehn, D., et al. Impact assessment of repeated exposure of organotypic 3D bronchial and nasal tissue culture models to whole cigarette smoke. J. Vis. Exp. , (2015).
- Draper, A. J., Madan, A., Parkinson, A. Inhibition of coumarin 7-hydroxylase activity in human liver microsomes. Arch. Biochem. Biophys. 341, 47-61 (1997).
- Jensen, K. G., Poulsen, H. E., Doehmer, J., Loft, S. Kinetics and inhibition by fluvoxamine of phenacetin O-deethylation in V79 cells expressing human CYP1A2. Pharmacol. Toxicol. 76, 286-288 (1995).
- Yamazaki, H., Tanaka, M., Shimada, T. Highly sensitive high-performance liquid chromatographic assay for coumarin 7-hydroxylation and 7-ethoxycoumarin O-deethylation by human liver cytochrome P450 enzymes. J. Chromatogr. B. Biomed. Sci. Appl. 721, 13-19 (1999).
- Turpeinen, M., Raunio, H., Pelkonen, O. The functional role of CYP2B6 in human drug metabolism: substrates and inhibitors in vitro, in vivo and in silico. Curr. Drug Metab. 7, 705-714 (2006).
- Kartha, J. S., Yost, G. S. Mechanism-based inactivation of lung-selective cytochrome P450 CYP2F enzymes. Drug Metab. Dispos. 36, 155-162 (2008).
- Sheets, P. L., Yost, G. S., Carlson, G. P. Benzene metabolism in human lung cell lines BEAS-2B and A549 and cells overexpressing CYP2F1. J. Biochem. Mol. Toxicol. 18, 92-99 (2004).
- Kharasch, E. D., Thummel, K. E., Mhyre, J., Lillibridge, J. H. Single-dose disulfiram inhibition of chlorzoxazone metabolism: a clinical probe for P450 2E1. Clin. Pharmacol. Ther. 53, 643-650 (1993).
- Graef, V., Furuya, E., Nishikaze, O. Hydrolysis of steroid glucuronides with beta-glucuronidase preparations from bovine liver, Helix pomatia, and E. coli. Clin. Chem. 23, 532-535 (1977).
- Baxter, A., et al. Targeted omics analyses, and metabolic enzyme activity assays demonstrate maintenance of key mucociliary characteristics in long term cultures of reconstituted human airway epithelia. Toxicol. In Vitro. 29, 864-875 (2015).
- Gomez-Lechon, M. J., Tolosa, L., Conde, I., Donato, M. T. Competency of different cell models to predict human hepatotoxic drugs. Expert. Opin. Drug Metab. Toxicol. 10, 1553-1568 (2014).
- Li, Z., et al. Assessment of metabolism-dependent drug efficacy and toxicity on a multilayer organs-on-a-chip. Integr. Biol. 8, 1022-1029 (2016).
- Takahashi, Y., et al. Three-dimensional (3D) spheroid cultures improve the metabolic gene expression profiles of HepaRG cells. Biosci. Rep. , (2015).

