Massespektrometri og luminogent tilgange til Karakterisere Fase I Metabolisk Kompetenceudvikling af<em> In vitro</em> Cell Cultures
Summary
Metabolisk kompetence in vitro systemer er en afgørende forudsætning for biotransformation og disposition af narkotika og giftstoffer. I denne protokol, beskriver vi anvendelsen af reference- metaboliske prober til at vurdere Fase I metabolismen i cellekulturer.
Abstract
Xenobiotiske enzymer spiller en nøglefunktion i biotransformationen af lægemidler og toksiske stoffer ved tilsætning af funktionelle grupper, som øger opløseligheden og lette udskillelse. Ved nogle lejligheder disse strukturelle modifikationer fører til dannelsen af nye giftige produkter. For at reducere dyreforsøg, kan kemisk risiko vurderes ved anvendelse metabolisk kompetente celler. Ekspressionen af metaboliske enzymer er imidlertid ikke stabil over tid i mange in vitro primære dyrkningssystemer og er ofte delvis eller fraværende i cellelinier. Derfor bør ideelt gennemførte undersøgelsen af lægemidler, tilsætningsstoffer og miljømæssige forureninger metabolisme in vitro i cellesystemer hvor metabolisk aktivitet er blevet karakteriseret. Vi forklare her en fremgangsmåde til måling af aktiviteten af en klasse af metaboliske enzymer (Human fase I) i 2D-cellelinjer og primære 3D kulturer under anvendelse af kemiske prober og deres metaboliske produkter kvantificerbare af UPLC massespektrometri ogluminometri. Fremgangsmåden kan gennemføres for at teste den metaboliske aktivitet i cellelinier og primære celler afledt fra en række væv.
Introduction
Xenobiotisk metabolisme er den proces, hvorigennem kemikalier er fremmede for kroppen er modificeret ved tilsætning af hydrofile grupper og konjugater at lette deres udskillelse 1. Typisk metabolismen af xenobiotiske stoffer er en to-trins proces med fase I består hovedsageligt af en oxidation med tilsætning af en eller flere hydroxylgrupper 1, 2. I fase II er hydroxylgrupperne anvendes som acceptorer for en hydrofil konjugat såsom glucuronid eller et sulfat-del 1, 2. Hvis en acceptorgruppe er allerede til stede på molekylerne, kan konjugeringen trin ske uafhængigt af fase I-metabolisme. Hver reaktion udføres ved en specifik gruppe af enzymer, fx CYP'er (cytochrom P450'er), som katalyserer hydroxyleringen (figur 1) og dealkylering af kemiske substrater 3. Conjugation katalyseres af sulfotransferaser, UDP-glucuronosyltransferaser (figur 1), glutathion-S-transferaser og N-acetyltransferaser 4. Hvert væv og organ vil have en specifik metabolisk enzym ekspressionsprofil, med lever udtrykker de fleste af disse proteiner.
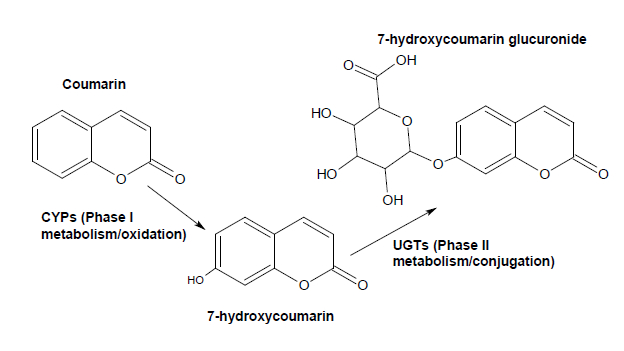
Figur 1: Eksempel på fase I og fase II Metabolism for coumarin. CYP2A6 / CYP2A13 katalysere 7-hydroxylering af coumarin. 7-hydroxycoumarin er konjugeret til et glucuroniddelen ved fase II enzymer UGT'er, med UGT1A6 og UGT1A9 viser den højeste aktivitet.
Forståelse metabolismen af xenobiotika er kritisk ved evaluering af lægemiddelsikkerhed og for risikovurdering af kemikalier af to grunde: reaktionskinetikken vil afgøre, hvor længe et lægemiddel eller kemisk vil forblive i kroppen i en aktiv eller inaktiv form before udskillelse; og stamforbindelsen kan modificeres til en mere reaktiv, ustabil og toksisk arter ved metaboliske enzymer. Sådanne reaktioner også kendt som "bioaktivering" er for det meste drevet af fase I CYP-enzymer, men også sjældnere lejligheder af fase II konjugering 5.
Baseret på denne evne til en in vitro model til præcist at forudsige risikoen i forbindelse med et lægemiddel eller et kemikalie er meget afhængig af den metaboliske kompetence cellesystemet. Cellelinier afledt fra syge væv eller fra transformationen af normale celler mister ofte en del, hvis ikke alle af det metaboliske enzym er repræsentativ deres væv af oprindelse 6. Opretholdelsen af den normale metaboliske enzym profil vises bedre i primære cellekulturer (mindst i korttidskulturer) og er yderligere forbedret, hvis vævet er dyrket i en matrix gør det muligt at bevare sin 3D-struktur 1. Derfor trækulletacterization af det metaboliske kompetence et in vitro celle er en vigtig indledende skridt i en vejledning Beslutningen om, hvilke celle model er hensigtsmæssigt at gennemføre kemiske sikkerhedsvurderinger.
I denne afhandling præsenterer vi en protokol til at profilere aktiviteten og ekspressionen af fase I CYP-enzymer in vitro med eksempler på deres anvendelse med en hepatisk cellelinie 7 og 3D primære lunge cellekulturer 8. CYP specifikke substrater, deres metaboliske produkter og inhibitor kontroller er beskrevet sammen med masse spectrometry- og luminogent-baserede kvantificeringsmetoder. Da nogle CYP'er er inducerbare og andre er konstitutive, vil eksempler også blive givet til de to scenarier.
Protocol
Representative Results
Discussion
I øjeblikket er mange standardiserede toksikologiske testsystemer bruge gensplejsede bakterier, cellelinjer, eller embryonale celler, som ikke er repræsentative for den normale menneskelige stofskifte 1. Dette kan føre til unøjagtige forudsigelser af den potentielle toksiske aktivitet af en kemisk eller medicin. Innovative in vitro modeller, såsom 3D-cellekulturer og organ på en chip, der udvikles i et forsøg på bedre at replikere den normale morfologi og metabolisk aktivitet af humane væv 21, 22, 23. Metabolisk kompetence er et kriterium, der kan anvendes til at dechifrere hvilke modeller er bedst egnet til toksikologiske undersøgelser vurdering og lægemiddel biotransformation.
Protokollen vi har skitseret i dette papir er designet til at måle aktiviteten af CYP-enzymer ved hjælp af levende celler. Den er fleksibel og kan anvendes til forskellige cellesystemer i 2D- eller 3D-cultures og giver mulighed for at bruge enten en luminogent probe- eller en massespektrometri-baseret tilgang. Begge metoder er følsomme nok til at opdage nanogram mængder af materialer og kræver kun et lille antal celler dyrket i et flere brønde format. De kan også anvendes til sfæroid eller celler dyrket i komplekse matricer. Udvælgelsen af sonden substratet er tydeligvis et kritisk element af protokollen. Specificiteten af assayet beror på proben være selektiv for CYP-enzym og et andet lag af sikkerhed kan opnås ved anvendelse af en selektiv CYP inhibitor. De substrater og inhibitorer, der er anført i dette papir er blot et par eksempler, men andre kan findes i litteraturen.
Det er vigtigt at overveje flere inkuberingstider når man arbejder med en ny celletype som en negativ CYP aktivitet resultat kunne skyldes enzymet, der udtrykkes på et lavt niveau. Tilsætningen af en celletype, der kan anvendes som en positiv kontrol er tilrådeligt at sikre, at ennegativt resultat er ikke knyttet til et teknisk spørgsmål og til at hjælpe med enhver fejlfinding. Primære leverceller er metabolisk kompetente og kan bruges som kontrol, for eksempel primære hepatocytter i suspension er meget nemme at bruge, men deres levedygtighed er begrænset i tid. Hepatiske cellelinier er mulige alternativer, som er relativt let at bruge som beskrevet i denne protokol, men nogle er bedre end andre, hvad angår metaboliske aktivitet 6, 21.
Da assayet er ikke-destruktiv, medmindre totalt protein kvantificeres, er det muligt at følge CYP-aktivitet over tid i længdesnitsundersøgelser 20. Dette er et vigtigt punkt, fordi nogle celler vil have variabel CYP-aktivitet over tid i kulturen. Et negativt resultat kan være forbundet med manglen på konfluens fremskridt med differentieringen eller dedifferentiering in vitro. I så fald, tilgangen er semi-quantitative da data ikke normaliseres ved den totale mængde af protein i hver celle kultur. Det er ikke altid muligt eller anbefalet at genbruge vævet efter måling af CYP-aktivitet som eksponering for prober, hæmmere eller induktorer kan have en toksisk virkning på væv som det er tilfældet for TCDD.
Cellefraktioner, såsom mikrosomer kunne også anvendes til at karakterisere CYP-aktivitet af en given celletype. Mikrosomekstrakter præparater kræver imidlertid en masse cellemateriale, tilsætning af tilstrækkelige cofaktorer og buffer for at sikre, at enzymerne forbliver aktive. Ved hjælp af levende celler eliminerer tricky mikrosom forberedelse trin og arbejder ud som buffere og cofaktorer fungerer bedst.
Som en generel anbefaling, er det en god praksis for yderligere at karakterisere ekspressionsprofilen af CYP'er i cellekulturer at kontrollere, at det passer til den enzymatiske aktivitet. Denne ekstra niveau af kontrol er anbefales, da de metaboliske sonder ikke er Entipåberåbe specifik for en enkelt CYP og det giver øget tillid til, at den målte metaboliske aktivitet modsvares af det tilsvarende enzym-ekspression. Da CYP'er er membranproteiner de er relativt vanskelige at fremstille til western blots, derfor kvantitativ RT-PCR har været den foretrukne metode til at profilere disse enzymer 20.
Det er vigtigt at bemærke, at denne protokol beskriver en fremgangsmåde til assay CYP enzymaktivitet, som kun repræsenterer en familie af metaboliske enzymer, omend vigtig. Fleksibiliteten i et massespektrometri metode tillader udviklingen af erhvervelse metoder til andre metaboliske omdannelser af probesubstrater. Men de skal udvikles en ad gangen, og der er i øjeblikket færre kendte specifikke prober og selektive inhibitorer for andre metaboliske enzymer familier. Denne kløft bør behandles for at muliggøre en samlet vurdering af den metaboliske kompetence in vitro celle systeFrk.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors thank Epithelix Sarl and Biopredic International for providing the airway cells and hepatic cells micrographies and Neil Smith for the figure illustrating the experimental procedure.
Materials
| Reagent & Cells | |||
| 2 μm syringe filter | Whatman | UN203NPEORG | |
| 24 well plate | Corning | 3524 | |
| 4-methylumbelliferone | Sigma Aldrich | M1381 | |
| 5-phenyl pentyne | Sigma Aldrich | CD5001437 | |
| 6-hydroxybupropion | Sigma Aldrich | H3167 | |
| 6-hydroxychlorzoxazone | Sigma Aldrich | UC148 | |
| 7-ethoxycoumarin | Sigma Aldrich | 195642 | |
| 7-hydroxycoumarin | Sigma Aldrich | H24003 | |
| 8-methoxypsoralen | Sigma Aldrich | M3501 | |
| acetic acid | Sigma Aldrich | 695092 | |
| acetonitrile | Fisher | A/0626/17 | |
| α-naphthoflavone | Sigma Aldrich | N5757 | |
| BCA kit | Thermo Scientific | 23227 | |
| b-glucuronidase/arylsulfatase | Sigma Aldrich | G0876 | |
| Bupropion | Sigma Aldrich | B102 | |
| Carbamazepine | Sigma Aldrich | C4024 | |
| chlorzoxasone | Sigma Aldrich | C4397 | |
| collagen | Cell Systems | 5005-B | |
| coumarin | Sigma Aldrich | C4261 | |
| disulfiram | Sigma Aldrich | 86720 | |
| fluvoxamine | Sigma Aldrich | F2802 | |
| Glutamax (Glutamine supplement) | Fisher | 35050061 | |
| HepaRG metabolism supplement | Merck | MMAD621 | |
| HepaRG thaw media supplement | Merck | MMADD671 | |
| HepaRG | Merck | MMHPR116 | |
| Luciferin-CEE | Promega | V8751 | |
| methanol | Fisher | M/4056/17 | |
| MucilAir airway cells | Epithelix | EP01 | |
| MucilAir airway cells maintenance media | Epithelix | EP04MM | |
| Phenomenex Kinetex 2.6μm, PFP 100A | Phenomenex | 00B-4477-AN | |
| TCDD | Sigma Aldrich | 48599 | |
| thioTEPA | Sigma Aldrich | T6069 | |
| Waters Acquity UPLC HSS T3 1.8µm 2.1 x 50mm | Waters | 86003538 | |
| Williams’ E media | Fisher | 17704-024 | |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| UPLC | Waters | Acquity | |
| QTRAP MS | Sciex | ABI Sciex 4000 | |
| QTRAP MS software | Sciex | Analyst 1.4.2 | |
| luminometer | Molecular Devices | SpectraMax M3 | |
| spectrophotometer | Molecular Devices | SpectraMax M3 | |
| cell counter | Beckman Coulter | Vi-Cell XR | |
| rotary evaporator | Eppendorf | Eppendorf-5301 |
References
- Garcia-Canton, C., Minet, E. Metabolic Characterization of Cell Systems Used in In Vitro Toxicology Testing. Encyclopedia of Drug Metabolism and Interactions. , 1-31 (2016).
- Croom, E. Metabolism of xenobiotics of human environments. Prog. Mol. Biol. Transl. Sci. 112, 31-88 (2012).
- Lewis, D. F. 57 varieties: the human cytochromes P450. Pharmacogenomics. 5, 305-318 (2004).
- Jancova, P., Anzenbacher, P., Anzenbacherova, E. Phase II drug metabolizing enzymes. Biomed. Pap. Med. Fac. Univ Palacky. 154, 103-116 (2010).
- Dekant, W. The role of biotransformation and bioactivation in toxicity. EXS. 99, 57-86 (2009).
- Donato, M. T., Lahoz, A., Castell, J. V., Gomez-Lechon, M. J. Cell lines: a tool for in vitro drug metabolism studies. Curr. Drug Metab. 9, 1-11 (2008).
- Guillouzo, A., et al. The human hepatoma HepaRG cells: a highly differentiated model for studies of liver metabolism and toxicity of xenobiotics. Chem. Biol. Interact. 168, 66-73 (2007).
- Huang, S., Wiszniewski, L., Constant, S., Roggen, E. Potential of in vitro reconstituted 3D human airway epithelia (MucilAir) to assess respiratory sensitizers. Toxicol. In Vitro. 27, 1151-1156 (2013).
- Sisson, J. H., Stoner, J. A., Ammons, B. A., Wyatt, T. A. All-digital image capture and whole-field analysis of ciliary beat frequency. J. Microsc. 211, 103-111 (2003).
- Kuehn, D., et al. Impact assessment of repeated exposure of organotypic 3D bronchial and nasal tissue culture models to whole cigarette smoke. J. Vis. Exp. , (2015).
- Draper, A. J., Madan, A., Parkinson, A. Inhibition of coumarin 7-hydroxylase activity in human liver microsomes. Arch. Biochem. Biophys. 341, 47-61 (1997).
- Jensen, K. G., Poulsen, H. E., Doehmer, J., Loft, S. Kinetics and inhibition by fluvoxamine of phenacetin O-deethylation in V79 cells expressing human CYP1A2. Pharmacol. Toxicol. 76, 286-288 (1995).
- Yamazaki, H., Tanaka, M., Shimada, T. Highly sensitive high-performance liquid chromatographic assay for coumarin 7-hydroxylation and 7-ethoxycoumarin O-deethylation by human liver cytochrome P450 enzymes. J. Chromatogr. B. Biomed. Sci. Appl. 721, 13-19 (1999).
- Turpeinen, M., Raunio, H., Pelkonen, O. The functional role of CYP2B6 in human drug metabolism: substrates and inhibitors in vitro, in vivo and in silico. Curr. Drug Metab. 7, 705-714 (2006).
- Kartha, J. S., Yost, G. S. Mechanism-based inactivation of lung-selective cytochrome P450 CYP2F enzymes. Drug Metab. Dispos. 36, 155-162 (2008).
- Sheets, P. L., Yost, G. S., Carlson, G. P. Benzene metabolism in human lung cell lines BEAS-2B and A549 and cells overexpressing CYP2F1. J. Biochem. Mol. Toxicol. 18, 92-99 (2004).
- Kharasch, E. D., Thummel, K. E., Mhyre, J., Lillibridge, J. H. Single-dose disulfiram inhibition of chlorzoxazone metabolism: a clinical probe for P450 2E1. Clin. Pharmacol. Ther. 53, 643-650 (1993).
- Graef, V., Furuya, E., Nishikaze, O. Hydrolysis of steroid glucuronides with beta-glucuronidase preparations from bovine liver, Helix pomatia, and E. coli. Clin. Chem. 23, 532-535 (1977).
- Baxter, A., et al. Targeted omics analyses, and metabolic enzyme activity assays demonstrate maintenance of key mucociliary characteristics in long term cultures of reconstituted human airway epithelia. Toxicol. In Vitro. 29, 864-875 (2015).
- Gomez-Lechon, M. J., Tolosa, L., Conde, I., Donato, M. T. Competency of different cell models to predict human hepatotoxic drugs. Expert. Opin. Drug Metab. Toxicol. 10, 1553-1568 (2014).
- Li, Z., et al. Assessment of metabolism-dependent drug efficacy and toxicity on a multilayer organs-on-a-chip. Integr. Biol. 8, 1022-1029 (2016).
- Takahashi, Y., et al. Three-dimensional (3D) spheroid cultures improve the metabolic gene expression profiles of HepaRG cells. Biosci. Rep. , (2015).

