Modellierung Fast-Scan Zyklische Voltammetrie Daten aus elektrisch stimulierten Dopamin Neurotransmission Daten mit QNsim1.0
Summary
Fast-Scan zyklische Voltammetrie kann in vivo Dopamin Neurotransmission im Zusammenhang mit Drogen, Krankheit und anderen experimentellen Manipulationen zu überwachen. Diese Arbeit beschreibt die Implementierung von QNsim1.0, einer Software zur Modellierung von elektrisch stimulierten Dopaminreaktionen gemäß dem quantitativen neurobiologischen Modell zur Quantifizierung von Schätzungen der Dopaminfreisetzung und Wiederaufnahmedynamik.
Abstract
Zentrale dopaminerge (DAergische) Wege haben eine wichtige Rolle in einer Vielzahl von Funktionen wie Aufmerksamkeit, Motivation und Bewegung. Dopamin (DA) ist an Krankheiten und Störungen einschließlich Aufmerksamkeitsdefizit-Hyperaktivitätsstörung, Parkinson-Krankheit und traumatischen Hirnverletzungen beteiligt. So sind DA Neurotransmission und die Methoden, um es zu studieren, von intensivem wissenschaftlichem Interesse. In vivo Fast-Scan-zyklische Voltammetrie (FSCV) ist eine Methode, die selektiv die Überwachung von DA-Konzentrationsänderungen mit feiner zeitlicher und räumlicher Auflösung ermöglicht. Diese Technik wird üblicherweise in Verbindung mit elektrischen Stimulationen von aufsteigenden DAergischen Wegen verwendet, um den Impulsfluss der Dopaminneurotransmission zu kontrollieren. Obwohl das stimulierte DA-Neurotransmission-Paradigma robuste DA-Antworten mit klaren Morphologien hervorbringen kann, was sie für die kinetische Analyse zugänglich macht, gibt es noch viel Diskussion darüber, wie man die Antworten in Bezug auf ihre DA-Freisetzung und Clearan interpretiertCE-Komponenten Um diesem Problem zu begegnen, wurde vor kurzem ein quantitatives neurobiologisches (QN) Framework der stimulierten DA-Neurotransmission entwickelt, um die Dynamik der DA-Freisetzung und Wiederaufnahme im Laufe einer stimulierten DA-Antwort realistisch zu modellieren. Die Grundlagen dieses Modells basieren auf experimentellen Daten aus stimulierter DA-Neurotransmission und auf Prinzipien der Neurotransmission aus verschiedenen Forschungsrichtungen. Das QN-Modell implementiert 12 Parameter, die sich auf die stimulierte DA-Freigabe und die Wiederaufnahmedynamik beziehen, um DA-Antworten zu modellieren. Diese Arbeit beschreibt, wie man DA-Antworten mit QNsim1.0 simuliert und auch detaillierte Prinzipien, die implementiert wurden, um systematisch Veränderungen in der stimulierten Dopaminfreisetzung und Wiederaufnahmedynamik zu erkennen.
Introduction
Dopamin (DA) Neurotransmission spielt eine wesentliche Rolle in verschiedenen kognitiven und Verhaltensfunktionen, und seine Dysfunktion ist in mehrere häufige Erkrankungen und Störungen verwickelt. Als solches ist es entscheidend, genaue Methoden zur quantitativen Untersuchung von DA-Neurotransmission in vivo zu entwickeln , um zu untersuchen, wie sich die DA-Neurotransmission im Kontext von Krankheitsmodellen und Arzneimittel-Pharmakologie ändert. Fast-Scan zyklische Voltammetrie (FSCV) ermöglicht die Überwachung in vivo DA Neurotransmission mit feiner räumlicher und zeitlicher Auflösung. Während es möglich ist, die physiologische DA-Neurotransmission in wachen, frei verhaltenden Tieren zu überwachen, kann die elektrische Stimulation von aufsteigenden dopaminergen Wegen bei anästhesierten Tieren robuste DA-Reaktionen hervorrufen, die der verbesserten kinetischen Analyse der DA-Neurotransmission zugänglich sind.
Elektrisch stimulierte DA-Antworten spiegeln ein dynamisches Zusammenspiel von DA-Freisetzung und Wiederaufnahme und Interpretationen widerDiese Antworten haben überwiegend ein einfaches Modell der stimulierten DA-Neurotransmission namens Michaelis-Menten (MM) Modell 12 verwendet. Das MM-Modell besteht aus 3 Variablen, um DA-Antworten in Bezug auf eine konstante DA-Freisetzungsrate und eine konstante Wiederaufnahme-Effizienz ( dh die Beziehung zwischen der DA-Wiederaufnahmerate und extrazellulären DA-Konzentrationen) zu beschreiben, wie durch Gleichung 1 beschrieben: 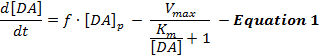
(DA-Freigabe) (DA-Wiederaufnahme)
In Gleichung 1 ist f die Häufigkeit der Stimulation; [DA] p ist die geschätzte DA-Konzentrationszunahme pro Puls der Stimulation; V max repräsentiert die geschätzte maximale Wiederaufnahmerate; Und Km ist die geschätzte MM-Konstante, die theoretisch äquivalent zu der extrazellulären DA-Konzentration ist, die 50% DAT sättigt, was zu einer halbmaximalen Wiederaufnahmerate führt. Dieses differentiGleichung kann integriert werden, um experimentelle DA-Antworten zu simulieren, indem die Parameter [DA] p , V max und K m geschätzt werden.
Obwohl das MM-Modell im Verständnis der DA-Neurotransmission-Kinetik in verschiedenen experimentellen Kontexten erhebliche Fortschritte erzielt hat, macht das MM-Modell vereinfachte fundamentale Annahmen, die seine Anwendbarkeit bei der Modellierung von DA-Reaktionen, die durch supraphysiologische Stimulationen 2 , 13 hervorgerufen werden, einschränken. Zum Beispiel kann das MM-Modell nur DA-Response-Formen approximieren, wenn sie konvex aufsteigen, aber es kann nicht für die allmählichen (konkaven) steigenden Reaktionen verantwortlich sein, die in den dorsalen striatalen Regionen gefunden werden 12 . So erfassen die MM-Modellannahmen die dynamischen Freisetzungs- und Wiederaufbauprozesse der stimulierten DA-Neurotransmission nicht genau.
Um stimulierte DA-Antworten nach einem realistischen Quant zu modellierenEs wurde das quantitative neurobiologische (QN) Framework entwickelt, das auf Prinzipien der stimulierten Neurotransmission Kinetik basiert, die aus komplementärer Forschung und Experimentierung gewonnen wurde. Verschiedene Linien der Neurotransmission-Forschung zeigen, dass (1) stimulierte Neurotransmitter-Freisetzung ein dynamischer Prozess ist, der im Laufe der Stimulation 14 abnimmt, (2) die Freisetzung setzt sich in der Nachstimulationsphase mit der zweiphasigen Zerfallskinetik 15 und (3) DA fort Wiederaufnahme-Effizienz wird während der Dauer der Stimulation selbst 2 , 16 fortschreitend gehemmt. Diese drei Konzepte dienen als Grundlage des QN-Frameworks und die drei Gleichungen, bestehend aus 12 Parametern, die die Dynamik der DA-Freisetzung und Wiederaufnahme beschreiben ( Tabelle 1 ). Das QN-Framework kann heterogene experimentelle DA-Response-Typen genau simulieren, ebenso wie die pGeronnene Effekte von experimentellen Manipulationen von Stimulationsparametern und Arzneimittelverabreichung 2 , 6 . Obwohl weitere Untersuchungen notwendig sind, um den Datenmodellierungsansatz zu verfeinern, können zukünftige Experimente von diesem neurobiologisch fundierten Modellierungsansatz profitieren, der die von dem stimulierten DA-Neurotransmission-Paradigma gezogenen Schlussfolgerungen wesentlich ergänzt.

Tabelle 1: Modellierung von Gleichungen und Parametern . Bitte klicken Sie hier, um eine größere Version dieser Figur zu sehen.
Dieses Tutorial beschreibt, wie man stimulierte DA-Response-Daten modelliert, um die DA-Freisetzung und die Wiederaufnahme der Kinetik mit QNsim 1.0 zu schätzen. Die eigentliche experimentelle Datenerhebung und prOcessing wird hier nicht beschrieben und benötigt nur zeitliche DA-Konzentrationsdaten. Die theoretische Unterstützung und Fundamente des QN-Frameworks wurden bisher ausführlich beschrieben 2 , aber eine praktische Perspektive auf die Anwendung des QN-Frameworks zur Modellierung von DA-Antwortdaten wird nachfolgend beschrieben.
Das QN-Framework modelliert das dynamische Zusammenspiel zwischen: 1) dynamischer DA-Freigabe, 2) DA-Wiederaufnahme und 3) den Auswirkungen von supraphysiologischen Stimulationen auf diese Prozesse, um aussagekräftige kinetische Informationen aus DA-Response-Daten zu extrahieren. Das QN-Framework eignet sich am besten für die Modellierung von FSCV-Daten, die mit hochgradig supraphysiologischen Stimulationen mit langer Dauer ( zB 60 Hz, 10 s Stimulationen) gewonnen wurden, die robuste DA-Reaktionen erzeugen, die für die kinetische Analyse geeignet sind. Nach der genauen Modellierung der zugrundeliegenden Release- und Reuptake-Prozesse können die Modellparameter verwendet werden, um eine DA-Antwort zu simulieren, die der Form der exPerimale DA-Antwort.
Die Gleichungen des QN-Frameworks beschreiben die Rate der DA-Freisetzung und Wiederaufnahme im Verlauf der stimulierten DA-Antworten. Das QN-Framework beschreibt die stimulierte DA-Freisetzungsrate als Funktion der Zeit vom Beginn der Stimulation (t stim ), wenn die DA-Freisetzungsrate im Laufe der Stimulation exponentiell abnimmt. Dies steht im Einklang mit der Erschöpfung eines leicht lösbaren Pools, mit einer addierten Steady-State-DA-Freisetzungsrate (DARS), um die Vesikel-Ergänzung zu berücksichtigen, ähnlich wie bei anderen Berichten (Gleichung 2 ) 14 , 17 .
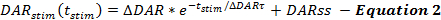
Manipulationen, die die DA-Freisetzungsrate erhöhen, wie z. B. das Erhöhen von & Dgr; DAR, & Dgr; DAR & tgr ; oder DARs, führen zu erhöhten Antwortamplituden auf DA-Zeit-Zeit-Plots. Jedes parameTer trägt unterschiedlich zu DA-Response-Formen bei. Die zunehmende DARss und Δ DAR τ machen die ansteigende Phase der Antworten linearer (weniger konvex). Die Verringerung von Δ DAR τ fördert die Konvexität, die durch die Größe von Δ DAR gesteuert wird. Basierend auf Modellierungserfahrung ist DARss im Allgemeinen weniger als 1/5 th von Δ DAR; Somit ist & Dgr; DAR der Freigabeparameter, der primär die Gesamtantwortamplitude einer DA-Antwort bestimmt.
Die Nachstimulations-DA-Freisetzungsrate wird durch Gleichung 3 als Fortsetzung der stimulierten DA-Freisetzungsrate vom Ende der Stimulation (DAR ES ) als Funktion der Zeit nach der Stimulation (t post ) modelliert. Die Nachstimulations-DA-Freisetzungsrate folgt einem zweiphasigen Abklingmuster, wie zuvor beschrieben, mit einer schnellen exponentiellen Abklingphase und einer verlängerten linearen Abklingphase, um zwei caLciumabhängige Neurotransmitter-Freisetzungsprozesse.
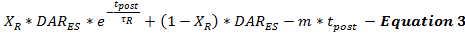
(Schneller exponentieller Zerfall) (verlängerter linearer Zerfall)
Es ist derzeit nicht möglich zu bestimmen, wie viel Post-Stimulation DA Release auftritt. Diese Begrenzung kann durch systematische Minimierung von Schätzungen der Nachstimulations-DA-Freisetzung und Validierung von Modellparametern über einen Satz von experimentellen DA-Antworten, die von der gleichen Aufzeichnungsstelle unter Verwendung unterschiedlicher Stimulationsdauern gesammelt wurden, behandelt werden. Diese Minimierung ermöglicht es Benutzern, konservative Schätzungen der Freisetzung und Wiederaufnahme zu machen. Weil elektrische Stimulationen zur Calciumakkumulation führen, die die poststimulierende Neurotransmitterfreisetzung fördert, beeinflusst die Dauer der Stimulation die poststimulierenden NeurotransenMitterfreigabeparameter 18 , 19 . Basierend auf der Modellierungserfahrung wurde festgestellt, dass mit zunehmender Stimulationsdauer τ R zunimmt und X R abnimmt, im Einklang mit den erwarteten Wirkungen einer größeren Calciumakkumulation 20 .
Gleichung 4 beschreibt die DA-Wiederaufnahmerate als Erweiterung des MM-Frameworks und beinhaltet einen dynamischen K m- Term, der bei der Stimulation zunimmt, um eine fortschreitend abnehmende Reuptakeffizienz durch die supraphysiologischen Stimulationen 2 , 16 zu modellieren. Die K m nach der Stimulation wird am K m -Wert am Ende der Stimulation (K mES ) konstant gehalten.
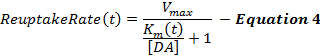
woher,
<img alt = "Gleichung 6" src = "/ files / ftp_upload / 55595 / 55595eq6.jpg" />
(Während der Stimulation) (nach Stimulation)
Stimulierte DA-Antworten, vor allem aus ventralen striatalen Regionen, sind oft unempfindlich gegenüber Veränderungen des anfänglichen K m -Wertes (K mi ), was die Definition eines K mi- Wertes problematisch macht. So wird, wie das ursprüngliche MM-Gerüst, K mi bei 0,1-0,4 & mgr; M für DA-Antworten angenähert, die von der Kontrolle unbehandelter Tiere gesammelt wurden. Der Δ K m Begriff bestimmt das Ausmaß der Reuptake Effizienz Veränderung während der Stimulation, die aus unserer Erfahrung etwa 20 ist81; M im Verlauf einer 60-Hz-10-s-Stimulation. Die k- und K- Minf- Werte bestimmen, wie sich K m im Laufe der Zeit ändert, und die Erhöhung einer dieser Begriffe fördert die Konkavität der aufsteigenden Phase. V max ist die maximale Wiederholungsrate, die sich teilweise auf die lokale DA-Transporter-Dichte bezieht, die einen ventromedialen bis dorsolateralen Gradienten 21 aufweist . Dementsprechend sind die V max -Werte im dorsalen Striatum (D-Str) im Allgemeinen größer als 30 μ M / s, aber im Allgemeinen weniger als 30 μ M / s in den ventralen Bereichen, wie der Nukleus accumbens (NAc) 6 .
Die oben genannten allgemeinen Richtlinien können bei der Modellierung von experimentellen DA-Antwortdaten helfen, aber die Erzeugung einer Simulation, die der experimentellen DA-Antwort angenähert wird, erfordert iterative Anpassung von Modellparametern. Die Genauigkeit der Modellparameter kann durch die Gewinnung von DA-Reaktionen auf supraphysiologische Stimulationen verbessert werdenEa robustes Substrat für die Simulation sowie durch die Erlangung und Modellierung mehrerer DA-Reaktionen auf Stimulierungen unterschiedlicher Dauer an der gleichen Aufnahmestelle ( zB 60-Hz, 5-s und 10-s-Stimulationen), um die Genauigkeit der Parameter zu validieren ( Siehe die Beispieldaten). Um zu demonstrieren, ist ein Datensatz mit dem Softwarepaket enthalten, das regiospezifische stimulierte DA-Antworten enthält, die im Nukleus accumbens und dorsal striatum gesammelt wurden, vor und nach einer pharmakologischen Herausforderung, die bereits mit dem QN-Framework modelliert wurde. Durch die Erweiterung werden die Benutzer finden, dass diese Methodik in ähnlicher Weise angewendet werden kann, um die Kinetik der DA-Neurotransmission in verschiedenen Krankheitszusammenhängen und pharmakologischen Manipulationen zu charakterisieren.
Protocol
Representative Results
Discussion
Die Verwendung von FSCV, um in vivo stimulierte DA Neurotransmission zu beginnen, entstand in den 1980er Jahren 30 und ist nach wie vor eine reiche Quelle für in vivo Neurotransmission Daten mit unvergleichlicher räumlicher und zeitlicher Auflösung. Stimulierte DA-Antworten spiegeln ein komplexes Gleichgewicht von DA-Freisetzung und Wiederaufnahme, die durch die elektrischen Stimulationen selbst moduliert werden. Das QN-Modell beinhaltet Prinzipien aus der zeitgenössischen N…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Wir bestätigen das UPMC Rehabilitation Institute für die Unterstützung dieser Arbeit.
Materials
| MATLAB R2016a for Mac | Mathworks | ||
| QNsim1.0 | In house software package | Software to model FSCV data using the QN framework |
References
- Taylor, I. M., et al. Kinetic diversity of dopamine transmission in the dorsal striatum. J Neurochem. 133 (4), 522-531 (2015).
- Harun, R., Grassi, C. M., Munoz, M. J., Torres, G. E., Wagner, A. K. Neurobiological model of stimulated dopamine neurotransmission to interpret fast-scan cyclic voltammetry data. Brain Res. 1599, 67-84 (2015).
- Taylor, I. M., Jaquins-Gerstl, A., Sesack, S. R., Michael, A. C. Domain-dependent effects of DAT inhibition in the rat dorsal striatum. Journal of neurochemistry. 122 (2), 283-294 (2012).
- Garris, P. A., Ciolkowski, E. L., Wightman, R. M. Heterogeneity of evoked dopamine overflow within the striatal and striatoamygdaloid regions. 신경과학. 59 (2), 417-427 (1994).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain Res. 487 (2), 311-320 (1989).
- Harun, R., et al. Fast-scan cyclic voltammetry demonstrates that L-DOPA produces dose-dependent regionally selective, bimodal effects on striatal dopamine kinetics in vivo. J Neurochem. , (2015).
- Jones, S. R., Garris, P. A., Wightman, R. M. Different effects of cocaine and nomifensine on dopamine uptake in the caudate-putamen and nucleus accumbens. The Journal of pharmacology and experimental therapeutics. 274 (1), 396-403 (1995).
- Budygin, E. A., John, C. E., Mateo, Y., Jones, S. R. Lack of cocaine effect on dopamine clearance in the core and shell of the nucleus accumbens of dopamine transporter knock-out mice. J Neurosci. 22 (10), RC222 (2002).
- Jones, S. R., et al. Loss of autoreceptor functions in mice lacking the dopamine transporter. Nat Neurosci. 2 (7), 649-655 (1999).
- Wagner, A. K., et al. Chronic methylphenidate treatment enhances striatal dopamine neurotransmission after experimental traumatic brain injury. J Neurochem. 108 (4), 986-997 (2009).
- Wagner, A. K., et al. Controlled cortical impact injury influences methylphenidate-induced changes in striatal dopamine neurotransmission. J Neurochem. 110 (3), 801-810 (2009).
- Wightman, R. M., et al. Real-time characterization of dopamine overflow and uptake in the rat striatum. 신경과학. 25 (2), 513-523 (1988).
- Moquin, K. F., Michael, A. C. Tonic autoinhibition contributes to the heterogeneity of evoked dopamine release in the rat striatum. J Neurochem. 110 (5), 1491-1501 (2009).
- Pyott, S. J., Rosenmund, C. The effects of temperature on vesicular supply and release in autaptic cultures of rat and mouse hippocampal neurons. J Physiol. 539 (Pt 2), 523-535 (2002).
- Atluri, P. P., Regehr, W. G. Delayed release of neurotransmitter from cerebellar granule cells. J Neurosci. 18 (20), 8214-8227 (1998).
- Wang, S. R., et al. Role of vesicle pools in action potential pattern-dependent dopamine overflow in rat striatum in vivo. J Neurochem. 119 (2), 342-353 (2011).
- Taschenberger, H., von Gersdorff, H. Fine-tuning an auditory synapse for speed and fidelity: developmental changes in presynaptic waveform, EPSC kinetics, and synaptic plasticity. J Neurosci. 20 (24), 9162-9173 (2000).
- Goda, Y., Stevens, C. F. Two components of transmitter release at a central synapse. Proc Nat Acad of Sci U S A. 91 (26), 12942-12946 (1994).
- Yao, J., Gaffaney, J. D., Kwon, S. E., Chapman, E. R. Doc2 is a Ca2+ sensor required for asynchronous neurotransmitter release. Cell. 147 (3), 666-677 (2011).
- Hagler, D. J., Goda, Y. Properties of synchronous and asynchronous release during pulse train depression in cultured hippocampal neurons. J Neurophysiol. 85 (6), 2324-2334 (2001).
- Ciliax, B. J., et al. The dopamine transporter: immunochemical characterization and localization in brain. J Neurosci. 15 (3 Pt 1), 1714-1723 (1995).
- Volz, T. J., Farnsworth, S. J., Rowley, S. D., Hanson, G. R., Fleckenstein, A. E. Methylphenidate-induced increases in vesicular dopamine sequestration and dopamine release in the striatum: the role of muscarinic and dopamine D2 receptors. J Pharm Exp Ther. 327 (1), 161-167 (2008).
- Dresel, S. H., Kung, M. P., Plossl, K., Meegalla, S. K., Kung, H. F. Pharmacological effects of dopaminergic drugs on in vivo binding of [99mTc]TRODAT-1 to the central dopamine transporters in rats. Eur J Nucl Med. 25 (1), 31-39 (1998).
- Near, J. A., Bigelow, J. C., Wightman, R. M. Comparison of uptake of dopamine in rat striatal chopped tissue and synaptosomes. J Pharm Exp Ther. 245 (3), 921-927 (1988).
- Michael, A. C., Ikeda, M., Justice, J. B. Dynamics of the recovery of releasable dopamine following electrical stimulation of the medial forebrain bundle. Neurosci Lett. 76 (1), 81-86 (1987).
- Fierro, L., DiPolo, R., Llano, I. Intracellular calcium clearance in Purkinje cell somata from rat cerebellar slices. The Journal of physiology. 510 (Pt 2), 499-512 (1998).
- Sandoval, V., Riddle, E. L., Hanson, G. R., Fleckenstein, A. E. Methylphenidate redistributes vesicular monoamine transporter-2: role of dopamine receptors. J Neurosci. 22 (19), 8705-8710 (2002).
- Daws, L. C., et al. Cocaine increases dopamine uptake and cell surface expression of dopamine transporters. Biochem Biophys Res Commun. 290 (5), 1545-1550 (2002).
- Little, K. Y., Kirkman, J. A., Carroll, F. I., Clark, T. B., Duncan, G. E. Cocaine use increases [3H]WIN 35428 binding sites in human striatum. Brain Res. 628 (1-2), 17-25 (1993).
- Ewing, A. G., Bigelow, J. C., Wightman, R. M. Direct in vivo monitoring of dopamine released from two striatal compartments in the rat. Science. 221 (4606), 169-171 (1983).
- Janezic, S., et al. Deficits in dopaminergic transmission precede neuron loss and dysfunction in a new Parkinson model. Proc Natl Acad Sci U S A. 110 (42), E4016-E4025 (2013).
- Macdonald, P. A., Monchi, O. Differential effects of dopaminergic therapies on dorsal and ventral striatum in Parkinson’s disease: implications for cognitive function. Parkinsons Dis. 2011, 572743 (2011).
- Kile, B. M., et al. Optimizing the Temporal Resolution of Fast-Scan Cyclic Voltammetry. ACS Chem Neurosci. 3 (4), 285-292 (2012).
- Venton, B. J., Troyer, K. P., Wightman, R. M. Response times of carbon fiber microelectrodes to dynamic changes in catecholamine concentration. Anal Chem. 74 (3), 539-546 (2002).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain research. 487 (2), 311-320 (1989).
- Wu, Q., Reith, M. E., Wightman, R. M., Kawagoe, K. T., Garris, P. A. Determination of release and uptake parameters from electrically evoked dopamine dynamics measured by real-time voltammetry. J Neurosci Methods. 112 (2), 119-133 (2001).

